Original Editor – Joanne Garvey and Naomi O’Reilly
Top Contributors – Joanne Garvey, Lucinda hampton, Rachael Lowe, Naomi O’Reilly and Tarina van der Stockt
Introduktion
Neurofysiologi är den gren av fysiologin som behandlar nervsystemets funktioner. Det vill säga studiet av de funktionella egenskaperna hos neuroner, glia och nätverk.
- Historiskt sett har den dominerats av elektrofysiologi – den elektriska registreringen av neuronala händelser som sträcker sig från det molära (elektroencefalogrammet, EEG) till det cellulära (intracellulär registrering av egenskaperna hos enskilda neuroner).
- Eftersom neuronen är en elektrokemisk maskin är det omöjligt att skilja elektriska händelser från de biokemiska och molekylära processer som ger upphov till dem.
- Neurofysiologer använder idag tekniker från kemi (kalciumavbildning), fysik (funktionell magnetresonansavbildning, fMRI) och molekylärbiologi (platsinriktade mutationer) för att studera hjärnans funktion.
Nedan kommer du att lära dig allt om
- Jonkanaler
- Vilande membran och aktionspotential
- Neuromuskulär förbindelse/synapser
- Nervledning
- Neurotransmittorer, Receptorer och vägar
Ionkanaler
En jonkanal är en proteinmakromolekyl som korsar membranets bredd och tillåter molekyler att passera. Jonerna rör sig i en riktning som bestäms av den elektrokemiska gradienten över membranet.
- Ioner tenderar att strömma från ett område med hög koncentration till ett område med låg koncentration.
- I närvaro av en spänningsgradient kan det hända att det inte sker något jonflöde trots ojämna koncentrationer.
- Ionkanaler kan vara öppna eller stängda.
- Öppning sker genom att ändra spänningen över membranet eller genom att binda en kemisk substans till en receptor.
- Den viktigaste rollen är att de ger neuronen elektrisk excitabilitet.
- Finns i alla delar av neuronen och i mindre utsträckning i neurogliacellerna.
Typer av kanaler
- Spänningsstyrda
- Kemiskt aktiverade
- Mekanisk sträckning/tryck.
Fundamentala egenskaper hos en jonkanal
- Den består av ett antal proteinunderenheter som sitter tvärs över membranet och tillåter joner att passera från den ena sidan till den andra. (Transmembranporer)
- Kanalen måste kunna gå från öppet till stängt tillstånd och tillbaka.
- Måste kunna öppnas som svar på lämpliga stimuli.
Vissa kanaler reagerar på kemisk stimulans (särskilt vid synapsen). Dessa kanaler har specifika receptorer för denna kemikalie, vilket leder till att kanalen öppnas.
Restande membran och aktionspotential
- I viloläget är neuronalcellens membran ganska ogenomträngligt för joner. Detta är avgörande för genereringen av vilomembranpotentialen.
- Den viktigaste intracellulära jonen är kalium (Det är natrium i den extracellulära vätskan).
- Det naturliga flödet av joner genom deras koncentrationsgradienter är att K+ lämnar cellen och Na+ kommer in.
- Denna rörelse av joner ut ur cellen leder till en negativ membranpotential – Hyperpolarisering.
- Det motsatta gäller för ett relativt inflöde av joner – Hypopolarisering.

Restmembranet är relativt ogenomträngligt för Na+-joner, medan det förblir genomträngligt för K+-joner. Så när membranet är i vila tenderar det att ske ett utflöde av K+-joner ur cellen, längs dess koncentrationsgradient, vilket lämnar överflödig negativ laddning kvar. Detta fortsätter tills den kemiska koncentrationsgradienten som driver ut K+ från cellen är exakt vid den punkt där den kompenseras av den elektriska potentialskillnaden som genereras av detta utflöde. (membranpotentialen) K+ dras då tillbaka in i cellen.
Detta stabila tillstånd för membranet kallas jämviktspotential.
Ekvationen för att härleda jämviktspotentialen kallas Nernst-ekvationen.
Det finns faktiskt en något oväntad ökad positiv laddning i axoner på grund av en liten permeabilitet för Na+-joner hos membranet i viloläget. Detta kompenseras av den ATP-beroende Na+/K+-utbytespumpen. Jag pumpar ut 3 Na+ joner för varje 3K+ joner som förs in i cellen. Den ger dock bara ett litet bidrag till cellens membranpotential i vila.
Aktionspotential
Definieras som en ”enskild elektrisk impuls som passerar längs en axon”.
Den är allt eller inget i sin verkan. Detta innebär att när tröskelvärdet för stimulansintensiteten uppnås kommer en aktionspotential att genereras.
Information i nervsystemet kodas och tolkas av eldningsfrekvensen, inte av storleken på aktionspotentialen.
Tröskelvärde för stimulusintensitet: Det värde vid vilket nettoströmmen inåt (bestämd av Na+-joner) är precis större än nettoströmmen utåt (som bärs av K+-joner). Det är normalt -55mV (kritisk tröskel för eldning)
Apnanostimulans inträffar lättast vid axonhålan eftersom det är där som det finns en större täthet av Na+-jonkanaler. Det är av denna anledning som detta är platsen för AP-initiering i neuronen.
Om tröskelvärdet inte uppnås kommer aktionspotentialen inte att genereras, och överföringen av signalen avslutas i den punkten.
Händelseföljd för att en aktionspotential ska genereras
- Depolorerande spänning aktiverar de spänningskänsliga Na+ jonkanalerna i neuronmembranet: Na+-joner strömmar nerför den elektrokemiska gradienten. Membranet depolariseras ytterligare. Ytterligare Na+-kanaler öppnas i en positiv återkopplingsslinga. När det finns en större inkommande ström av natriumjoner jämfört med utflödet av K+ -joner öppnas alla Na+ -kanaler snabbt. Detta depolariserar membranet mot jämviktspotentialen för Na+ (+55 mV). Det uppstår en spik av AP, men den når inte jämviktspotentialen för Na+ på grund av det ökande K+-utflödet.
- När Na+ kanalerna blir mindre aktiva sjunker AP. Denna inaktivering är spänningsberoende. Under den fallande fasen är K+-strömmen viktig eftersom den leder till en kort period av membranhyperpolarisering innan den avaktiveras.
- Membranpotentialen återgår till vilostadiet.
Neuromuskulär förbindelse/synapser
Synapse
En synaps är förbindelsen mellan två neuroner. Den kemiska synapsen är den dominerande synapsen som finns i nervsystemet, men elektriska synapser finns i hjärtmuskel- och gliaceller.
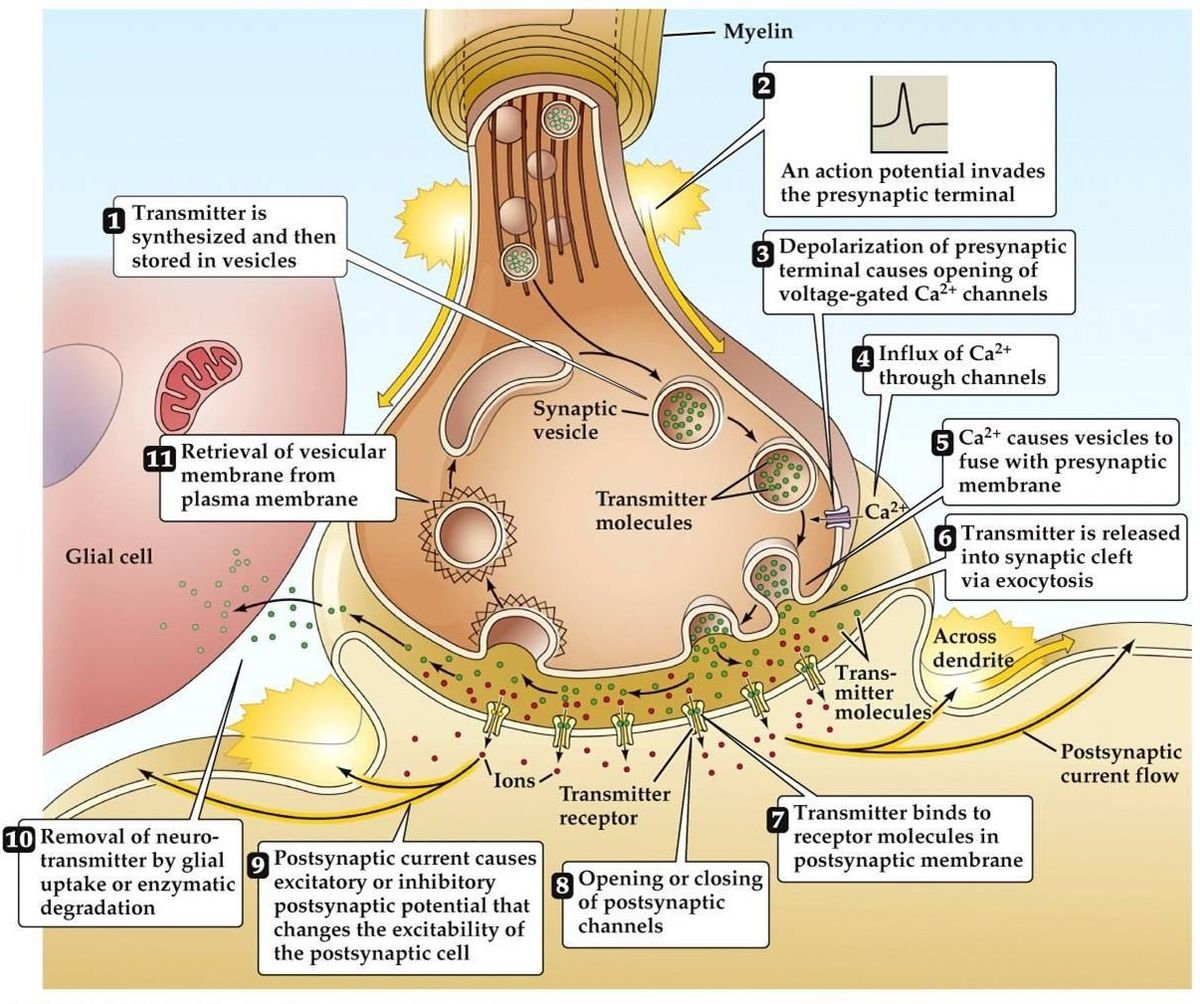
Synaptisk överföring
- Aktionspotential anländer, leder till depolarisering av den presynaptiska terminalen. Spänningsberoende Ca2+-kanaler öppnas i terminalens aktiva zoner. Detta leder till inflöde av Ca2+.
- Inflödet av Ca2+ leder till fosforylering och förändring av mängden presynaptiska kalciumbindande proteiner. Detta frigör vesikeln från sitt presynaptiska aktinnätverk, Den binder sedan till det presynaptiska membranet.
- Förening av vesikeln med membranet leder till att en liten kanal bildas, som snabbt expanderar och släpper ut sitt innehåll i den synaptiska klyftan. Vesikelmembranet återvinns genom endocytos.
- Framställd neurotransmittor diffunderar genom den synaptiska klyftan med målet att binda till den postsynaptiska receptorn.
- Aktivering av den postsynaptiska receptorn leder till en förändring av den postsynaptiska membranpotentialen.
- Det finns alternativa teorier som föreslår att neurotransmittorn levereras via molekyler eller membrankanaler snarare än vesiklar.
Nervledning
Aktionspotentialutbredning uppnås genom lokal strömspridning.
Nerven är isolerad med myelin om dess storlek är över en viss diameter, med Ranviers noder med olika intervall längs dess längd.
Unmyeliniserade axoner
Aktionspotential leder till depolarisering av membranet omedelbart framför (och bakom). Membranet befinner sig i ett refraktärt tillstånd, så aktionspotentialen leds endast i en riktning. Detta är genomförbart i små axoner, men spridningen av strömmen är långsam.
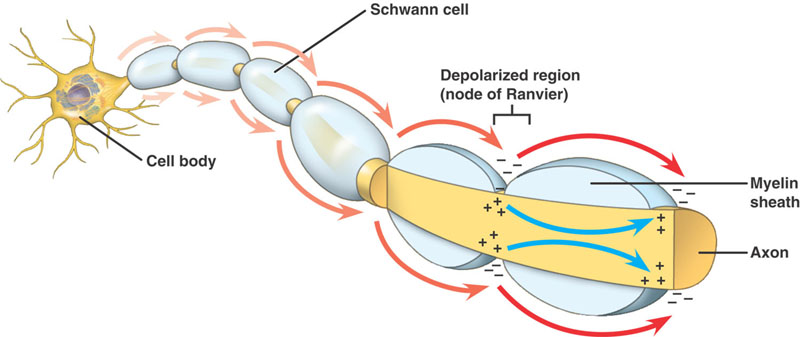
Myeliniserade axoner
Samma händelseförlopp som i de icke myeliniserade axonerna. Det finns dock en betydande skillnad. Den fortskridande aktionspotentialen möter en struktur med högt motstånd och låg kapacitet – myelin som är lindat runt axonen. Den depolariserande strömmen passerar längs axoplasman tills den når den låg resistenta Node of Ranvier med sin stora mängd Na+-kanaler. Handlingspotentialen genereras sedan på denna plats. Aktionspotentialen leds från knutpunkt till knutpunkt. Detta kallas saltatorisk ledning.
Fördelar med myelinisering
- Gör det möjligt att snabbt leda aktionspotentialen
- Minimerar de metaboliska kraven på cellen.
- Ökar packningskapaciteten hos NS, vilket gör att fler fibrer kan packas in i 1 nerv.
De flesta nerver som är större än 1 mikrometer är myeliniserade.
Störningar i ledningen beror normalt på demyeliniseringspatologier. De omfattar Guillan Barre-syndromet och multipel skleros.
Postsynaptisk integration:
Varje central neuron får många hundra synapser. Var och en av dessa ingångar integreras sedan i ett svar av just den neuronen. Detta innebär att alla inflöden som kommer in vid varje tidpunkt måste bearbetas. Detta kallas spatial summering. Behandling av inflöden under en viss tidsperiod kallas temporal summering. Det kommer att finnas en blandning av excitatoriska och inhiberande synapser som verkar vid denna punkt.
Excitatoriska postsynaptiska potentialer
- Bindning av neurotransmittor leder till att jonkanaler öppnas.
- Det sker katjoninflöde i den postsynaptiska processen
- Depolarisering av membranet sker.
- EPSPs depolariseringar som registreras i den postsynaptiska cellen vid ett visst excitatoriskt stimulus.
- Depolariseringar associerade med EPSPs kan fortsätta att utlösa APs om summering sker vid synapsen.
Hämmande postsynaptiska potentialer
- Ionkanaler tillåter postsynaptiskt anjoninflöde när de är öppna.
- Hyperpolarisering av membranet sker på grund av inflöde av CL- och utflöde av K+
- Viktigt för att modulera neuronernas svar på excitatoriskt inflöde vid synapsen.
- Finns på strategiskt viktiga platser i neuronen, t.ex. den proximala dendriten och soman.
- De har ett stort inflytande på det dendritiska trädet
- Vissa neuroner ger sitt eget hämmande inflytande genom att ha axonkollateraler och egna hämmande internuroner. Detta kallas återkopplingshämning. T.ex. motorneuroner och Renshaw-celler i ryggmärgen.
Neurotransmittorer, receptorer och vägar
Neurotransmittorn frigörs vid synapsen och arbetar med ett specifikt protein i det postsynaptiska membranet som kallas receptor. I vissa synapser kan neurotransmittorn också interagera med en presynaptisk autoreceptor. PSA fungerar som en reglerare av hur mycket transmittor som frigörs.
Receptorer är normalt specifika för en viss neurotransmittor. Det finns flera olika typer av receptorer. Neurotransmittorer som frisätts samtidigt kan reglera bindningen av en annan transmittor.
Receptorer för specifika neurotransmittorer kan antingen vara kopplade direkt till jonkanaler eller till ett membranenzym där neurotransmittorns bindning till receptorn antingen öppnar en jonkanal via en intracellulär enzymkaskad eller indirekt modulerar sannolikheten för att andra jonkanaler öppnas som svar på spänningsändringar. (Neuromodulering)
Aktiverad receptor kan endast återgå till sitt vilotillstånd när neurotransmittorn avlägsnas genom processen med enzymatisk hydrolys (upptag) i den presynaptiska nervterminalen eller i de närliggande gliacellerna.
Dessitisering/nedreglering: En minskning av receptorns affinitet för transmittorn på kort sikt, på lång sikt leder detta till en minskning av antalet receptorer.
Överkänslighet/uppreglering: En ökad affinitet hos receptorn för transmittorn på kort sikt kan leda till en ökning av antalet kanaler på lång sikt.
Receptorer:
- Ionotropa: N-metyl-D-aspartat (NMDA)
- Non NMDA.
- Metabotropa: G-proteinassocierade glutamatreceptorer som reagerar genom att initiera intracellulära biokemiska händelser och modulera synaptisk överföring.
Det finns ett stort antal neurotransmittorer:
- Excitatoriska aminosyror: Dessa är de viktigaste excitatoriska NTs i CNS. Den viktigaste NT i denna grupp är glutamat som verkar på ett antal receptorer.
- Hämmande aminosyror: Dessa är de viktigaste hämmande neurotransmittorerna, varav den viktigaste är GABA, som finns i hela CNS. Glycin, finns främst i ryggmärgen.
- Monoaminer: Finns i små grupper av neuroner i hjärnstammen, som projicerar sig långt ut i CNS. Finns i det autonoma NS. De binder till en mängd receptorer.
- Acetylkolin: Utbredd i hela nervsystemet, inklusive den neuromuskulära korsningen och det autonoma NS.
- Neuropeptider: Finns över hela NS. Frisätts ofta samtidigt med andra NTs.
Det har dessutom hittats över 50 neuroaktiva peptider, och nya upptäcks regelbundet. Många av dessa ”frisätts samtidigt” tillsammans med en småmolekylär transmittor. I vissa fall är dock en peptid den primära sändaren vid en synaps. β-endorfin är ett relativt välkänt exempel på en peptidneurotransmittor eftersom den ingår i mycket specifika interaktioner med opioidreceptorer i det centrala nervsystemet.
Enskilda joner (t.ex. synaptiskt frigjort zink) betraktas också av vissa som neurotransmittorer, liksom vissa gasformiga molekyler som kväveoxid (NO), kolmonoxid (CO) och vätesulfid (H2S). Gaserna produceras i den neurala cytoplasman och sprids omedelbart genom cellmembranet till den extracellulära vätskan och till närliggande celler för att stimulera produktionen av andra budbärare. Lösliga gasneurotransmittorer är svåra att studera, eftersom de verkar snabbt och omedelbart bryts ned och existerar endast i några sekunder.
Den vanligaste sändaren är glutamat, som är excitatoriskt vid mer än 90 procent av synapserna i den mänskliga hjärnan. Den näst vanligaste är gamma-aminosmörsyra, GABA, som är hämmande vid mer än 90 procent av de synapser som inte använder glutamat. Även om andra transmittorer används i färre synapser kan de vara mycket viktiga funktionellt: den stora majoriteten av psykoaktiva droger utövar sina effekter genom att förändra verkan av vissa neurotransmittorsystem, som ofta verkar genom andra transmittorer än glutamat eller GABA. Beroendeframkallande droger som kokain och amfetamin utövar sina effekter främst på dopaminsystemet. De beroendeframkallande opiatdrogerna utövar sina effekter främst som funktionella analoger av opioidpeptider, som i sin tur reglerar dopaminnivåerna.