Původní editor – Joanne Garvey a Naomi O’Reilly
Nejlepší přispěvatelé – Joanne Garvey, Lucinda hampton, Rachael Lowe, Naomi O’Reilly a Tarina van der Stockt
Úvod
Neurofyziologie je obor fyziologie zabývající se funkcemi nervového systému. Tj. studium funkčních vlastností neuronů, glie a sítí.
- Historicky jí dominuje elektrofyziologie – elektrický záznam neuronálních dějů od molárních (elektroencefalogram, EEG) po buněčné (intracelulární záznam vlastností jednotlivých neuronů).
- Protože neuron je elektrochemický stroj, není možné oddělit elektrické události od biochemických a molekulárních procesů, které je vyvolávají.
- Neurofyziologové dnes ke studiu funkce mozku používají techniky z chemie (zobrazování vápníku), fyziky (funkční magnetická rezonance, fMRI) a molekulární biologie (mutace zaměřené na místo).
Níže se dozvíte vše o
- Iontových kanálech
- Klidovém membránovém a akčním potenciálu
- Neuromuskulárním spojení / synapsích
- Nervovém vedení
- Neurotransmiterech, Receptory a dráhy
Iontové kanály
Iontový kanál je proteinová makromolekula, která překračuje šířku membrány a umožňuje průchod molekul. Ionty se pohybují ve směru určeném elektrochemickým gradientem přes membránu.
- Ionty mají tendenci proudit z oblasti s vysokou koncentrací do oblasti s nízkou koncentrací.
- V přítomnosti napěťového gradientu nemusí docházet k toku iontů navzdory nerovnoměrné koncentraci.
- Iontové kanály mohou být otevřené nebo uzavřené.
- Otevření je způsobeno změnou napětí na membráně nebo navázáním chemické látky na receptor.
- Nejdůležitější úlohou je, že zajišťují elektrickou vzrušivost neuronu.
- Nalézají se ve všech částech neuronu a v menší míře v neurogliových buňkách.
Typy kanálů
- Napěťově řízené
- Chemicky aktivované
- Mechanický tah/tlak.
Základní vlastnosti iontového kanálu
- Skládá se z řady proteinových podjednotek, které sedí napříč membránou a umožňují přechod iontů z jedné strany na druhou. (Transmembránový pór)
- Kanál musí být schopen přecházet z otevřeného do uzavřeného stavu a zpět.
- Musí být schopen se otevřít v reakci na příslušný podnět.
Některé kanály reagují na chemické podněty (zejména v synapsi). Tyto kanály mají specifické receptory pro danou chemickou látku, která vede k otevření kanálu.
Klidová membrána a akční potenciál
- V klidovém stavu je membrána neuronální buňky poměrně nepropustná pro ionty. To je rozhodující pro tvorbu klidového membránového potenciálu.
- Hlavním intracelulárním iontem je draslík (V extracelulární tekutině je to sodík).
- Přirozený tok iontů prostřednictvím jejich koncentračního gradientu spočívá v tom, že K+ buňku opouští a Na+ do ní vstupuje.
- Tento pohyb iontů ven z buňky vede k zápornému membránovému potenciálu – hyperpolarizaci.
- Opačný případ nastává při relativním přílivu iontů – Hypopolarizace.

Membrána v klidovém stavu je relativně nepropustná pro ionty Na+, zatímco pro ionty K+ zůstává propustná. Když je tedy membrána v klidu, bude mít tendenci odtékat ionty K+ z buňky po jejím koncentračním gradientu a zanechávat za sebou přebytečný záporný náboj. To pokračuje tak dlouho, dokud se chemický koncentrační gradient, který vytlačuje K+ z buňky, nedostane přesně do bodu, kdy je vyrovnán rozdílem elektrických potenciálů, který vzniká tímto výtokem. (membránový potenciál) K+ je pak vtahován zpět do buňky.
Tento ustálený stav membrány se nazývá rovnovážný potenciál.
Rovnice pro odvození rovnovážného potenciálu se nazývá Nernstova rovnice.
V axonech je ve skutečnosti mírně neočekávaně zvýšený kladný náboj v důsledku malé propustnosti membrány pro ionty Na+ v klidovém stavu. To je kompenzováno ATP závislou Na+/K+ výměnnou pumpou. Vypumpuje 3 ionty Na+ na každé 3 ionty K+ přivedené do buňky. Ke klidovému membránovému potenciálu buňky však přispívá jen nepatrně.
Akční potenciál
Definován jako „jednotlivý elektrický impuls procházející axonem“.
V jeho působení je všechno nebo nic. To znamená, že jakmile je dosaženo prahové intenzity podnětu, vznikne akční potenciál.
Informace v nervové soustavě jsou kódovány a interpretovány podle frekvence výboje, nikoli podle velikosti akčního potenciálu.
Prahová intenzita podnětu: Hodnota, při které je čistý vstupní proud(určovaný ionty Na+) právě větší než čistý výstupní proud (přenášený ionty K+). Obvykle je to -55 mV (kritický práh vypálení)
K AP nejsnáze dochází na axonálním pahorku, protože zde je větší hustota Na+ iontových kanálů. Právě z tohoto důvodu je toto místo místem iniciace AP v neuronu.
Pokud není dosaženo prahu, akční potenciál se nevytvoří a přenos signálu je v tomto místě ukončen.
Sekvence událostí pro vznik akčního potenciálu
- Depolarizační napětí aktivuje napěťově citlivé Na+ iontové kanály v membráně neuronu: Na+ ionty proudí po elektrochemickém gradientu dolů. Membrána se dále depolarizuje. Další Na+ kanály se otevírají ve smyčce pozitivní zpětné vazby. Když je větší vstupní proud sodíkových iontů ve srovnání s odtokem K+ iontů, dochází k rychlému otevření všech Na+ kanálů. Tím se membrána depolarizuje směrem k rovnovážnému potenciálu pro Na+ (+55 mV). Vzniká hrot AP, který však nedosáhne rovnovážného potenciálu pro Na+ v důsledku rostoucího výtoku K+.
- Když jsou Na+ kanály méně aktivní, AP klesá. Tato inaktivace je závislá na napětí. Během klesající fáze je důležitý proud K+, protože vede ke krátkému období hyperpolarizace membrány, než se deaktivuje.
- Membránový potenciál se vrací do klidového stavu.
Neuromuskulární spojení / synapse
Synapse
Synapse je spojení dvou neuronů. V nervové soustavě převažuje chemická synapse, elektrické synapse se však vyskytují v srdečním svalu a gliových buňkách.
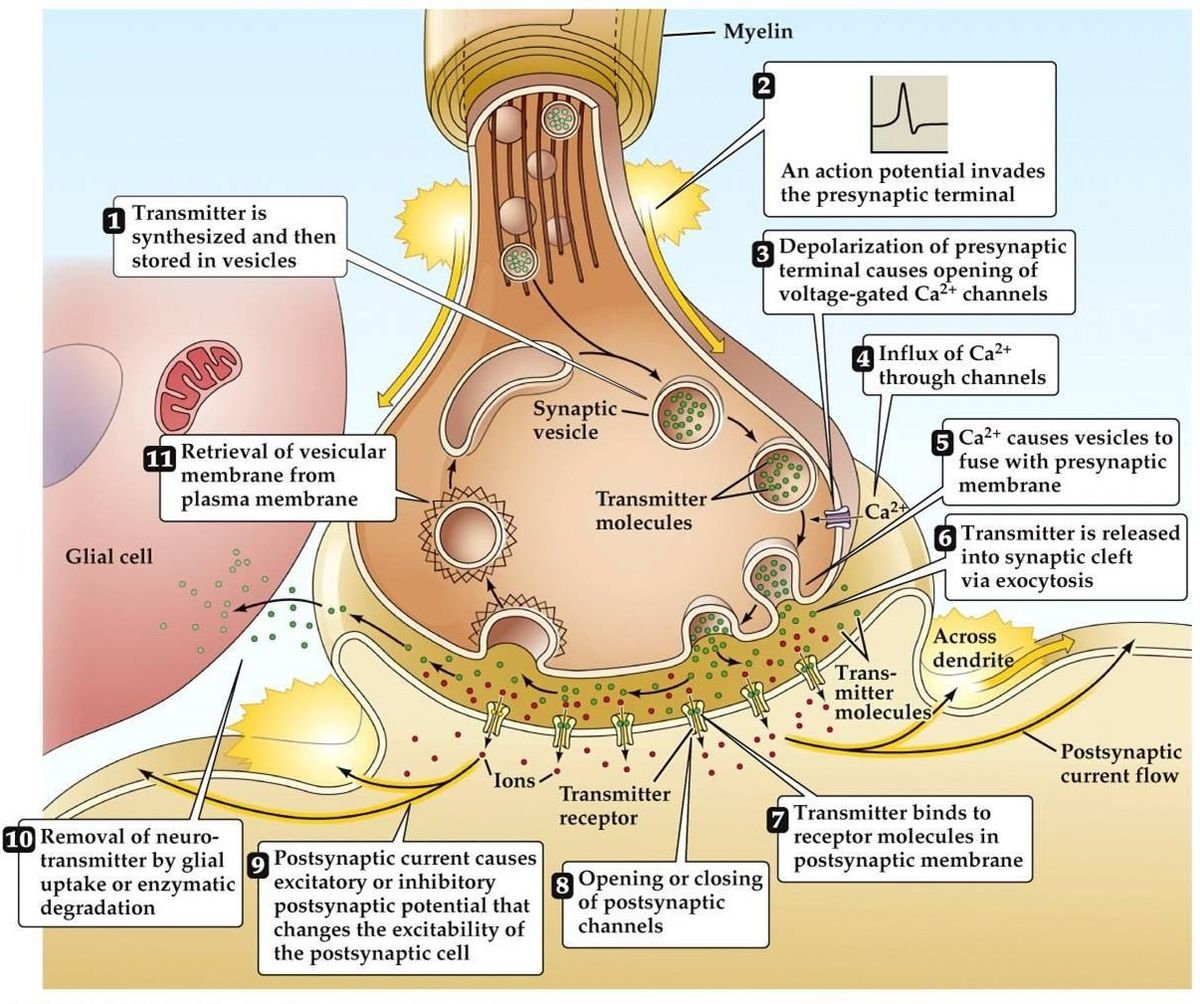
Synaptický přenos
- Příchod akčního potenciálu vede k depolarizaci presynaptického terminálu. V aktivních zónách terminálu se otevřou napěťově závislé Ca2+ kanály. To vede k influxu Ca2+.
- Příliv Ca2+ vede k fosforylaci a změně množství presynaptických proteinů vázajících vápník. Tím se vezikula uvolní z presynaptické aktinové sítě, Poté se naváže na presynaptickou membránu.
- Spojení vezikuly s membránou vede k vytvoření malého kanálu, který se rychle rozšíří a uvolní svůj obsah do synaptické štěrbiny. Membrána vezikuly je recyklována endocytózou.
- Uvolněný neurotransmiter difunduje přes synaptickou štěrbinu s cílem navázat se na postsynaptický receptor.
- Aktivace postsynaptického receptoru vede ke změně postsynaptického membránového potenciálu.
- Existují alternativní teorie, které předpokládají, že neurotransmiter je dodáván spíše prostřednictvím molekul nebo membránových kanálů než vezikul.
Nervové vedení
Šíření akčního potenciálu je dosaženo lokálním šířením proudu.
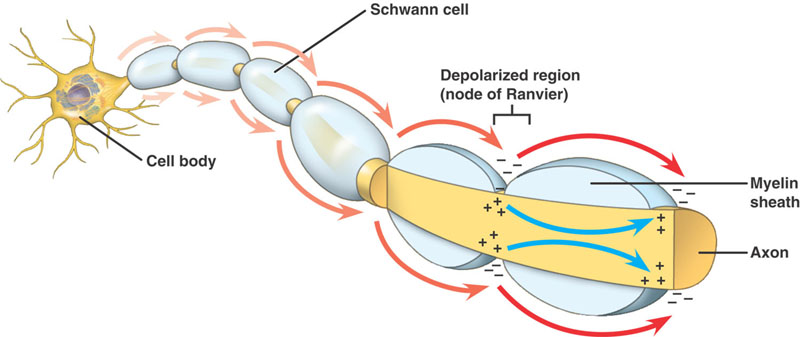
Nerv je izolován myelinem, pokud jeho velikost přesahuje určitý průměr, s Ranvierovými uzly v různých intervalech po jeho délce.
Nemyelinizované axony
Akční potenciál vede k depolarizaci membrány bezprostředně před ní (a za ní). Membrána je v refrakterním stavu, takže akční potenciál je veden pouze 1 směrem. To je možné u malých axonů, ale šíření proudu je pomalé.
Myelinizované axony
Stejný sled událostí jako u nemyelinizovaných axonů. Je zde však významný rozdíl. Postupující akční potenciál narazí na strukturu s vysokým odporem a nízkou kapacitou – myelin ovinutý kolem axonu. Depolarizující proud prochází podél axoplazmy, až dosáhne Ranvierova uzlu s nízkým odporem a velkým množstvím Na+ kanálů. V tomto místě pak vzniká akční potenciál. Akční potenciál je veden od uzlu k uzlu. Tento proces se nazývá slaná vodivost.
Výhody myelinizace
- Umožňuje rychlé vedení akčního potenciálu
- Minimalizuje metabolické nároky na buňku.
- Zvyšuje kapacitu balení NS, což umožňuje vtěsnat více vláken do 1 nervu.
Většina nervů větších než 1 mikron je myelinizovaná.
Narušení vedení je obvykle způsobeno patologickými stavy demyelinizace. Patří k nim Guillan Barreho syndrom a roztroušená skleróza.
Postsynaptická integrace:
Každý centrální neuron přijímá mnoho set synapsí. Každý z těchto vstupů je poté integrován do odpovědi daného neuronu. To zahrnuje zpracování všech vstupů, které přicházejí v daném okamžiku. Tomu se říká prostorová sumace. Zpracování vstupů za určité časové období se nazývá časová sumace. V tomto bodě bude působit směs excitačních a inhibičních synapsí.
Excitační postsynaptické potenciály
- Vazba neurotransmiteru vede k otevření iontových kanálů.
- V postsynaptickém procesu dochází k přílivu kationtů
- Dochází k depolarizaci membrány.
- EPSP depolarizace zaznamenané v postsynaptické buňce na určitý excitační podnět.
- Depolarizace spojené s EPSPs mohou dále vyvolat AP, pokud v synapsích dochází k sumarizaci.
Inhibiční postsynaptické potenciály
- Iontové kanály umožňují při otevření postsynaptický influx aniontů.
- Dochází k hyperpolarizaci membrány v důsledku influxu CL- a efluxu K+
- důležité pro modulaci odpovědi neuronů na excitační vstup na synapsích.
- Nalézá se ve strategicky důležitých místech neuronu, jako je proximální dendrit a soma.
- Mají velký vliv na dendritický strom
- Některé neurony zajišťují vlastní inhibiční vliv tím, že mají axonové kolaterály a vlastní inhibiční interneurony. To se označuje jako zpětnovazební inhibice. Např. motorneurony a Renshawovy buňky v míše.
Neurotransmitery, receptory a dráhy
Neurotransmiter se uvolňuje v synapsích a spolupracuje se specifickou bílkovinou v postsynaptické membráně zvanou receptor. V některých synapsích může neurotransmiter také interagovat s presynaptickým autoreceptorem. PSA působí jako regulátor množství uvolňovaného transmiteru.
Receptory jsou obvykle specifické pro určitý neurotransmiter. Existuje několik typů receptorů. Současně uvolňované neurotransmitery mohou regulovat vazbu jiného transmiteru.
Receptory pro specifické neurotransmitery mohou být buď přímo spojeny s iontovými kanály, nebo s membránovým enzymem, kdy vazba neurotransmiteru na receptor buď otevírá iontový kanál prostřednictvím intracelulární enzymové kaskády, nebo nepřímo moduluje pravděpodobnost otevření jiných iontových kanálů v reakci na změny napětí. (neuromodulace)
Aktivovaný receptor se může vrátit do klidového stavu až poté, co je neurotransmiter odstraněn procesem enzymatické hydrolýzy (vychytávání) do presynaptického nervového zakončení nebo do blízkých gliových buněk.
Desenzitizace/snížená regulace: Snížení afinity receptoru k transmiteru v krátkodobém horizontu, v dlouhodobém horizontu to vede ke snížení počtu receptorů.
Supersenzitivita/Zvýšená regulace: Zvýšená afinita receptoru k transmiteru v krátkodobém horizontu může v dlouhodobém horizontu vést ke zvýšení počtu kanálů.
Receptory:
- Ionotropní: N-methyl-D-aspartát(NMDA)
- Non NMDA.
- Metabotropní : glutamátové receptory spojené s G-proteinem, které reagují spuštěním intracelulárních biochemických dějů a modulují synaptický přenos
Existuje velké množství neurotransmiterů:
- Excitační aminokyseliny: Jedná se o hlavní excitační NT v CNS. Hlavním NT v této skupině je glutamát, který působí na řadu receptorů.
- Inhibiční aminokyseliny: Jedná se o hlavní inhibiční neurotransmitery, z nichž hlavní je GABA, přítomná v celém CNS. Glycin, který se nachází hlavně v míše.
- Monoaminy: Nacházejí se v malých skupinách neuronů v mozkovém kmeni, vystupují široce do CNS. Nacházejí se v autonomním NS. Vážou se na řadu receptorů.
- Acetylcholin: Široce rozšířen v celém nervovém systému, včetně nervosvalového spojení a autonomního NS.
- Neuropeptidy: Nacházejí se v celém NS. Často se uvolňují současně s jinými NS.
Kromě toho bylo nalezeno více než 50 neuroaktivních peptidů a pravidelně jsou objevovány nové. Mnohé z nich jsou „spoluuvolňovány“ spolu s malomolekulárním transmiterem. Nicméně v některých případech je peptid primárním transmiterem v synapsích. Poměrně známým příkladem peptidového neurotransmiteru je β-endorfin, protože vstupuje do vysoce specifických interakcí s opioidními receptory v centrálním nervovém systému.
Někteří považují za neurotransmitery také jednotlivé ionty (například synapticky uvolňovaný zinek) a některé plynné molekuly, například oxid dusnatý (NO), oxid uhelnatý (CO) a sirovodík (H2S). Tyto plyny vznikají v nervové cytoplazmě a okamžitě difundují přes buněčnou membránu do extracelulární tekutiny a do okolních buněk, kde stimulují produkci druhých poslů. Rozpustné plynné neurotransmitery je obtížné studovat, protože působí rychle a okamžitě se rozkládají, existují jen několik sekund.
Nejrozšířenějším přenašečem je glutamát, který působí excitačně na více než 90 % synapsí v lidském mozku. Dalším nejrozšířenějším je kyselina gama-aminomáselná neboli GABA, která je inhibiční na více než 90 % synapsí, které nepoužívají glutamát. Ačkoli se jiné transmitery používají v menším počtu synapsí, mohou být funkčně velmi důležité: velká většina psychoaktivních drog uplatňuje své účinky změnou působení některých neurotransmiterových systémů, často působících prostřednictvím jiných transmiterů než glutamátu nebo GABA. Návykové látky, jako je kokain a amfetaminy, uplatňují své účinky především na dopaminový systém. Návykové opiáty uplatňují své účinky především jako funkční analogy opioidních peptidů, které zase regulují hladiny dopaminu.