Original Editor – Joanne Garvey and Naomi O’Reilly
Top Contributors – Joanne Garvey, Lucinda hampton, Rachael Lowe, Naomi O’Reilly and Tarina van der Stockt
Introduzione
Neurofisiologia è la branca della fisiologia che si occupa delle funzioni del sistema nervoso. Cioè lo studio delle proprietà funzionali dei neuroni, della glia e delle reti.
- Storicamente è stata dominata dall’elettrofisiologia – la registrazione elettrica degli eventi neuronali che vanno dal molare (l’elettroencefalogramma, EEG) al cellulare (registrazione intracellulare delle proprietà dei singoli neuroni).
- Poiché il neurone è una macchina elettrochimica, è impossibile separare gli eventi elettrici dai processi biochimici e molecolari che li determinano.
- I neurofisiologi oggi usano tecniche della chimica (imaging del calcio), della fisica (risonanza magnetica funzionale, fMRI) e della biologia molecolare (mutazioni site directed) per studiare la funzione del cervello.
Di seguito imparerai tutto su
- Canali ionici
- Membrana a riposo e potenziale d’azione
- Giunzione neuromuscolare / Sinapsi
- Conduzione nervosa
- Neurotrasmettitori, Recettori e percorsi
Canali ionici
Un canale ionico è una macromolecola proteica che attraversa la larghezza di una membrana e permette il passaggio di molecole. Gli ioni si muovono in una direzione determinata dal gradiente elettrochimico attraverso la membrana.
- Gli ioni tendono a fluire da una zona di alta concentrazione a una zona di bassa concentrazione.
- In presenza di un gradiente di tensione, ci può essere nessun flusso di ioni nonostante le concentrazioni disuguali.
- I canali ionici possono essere aperti o chiusi.
- L’apertura si ottiene cambiando la tensione attraverso la membrana, o legando una sostanza chimica ad un recettore.
- Il ruolo più importante è quello di fornire al neurone l’eccitabilità elettrica.
- Si trovano in tutte le parti del neurone e in misura minore nelle cellule neurogliali.
Tipi di canali
- Voltage Gated
- Attivati chimicamente
- Tensione meccanica/Pressione.
Proprietà fondamentali di un canale ionico
- E’ composto da un certo numero di subunità proteiche, che si trovano attraverso la membrana, permettendo agli ioni di passare da una parte all’altra. (Poro transmembrana)
- Il canale deve essere in grado di passare dallo stato aperto a quello chiuso, e viceversa.
- Deve essere in grado di aprirsi in risposta agli stimoli appropriati.
Alcuni canali rispondono a stimoli chimici (in particolare alla sinapsi). Questi canali hanno recettori specifici per quella sostanza chimica, che porta all’apertura del canale.
Membrana a riposo e potenziale d’azione
- Nello stato di riposo, la membrana cellulare neuronale è abbastanza impermeabile agli ioni. Questo è cruciale per la generazione del potenziale di membrana a riposo.
- Il principale ione intracellulare è il potassio (è il sodio nel liquido extracellulare).
- Il flusso naturale degli ioni attraverso i loro gradienti di concentrazione è per K+ di lasciare la cellula e Na+ di entrare.
- Questo movimento di ioni fuori dalla cellula porta ad un potenziale di membrana negativo – iperpolarizzazione.
- Il contrario è vero per un relativo afflusso di ioni – Ipopolarizzazione.

La membrana a riposo è relativamente impermeabile agli ioni Na+, mentre rimane permeabile agli ioni K+. Così, quando la membrana è a riposo, ci sarà un efflusso di ioni K+ fuori dalla cellula, lungo il suo gradiente di concentrazione, lasciando dietro di sé un eccesso di carica negativa. Questo continua fino a quando il gradiente di concentrazione chimica che sta spingendo fuori il K+ dalla cellula è esattamente al punto in cui è compensato dalla differenza di potenziale elettrico generato da questo efflusso. (il potenziale di membrana) Il K+ viene quindi richiamato nella cellula.
Questo stato stazionario della membrana è chiamato il potenziale di equilibrio.
L’equazione per derivare il potenziale di equilibrio è chiamata equazione di Nernst.
C’è in realtà un aumento di carica positiva leggermente inaspettato negli assoni dovuto a una piccola permeabilità agli ioni Na+ della membrana nello stato di riposo. Questo è compensato dalla pompa di scambio Na+/K+ dipendente dall’ATP. Pompa fuori 3 ioni Na+ per ogni 3 ioni K+ portati nella cellula. Tuttavia, dà solo un piccolo contributo al potenziale di membrana a riposo della cellula.
Potenziale d’azione
Definito come un “singolo impulso elettrico che passa lungo un assone”.
È tutto o niente nella sua azione. Ciò significa che una volta raggiunta l’intensità soglia dello stimolo, si genera un potenziale d’azione.
Le informazioni nel sistema nervoso sono codificate e interpretate dalla frequenza degli spari, non dalla dimensione del potenziale d’azione.
Intensità dello stimolo di soglia: Il valore al quale la corrente netta in entrata (determinata dagli ioni Na+) è appena superiore alla corrente netta in uscita (portata dagli ioni K+). È normalmente -55mV (soglia critica di accensione)
L’AP si verifica più facilmente alla collinetta dell’assone perché è lì che c’è una maggiore densità di canali ionici Na+. È per questa ragione che questo è il sito di inizio dell’AP nel neurone.
Se la soglia non viene raggiunta, il potenziale d’azione non viene generato e la trasmissione del segnale termina in quel punto.
Sequenza di eventi per la generazione di un potenziale d’azione
- La tensione depolarizzante attiva i canali ionici Na+ sensibili alla tensione nella membrana neuronale: Gli ioni Na+ scendono lungo il gradiente elettrochimico. La membrana si depolarizza ulteriormente. Altri canali Na+ si aprono in un ciclo di feedback positivo. Quando c’è una maggiore corrente in entrata di ioni sodio rispetto all’efflusso di ioni K+, c’è una rapida apertura di tutti i canali Na+. Questo depolarizza la membrana verso il potenziale di equilibrio per il Na+ (+55mV). Viene generato un picco di AP, ma non riesce a raggiungere l’equilibrio. potenziale di Na+ a causa dell’aumento dell’efflusso di K+.
- Come i canali Na+ diventano meno attivi, l’AP cade. Questa inattivazione è dipendente dal voltaggio. Durante la fase di caduta la corrente K+ è importante perché porta ad un breve periodo di iperpolarizzazione della membrana prima che si disattivi.
- Il potenziale di membrana ritorna allo stato di riposo.
Giunzione neuromuscolare / Sinapsi
Sinapsi
Una sinapsi è la giunzione di due neuroni. La sinapsi chimica è quella predominante nel sistema nervoso, tuttavia le sinapsi elettriche si trovano nel muscolo cardiaco e nelle cellule gliali.
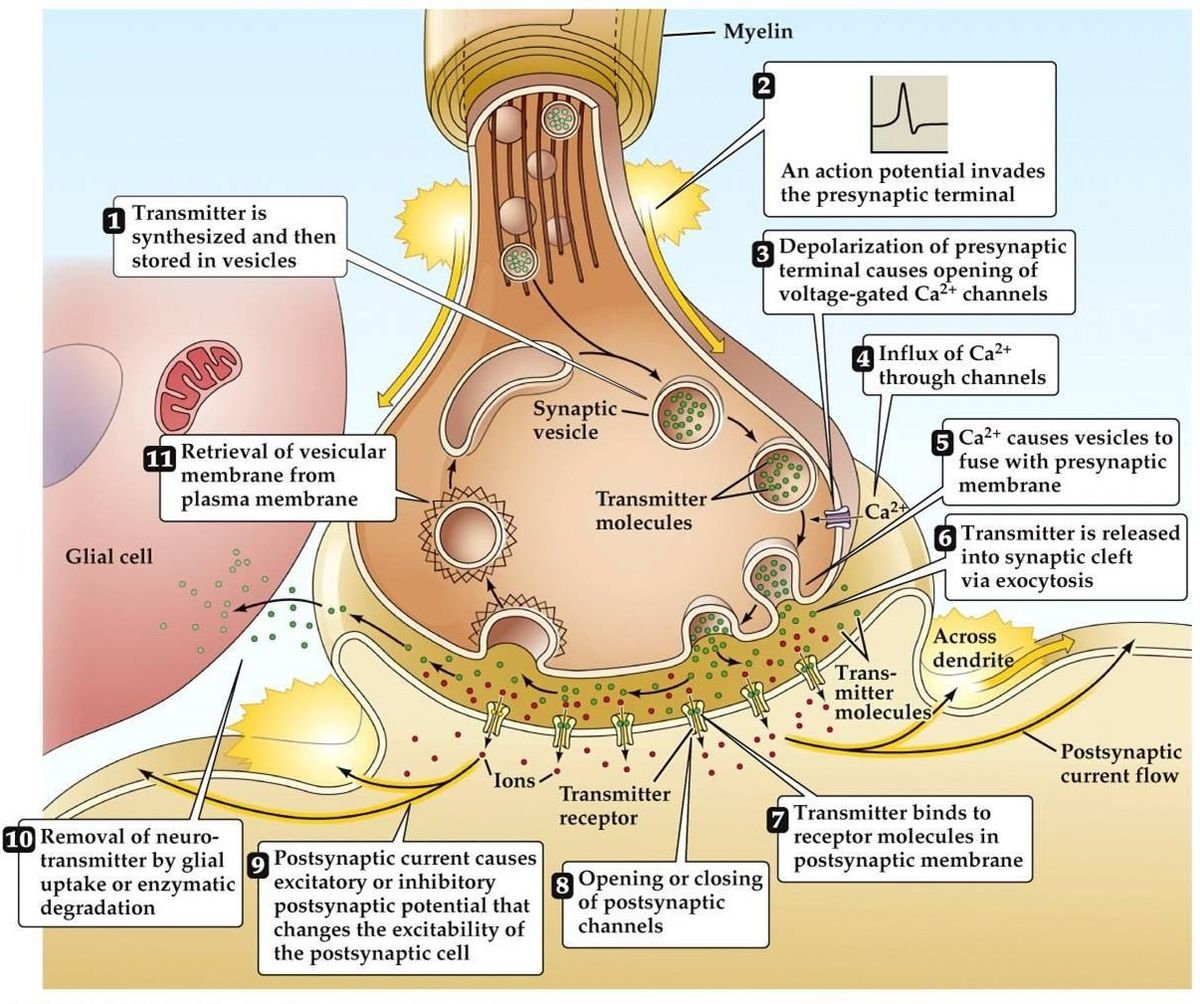
Trasmissione sinaptica
- Il potenziale d’azione arriva, porta alla depolarizzazione del terminale presinaptico. I canali Ca2+ dipendenti dalla tensione si aprono nelle zone attive del terminale. Questo porta all’afflusso di Ca2+.
- L’afflusso di Ca2+ porta alla fosforilazione e all’alterazione della quantità di proteine presinaptiche leganti il calcio. Questo libera la vescicola dalla sua rete di actina presinaptica, quindi si lega alla membrana presinaptica.
- La fusione della vescicola alla membrana porta alla formazione di un piccolo canale, che si espande rapidamente e rilascia il suo contenuto nella fessura sinaptica. La membrana della vescicola viene riciclata per endocitosi.
- Il neurotrasmettitore rilasciato si diffonde attraverso la fessura sinaptica con l’obiettivo di legarsi al recettore postsinaptico.
- L’attivazione del recettore postsinaptico porta a un cambiamento del potenziale di membrana postsinaptico.
- Ci sono teorie alternative che suggeriscono che il neurotrasmettitore è consegnato tramite molecole o canali di membrana piuttosto che vescicole.
Conduzione nervosa
La propagazione del potenziale d’azione è ottenuta tramite la diffusione locale della corrente.
Il nervo è isolato con mielina se le sue dimensioni superano un certo diametro, con i Nodi di Ranvier a vari intervalli sulla sua lunghezza.
Assi non mielinizzati
Il potenziale d’azione porta alla depolarizzazione della membrana immediatamente davanti (e dietro). La membrana è in uno stato refrattario, quindi il potenziale d’azione è condotto solo in 1 direzione. Questo è fattibile in piccoli assoni, ma la diffusione della corrente è lenta.
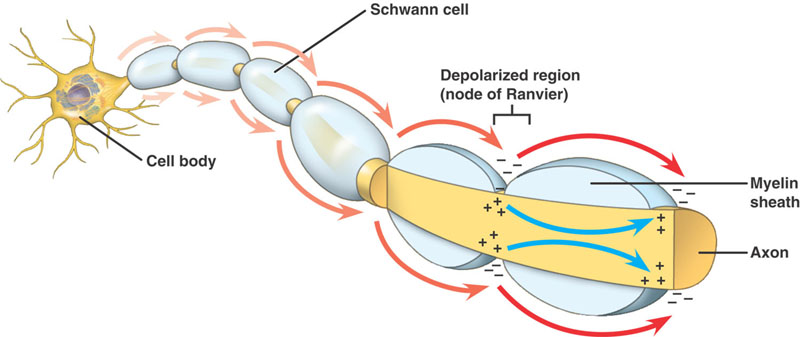
Assoni mielinizzati
Stessa sequenza di eventi come negli assoni non mielinizzati. C’è tuttavia una differenza significativa. Il potenziale d’azione che avanza incontra una struttura ad alta resistenza e bassa capacità – la mielina avvolta intorno all’assone. La corrente depolarizzante passa lungo l’assoplasma, fino a raggiungere il Nodo di Ranvier a bassa resistenza con la sua grande quantità di canali Na+. Il potenziale d’azione è quindi generato in questo sito. Il potenziale d’azione è condotto da nodo a nodo. Questa è chiamata conduzione saltatoria.
Vantaggi della mielinizzazione
- Consente una rapida conduzione del potenziale d’azione
- Minima richiesta metabolica alla cellula.
- Aumenta la capacità di impacchettamento dei NS, permettendo di stipare più fibre in un nervo.
La maggior parte dei nervi superiori a 1 micron sono mielinizzati.
I disturbi della conduzione sono normalmente dovuti a patologie di demielinizzazione. Essi comprendono la sindrome di Guillan Barre e la sclerosi multipla.
Integrazione postsinaptica:
Ogni neurone centrale riceve molte centinaia di sinapsi. Ognuno di questi input è poi integrato in una risposta da quel particolare neurone. Questo implica l’elaborazione di tutti gli input che arrivano in un dato momento. Questo è chiamato somma spaziale. L’elaborazione degli input in un determinato periodo di tempo è chiamata sommatoria temporale. Ci sarà un mix di sinapsi eccitatorie e inibitorie che agiscono in questo punto.
Potenziali postsinaptici eccitatori
- Il legame del neurotrasmettitore porta all’apertura dei canali ionici.
- C’è afflusso di cationi nel processo postsinaptico
- Si verifica la depolarizzazione della membrana.
- EPSPs depolarizzazioni registrate nella cellula post-sinaptica ad un particolare stimolo eccitatorio.
- Le depolarizzazioni associate agli EPSP possono continuare ad innescare gli AP se la somma si verifica nella sinapsi.
Potenziali postsinaptici inibitori
- I canali ionici permettono l’afflusso di anioni postsinaptici quando sono aperti.
- L’iperpolarizzazione della membrana avviene a causa dell’afflusso di CL- e dell’efflusso di K+
- importante per modulare la risposta dei neuroni all’input eccitatorio alla sinapsi.
- Si trova in siti strategicamente importanti del neurone come il dendrite prossimale e il soma.
- Hanno una grande influenza sull’albero dendritico
- Alcuni neuroni forniscono la propria influenza inibitoria avendo collaterali assonali e propri interneuroni inibitori. Questo è chiamato inibizione di ritorno. Per esempio, i motoneuroni e le cellule di Renshaw nel midollo spinale.
Neurotrasmettitori, recettori e vie
Il neurotrasmettitore è rilasciato nella sinapsi e lavora con una specifica proteina nella membrana postsinaptica chiamata recettore. In alcune sinapsi il neurotrasmettitore può anche interagire con un autorecettore presinaptico. Il PSA agisce come regolatore della quantità di trasmettitore rilasciato.
I recettori sono normalmente specifici per un particolare neurotrasmettitore. Esistono diversi tipi di recettori. I neurotrasmettitori co-rilasciati possono regolare il legame di un altro trasmettitore.
I recettori per neurotrasmettitori specifici possono essere accoppiati direttamente ai canali ionici o a un enzima di membrana dove il legame del neurotrasmettitore al recettore apre un canale ionico attraverso una cascata enzimatica intracellulare o modula indirettamente la probabilità di apertura di altri canali ionici in risposta ai cambiamenti di tensione. (neuromodulazione)
Il recettore attivato può ritornare al suo stato di riposo solo quando il neurotrasmettitore viene rimosso dal processo di idrolisi enzimatica (assorbimento) nel terminale nervoso presinaptico o nelle cellule gliali vicine.
Desensibilizzazione/Down regulation: Una diminuzione dell’affinità del recettore per il trasmettitore a breve termine, a lungo termine, questo porta a una diminuzione del numero di recettori.
Supersensibilità/Up regulation: Una maggiore affinità del recettore per il trasmettitore a breve termine può portare ad un aumento dei canali a lungo termine.
Ricettori:
- Ionotropi: N-metil-D-aspartato (NMDA)
- Non NMDA.
- Metabotropi: recettori del glutammato associati a proteine G che rispondono dando inizio a eventi biochimici intracellulari, modulando la trasmissione sinaptica.
C’è un gran numero di neurotrasmettitori:
- Aminoacidi eccitatori: Sono le principali NT eccitatorie del SNC. Il principale NT di questo gruppo è il glutammato che agisce su un certo numero di recettori.
- Aminoacidi inibitori: Questi sono i principali neurotrasmettitori inibitori, il principale dei quali è il GABA, presente in tutto il SNC. La glicina, presente soprattutto nel midollo spinale.
- Monoammine: Trovate in piccoli gruppi di neuroni nel tronco cerebrale, che proiettano ampiamente nel SNC. Si trovano nel NS autonomo. Si legano a una serie di recettori.
- Acetilcolina: Ampiamente distribuita in tutto il sistema nervoso, compresa la giunzione neuromuscolare e il NS autonomo.
- Neuropeptidi: Trovati in tutto il NS. Spesso rilasciati simultaneamente ad altri NT.
Inoltre, sono stati trovati più di 50 peptidi neuroattivi, e nuovi vengono scoperti regolarmente. Molti di questi sono “co-rilasciati” insieme a un trasmettitore a piccole molecole. Tuttavia, in alcuni casi un peptide è il trasmettitore primario in una sinapsi. La β-endorfina è un esempio relativamente noto di un neurotrasmettitore peptidico perché si impegna in interazioni altamente specifiche con i recettori oppioidi nel sistema nervoso centrale.
Singoli ioni (come lo zinco rilasciato sinapticamente) sono anche considerati neurotrasmettitori da alcuni, così come alcune molecole gassose come l’ossido nitrico (NO), il monossido di carbonio (CO) e il solfuro di idrogeno (H2S). I gas sono prodotti nel citoplasma neurale e sono immediatamente diffusi attraverso la membrana cellulare nel fluido extracellulare e nelle cellule vicine per stimolare la produzione di secondi messaggeri. I neurotrasmettitori gassosi solubili sono difficili da studiare, poiché agiscono rapidamente e vengono immediatamente scomposti, esistendo solo per pochi secondi.
Il trasmettitore più prevalente è il glutammato, che è eccitatorio in ben oltre il 90% delle sinapsi nel cervello umano. Il successivo più prevalente è l’acido gamma-amminobutirrico, o GABA, che è inibitorio in più del 90% delle sinapsi che non usano il glutammato. Anche se altri trasmettitori sono usati in meno sinapsi, possono essere molto importanti dal punto di vista funzionale: la grande maggioranza delle droghe psicoattive esercitano i loro effetti alterando le azioni di alcuni sistemi di neurotrasmettitori, spesso agendo attraverso trasmettitori diversi dal glutammato o dal GABA. Le droghe che creano dipendenza, come la cocaina e le anfetamine, esercitano i loro effetti principalmente sul sistema della dopamina. Le droghe che creano dipendenza da oppiacei esercitano i loro effetti principalmente come analoghi funzionali dei peptidi oppioidi, che, a loro volta, regolano i livelli di dopamina.