Editor Original – Joanne Garvey e Naomi O’Reilly
Top Contributors – Joanne Garvey, Lucinda hampton, Rachael Lowe, Naomi O’Reilly e Tarina van der Stockt
Introdução
Neurofisiologia é o ramo da fisiologia que lida com as funções do sistema nervoso. Ou seja, o estudo das propriedades funcionais dos neurônios, glia e redes.
- Historicamente tem sido dominado pela eletrofisiologia – o registro elétrico de eventos neuronais que vão desde o molar (o eletroencefalograma, EEG) até o celular (registro intracelular das propriedades de neurônios isolados).
- Como o neurônio é uma máquina eletroquímica, é impossível separar os eventos elétricos dos processos bioquímicos e moleculares que os originam.
- Neurofisiologistas hoje usam técnicas da química (imagem de cálcio), física (ressonância magnética funcional, fMRI), e biologia molecular (mutações dirigidas ao local) para estudar a função cerebral.
Below you will learn all about
- Canais de íons
- Membrana de repouso e potencial de ação
- Junção Neuromuscular / Sinapses
- Condução nervosa
- Neurotransmissores, Receptores e Caminhos
Canais de íons
Um canal de íons é uma macromolécula proteica que atravessa a largura de uma membrana e permite a passagem das moléculas. Os íons se movem em uma direção determinada pelo gradiente eletroquímico através da membrana.
- Os íons tendem a fluir de uma área de alta concentração para uma área de baixa concentração.
- Na presença de um gradiente de tensão, pode não haver fluxo de íons, apesar de concentrações desiguais.
- Os canais de íons podem ser abertos ou fechados.
- Abertura é provocada pela alteração da tensão através da membrana, ou ligando uma substância química a um receptor.
- O papel mais importante é que eles fornecem o neurônio com excitabilidade elétrica.
- Fundados em todas as partes do neurônio e em menor extensão nas células neurogliais.
Tipos de Canal
- Portões de Tensão
- Ativados quimicamente
- Estiramento/Pressão Mecânica.
Propriedades Fundamentais de um Canal de Iões
- É composto por um número de subunidades de proteínas, sentadas através da membrana, permitindo que os iões se cruzem de um lado para o outro. (Poro transmembrana)
- O canal deve ser capaz de se mover do estado aberto para o estado fechado, e para trás.
- Deve ser capaz de abrir em resposta aos estímulos apropriados.
Alguns canais respondem a estímulos químicos (particularmente na sinapse). Estes canais têm receptores específicos para aquele produto químico, o que leva à abertura do canal.
Membrana de repouso e potencial de ação
- No estado de repouso, a membrana da célula neuronal é bastante impermeável aos íons. Isto é crucial para a geração do potencial da membrana em repouso.
- O íon intracelular principal é o Potássio (É sódio no fluido extracelular).
- O fluxo natural de íons por meio de seus gradientes de concentração é para K+ deixar a célula e Na+ entrar.
- Este movimento de íons para fora da célula leva a um potencial negativo de membrana – Hiperpolarização.
- O contrário é verdadeiro para um relativo influxo de íons – Hipopolarização.

A membrana de repouso é relativamente impermeável aos íons Na+, enquanto permanece permeável aos íons K+. Assim, quando a membrana está em repouso, haverá uma tendência de efluxo de íons K+ para fora da célula, diminuindo seu gradiente de concentração, deixando para trás o excesso de carga negativa. Isto continua até que o gradiente de concentração química que está expulsando o K+ da célula esteja exatamente no ponto em que ele é compensado pela diferença de potencial elétrico gerado por este efluxo. (o potencial de membrana) K+ é então puxado de volta para dentro da célula.
Este estado estável da membrana é chamado de Potencial de Equilíbrio.
A equação para derivar o potencial de equilíbrio é chamada de equação de Nernst.
Existe na verdade uma carga positiva aumentada ligeiramente inesperada nos axônios devido a uma pequena permeabilidade aos íons Na+ da membrana no estado de repouso. Isto é compensado pela bomba de troca Na+/K+ dependente de ATP. Eu bombeio 3 íons Na+ para cada íons 3K+ trazidos para a célula. No entanto, ela contribui muito pouco para o potencial de repouso da membrana da célula.
Potencial de ação
Definido como um “único impulso elétrico passando por um axônio”.
É tudo ou nada na sua acção. Isto significa que uma vez atingida a intensidade do limiar de estímulo, será gerado um potencial de ação.
A informação no sistema nervoso é codificada e interpretada pela freqüência de disparo, não pelo tamanho do potencial de ação.
Intensidade do estímulo de limiar: O valor em que a corrente líquida interna (determinada por íons Na+) é apenas maior do que a corrente líquida externa (transportada por íons K+). É normalmente -55mV (limiar crítico de queima)
O PA ocorre mais prontamente na colina axon porque é onde há uma maior densidade de canais de íons Na+. É por esta razão que este é o local de iniciação do PA no neurônio.
Se o limiar não for atingido, o potencial de ação não será gerado, e a transmissão do sinal é terminada naquele ponto.
Sequência de eventos para um potencial de ação a ser gerado
- A tensão descorante ativa os canais de íons Na+ sensíveis à tensão na membrana neuronal: Os íons Na+ fluem pelo gradiente eletroquímico. A membrana é despolarizada ainda mais. Outros canais de Na+ abrem-se num laço de realimentação positiva. Quando há uma maior corrente interna de íons sódio em comparação com o efluxo de íons K+, há uma abertura rápida de todos os canais de Na+. Isto despolariza a membrana em direção ao potencial de equilíbrio para Na+(+55mV). O pico de AP é gerado, mas não alcança o potencial de equilíbrio. de Na+ devido ao aumento do efluxo de K+.
- As canais de Na+ tornam-se menos activos, o AP cai. Esta inactivação é dependente da tensão. Durante a fase de queda a corrente de K+ é importante pois leva a um curto período de hiperpolarização da membrana antes de ser desativada.
- Potencial de membrana retorna ao estado de repouso.
Junção Neuromuscular / Sinapses
Synapse
Uma sinapse é a junção de dois neurónios. A sinapse química é a predominante encontrada no sistema nervoso, porém as sinapses elétricas são encontradas no músculo cardíaco e nas células gliais.
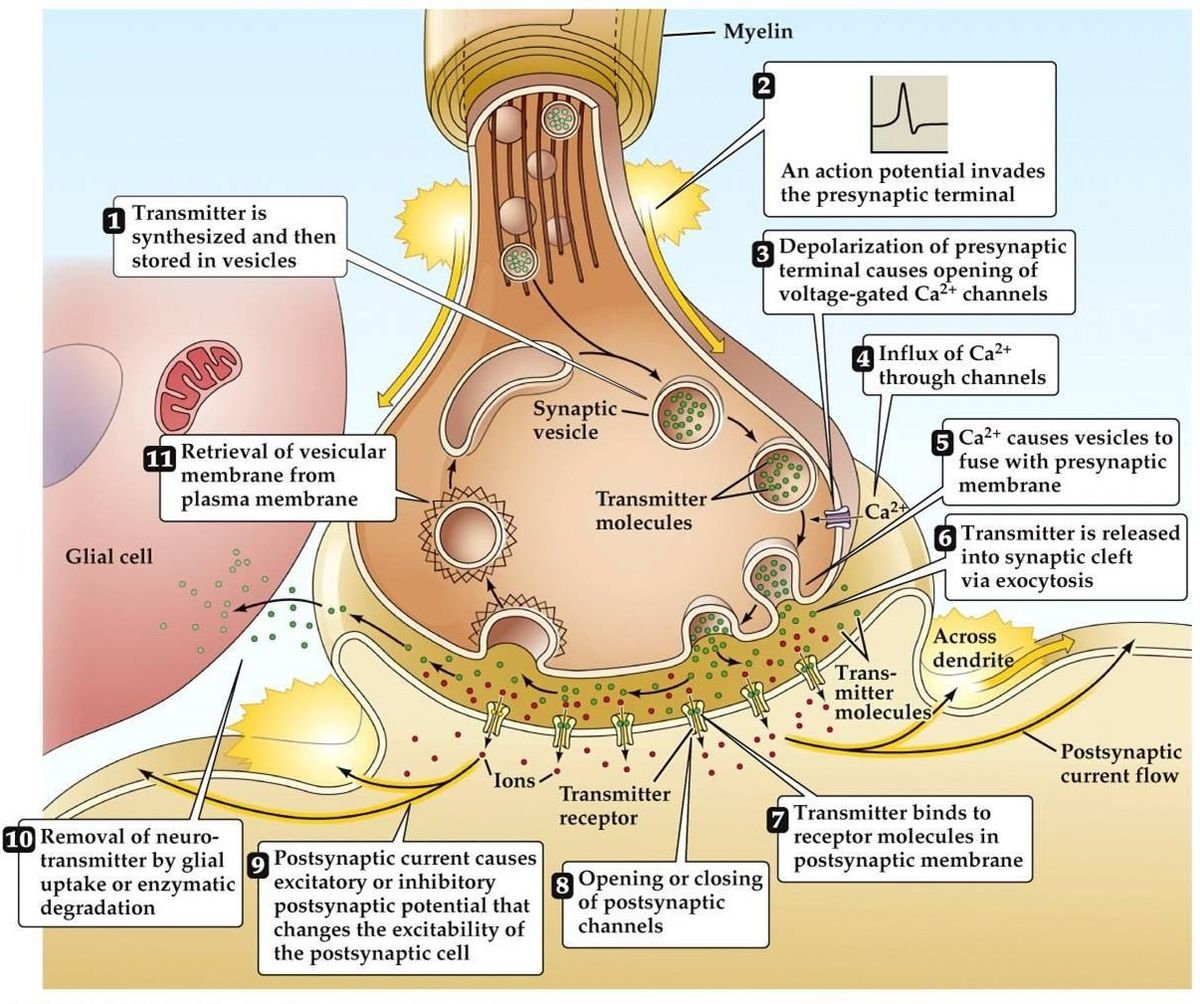
Transmissão sináptica
- Potencial de ação chega, leva à despolarização do terminal pré-sináptico. Canais Ca2+ dependentes da tensão abertos nas zonas activas do terminal. Isto leva ao influxo de Ca2+.
- Influxo de Ca2+ leva à fosforilação e à alteração da quantidade de proteínas de ligação ao cálcio pré-sináptico. Isto liberta a vesícula da sua rede de actina pré-sináptica, ligando-se depois à membrana pré-sináptica.
- A fusão da vesícula à membrana leva à formação de um pequeno canal, que se expande rapidamente e liberta o seu conteúdo para a fenda sináptica. A membrana da vesícula é reciclada por endocitose.
- Neurotransmissor liberado se difunde através da fenda sináptica com o objetivo de ligar-se ao receptor pós-sináptico.
- Ativação do receptor pós-sináptico leva a uma mudança no potencial da membrana pós-sináptica.
- Existem teorias alternativas que sugerem que o neurotransmissor é entregue através de moléculas ou canais de membrana em vez de vesículas.
Condução nervosa
A propagação do potencial de ação é alcançada pela propagação da corrente local.
O nervo é isolado com mielina se seu tamanho estiver acima de um certo diâmetro, com os Nodos de Ranvier em vários intervalos ao longo de seu comprimento.
Eixos não mielinizados
O potencial de ação leva à despolarização da membrana imediatamente à frente (e atrás). A membrana está em estado refratário, portanto o potencial de ação só é conduzido em 1 direção. Isto é viável em pequenos axônios, mas a propagação da corrente é lenta.
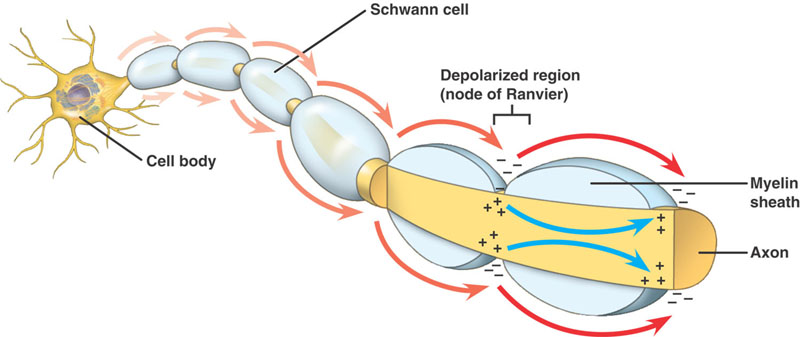
Eixos mielinizados
Sua sequência de eventos como nos eixos não mielinizados. Há, no entanto, uma diferença significativa. O potencial de ação em progresso encontra alta resistência, estrutura de baixa capacitância – mielina enrolada ao redor do axônio. A corrente despolarizante passa ao longo do axoplasma, até atingir o Nó de baixa resistência de Ranvier com a sua grande quantidade de canais de Na+. O potencial de ação é então gerado neste local. O potencial de ação é conduzido de nó a nó. Isto é chamado de Condução Salitatória.
Vantagens da mielinização
- Permite a condução rápida do potencial de ação
- Minimiza as demandas metabólicas sobre a célula.
- Aprimora a capacidade de empacotamento do NS, permitindo que mais fibras sejam amontoadas em 1 nervo.
Muitos nervos maiores que 1 mícron são mielinizados.
Perturbações na condução são normalmente devidas a patologias de desmielinização. Elas incluem síndrome de Guillan Barre e Esclerose múltipla.
Postsynaptic Integration:
Cada neurónio central recebe muitas centenas de sinapses. Cada uma dessas entradas é então integrada em uma resposta por aquele neurônio em particular. Isto envolve o processamento de todos os inputs que chegam a qualquer momento. Isto é chamado de soma espacial. O processamento de inputs durante um determinado período de tempo é chamado de soma temporal. Haverá uma mistura de sinapses excitatórias e inibitórias atuando neste ponto.
Potenciais pós-sinápticos excitatórios
- A ligação do neurotransmissor leva à abertura dos canais de íons.
- Existe influxo catiónico no processo pós-sináptico
- Depolarização da membrana ocorre.
- Existe despolarização de EPSPs registada na célula pós-sináptica para um determinado estímulo excitatório.
- As despolarizações associadas a EPSPs podem passar a disparar APs se a soma ocorrer na sinapse.
Potenciais pós-sinápticos inibidores
- Canais de íons permitem o influxo de anions pós-sinápticos quando abertos.
- Hiperpolarizações da membrana ocorrem devido ao influxo de CL- e efluxo de K+
- importante para modular a resposta dos neurónios à entrada excitatória na sinapse.
- Fundado em locais estrategicamente importantes do neurônio, como o dendrito proximal e o soma.
- Têm uma grande influência na árvore dendrítica
- Alguns neurónios fornecem a sua própria influência inibitória tendo axónios colaterais e os seus próprios interneurónios inibitórios. Isto é chamado de inibição de feedback. Ex. motorneurônios e células de Renshaw na medula espinhal.
Neurotransmissores, Receptores e Caminhos
O neurotransmissor é liberado na sinapse e funciona com uma proteína específica na membrana pós-sináptica chamada receptor. Em algumas sinapses o neurotransmissor pode também interagir com um autorreceptor pré-sináptico. O PSA age como um regulador da quantidade de transmissor liberada.
Receptores são normalmente específicos para um determinado neurotransmissor. Existem vários tipos de receptores. Os neurotransmissores co-lançados podem regular a ligação de outro transmissor.
Receptores para neurotransmissores específicos podem ser acoplados diretamente a canais iônicos ou a uma enzima de membrana onde a ligação do neurotransmissor ao receptor ou abre um canal iônico através de uma cascata de enzimas intracelulares ou modulando indiretamente a probabilidade de abertura de outros canais iônicos em resposta a mudanças de tensão. (neuromodulação)
O receptor ativado só pode retornar ao seu estado de repouso quando o neurotransmissor for removido pelo processo de hidrólise enzimática (captação) no terminal do nervo pré-sináptico ou nas células gliais próximas.
Dessensibilização/regulação para baixo: Uma diminuição da afinidade do receptor para o transmissor a curto prazo, a longo prazo, isto leva a uma diminuição no número de receptores.
Regulação da super-sensibilidade/regulação da potência: Um aumento da afinidade do receptor para o transmissor a curto prazo pode levar a um aumento dos canais a longo prazo.
Receptores:
- Ionotrópico: N-metil-D-aspartate(NMDA)
- Não NMDA.
- Metabotropic: receptores de glutamato associados à proteína G que respondem iniciando eventos bioquímicos intracelulares, modulando a transmissão sináptica.
Existe um grande número de Neurotransmissores:
- Aminoácidos Excitatórios: Estes são os principais TNs excitatórios no SNC. A TN principal neste grupo é o Glutamato, que atua em vários receptores.
- Aminoácidos inibitórios: Estes são os principais neurotransmissores inibitórios, o principal dos quais é GABA, presentes em todo o SNC. Glycine, encontrado principalmente na medula espinhal.
- Monoaminas: Encontrados em pequenos grupos de neurónios no tronco cerebral, projectando-se amplamente no SNC. Encontrada na NS autonómica. Ligam-se a um conjunto de receptores.
- Acetylcholine: Amplamente distribuída por todo o sistema nervoso, incluindo a junção neuromuscular e a NS autonómica.
- Neuropeptídeos: Encontrado em toda a NS. Muitas vezes liberados simultaneamente com outras NTs.
Além disso, mais de 50 peptídeos neuroativos foram encontrados, e novos são descobertos regularmente. Muitos destes são “co-lançados” juntamente com um transmissor de pequenas moléculas. No entanto, em alguns casos, um peptídeo é o principal transmissor de uma sinapse. β-endorphin é um exemplo relativamente bem conhecido de um neurotransmissor peptídeo porque ele se envolve em interações altamente específicas com receptores opióides no sistema nervoso central.
Iões únicos (como zinco sinapticamente liberado) também são considerados neurotransmissores por alguns, assim como algumas moléculas gasosas como óxido nítrico (NO), monóxido de carbono (CO), e sulfeto de hidrogênio (H2S). Os gases são produzidos no citoplasma neural e são imediatamente difundidos através da membrana celular no fluido extracelular e nas células próximas para estimular a produção de segundos mensageiros. Os neurotransmissores de gases solúveis são difíceis de estudar, pois agem rapidamente e são imediatamente decompostos, existindo por apenas alguns segundos.
O transmissor mais prevalente é o glutamato, que é excitatório em bem mais de 90% das sinapses do cérebro humano. O próximo mais prevalente é o ácido gama-aminobutírico, ou GABA, que é inibitório em mais de 90% das sinapses que não usam glutamato. Embora outros transmissores sejam usados em menos sinapses, eles podem ser muito importantes funcionalmente: a grande maioria das drogas psicoativas exercem seus efeitos alterando as ações de alguns sistemas neurotransmissores, muitas vezes agindo através de transmissores que não o glutamato ou GABA. As drogas viciantes como a cocaína e as anfetaminas exercem seus efeitos principalmente sobre o sistema dopaminérgico. As drogas opiáceas viciantes exercem seus efeitos principalmente como análogos funcionais de peptídeos opióides, que, por sua vez, regulam os níveis de dopamina.