Introduction
Recurrent respiratory papillomatosis (RRP) on krooninen sairaus, jonka aiheuttaa ihmisen papilloomavirus (HPV), yleensä tyypit 6 ja 11. RRP:n leesiot esiintyvät useimmiten kurkunpäässä (kuva 1), mutta niitä voi ilmaantua myös suuhun, henkitorveen, keuhkoputkiin, keuhkoparenkyymiin ja ruokatorveen. RRP:n nuoruusiän muoto, jossa oireet ilmenevät ennen 12 vuoden ikää, on aggressiivisempi kuin aikuisiän muoto, ja oireet ovat vaikeampia. Papilloomien uusiutuminen on erityisen nopeaa alle 3-vuotiailla lapsilla, joilla kirurgisten toimenpiteiden väli on lyhyempi ja leikkauksia tehdään siten enemmän. Todennäköisyys, että infektio leviää kurkunpään ulkopuolelle, ja henkitorven auki pitämiseksi tarvittavan trakeostomian esiintyvyys ovat myös suuremmat tässä väestössä (1). Potilaille, joilla on nuoruusiässä alkava RRP, tehdään keskimäärin 20 kirurgista toimenpidettä, joista suurin osa lapsuudessa (2).
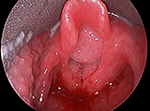
KUVIO 1. Potilaat, joilla on nuoruusiässä alkava RRP. Suora laryngoskooppinen kuva suurikokoisesta kookkaasta hengitystiepapillomatoosista, joka tukkii kurkunpään sisäänmenoaukon.
Perinteisessä kirurgisessa poistomenetelmässä käytettiin klassisesti KTP- (kaliumtitanyylifosfaatti) tai hiilidioksidilasereita (3). Ottaen huomioon laserablaation mahdolliset vakavat sivuvaikutukset, mukaan lukien hengitysteiden palovammat ja kurkunpään arpeutuminen, mikrodebridereistä on tullut yhä suositumpi kirurginen työkalu erityisesti lasten otolaryngologien keskuudessa, kun kyseessä on kookas tauti (3). Tällä käsikäyttöisellä laitteella voidaan poistaa sairastunut kudos tarkemmin ja vähentää ympäröivien kudosten vaurioita (3). Kun otetaan huomioon nuoruusiän RRP:n aggressiivinen luonne, poistoleikkaukset ovat kuitenkin edelleen yleisiä, ja ajan mittaan ne kuluttavat edelleen alla olevaa kudosta merkittävästi, ja arpien muodostuminen on yleistä. Tämän vuoksi on tutkittu useita lääkehoitoja, joilla pyritään parantamaan leikkaustulosta pidentämällä leikkausten välistä aikaa tai minimoimalla RRP-vaurioiden uusiutuminen.
Interferoni α
Interferoni α, proteiini, jota leukosyytit tuottavat reagoidessaan erilaisiin ärsykkeisiin, kuten virusinfektioon, oli yksi ensimmäisistä tutkituista mahdollisista lääkehoidoista (4). Sen arvo liitännäishoitona on kiistanalainen. Laajassa tutkimuksessa, johon osallistui 85 lasta ja 84 aikuista, 58 prosenttia lapsista lopetti vuoden kestäneen hoitojakson, jonka aikana heille annettiin lihaksensisäisiä interferoni α -injektioita kolme kertaa viikossa, ilman merkkejä RRP:stä (5). Papilloomien uusiutumistiheys väheni 74 prosentilla kaikista hoidetuista lapsista (5). Satunnaistetussa kontrollitutkimuksessa, johon osallistui 123 alle 21-vuotiasta potilasta, papilloomien kasvunopeuden hidastuminen koeryhmässä, joka sai interferoni α:n lihaksensisäisiä injektioita, ei kuitenkaan säilynyt vuoden mittaisen hoidon aikana (6). Samoin eräässä toisessa tutkimuksessa todettiin, että 20 vuotta interferoni α -hoidon päättymisen jälkeen vain 42 prosentilla potilaista oli pitkäaikainen hoitovaste, ja kaikilla uusiutuneilla potilailla oli RRP:n nuoruusiän muoto (7). Useimmissa interferoni α:ta tutkineissa tutkimuksissa on myös raportoitu vakavia sivuvaikutuksia, kuten neurologisia häiriöitä, leukopeniaa ja trombosytopeniaa (5). Näistä syistä sen käyttö lasten otolaryngologeilla on vähentynyt, eikä sitä yleensä suositella (1). Vuonna 2014 vain 4 % RRP:tä sairastavista lapsista sai interferoni α:ta liitännäishoitona (1).
Cidofoviiri
Tämä viruksen DNA-polymeraaseja estävä laajakirjoinen viruslääke on osoittautunut lupaavaksi RRP:n leikkauksen liitännäishoitona. Intralesionaliset tsidofoviiri-injektiot ovat yleisimmin käytetty RRP:n lääkehoito lasten otolaryngologien keskuudessa (1). Kaikissa vuosina 1998-2011 julkaistuissa artikkeleissa, joissa tutkittiin intralesionalisen tsidofoviirin tehoa, raportoitiin vähintään yksi taudin remissiotapaus (8). Koska useimmat näistä tutkimuksista ovat kuitenkin kontrolloimattomia tapaustutkimuksia, on epäselvää, johtuvatko hyödyt tsidofoviirista vai ovatko ne osa taudin luonnollista kulkua. Satunnaistetussa kontrolloidussa tutkimuksessa todettiin, että papillooman vaikeusasteessa tai terveyteen liittyvässä elämänlaadussa ei ollut tilastollisesti merkitseviä eroja kontrolliryhmän, jota hoidettiin tarpeen mukaan kirurgisilla toimenpiteillä ja suolaliuoksen intralesionaalisilla injektioilla, ja koeryhmän, jota hoidettiin leikkauksella ja intralesionaalisella Cidofoviirilla, välillä 12 kuukauden hoidon jälkeen (9). Molemmissa ryhmissä taudin vakavuus väheni merkittävästi vuoden aikana, mikä osoittaa, että tauti voi taantua ajan myötä itsestään (9). Toisessa katsauksessa, jossa tarkasteltiin 27:ää tsidofoviirin antoa koskevaa tutkimusta, jotka kaikki julkaistiin ennen vuotta 2011, todettiin, että keskimääräinen täydellinen remissioaste tsidofoviirilla oli 37 % pediatrisissa tutkimuksissa (10). Sidofoviiriin on liittynyt myös joitakin vakavia sivuvaikutuksia, sillä katsauksessa todettiin, että 447 RRP-potilaasta 1,7 prosentilla ilmeni pahanlaatuinen muutos ja 1 prosentilla nefrotoksisuutta (8). Muita haittavaikutuksia ovat ihottuma, päänsärky ja äänihuulten arpeutuminen (11). Kun otetaan huomioon nämä mahdolliset komplikaatiot ja se, että annostusta tai antotiheyttä koskevaa hyväksyttyä protokollaa ei ole, tämä lääke ei ole luotettava adjuvantti (4).
Kidofoviiriä on myös annettu systeemisenä eikä paikallishoitona RRP-tapauksissa, joihin liittyy keuhkosairaus. Neljä yksittäistapaustutkimusta on osoittanut, että laskimonsisäinen tsidofoviiri johti taudin remissioon, mikä ei ole taudin normaali eteneminen keuhkojen osallistuessa (11). Kaikissa näissä tutkimuksissa käytettiin hyperhydraatiota ja probenesidiä, virtsahapon vähentäjää, nefrotoksisuuden mahdollisuuksien vähentämiseksi (11). Vain yhdellä potilaalla ilmeni sivuvaikutuksia, osittaista hiustenlähtöä ja leukopeniaa, tsidofoviirin ja interferonin yhdistelmähoidosta (12). Molempien lääkkeiden annoksia pienennettiin tämän seurauksena. Kahdeksantoista kuukauden kuluttua hoidon päättymisestä potilas oli tarvinnut leikkausta RRP:n vuoksi vain kerran, ja hänen keuhkosairautensa oli vakiintunut (12).
Tidofoviirin uusi antotapa on inhalaatio. Tämän menetelmän tehoa on tutkittu vain harvoissa tutkimuksissa, mutta se voi olla lupaava potilaille, jotka eivät ole vastanneet muihin hoitomuotoihin, kuten 4 kuukauden ikäiselle pojalle, jonka oireet pahenivat kahden viikon välein suoritettavista mikrohoidoista ja intralesionalisista Cidofoviiri- ja laskimonsisäisistä interferoni α -injektioista huolimatta (13). Kuusi viikkoa kestäneen 40 mg:n sumutetun Cidofoviirin päivittäisen annostelun (12 päivää ja 2 päivää pois) jälkeen poistojen välinen aika pidentyi (13). Kuusi kuukautta myöhemmin potilaalla ei ollut enää oireita (13). Yhteenvetona voidaan todeta, että vaikka tsidofoviiria eri antomuotoina käytetään edelleen laajalti, sen hoitotulokset ovat parhaimmillaankin vaihtelevia ja sen mahdolliset haittavaikutukset jonkin verran rajoittavia.
Fotodynaaminen hoito
Fotodynaamisessa hoidossa (PDT) valoherkkää ainetta, jota kutsutaan valoherkistimeksi, syötetään suun kautta tai injektion avulla sairaaseen kudokseen ja aktivoidaan aine laservalolla nekroosin aikaansaamiseksi. Yksi PDT:n suurimmista eduista on kyky tuhota kasvaimia vaikuttamatta ympäröivään kudokseen (4). Tapaustutkimukset ovat osoittaneet, että papilloomien uusiutumisnopeus on huomattavasti hitaampi pian adjuvantti- tai erillishoitona annetun PDT:n jälkeen, ja joissakin tapauksissa tautia ei ole esiintynyt useiden viikkojen kuluttua (14, 15). PDT:n vaikutusta on tutkittu vain muutamissa satunnaistetuissa kontrollikokeissa, mutta viimeisimmässä todettiin, että tauti uusiutuu 3-5 vuoden kuluttua, mikä johtuu todennäköisesti siitä, että PDT tuottaa vaikutuksensa lyhytaikaisen immuunivasteen kautta (16). Lisätutkimuksia olisi tehtävä sen tehokkuuden ja turvallisuuden selvittämiseksi.
Indoli-3-karbinoli
Suurina pitoisuuksina ristikukkaisissa vihanneksissa, kuten parsakaalissa ja kaalissa, esiintyvä indoli-3-karbinoli muuttaa estrogeenimetaboliaa muuttaakseen solujen proliferaatiota ja DNA-synteesiä. Viimeisimmässä kliinisessä tutkimuksessa todettiin, että kun indoli-3-karbinolia oli otettu kahdesti päivässä 200 mg:n annoksella aikuisille ja painon mukaan määräytyvällä annoksella lapsille keskimäärin 50,2 kuukauden ajan, 70 %:lla tutkittavista saavutettiin joko täydellinen tai osittainen vaste (17). Pediatrisista potilaista yksi sai täydellisen vasteen, kolme osittaisen vasteen ja viisi ei saanut vastetta lainkaan (17). On epäselvää, miksi aikuispotilaat vastasivat indoli-3-karbinoliin paremmin kuin lapsipotilaat. Aikuisten RRP:n vähemmän aggressiivinen luonne voi olla yksi tekijä. Koska tulokset pediatrisessa populaatiossa eivät ole olleet lupaavia, nuoruusiän RRP:n hoitoa indoli-3-karbinolilla ei ole juurikaan tutkittu.
Telekoksibi
Telekoksibi on tulehduskipulääke, joka estää tulehdusta ja kipua aiheuttavaa entsyymiä syklooksygenaasi-2:ta (COX-2), ja sitä käytetään yleisesti niveltulehduksen hoitoon. In vitro -tutkimukset ovat osoittaneet, että papilloomasolut yliekspressoivat COX-2:ta lisääntyneen epidermaalisen kasvutekijäreseptorin (EGFR) signaloinnin seurauksena ja että tämä aktiivisuus on tärkeää niiden kasvun kannalta (18). Selloksibin ja EGFR-kinaasin estäjän, erlotinibin, yhdistelmähoito auttoi hallitsemaan etenevää RRP:tä 58-vuotiaalla miehellä hidastamalla papillooman kasvua ja tekemällä lisäleikkaukset tarpeettomiksi (19). Northwell Healthin sponsoroimassa meneillään olevassa satunnaistetussa kontrollitutkimuksessa pyritään selvittämään, voiko celecoxib vähentää papillooman uusiutumisnopeutta sekä aikuis- että lapsipotilailla (4).
Refluksilääkitys
Tapaustutkimukset ovat osoittaneet, että gastroesofageaalisen refluksitaudin (GERD) hoitaminen refluksilääkkeellä potilailla, joilla on nuoruusiän RRP, voi auttaa hidastamaan papillooman uusiutumisnopeutta (20, 21). Yhdessä tutkimuksessa potilaat, jotka eivät noudattaneet GERD-hoitoa, sairastuivat uusiutumiseen (20). Retrospektiivinen karttatarkastelu osoitti myös, että RRP:n vuoksi hoidetuille lapsipotilaille, joita ei hoidettu refluksin vuoksi, kehittyi huomattavasti todennäköisemmin kurkunpään verkkoja papillooman kirurgisen poiston jälkeen (22). Vaikka ei ole yksiselitteistä näyttöä siitä, että GERD pahentaa RRP:tä, sen hoitaminen on järkevää niiden potilaiden kohdalla, joilla on GERD:n kliininen oirekuva ja monimutkaisia, eteneviä RRP-tapauksia (23).
Lämpösokkiproteiini
Joista 700:sta RRP:tä sairastavasta lapsesta, joita oli hoitanut 74 lasten korvatulehduslääkäriä, jotka tekivät kyselytutkimuksen adjuvanttihoidon käytöstä, 11 potilasta sai HSP-E7:ää, joka on lämpösokkiproteiini 65:stä (Heat Shock Protein 65, Hsp65) ja HPV:n tyypin 16 E7-proteiinista koostuva rekombinanttinen fuusioproteiini (1). HSP-E7:ää on tutkittu hoitona useissa HPV:stä johtuvissa sairauksissa, kuten sukupuolielinten syylien ja intraepiteliaalisen neoplasian hoidossa (24). Todisteet viittaavat siihen, että se saattaa reagoida useampia HPV-kantoja kuin vain HPV 16:ta vastaan (24). Avoimessa tutkimuksessa, johon osallistui 27 pediatrista RRP-potilasta, HSP-E7-hoidon jälkeinen leikkausväli pidentyi merkittävästi hoitoa edeltävään mediaaniin verrattuna (24). Komplikaatioita esiintyi vähän, ainoastaan lieviä tai kohtalaisia injektiokohdan reaktioita. Vaikka meneillään ei ole kliinisiä tutkimuksia, joissa tutkittaisiin Hsp-E7:n tehoa, se on lupaava hoitomuoto.
HPV-rokote
Muutamissa tapausraporteissa ja tutkimuksissa on dokumentoitu HPV-rokotteen käyttöä adjuvanttihoitona. Tällä hetkellä on kolme hyväksyttyä HPV-rokotetta: bivalentti Cervarix, tetravalentti Gardasil ja nonvalentti Gardasil 9. Tetravalentin rokotteen kohteena ovat HPV-6, HPV-11, HPV-16 ja HPV-18. Hiljattain tehdyssä järjestelmällisessä katsauksessa ja meta-analyysissä todettiin, että 63:lla nuorella ja aikuisella RRP-potilaalla leikkausten välinen keskimääräinen kesto pidentyi HPV-rokotuksen jälkeen merkittävästi, keskimäärin 7:stä 34 kuukauteen (25). Tutkimuksessa ei havaittu merkittäviä eroja RRP:n puhkeamisiän mukaan (25). Myös muut tapaustutkimukset, jotka eivät sisältyneet meta-analyysiin, ovat osoittaneet Gardasilin tehon lapsipotilailla, sillä se pidentää leikkausten välistä aikaa merkittävästi tai joissakin tapauksissa aiheuttaa täydellisen remissiotilan (26, 27).
Intramuskulaarinen HPV-rokotus saattaa olla tehokkaampi kuin aiemmin tunnistetut, yleisemmin käytetyt hoitomuodot, kuten intralesonaalinen tsidofoviiri. Retrospektiivisessä tapaustutkimuksessa, jossa seurattiin nuoruusiän ja aikuisiän RRP-potilaita 22 vuoden ajan, todettiin, että leikkauksella ja Gardasililla hoidetuista 13 potilaasta vain kaksi uusiutui, kun taas kaikilla kontrollipotilailla, joita hoidettiin leikkauksella ja tsidofoviirilla, papilloomat kasvoivat uudelleen (28). Myös keskimääräinen aika taudin uusiutumiseen oli hoidetuilla potilailla huomattavasti pidempi kuin kontrollipotilailla (28).
Yksi HPV:n lupaavimmista puolista liitännäishoitona on se, että sillä ei ole vakavia sivuvaikutuksia. Lisäksi rokotusmäärän lisääntyessä juveniilin RRP:n esiintyvyys saattaa kaiken kaikkiaan vähentyä, sillä tämä tautimuoto saadaan yleisesti, kun lapsi altistuu HPV 6- tai 11-viruksen aiheuttamille sukupuolielinten syyliä aiheuttaville syyliä aiheuttaville viruksille synnytyksen aikana (4).
Sikotautirokote
Sikotautirokotteen tehosta adjuvanttihoitona on tehty vain vähän tutkimuksia, vaikka tämänhetkiset tutkimukset ovatkin lupaavia. Eräässä tapaustutkimuksessa todettiin, että remissio saatiin aikaan yhdeksällä yhdestätoista lapsipotilaasta, joita hoidettiin 3-12 viikon välein annetuilla rokotteen intralesionalisilla injektioilla yhdessä laserleikkauksen kanssa (29). Retrospektiivisessä tutkimuksessa, jossa verrattiin didofoviiria ja tuhkarokko-, sikotauti- ja vihurirokkorokotetta (MMR-rokote) adjuvanttihoitona pediatrisessa populaatiossa, todettiin, että ei ollut merkittäviä eroja niiden lasten välillä, joita hoidettiin intralesionaalisilla didofoviiri- ja MMR-injektioilla silpomishoidon jälkeen (30).
Bevatsitsumabi
Bevatsitsumabi on ihmisen monoklonaalinen vasta-aine, joka sitoutuu verisuonten endoteelin kasvutekijän (VEGF) reseptoreihin ja estää niiden vuorovaikutuksen. VEGF:n aktiivisuudella on merkitystä RRP:n kehittymisessä, sillä in vitro -tutkimuksissa on osoitettu VEGF-A:n voimakasta ilmentymistä papilloomaepiteelissä ja VEGFR-1- ja VEGFR-2-lähetti-RNA:iden ilmentymistä taustalla olevissa verisuonten sisäisissä endoteelisoluissa (31).
Ensimmäisissä tutkimuksissa, joissa tarkasteltiin bevasitsumabia RRP:n hoitona, selvitettiin injektionesteiden hyötyjä leikkauksen lisähoitona. Tutkimuksessa, johon osallistui kolme 3-6-vuotiasta potilasta, joilla oli vaikea RRP (eli vähintään neljä toimenpidettä vuodessa), havaittiin, että kaikilla potilailla kirurgisen debridementin ja pulssitetun KTP-laserhoidon välinen aika oli pidentynyt ja RRP:n vaikeus oli lieventynyt useita viikkoja bevasitsumabihoidon lopettamisen jälkeen aiempaan verrattuna (32). Heillä havaittiin myös parempaa ääneen liittyvää elämänlaatua (32).
Tapauskertomusten lisäksi on tehty myös tapauskontrollitutkimuksia, joissa on tutkittu bevasitsumabin tehoa adjuvanttihoitona. Kun 532 nm:n KTP-laserhoitoa seurasivat sublesionaaliset bevasitsumabi-injektiot sairaampaan äänihuulten poimuun ja suolaliuosinjektiot toiseen poimuun, 16:lla 20:stä aikuispotilaasta, joilla oli molemminpuolinen äänihuulten poimun RRP, oli vähemmän papilloomia hoidetussa poimussa endoskooppisella kuvantamisella määritettynä (33). Kolmella potilaalla 20:stä ei ollut tautia kummassakaan taitekohdassa, eikä yhdelläkään potilaalla ollut hoidon aiheuttamia komplikaatioita (33).
Tämän lupaavan tuloksen perusteella tehtiin laajempi tutkimus, jossa tarkasteltiin bevasitsumabin tehoa lapsiväestössä. Kymmenelle 18 kuukauden ja 18 vuoden ikäiselle lapselle, joilla oli etenevä, ei-reagoiva RRP, kolme intralesionaalista 2,5 mg/ml:n bevasitsumabi-injektiota 2-3 viikon välein yhdessä laserhoidon kanssa pidentivät kirurgisten toimenpiteiden välisen ajan mediaaniaikaa, vähensivät toimenpiteiden mediaanimäärää vuodessa ja paransivat ääneen liittyvää elämänlaatua (3). Yksi tutkimuksen rajoituksista on se, että annostelu on arvio, joka perustuu lasten silmälääketieteen annoksiin. Pailloomiin ruiskutettu määrä ei myöskään ollut sama jokaisella potilaalla, sillä se vaihteli taudin vaikeusasteen mukaan.
Joissakin tutkimuksissa on pyritty määrittämään optimaaliset annokset. Eräässä toisessa tutkimuksessa, jossa tarkasteltiin yhdeksää pediatrista potilasta, joilla oli nuoruusiässä alkanut RRP, todettiin myös, että viiden 4-6 viikon välein annetun subepiteelipistosarjan jälkeen, jossa keskimääräinen annos oli 14,25 mg, yhdessä KTP-laserablaation kanssa, kaikkien yhdeksän potilaan (mediaani-ikä 8 vuotta) kohdalla injektioiden välinen aikaväli kasvoi (34). Nämä tulokset osoittavat, että osoitti, että suuriannoksisella bevasitsumabihoidolla ei ole komplikaatioita ja se voi olla erittäin tehokasta.
Sen jälkeen, kun todisteet osoittivat intralesionalisen bevasitsumabin tehokkuuden, tutkimus kääntyi käsittelemään systeemistä bevasitsumabia, joka on erityisen lupaava hoito potilaille, joilla on monimutkaisia diagnooseja. Ensimmäinen raportti laskimonsisäisestä annostelusta osoitti, että kaikkien hoidettujen potilaiden, joilla oli etenevä RRP, papilloomat taantuivat 6 hoitojakson mediaanilla annoksilla 5, 10 ja 15 mg/kg (35). Potilaiden joukossa oli neljä aikuisiällä alkanutta RRP:tä ja yksi nuoruusiässä alkanut RRP. Viidelle potilaalle tehtiin yhteensä 18 kirurgista toimenpidettä bevasitsumabia edeltäneenä vuonna, mutta vain aikuistapauksessa tarvittiin hoidon jälkeen leikkaus, koska seuraavana vuonna ilmeni pahanlaatuinen muutos (35).
Muut yksittäiset tapausraportit ovat vahvistaneet systeemisen bevasitsumabin tehon havaitsematta komplikaatioita, vaikkakin useimmat näistä ovat aikuispotilailla. Vaikeaa henkitorven RRP:tä sairastaneella 42-vuotiaalla miehellä pieni 5 mg/kg:n annos, jota nostettiin ajan myötä 10 mg/kg:aan bevasitsumabia, auttoi saavuttamaan taudin taantumisen 3 kuukautta hoidon lopettamisen jälkeen (36). 12 kuukauden seurannassa kävi ilmi, että potilas oli edelleen tautivapaa. Kuusi hoitojaksoa systeemistä bevasitsumabihoitoa (5 mg/kg kahden viikon välein) 87-vuotiaalle potilaalle, joka ei ollut reagoinut intralesionaaliseen tsidofoviiriin, endobronkiaaliseen stenttiin tai HPV-rokotukseen, auttoivat myös vähentämään merkittävästi keuhkolohkon massaa ja saamaan keuhkoputken avoimeksi (37). Kahden 10 mg/kg:n kahden viikon välein annettujen laskimonsisäisten injektioiden jälkeen 63-vuotiaalla vaikeasta RRP:stä kärsineellä henkilöllä keuhkojen osallistuminen oli vähentynyt eikä merkkejä henkitorven tukkeutumisesta ollut (37).
Ainoa julkaistu tapausraportti lapsista koskee 12-vuotiasta tyttöä, jolla oli etenevä kurkunpään ja kurkunpään papillomatoosi ja keuhkojen osallistuminen, ja joka kolme kuukautta systeemisen bevasitsumabihoidon aloittamisen jälkeen osoitti osittaista hoitovastetta kurkunpäässä ja lähes täydellistä hoitovastetta henkitorvessa (38). Viiden kuukauden kuluttua potilaalla ei ollut enää keuhko-osuutta. Nämä tulokset ovat vieläkin vaikuttavampia, kun otetaan huomioon, että 10 vuoden aikana potilaalle oli aloitettu Gardasil-hoito, interferonihoito, selloksibihoito, refluksilääkitys, sitromysiini ja propranololi, eikä hän ollut saanut vastetta mihinkään (38).
Systeemisen bevasitsumabin potentiaalia RRP:n aggressiivisimpien muotojen hoitona kuvaavat parhaiten American Society of Pediatric Otolaryngologyn, American Broncho-Esophagological Associationin RRP-työryhmän, American Broncho-Esophagological Associationin ja RRP:tä systeemisellä bevasitsumabilla hoitaneiden lääkäreiden sähköisen tutkimuksen tulokset (39). Yhdeksästä lääketieteellisestä keskuksesta saadut 11 täytettyä kyselyä osoittivat, että suurimmalla osalla bevasitsumabilla hoidetuista potilaista oli pitkäaikainen, nuoruusiässä alkanut RRP, eikä heillä ollut pysyvää vastetta tsidofoviiriin, interferoniin ja celecoxibiin. Lääkärit antoivat hoitoa välillä 5-10 mg/kg annosta kohti. Seitsemän kahdeksasta hoidetusta potilaasta sai osittaisen vasteen ja yksi sai täydellisen vasteen hoitoon (39). Kaikilla potilailla leikkausten välinen aika pidentyi, nyt kuukausien luokkaa. Neljästä keuhkoihin osallistuneesta potilaasta kolmella keuhkopapillooma parani tai hävisi ja yhdellä tauti vakiintui. Vain kahdella potilaalla ilmeni vähäisiä komplikaatioita, hemoptyysiä ja proteinuriaa.
Bevakitsumabin kausaalisen vaikutuksen selvittämiseksi, sopivien annosten määrittämiseksi ja mahdollisten komplikaatioiden tunnistamiseksi on suoritettava satunnaistettuja kontrollitutkimuksia ja suurempia tapauskontrollitutkimuksia. Lisäksi on laadittava protokollat hoidon keston määrittelemiseksi ja mahdollisten rebound-vaikutusten kontrolloimiseksi.
Johtopäätökset
Vaikka optimaalista, yleisesti tehokasta lääkkeellistä adjuvanttihoitoa RRP:lle ei ole vielä löydetty, lupaavat tulokset RRP-rokotuksesta terapeuttisena lähestymistapana yhdessä systeemisen bevasitsumabin käytön kanssa antavat toivoa parempiin tuloksiin näillä lapsilla lähivuosina. Optimaaliset hoitoprotokollat olisi kehitettävä lähitulevaisuudessa.
Tekijöiden panos
Kaikki luetellut kirjoittajat ovat antaneet merkittävän, välittömän ja älyllisen panoksensa työhön ja hyväksyneet sen julkaistavaksi.
Erityskonfliktilausunto
Kirjoittajat ilmoittavat, että tutkimus suoritettiin ilman kaupallisia tai taloudellisia sidonnaisuuksia, jotka voitaisiin tulkita mahdolliseksi eturistiriidaksi.
Käsittelijätoimittaja ilmoitti, että hän on aiemmin ollut yhteiskirjoittaja yhden kirjoittajan DP:n kanssa.
1. Schraff S, Derkay CS, Burke B, Lawson L. American Society of Pediatric Otolaryngology members’ experience with recurrent respiratory papillomatosis and the use of adjuvant therapy. Arch Otolaryngol Head Neck Surg. (2004) 130:1039-42. doi: 10.1001/archotol.130.9.1039
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Krstic M, Pavlović JM, Stanković P, Milenković MT. Toistuvan kurkunpään papillomatoosin etiopatogeneesi ja nykyaikaiset hoitostrategiat. Acta Med Medianae. (2014) 53:64-74. doi: 10.5633/amm.2014.0411
CrossRef Full Text | Google Scholar
3. Rogers DJ, Ojha S, Maurer R, Hartnick CJ. Adjuvanttisen intralesionaalisen bevasitsumabin käyttö lasten aggressiivisen hengitystiepapillomatoosin hoidossa. JAMA Otolaryngol Head Neck Surg. (2013) 139:496-501. doi: 10.1001/jamaoto.2013.1810
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Jamaoto. Carifi M, Napolitano D, Morandi M, Dall’Olio D. Toistuva hengitysteiden papillomatoosi: nykyiset ja tulevaisuuden näkymät. Ther Clin Risk Manag. (2015) 11:731-8. doi: 10.2147/TCRM.S81825
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Fysioterapeutit ja lääkäreitä. Nodarse-Cuní H, Iznaga-Marín N, Viera-Alvarez D, Rodríguez-Gómez H, Fernández-Fernández H, Blanco-López Y, et al. Interferoni alfa-2b toistuvan hengitysteiden papillomatoosin liitännäishoitona Kuubassa: kansallinen ohjelma (raportti 1994-1999). J Laryngol Otol. (2004) 118:681-7. doi: 10.1258/0022215042244741
PubMed Abstract | CrossRef Full Text | Google Scholar
6. JOHDANTO (2004) 118:681-7. Healy GB, Gelber RD, Trowbridge AL, Grundfast KM, Ruben RJ, Price KN. Toistuvan hengitysteiden papillomatoosin hoito ihmisen leukosyyttiinterferonilla. New Engl J Med. (1988) 319:401-7. doi: 10.1056/NEJM198808183190704
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gerein V, Rastorguev E, Gerein J, Jecker P, Pfister H. Interferoni-alfan käyttö uusiutuvassa hengitysteiden papillomatoosissa: 20 vuoden seuranta. Ann Otol Rhinol Laryngol. (2005) 114:463-71. doi: 10.1177/000348940511400608
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Johtopäätökset ja suositukset. Jackowska J, Piersiala K, Klimza H, Wierzbicka M. Bevasitsumabi- ja tsidofoviirihoidon tulokset HPV:hen liittyvässä toistuvassa hengitysteiden papillomatoosissa-kirjallisuuskatsaus. Otolaryngol Pol. (2018) 72:1-8. doi: 10.5604/01.3001.0012.0484
PubMed Abstract | CrossRef Full Text | Google Scholar
9. McMurray JS, Connor N, Ford CN. Sidofoviirin teho toistuvassa hengitysteiden papillomatoosissa: satunnaistettu, kaksoissokkoutettu, lumekontrolloitu tutkimus. Ann Otol Rhinol Laryngol. (2008) 117:477-83. doi: 10.1177/000348940811700702
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Chadha NK. Intralesionaalinen tsidofoviiri toistuvan hengitysteiden papillomatoosin hoitoon: systemaattinen katsaus tehosta ja turvallisuudesta. J Laryngol Voice. (2011) 1:22-6. doi: 10.4103/2230-9748.76133
CrossRef Full Text | Google Scholar
11. Garyngaryngaryntiikka. Broekema FI, Dikkers FG. Sidofoviirin sivuvaikutukset toistuvan hengitysteiden papillomatoosin hoidossa. Eur Arch Otorhinolaryngol. (2008) 265:871-9. doi: 10.1007/s00405-008-0658-0
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Dancey DR, Chamberlain DW, Krajden M, Palefsky J, Alberti PW, Downey GP. Nuorten kurkunpään papillomatoosiin liittyvän monikystisen keuhkosairauden menestyksekäs hoito tsidofoviirilla: tapausselostus ja kirjallisuuskatsaus. Chest. (2000) 118:1210-4. doi: 10.1378/chest.118.4.1210
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Johtopäätökset. Ksiazek J, Prager JD, Sun GH, Wood RE, Arjmand EM. Inhaloitava tsidofoviiri toistuvan hengitysteiden papillomatoosin liitännäishoitona. Otolaryngol Head Neck Surg. (2011) 144:639-41. doi: 10.1177/0194599810395353
PubMed Abstract | CrossRef Full Text | Google Scholar
14. TUTKIMUKSEN TULOKSET (2011) 144:639-41. Abramson AL, Shikowitz MJ, Mullooly VM, Steinberg BM, Amella CA, Rothstein HR. Fotodynaamisen hoidon kliiniset vaikutukset uusiutuviin kurkunpään papilloomiin. Arch Otolaryngol Head Neck Surg. (1992) 118:25-9. doi: 10.1001/archotol.1992.01880010029011
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Vrt. esim. Feyh J, Kastenbauer E. Kurkunpään papillomatoosin hoito fotodynaamisella laserhoidolla. Laryngorhinootologie. (1992) 71:190-2.
PubMed Abstract | Google Scholar
16. Lieder A, Khan MK, Lippert BM. Fotodynaaminen hoito uusiutuvan hengitysteiden papillomatoosin hoitoon. Cochrane Database Syst Rev. (2014) 5:CD009810. doi: 10.1002/14651858.CD009810.pub2
CrossRef Full Text | Google Scholar
17. Cochrane Database Syst Rev. (2014) 5:CD009810. Rosen CA, Bryson PC. Indoli-3-karbinoli toistuvan hengitysteiden papillomatoosin hoitoon: pitkäaikaistulokset. J Voice. (2004) 18:248-53. doi: 10.1016/j.jvoice.2003.05.005
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Wu R, Abramson AL, Shikowitz MJ, Dannenberg AJ, Steinberg BM. Epidermaalisen kasvutekijän indusoima syklooksigenaasi-2:n ilmentyminen välittyy fosfatidyyliinositoli-3-kinaasin, ei mitogeeniaktivoituneen proteiinin / ekstrasellulaarisen signaalin säätelemän kinaasikinaasin, kautta toistuvissa hengitysteiden papilloomissa. Clin. Cancer Res. (2005) 11:6155-61. doi: 10.1158/1078-0432.CCR-04-2664
CrossRef Full Text | Google Scholar
19. Syöpäkasvaimet. Limsukon A, Susanto I, Soo Hoo GW, Dubinett SM, Batra RK. Uusiutuvan hengitysteiden papillomatoosin taantuminen celecoxibin ja erlotinibin yhdistelmähoidolla. Chest. (2009) 136:924-6. doi: 10.1378/chest.08-2639
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Mahdolliset muutoksiin vaikuttavat tekijät. McKenna M, Brodsky L. Ekstraesofageaalinen happorefluksi ja toistuva hengitystiepapillooma lapsilla. Int. J. Pediatr. Otorhinolaryngol. (2005) 69:597-605. doi: 10.1016/j.ijporl.2004.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Suomenkielinen julkaisu. Borkowski G, Sommer P, Stark T, Sudhoff H, Luckhaupt H. Gastroesofageaaliseen refluksitautiin liittyvä toistuva hengitysteiden papillomatoosi lapsilla. Eur Arch Otorhinolaryngol. (1999) 256:370-2. doi: 10.1007/s004050050166
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Holland BW, Koufman JA, Postma GN, McGuirt WF Jr. Laryngofaryngeaalinen refluksi ja kurkunpään verkkomuodostus potilailla, joilla on pediatrisia toistuvia hengitystiepapilloomia. Laryngoscope. (2002) 112:1926-9. doi: 10.1097/00005537-200211000-00003
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Garyngosoppa. San Giorgi MRM, Helder HM, Lindeman RJS, de Bock GH, Dikkers FG. Yhteys gastroesofageaalisen refluksitaudin ja toistuvan hengitysteiden papillomatoosin välillä: systemaattinen katsaus. Laryngoscope. (2016) 126:2330-9. doi: 10.1002/lary.25898
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Derkay CS, Smith RJH, McClay J, van Burik JAH, Wiatrak BJ, Arnold J, et al. HspE7-hoito lasten toistuvassa hengitysteiden papillomatoosissa: avoimen tutkimuksen lopulliset tulokset. Ann Otol Rhinol Laryngol. (2005) 114:730-7. doi: 10.1177/000348940511400913
PubMed Abstract | CrossRef Full Text | Google Scholar
25. PubMed Abstract | CrossRef Full Text | Google Scholar. Rosenberg T, Philipsen BB, Mehlum CS, Dyrvig AK, Wehberg S, Chirilǎ M, et al. Therapeutic use of the human papillomavirus vaccine on recurrent respiratory papillomatosis: a systematic review and meta-analysis. J Infect Dis. (2019) 219:1016-25. doi: 10.1093/infdis/jiy616
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Johtopäätökset. Mudry P, Vavrina M, Mazanek P, Machalova M, Litzman J, Sterba J. Toistuva kurkunpään papillomatoosi: onnistunut hoito ihmisen papilloomavirusrokotuksella. Arch Dis Child. (2011) 96:476-7. doi: 10.1136/adc.2010.198184
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Förster G, Boltze C, Seidel J, Pawlita M, Müller A. Juvenile laryngeal papillomatosis-immunisaatio polyvalentilla rokotteella gardasil. Laryngorhinootologie. (2008) 87:796-9. doi: 10.1055/s-2008-1077527
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Mauz PS, Schäfer FA, Iftner T, Gonser P. HPV-rokotus uusiutuvan hengitysteiden papillomatoosin ennaltaehkäisevänä lähestymistapana – 22 vuoden retrospektiivinen kliininen analyysi. BMC Infect Dis. (2018) 18:343. doi: 10.1186/s12879-018-3260-0
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
29. Pashley NRT. Voiko sikotautirokote saada aikaan remissiota toistuvassa hengitystiepapilloomassa? Arch Otolaryngol Head Neck Surg. (2002) 128:783-6. doi: 10.1001/archotol.128.7.783
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Meacham RK, Thompson JW. Sidofoviirin ja tuhkarokko-, sikotauti- ja vihurirokkorokotteen vertailu toistuvan hengitysteiden papillomatoosin hoidossa. Ear Nose Throat J. (2017) 96:69-74. doi: 10.1177/014556131709600209
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Korva-, nenä- ja kurkkutautien hoito. Rahbar R, Vargas SO, Folkman J, McGill TJ, Healy GB, Tan X, et al. Vaskulaarisen endoteelin kasvutekijä-a:n rooli toistuvassa hengitysteiden papillomatoosissa. Ann Otol Rhinol Laryngol. (2005) 114:289-95. doi: 10.1177/000348940511400407
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Maturo S, Hartnick CJ. 532-Nm:n pulssitetun kaliumtitanyylifosfaattilaserin ja adjuvanttisen intralesionaalisen bevasitsumabin käyttö aggressiivisen hengitysteiden papillomatoosin hoidossa lapsilla: ensimmäiset kokemukset. Arch Otolaryngol Head Neck Surg. (2010) 136:561-5. doi: 10.1001/archoto.2010.81
PubMed Abstract | CrossRef Full Text | Google Scholar
33. PubMed Abstract | CrossRef Full Text | Google Scholar. Zeitels SM, Barbu AM, Landau-Zemer T, Lopez-Guerra G, Burns JA, Friedman AD, ym. bevasitsumabin (Avastin) paikallinen injektio ja angiolyyttinen KTP-laserhoito äänihuulten toistuvassa hengitysteiden papillomatoosissa: prospektiivinen tutkimus. Ann Otol Rhinol Laryngol. (2011) 120:627-34. doi: 10.1177/000348941112001001
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Vrt. Sidell DR, Nassar M, Cotton RT, Zeitels SM, de Alarcon A. Korkea annos sublesionaalista bevasitsumabia (Avastin) lasten toistuvan hengitysteiden papillomatoosin hoitoon. Ann Otol Rhinol Laryngol. (2014) 123:214-21. doi: 10.1177/0003489414522977
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Millainen se on? Mohr M, Schliemann C, Biermann C, Schmidt LH, Kessler T, Schmidt J, et al. Rapid response to systemic bevacizumab therapy in recurrent respiratory papillomatosis. Oncol Lett. (2014) 8:1912-8. doi: 10.3892/ol.2014.2486
PubMed Abstract | CrossRef Full Text | Google Scholar
36. Fernandez-Bussy S, Labarca G, Vial MR, Soto R, Mehta HJ, Jantz M, et al. Recurrent respiratory papillomatosis and bevacizumab treatment. Am J Respir Crit Care Med. (2017) 197:539-41. doi: 10.1164/rccm.201702-0279LE
PubMed Abstract | CrossRef Full Text | Google Scholar
37. Bedoya A, Glisinski K, Clarke J, Lind RN, Buckley CE, Shofer S. Systeeminen bevasitsumabi uusiutuneen hengitysteiden papillomatoosin hoitoon: yhden keskuksen kokemus kahdesta tapauksesta. Am J Case Rep. (2017) 18:842-6. doi: 10.12659/AJCR.904416
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Am J Case Rep. Zur KB, Fox E. Bevasitsumabi-sytostaattihoito keuhkojen ja kurkunpään ja kurkunpään papillomatoosin hoidossa lapsella. Laryngoscope. (2017) 127:1538-42. doi: 10.1002/lary.26450
PubMed Abstract | CrossRef Full Text | Google Scholar
39. Laryngoskooppi. Best SR, Mohr M, Zur KB. Systeeminen bevasitsumabi uusiutuvan hengitysteiden papillomatoosin hoidossa: kansallinen tutkimus. Laryngoscope. (2017) 127:2225-9. doi: 10.1002/lary.26662
PubMed Abstract | CrossRef Full Text | Google Scholar