Úvod
Recurrentní respirační papilomatóza (RRP) je chronické onemocnění způsobené lidským papilomavirem (HPV), obvykle typy 6 a 11. Léze RRP se nejčastěji objevují v hrtanu (obrázek 1), ale mohou se objevit také v ústech, průdušnici, průduškách, plicním parenchymu a jícnu. Juvenilní forma RRP, u níž se příznaky objevují před 12. rokem věku, je agresivnější než forma pro dospělé a příznaky jsou závažnější. Recidiva papilomů je obzvláště rychlá u dětí mladších 3 let, u kterých jsou intervaly mezi chirurgickými zákroky kratší, a tedy celkově více operací. V této populaci je také vyšší pravděpodobnost rozšíření infekce mimo hrtan a výskyt tracheostomie, která pomáhá udržet průdušnici otevřenou (1). Pacienti s juvenilním začátkem RRP podstoupí v průměru 20 chirurgických zákroků, z nichž většina je v dětském věku (2).
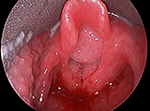
Obrázek 1. Přímý laryngoskopický obraz velké objemné papilomatózy dýchacích cest obturující hrtanový vchod.
Tradiční chirurgická metoda chirurgické exstirpace klasicky zahrnovala KTP (titanylfosfát draselný) nebo laser s oxidem uhličitým (3). Vzhledem k potenciálně závažným vedlejším účinkům laserové ablace, včetně popálenin dýchacích cest a jizvení hrtanu, se mikrodebridery stávají stále oblíbenějším chirurgickým nástrojem, zejména mezi dětskými otolaryngology, pro objemná onemocnění (3). Toto ruční zařízení dokáže přesněji odstranit nemocnou tkáň, čímž se sníží poškození okolních tkání (3). Vzhledem k agresivní povaze juvenilní RRP jsou však debridementy stále časté a v průběhu času stále výrazně opotřebovávají základní tkáň s vysokým výskytem tvorby jizev. Proto bylo zkoumáno několik medikamentózních léčebných postupů, které mají zlepšit výsledek operace prodloužením doby mezi operacemi nebo minimalizací recidivy lézí RRP.
Interferon α
Interferon α, protein produkovaný leukocyty v reakci na různé podněty, včetně virové infekce, byl jedním z prvních zkoumaných potenciálních medikamentózních léčebných postupů (4). Jeho hodnota jako adjuvantní léčby je sporná. V rozsáhlé studii, které se zúčastnilo 85 dětí a 84 dospělých, ukončilo 58 % dětí roční období léčby intramuskulárními injekcemi interferonu α třikrát týdně bez známek RRP (5). Četnost recidivy papilomu se snížila u 74 % všech léčených dětí (5). V randomizované kontrolní studii se 123 pacienty mladšími 21 let se však zpomalení růstu papilomů v experimentální skupině, která dostávala intramuskulární injekce interferonu α, v průběhu roční léčby neudrželo (6). Podobně jiná studie zjistila, že 20 let po ukončení léčby interferonem α vykazovalo dlouhodobou odpověď pouze 42 % pacientů a všichni, u nichž došlo k recidivě, měli juvenilní formu RRP (7). Většina studií zabývajících se interferonem α také uvádí závažné vedlejší účinky, jako jsou neurologické poruchy, leukopenie a trombocytopenie (5). Z těchto důvodů se jeho používání dětskými otolaryngology snížilo a obecně se nedoporučuje (1). V roce 2014 dostávala interferon α jako adjuvantní léčbu pouze 4 % dětí s RRP (1).
Cidofovir
Tento širokospektrý antivirový lék, který inhibuje virové DNA polymerázy, se ukázal jako slibný jako adjuvantní intralezionální léčba k operaci RRP. Intralezionální injekce cidofoviru jsou mezi dětskými otolaryngology nejčastěji podávanou medikamentózní léčbou RRP (1). Všechny práce publikované v letech 1998-2011, které se zabývaly účinností intralezionálního cidofoviru, uváděly alespoň jeden případ remise onemocnění (8). Protože se však ve většině těchto studií jedná o nekontrolované případové studie, není jasné, zda je tento přínos způsoben cidofovirem, nebo je součástí přirozeného průběhu onemocnění. Randomizovaná kontrolní studie zjistila, že mezi kontrolní skupinou, léčenou chirurgickými zákroky podle potřeby a intralezionálními injekcemi fyziologického roztoku, a experimentální skupinou, léčenou chirurgickými zákroky a intralezionálním Cidofovirem, nebyly po 12 měsících léčby statisticky významné rozdíly v závažnosti papilomu ani v kvalitě života související se zdravím (9). U obou skupin došlo v průběhu roku k významnému poklesu závažnosti onemocnění, což naznačuje, že onemocnění může časem samo regredovat (9). Jiný přehled, který se zabýval 27 studiemi podávání cidofoviru, všechny publikované před rokem 2011, zjistil, že průměrná míra kompletní remise při podávání cidofoviru byla v pediatrických studiích 37 % (10). S cidofovirem byly také spojeny některé závažné nežádoucí účinky, neboť přehled zjistil, že u 1,7 % ze 447 pacientů s RRP došlo k maligní transformaci a u 1 % k nefrotoxicitě (8). Mezi další nežádoucí účinky patří kožní vyrážka, bolest hlavy a zjizvení hlasivek (11). Vzhledem k těmto možným komplikacím a neexistenci přijatého protokolu pro dávkování nebo frekvenci podávání není tento lék spolehlivým adjuvans (4).
Cidofovir byl také podáván jako systémová, nikoli lokální léčba u případů RRP, které jsou komplikovány plicním onemocněním. Čtyři jednotlivé případové studie prokázaly, že intravenózní podání cidofoviru vedlo k remisi onemocnění, což není obvyklý průběh onemocnění s postižením plic (11). Ve všech těchto studiích byla použita hyperhydratace a probenecid, reduktor kyseliny močové, aby se snížila pravděpodobnost nefrotoxicity (11). Pouze u jednoho pacienta se vyskytly vedlejší účinky, částečná alopecie a leukopenie, při kombinované léčbě cidofovirem a interferonem (12). V reakci na to byly dávky obou léků sníženy. Osmnáct měsíců po ukončení léčby pacientka pouze jednou potřebovala operaci pro RRP a její plicní onemocnění se stabilizovalo (12).
Nový způsob podávání cidofoviru je inhalace. Účinnost této metody zkoumalo jen málo studií, ale může být slibná pro pacienty, kteří nereagovali na jiné formy léčby, jako například čtyřměsíční chlapec, u kterého se navzdory dvoutýdenním mikrodestičkám a intralezionálním injekcím Cidofoviru a intravenóznímu interferonu α zhoršovaly příznaky (13). Během 6 týdnů podávání 40 mg rozprašovaného Cidofoviru denně, 12 dní denně a 2 dny denně, se doba mezi debridementy prodloužila (13). O šest měsíců později pacient nevykazoval žádné příznaky (13). Souhrnně lze říci, že ačkoli je Cidofovir v různých formách podání stále široce používán, výsledky jeho léčby jsou přinejlepším smíšené a jeho potenciál nežádoucích účinků je poněkud omezující.
Fotodynamická terapie
Fotodynamická terapie (PDT) zahrnuje zavedení látky citlivé na světlo, tzv. fotosenzibilizátoru, perorálně nebo injekčně do nemocné tkáně a aktivaci této látky laserovým světlem za účelem vyvolání nekrózy. Jednou z hlavních výhod PDT je schopnost ničit nádory, aniž by byla zasažena okolní tkáň (4). Případové studie prokázaly výrazně pomalejší míru opětovného růstu papilomů brzy po PDT, podávané jako adjuvantní nebo samostatná terapie, a v některých případech i absenci onemocnění po několika týdnech (14, 15). Bylo provedeno pouze několik randomizovaných kontrolních studií, které zkoumaly vliv PDT, ale nejnovější z nich zjistila, že onemocnění recidivuje po 3-5 letech, pravděpodobně proto, že generuje svůj vliv prostřednictvím krátkodobé imunitní odpovědi (16). Je třeba provést další výzkum, aby se zjistila její účinnost a bezpečnost.
Indol-3-karbinol
Indol-3-karbinol, který se nachází ve vysokých koncentracích v brukvovité zelenině, jako je brokolice a zelí, modifikuje metabolismus estrogenů a mění buněčnou proliferaci a syntézu DNA. Nejnovější klinická studie zjistila, že po užívání indol-3-karbinolu dvakrát denně v dávce 200 mg pro dospělé a v dávkách podle hmotnosti pro děti po dobu průměrně 50,2 měsíce došlo u 70 % subjektů k úplné nebo částečné odpovědi (17). Z dětských pacientů došlo u jednoho k úplné odpovědi, u tří k částečné odpovědi a u pěti k žádné odpovědi (17). Není jasné, proč dospělí pacienti reagovali na indol-3-karbinol lépe než pediatričtí pacienti. Jedním z faktorů může být méně agresivní povaha RRP u dospělých. Vzhledem k neperspektivním výsledkům u pediatrické populace neproběhl další výzkum léčby juvenilní RRP pomocí indol-3-karbinolu.
Celekoxib
Celekoxib je protizánětlivý lék, který inhibuje cyklooxygenázu-2 (COX-2), enzym vedoucí k zánětu a bolesti, a běžně se používá k léčbě artritidy. Studie in vitro ukázaly, že papilomové buňky nadměrně exprimují COX-2 v důsledku zvýšené signalizace receptoru pro epidermální růstový faktor (EGFR) a že tato aktivita je důležitá pro jejich růst (18). Kombinovaná léčba celekoxibem a erlotinibem, inhibitorem kinázy EGFR, pomohla kontrolovat progresivní RRP u 58letého muže a tím, že zpomalila růst papilomů, takže další operace nebyla nutná (19). Probíhající randomizovaná kontrolní studie sponzorovaná společností Northwell Health má za cíl zjistit, zda celekoxib může snížit míru recidivy papilomů u dospělých i dětských pacientů (4).
Léky proti refluxu
Případové studie ukázaly, že léčba gastroezofageální refluxní choroby (GERD) léky proti refluxu u pacientů s juvenilní RRP může pomoci zpomalit míru opětovného růstu papilomů (20, 21). V jedné studii došlo u pacientů, kteří nedodržovali léčbu GERD, k recidivě (20). Retrospektivní přehled karet také ukázal, že u dětských pacientů léčených pro RRP, kteří nebyli léčeni pro reflux, byla významně vyšší pravděpodobnost vzniku hrtanových pavučin po chirurgickém odstranění papilomů (22). Ačkoli neexistují přesvědčivé důkazy o tom, že GERD zhoršuje RRP, její léčba má smysl u pacientů, kteří mají klinický obraz GERD a komplikované, progredující případy RRP (23).
Heat Shock Protein
Ze 700 dětí s RRP, které byly vedeny 74 dětskými otolaryngology, kteří byli dotazováni na použití adjuvantní léčby, dostávalo 11 pacientů HSP-E7, rekombinantní fúzní protein složený z proteinu tepelného šoku 65 (Hsp65) a proteinu E7 HPV typu 16 (1). HSP-E7 byl zkoumán jako léčba několika onemocnění, která mají původ v HPV, včetně genitálních bradavic a intraepiteliální neoplazie (24). Důkazy naznačují, že může být reaktivní vůči více kmenům HPV než jen HPV 16 (24). V otevřené studii s 27 dětskými pacienty s RRP byl medián intervalu mezi operacemi po léčbě HSP-E7 významně prodloužen ve srovnání s mediánem před léčbou (24). Komplikací bylo málo, pouze mírné až středně závažné reakce v místě vpichu. Přestože neprobíhají žádné klinické studie, které by zkoumaly účinnost Hsp-E7, jedná se o slibnou léčbu.
HPV vakcína
Několik kazuistik a studií dokumentuje použití HPV vakcíny jako adjuvantní terapie. V současné době existují tři schválené vakcíny proti HPV: bivalentní vakcína Cervarix, tetravalentní vakcína Gardasil a neavalentní vakcína Gardasil 9. Tetravalentní vakcína působí cíleně proti HPV-6, HPV-11, HPV-16, HPV-18. Nedávný systematický přehled a metaanalýza zjistily, že průměrná doba mezi operacemi u 63 mladistvých a dospělých pacientů s RRP se po očkování proti HPV významně prodloužila, v průměru ze 7 na 34 měsíců (25). Studie nezjistila žádné významné rozdíly podle věku vzniku RRP (25). Další případové studie, které nebyly zahrnuty do metaanalýzy, rovněž prokázaly účinnost přípravku Gardasil u dětských pacientů, neboť významně prodloužil dobu mezi operacemi nebo v některých případech způsobil úplnou remisi (26, 27).
Intramuskulární očkování proti HPV by mohlo být účinnější než dříve zjištěné, běžnější léčebné postupy, jako je intralezionální cidofovir. Retrospektivní případová studie, která sledovala juvenilní a dospělé pacienty s RRP po dobu 22 let, zjistila, že pouze u dvou ze 13 pacientů léčených chirurgicky a Gardasilem došlo k recidivě, zatímco u všech kontrolních pacientů léčených chirurgicky a cidofovirem došlo k opětovnému růstu papilomů (28). Průměrná doba do recidivy onemocnění byla u léčených pacientek také výrazně delší než u kontrol (28).
Jedním z nejslibnějších aspektů HPV jako adjuvantní léčby je, že nemá žádné závažné vedlejší účinky. Navíc se zvyšující se mírou očkování může celkově klesnout výskyt juvenilní RRP, protože tato forma onemocnění se běžně získává, když je dítě během porodu vystaveno genitálním bradavicím způsobeným virem HPV 6 nebo 11 (4).
Vakcína proti příušnicím
O účinnosti vakcíny proti příušnicím jako adjuvantní terapie bylo provedeno jen velmi málo studií, ačkoli současný výzkum je slibný. Případová studie zjistila, že u devíti z 11 dětských pacientů léčených intralezionálními injekcemi vakcíny v intervalu 3 až 12 týdnů spolu s laserovou operací byla navozena remise (29). Retrospektivní studie srovnávající cidofovir a vakcínu proti spalničkám, příušnicím a zarděnkám (MMR) jako adjuvantní terapii u dětské populace zjistila, že mezi dětmi léčenými intralezionálními injekcemi cidofoviru a MMR nebyly po debridementu žádné významné rozdíly (30).
Bevacizumab
Bevacizumab je lidská monoklonální protilátka, která se váže na vaskulární endoteliální růstový faktor (VEGF) a zabraňuje jeho interakci s receptory. Aktivita VEGF hraje roli ve vývoji RRP, protože studie in vitro prokázaly silnou expresi VEGF-A v epitelu papilomu a expresi messengerových RNA VEGFR-1 a VEGFR-2 v základních cévních endoteliálních buňkách (31).
První studie zabývající se bevacizumabem jako léčbou RRP zkoumaly přínos intralezionálních injekcí jako adjuvantní terapie k chirurgickému zákroku. Studie tří pacientů ve věku od 3 do 6 let s těžkou RRP (tj. s nejméně čtyřmi zákroky za rok) zjistila, že u všech pacientů došlo k prodloužení doby mezi chirurgickým odstraněním a ošetřením pulzním KTP laserem a k méně závažné RRP několik týdnů po ukončení léčby bevacizumabem ve srovnání s dobou před ní (32). Rovněž u nich došlo ke zlepšení kvality života související s hlasem (32).
Kromě kazuistik byly provedeny také případové studie, které zkoumaly účinnost bevacizumabu jako adjuvantní léčby. Po ošetření 532 nm KTP laserem, po kterém následovaly sublesionální injekce bevacizumabu do více postižené hlasivkové řasy a injekce fyziologického roztoku do druhé řasy, mělo 16 z 20 dospělých pacientů s oboustrannou RRP hlasivkové řasy méně papilomů v léčené řase, jak bylo zjištěno endoskopickým zobrazením (33). Tři z 20 pacientů neměli žádné onemocnění v obou složkách a u žádného z pacientů se nevyskytly žádné komplikace léčby (33).
Na základě těchto slibných výsledků byla provedena rozsáhlejší studie zabývající se účinností bevacizumabu u dětské populace. U 10 dětí ve věku od 18 měsíců do 18 let s progresivní, nereagující RRP se třemi intralezionálními injekcemi bevacizumabu v dávce 2,5 mg/ml s odstupem 2-3 týdnů spolu s laserovou terapií prodloužila medián doby mezi chirurgickými zákroky, snížil se medián počtu zákroků za rok a zlepšila se kvalita života související s hlasem (3). Jedním z omezení studie je, že dávkování je odhadem založeným na dávkách v dětské oftalmologii. Množství aplikované do paillomů také nebylo u každého pacienta stejné, protože se lišilo podle závažnosti onemocnění.
Některé studie se snažily určit optimální dávkování. Jiná studie zabývající se devíti dětskými pacienty s juvenilním začátkem RRP také zjistila, že po sérii pěti subepiteliálních injekcí podávaných ve 4-6týdenních intervalech s průměrnou dávkou 14,25 mg spolu s laserovou ablací KTP došlo u všech devíti pacientů (s průměrným věkem 8 let) ke zvýšení časového intervalu mezi injekcemi (34). Tyto výsledky naznačují, že ukázaly, že léčba vysokými dávkami bevacizumabu nemá žádné komplikace a může být vysoce účinná.
Po důkazech, které prokázaly účinnost intralezionálního bevacizumabu, se výzkum obrátil k řešení systémového bevacizumabu, který je zvláště slibnou léčbou pro pacienty s komplexními diagnózami. První zpráva o intravenózním podávání ukázala, že při mediánu 6 cyklů v dávkách 5, 10, 15 mg/kg došlo u všech léčených pacientů s progresivní RRP k regresi papilomu (35). Mezi pacienty byly čtyři případy RRP s nástupem u dospělých a jeden s nástupem u mladistvých. Pět pacientů společně podstoupilo 18 chirurgických zákroků v roce před podáním bevacizumabu, ale pouze případ dospělého pacienta vyžadoval po léčbě operaci kvůli maligní transformaci v následujícím roce (35).
Další jednotlivé kazuistiky potvrdily účinnost systémového bevacizumabu bez nálezu komplikací, i když většina z nich se týká dospělých pacientů. U 42letého muže s těžkou tracheální RRP pomohla nízká dávka 5 mg/kg, postupem času zvýšená na 10 mg/kg bevacizumabu, dosáhnout regrese onemocnění 3 měsíce po ukončení léčby (36). Dvanáctiměsíční sledování ukázalo, že pacient zůstal bez onemocnění. Šest cyklů systémové léčby bevacizumabem v dávce 5 mg/kg každé 2 týdny u 87letého pacienta, který nereagoval na intralezionální cidofovir, endobronchiální stent ani očkování proti HPV, rovněž pomohlo dosáhnout významného poklesu masy laloku a patentního bronchu (37). Po dvou cyklech intravenózních injekcí v dávce 10 mg/kg každé 2 týdny se u 63letého pacienta s těžkou RRP projevilo menší postižení plic a žádné známky tracheální obstrukce (37).
Jediná publikovaná kazuistika u dětí se týká 12leté pacientky s progredující laryngotracheální papilomatózou a postižením plic, u níž se po 3 měsících od zahájení systémové léčby bevacizumabem projevila částečná odpověď v hrtanu a téměř úplná odpověď v průdušnici (38). Po 5 měsících již pacient nevykazoval plicní postižení. Tyto výsledky jsou o to působivější, že v průběhu 10 let byl pacientovi nasazen Gardasil, interferon, celekoxib, antirefluxní léky, zithromycin a propranolol a na žádný z nich nereagoval (38).
Potenciál systémového bevacizumabu jako léčby nejagresivnějších forem RRP nejlépe shrnují výsledky elektronického průzkumu pracovní skupiny pro RRP Americké společnosti dětské otolaryngologie, Americké broncho-esofagologické asociace a lékařů, kteří léčili RRP systémovým bevacizumabem (39). Z 11 vyplněných dotazníků získaných z devíti lékařských center vyplynulo, že většina pacientů léčených bevacizumabem měla dlouhou anamnézu juvenilní RRP a nevykazovala trvalou odpověď na cidofovir, interferon a celekoxib. Lékaři podávali léčbu v rozmezí 5-10 mg/kg na dávku. U sedmi z osmi léčených pacientů došlo k částečné odpovědi a jeden pacient vykázal úplnou odpověď na léčbu (39). U všech pacientů došlo k prodloužení doby mezi operacemi, nyní v řádu měsíců. U tří ze čtyř pacientů s postižením plic došlo ke zlepšení nebo vymizení plicního papilomu a u jednoho ke stabilizaci onemocnění. Pouze u dvou pacientů se vyskytly drobné komplikace, hemoptýza a proteinurie.
Pro zjištění kauzálního účinku bevacizumabu, stanovení vhodných dávek a identifikaci případných komplikací je třeba provést randomizované kontrolní studie a větší případové studie. Kromě toho je třeba vypracovat protokoly, které by definovaly délku léčby a zároveň kontrolovaly případné rebound účinky.
Závěry
Přestože dosud nebyla nalezena optimální, univerzálně účinná medikamentózní adjuvantní léčba RRP, slibné výsledky vakcinace RRP jako terapeutického přístupu spolu s použitím systémového bevacizumabu dávají naději na zlepšení výsledků těchto dětí v nadcházejících letech. V blízké budoucnosti by měly být vypracovány optimální protokoly pro léčbu.
Příspěvky autorů
Všichni uvedení autoři se na práci významně, přímo a intelektuálně podíleli a schválili její publikování.
Prohlášení o střetu zájmů
Autoři prohlašují, že výzkum byl prováděn bez jakýchkoli komerčních nebo finančních vztahů, které by mohly být chápány jako potenciální střet zájmů.
Zpracovávající redaktor prohlásil, že v minulosti byl spoluautorem jednoho z autorů DP.
1. Schraff S, Derkay CS, Burke B, Lawson L. American Society of Pediatric Otolaryngology‘ experience with recurrent respiratory papillomatosis and the use of adjuvant therapy. Arch Otolaryngol Head Neck Surg. (2004) 130:1039-42. doi: 10.1001/archotol.130.9.1039
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Zprávy z konference, která se konala v roce 2004 v Praze. Krstic M, Pavlović JM, Stanković P, Milenković MT. Etiopatogeneze recidivující laryngeální papilomatózy a současné strategie léčby. Acta Medianae. (2014) 53:64-74. doi: 10.5633/amm.2014.0411
CrossRef Full Text | Google Scholar
3. Rogers DJ, Ojha S, Maurer R, Hartnick CJ. Použití adjuvantního intralezionálního bevacizumabu u agresivní respirační papilomatózy u dětí. JAMA Otolaryngol Head Neck Surg. (2013) 139:496-501. doi: 10.1001/jamaoto.2013.1810
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Děkujeme za spolupráci. Carifi M, Napolitano D, Morandi M, Dall’Olio D. Rekurentní respirační papilomatóza: současné a budoucí perspektivy. Ther Clin Risk Manag. (2015) 11:731-8. doi: 10.2147/TCRM.S81825
PubMed Abstract | CrossRef Full Text | Google Scholar
5. PupMed Abstrakt | CrossRef Full Text | Google Scholar
5. Nodarse-Cuní H, Iznaga-Marín N, Viera-Alvarez D, Rodríguez-Gómez H, Fernández-Fernández H, Blanco-López Y, et al. Interferon alfa-2b as adjuvant treatment of recurrent respiratory papillomatosis in Cuba: national programme (1994-1999 Report). J Laryngol Otol. (2004) 118:681-7. doi: 10.1258/0022215042244741
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Srov. Healy GB, Gelber RD, Trowbridge AL, Grundfast KM, Ruben RJ, Price KN. Léčba recidivující respirační papilomatózy lidským leukocytárním interferonem. New Engl J Med. (1988) 319:401-7. doi: 10.1056/NEJM198808183190704
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gerein V, Rastorguev E, Gerein J, Jecker P, Pfister H. Use of interferon-alpha in recurrent respiratory papillomatosis: 20-year follow-up. Ann Otol Rhinol Laryngol. (2005) 114:463-71. doi: 10.1177/000348940511400608
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Zprávy z konference, která se konala v roce 2005 v Praze. Jackowska J, Piersiala K, Klimza H, Wierzbicka M. Outcomes of bevacizumab and cidofovir treatment in HPV-associated recurrent respiratory papillomatosis-review of the literature. Otolaryngol Pol. (2018) 72:1-8. doi: 10.5604/01.3001.0012.0484
PubMed Abstract | CrossRef Text | Google Scholar
9. Vydání publikace v angličtině. McMurray JS, Connor N, Ford CN. Účinnost cidofoviru u recidivující respirační papilomatózy: randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie. Ann Otol Rhinol Laryngol. (2008) 117:477-83. doi: 10.1177/000348940811700702
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Vyzkoušeno v roce 2008. Chadha NK. Intralezionální cidofovir u recidivující respirační papilomatózy: systematický přehled účinnosti a bezpečnosti. J Laryngol Voice. (2011) 1:22-6. doi: 10.4103/2230-9748.76133
CrossRef Full Text | Google Scholar
11. Zprávy o léčbě chřipkových onemocnění. Broekema FI, Dikkers FG. Vedlejší účinky cidofoviru při léčbě recidivující respirační papilomatózy. Eur Arch Otorhinolaryngol. (2008) 265:871-9. doi: 10.1007/s00405-008-0658-0
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Zprávy o léčbě kardiovaskulárních onemocnění. Dancey DR, Chamberlain DW, Krajden M, Palefsky J, Alberti PW, Downey GP. Úspěšná léčba multicystického plicního onemocnění souvisejícího s juvenilní laryngeální papilomatózou pomocí cidofoviru: kazuistika a přehled literatury. Chest. (2000) 118:1210-4. doi: 10.1378/chest.118.4.1210
PubMed Abstract | CrossRef Full Text | Google Scholar
13. září 2000. Ksiazek J, Prager JD, Sun GH, Wood RE, Arjmand EM. Inhalační cidofovir jako adjuvantní léčba recidivující respirační papilomatózy. Otolaryngol Head Neck Surg. (2011) 144:639-41. doi: 10.1177/0194599810395353
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Děkuji. Abramson AL, Shikowitz MJ, Mullooly VM, Steinberg BM, Amella CA, Rothstein HR. Klinické účinky fotodynamické terapie recidivujících papilomů hrtanu. Arch Otolaryngol Head Neck Surg. (1992) 118:25-9. doi: 10.1001/archotol.1992.01880010029011
PubMed Abstract | CrossRef Full Text | Google Scholar
15. září 1992. Feyh J, Kastenbauer E. Léčba papilomatózy hrtanu fotodynamickou laserovou terapií. Laryngorhinootologie. (1992) 71:190-2.
PubMed Abstract | Google Scholar
16. Laryngologie a laryngologie. Lieder A, Khan MK, Lippert BM. Fotodynamická terapie recidivující respirační papilomatózy. Cochrane Database Syst Rev. (2014) 5:CD009810. doi: 10.1002/14651858.CD009810.pub2
CrossRef Full Text | Google Scholar
17. Cochrane Database Syst Rev. (2014) 5:CD009811. Rosen CA, Bryson PC. Indol-3-karbinol u recidivující respirační papilomatózy: dlouhodobé výsledky. J Voice. (2004) 18:248-53. doi: 10.1016/j.jvoice.2003.05.005
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Vyzkoušejte si, jak se vám bude dařit při léčbě papilomatózy. Wu R, Abramson AL, Shikowitz MJ, Dannenberg AJ, Steinberg BM. Epidermálním růstovým faktorem indukovaná exprese cyklooxygenázy-2 je u recidivujících respiračních papilomů zprostředkována fosfatidylinositol-3 kinázou, nikoliv mitogenem aktivovaným proteinem/extracelulárním signálem regulovanou kinázou. Clin. Cancer Res. (2005) 11:6155-61. doi: 10.1158/1078-0432.CCR-04-2664
CrossRef Full Text | Google Scholar
19. Cancer Res. Limsukon A, Susanto I, Soo Hoo GW, Dubinett SM, Batra RK. Regrese recidivující respirační papilomatózy při kombinované léčbě celekoxibem a erlotinibem. Chest. (2009) 136:924-6. doi: 10.1378/chest.08-2639
PubMed Abstract | CrossRef Full Text | Google Scholar
20. září 2009. McKenna M, Brodsky L. Extraezofageální kyselý reflux a recidivující respirační papilom u dětí. Int. J. Pediatr. Otorhinolaryngol. (2005) 69:597-605. doi: 10.1016/j.ijporl.2004.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Srov. např. Borkowski G, Sommer P, Stark T, Sudhoff H, Luckhaupt H. Recurrent respiratory papillomatosis associated with gastroesophageal reflux disease in children. Eur Arch Otorhinolaryngol. (1999) 256:370-2. doi: 10.1007/s004050050166
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Vydáno v roce 1999. Holland BW, Koufman JA, Postma GN, McGuirt WF Jr. Laryngofaryngeální reflux a tvorba hrtanové sítě u pacientů s dětskými recidivujícími respiračními papilomy. Laryngoscope. (2002) 112:1926-9. doi: 10.1097/00005537-200211000-00003
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Laryngologický časopis. San Giorgi MRM, Helder HM, Lindeman RJS, de Bock GH, Dikkers FG. The Association between gastroesophageal reflux disease and recurrent respiratory papillomatosis: a systematic review. Laryngoscope. (2016) 126:2330-9. doi: 10.1002/lary.25898
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Vydáno v roce 2016. Derkay CS, Smith RJH, McClay J, van Burik JAH, Wiatrak BJ, Arnold J, et al. HspE7 treatment of pediatric recurrent respiratory papillomatosis: final results of an open-label trial. Ann Otol Rhinol Laryngol. (2005) 114:730-7. doi: 10.1177/000348940511400913
PubMed Abstract | CrossRef Full Text | Google Scholar
25. září 2005. Rosenberg T, Philipsen BB, Mehlum CS, Dyrvig AK, Wehberg S, Chirilǎ M, et al. Therapeutic use of the human papillomavirus vaccine on recurrent respiratory papillomatosis: a systematic review and meta-analysis. J Infect Dis. (2019) 219:1016-25. doi: 10.1093/infdis/jiy616
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Zprávy o prevenci infekčních onemocnění v České republice. Mudry P, Vavrina M, Mazanek P, Machalova M, Litzman J, Sterba J. Recurrent laryngeal papillomatosis: successful treatment with human papillomavirus vaccination. Arch Dis Child. (2011) 96:476-7. doi: 10.1136/adc.2010.198184
PubMed Abstract | CrossRef Text | Google Scholar
27. 1. 2011. Förster G, Boltze C, Seidel J, Pawlita M, Müller A. Juvenilní laryngeální papilomatóza – imunizace polyvalentní vakcínou gardasil. Laryngorhinootologie. (2008) 87:796-9. doi: 10.1055/s-2008-1077527
PubMed Abstract | CrossRef Full Text | Google Scholar
28. září 2008. Mauz PS, Schäfer FA, Iftner T, Gonser P. HPV vakcinace jako preventivní přístup k recidivující respirační papilomatóze – 22letá retrospektivní klinická analýza. BMC Infect Dis. (2018) 18:343. doi: 10.1186/s12879-018-3260-0
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Zprávy o prevenci infekcí proti HPV. Pashley NRT. Může vakcína proti příušnicím navodit remisi u recidivujícího respiračního papilomu? Arch Otolaryngol Head Neck Surg. (2002) 128:783-6. doi: 10.1001/archotol.128.7.783
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Meacham RK, Thompson JW. Srovnání cidofoviru a vakcíny proti spalničkám, příušnicím a zarděnkám při léčbě recidivující respirační papilomatózy. Ear Nose Throat J. (2017) 96:69-74. doi: 10.1177/014556131709600209
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Vědci, kteří se zabývají problematikou zhoubných novotvarů. Rahbar R, Vargas SO, Folkman J, McGill TJ, Healy GB, Tan X, et al. Role vaskulárního endoteliálního růstového faktoru-a u recidivující respirační papilomatózy. Ann Otol Rhinol Laryngol. (2005) 114:289-95. doi: 10.1177/000348940511400407
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Srov. např. Maturo S, Hartnick CJ. Použití 532-Nm pulzního draselného titanylfosfátového laseru a adjuvantního intralezionálního bevacizumabu u agresivní respirační papilomatózy u dětí: první zkušenosti. Arch Otolaryngol Head Neck Surg. (2010) 136:561-5. doi: 10.1001/archoto.2010.81
PubMed Abstract | CrossRef Full Text | Google Scholar
33. Vydání publikace v angličtině. Zeitels SM, Barbu AM, Landau-Zemer T, Lopez-Guerra G, Burns JA, Friedman AD, et al. Lokální injekce bevacizumabu (Avastin) a angiolytická léčba KTP laserem recidivující respirační papilomatózy hlasivek: prospektivní studie. Ann Otol Rhinol Laryngol. (2011) 120:627-34. doi: 10.1177/000348941112001001
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Sborník příspěvků z konference, která se konala v roce 2011 v Praze. Sidell DR, Nassar M, Cotton RT, Zeitels SM, de Alarcon A. Vysoké dávky sublesionálního bevacizumabu (Avastin) u recidivující respirační papilomatózy u dětí. Ann Otol Rhinol Laryngol. (2014) 123:214-21. doi: 10.1177/0003489414522977
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Děkuji. Mohr M, Schliemann C, Biermann C, Schmidt LH, Kessler T, Schmidt J, et al. Rapid response to systemic bevacizumab therapy in recurrent respiratory papillomatosis. Oncol Lett. (2014) 8:1912-8. doi: 10.3892/ol.2014.2486
PubMed Abstract | CrossRef Full Text | Google Scholar
36. V roce 2014 se uskutečnil první ročník mezinárodní konference o léčbě papilomatózy. Fernandez-Bussy S, Labarca G, Vial MR, Soto R, Mehta HJ, Jantz M, et al. Recurrent respiratory papillomatosis and bevacizumab treatment. Am J Respir Crit Care Med. (2017) 197:539-41. doi: 10.1164/rccm.201702-0279LE
PubMed Abstract | CrossRef Full Text | Google Scholar
37. Srov. např. Bedoya A, Glisinski K, Clarke J, Lind RN, Buckley CE, Shofer S. Systemic bevacizumab for recurrent respiratory papillomatosis: a single center experience of two cases. Am J Case Rep. (2017) 18:842-6. doi: 10.12659/AJCR.904416
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Zjistěte, jaká je situace v tomto případě. Zur KB, Fox E. Chemoterapie bevacizumabem při léčbě plicní a laryngotracheální papilomatózy u dítěte. Laryngoskop. (2017) 127:1538-42. doi: 10.1002/lary.26450
PubMed Abstract | CrossRef Full Text | Google Scholar
39. Laryngoskopie. Best SR, Mohr M, Zur KB. Systémový bevacizumab u recidivující respirační papilomatózy: národní průzkum. Laryngoscope. (2017) 127:2225-9. doi: 10.1002/lary.26662
PubMed Abstract | CrossRef Full Text | Google Scholar
.