Introduktion
Recidiverande respiratorisk papillomatos (RRP) är en kronisk sjukdom som orsakas av humant papillomvirus (HPV), vanligen typ 6 och 11. Läsionerna vid RRP uppträder oftast i larynx (figur 1), men kan också uppstå i munnen, luftstrupen, bronkerna, lungparenkymet och matstrupen. Den juvenila formen av RRP, där symtomen uppträder före 12 års ålder, är mer aggressiv än den vuxna formen, och symtomen är allvarligare. Papillomåterfallet är särskilt snabbt hos barn under 3 år, som upplever kortare intervaller mellan kirurgiska ingrepp och därmed fler operationer totalt sett. Sannolikheten att infektionen sprider sig utanför struphuvudet och förekomsten av trakeostomi, för att hjälpa till att hålla luftstrupen öppen, är också större i denna population (1). Patienter med RRP med juvenil debut genomgår i genomsnitt 20 kirurgiska ingrepp, varav de flesta i barndomen (2).
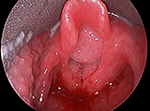
Figur 1. Direkt laryngoskopisk bild av stor skrymmande luftvägspapillomatos som blockerar larynxintaget.
Den traditionella kirurgiska metoden för kirurgisk extirpation innebar klassiskt sett KTP- (kaliumtitanylfosfat) eller koldioxidlaser (3). Med tanke på de potentiellt allvarliga biverkningarna av laserablation, inklusive brännskador i luftvägarna och ärrbildning i larynx, har mikrodebrider blivit ett alltmer populärt kirurgiskt verktyg, särskilt bland barn- och öronläkare, för skrymmande sjukdomar (3). Denna handhållna anordning kan avlägsna den sjuka vävnaden mer exakt och minska skadorna på omgivande vävnader (3). Med tanke på den aggressiva karaktären hos juvenil RRP är debrideringar dock fortfarande frekventa, och med tiden slits den underliggande vävnaden fortfarande avsevärt, med hög förekomst av ärrbildning. Därför har flera medicinska behandlingar undersökts för att förbättra resultatet av kirurgi, genom att förlänga tiden mellan operationerna eller genom att minimera återfall av RRP-lesioner.
Interferon α
Interferon α, ett protein som produceras av leukocyter som reaktion på olika stimuli, inklusive virusinfektion, var en av de första potentiella medicinska behandlingar som studerades (4). Dess värde som adjuvant behandling är kontroversiellt. I en stor studie av 85 barn och 84 vuxna avslutade 58 % av barnen den ettåriga behandlingsperioden med intramuskulära interferon α-injektioner tre gånger i veckan utan tecken på RRP (5). Frekvensen av papillomåterfall minskade hos 74 % av alla behandlade barn (5). I en randomiserad kontrollstudie med 123 patienter under 21 år var dock den minskade tillväxten av papillom i experimentgruppen som fick intramuskulära interferon α-injektioner inte hållbar under den ettåriga behandlingen (6). På samma sätt visade en annan studie att 20 år efter avslutad behandling med interferon α visade endast 42 % av patienterna på ett långsiktigt svar, och alla som fick återfall hade den juvenila debutformen av RRP (7). De flesta studier som undersöker interferon α har också rapporterat allvarliga biverkningar, som neurologiska störningar, leukopeni och trombocytopeni (5). Av dessa skäl har dess användning av pediatriska otolaryngologer minskat och rekommenderas i allmänhet inte (1). År 2014 fick endast 4 % av barnen med RRP interferon α som adjuvant behandling (1).
Cidofovir
Detta antivirala läkemedel med brett spektrum som hämmar virala DNA-polymeraser har visat sig vara lovande som adjuvant intralesional behandling till kirurgi för RRP. Intralesionella cidofovirinjektioner är den vanligaste medicinska behandlingen för RRP bland barnöronläkare (1). Alla artiklar som publicerades mellan 1998 och 2011 och som undersökte effekten av intralesionell cidofovir rapporterade minst ett fall av sjukdomsremiss (8). Eftersom de flesta av dessa studier är okontrollerade fallstudier är det dock oklart om fördelarna orsakas av Cidofovir eller om de är en del av sjukdomens naturliga förlopp. I en randomiserad kontrollstudie konstaterades att det inte fanns några statistiskt signifikanta skillnader i papillomets svårighetsgrad eller hälsorelaterad livskvalitet mellan en kontrollgrupp, som behandlades med kirurgiska ingrepp vid behov och intralesionella injektioner av koksaltlösning, och experimentgruppen, som behandlades med kirurgi och intralesionellt Cidofovir, efter 12 månaders behandling (9). Båda grupperna upplevde en signifikant minskning av sjukdomens svårighetsgrad under årets lopp, vilket tyder på att sjukdomen kan regrediera med tiden på egen hand (9). En annan genomgång som tittade på 27 studier av Cidofovir-administration, alla publicerade före 2011, visade att den genomsnittliga andelen fullständig remission med cidofovir var 37 % i pediatriska studier (10). Det har också funnits en del allvarliga biverkningar i samband med cidofovir, eftersom en genomgång visade att 1,7 och 1 % av 447 RRP-patienter drabbades av malign omvandling respektive nefrotoxicitet (8). Andra biverkningar är hudutslag, huvudvärk och ärrbildning i stämbanden (11). Med tanke på dessa potentiella komplikationer och avsaknaden av ett accepterat protokoll för dosering eller administreringsfrekvens är detta läkemedel inte ett tillförlitligt adjuvans (4).
Cidofovir har också administrerats som en systemisk snarare än lokal behandling för RRP-fall som kompliceras av lungsjukdom. Fyra enstaka fallstudier har visat att intravenöst cidofovir ledde till remission av sjukdomen, vilket inte är den normala utvecklingen av sjukdomen med lunginblandning (11). I alla dessa studier användes hyperhydrering och probenecid, en urinsyrareducerare, för att minska risken för nefrotoxicitet (11). Endast en patient fick biverkningar, partiell alopeci och leukopeni, av en kombinationsbehandling med cidofovir och interferon (12). Doserna av båda läkemedlen minskades som svar på detta. Arton månader efter avslutad behandling hade patienten endast behövt opereras för RRP en gång och hennes lungsjukdom hade stabiliserats (12).
En ny metod för tillförsel av cidofovir är inhalation. Få studier har undersökt effekten av denna metod, men den kan vara lovande för patienter som inte har svarat på andra former av behandling, som en 4 månader gammal pojke som trots mikrodebrideringar varannan vecka och intralesionella Cidofovir- och intravenösa interferon α-injektioner upplevde försämrade symtom (13). Inom 6 veckor av 40 mg nebuliserat Cidofovir dagligen, 12 dagar på och 2 dagar av, ökade tiden mellan debrideringarna (13). Sex månader senare uppvisade patienten inga symtom (13). Sammanfattningsvis kan man säga att även om Cidofovir i olika administreringsformer fortfarande används i stor utsträckning, är dess behandlingsresultat i bästa fall blandade och dess potential för biverkningar är något begränsande.
Fotodynamisk terapi
Fotodynamisk terapi (PDT) innebär att en ljuskänslig substans, en s.k. fotokänslig substans, som kallas fotokänslig, introduceras oralt eller genom injektion i den sjuka vävnaden och att substansen aktiveras med laserljus för att framkalla nekros. En av de stora fördelarna med PDT är förmågan att förstöra tumörer utan att påverka omgivande vävnad (4). Fallstudier har visat betydligt långsammare återväxt av papillom kort efter PDT, administrerad som adjuvant eller fristående behandling, och i vissa fall avsaknad av sjukdom efter flera veckor (14, 15). Det har endast funnits ett fåtal randomiserade kontrollstudier för att undersöka effekten av PDT, men i den senaste konstaterades att sjukdomen återkom efter 3-5 år, sannolikt på grund av att den genererar sin effekt genom ett kortsiktigt immunsvar (16). Ytterligare forskning bör genomföras för att fastställa dess effekt och säkerhet.
Indol-3-karbinol
Indol-3-karbinol, som finns i höga koncentrationer i korsblommiga grönsaker som broccoli och kål, modifierar östrogenmetabolismen för att förändra cellulär proliferation och DNA-syntes. Den senaste kliniska studien visade att efter att ha tagit indol-3-karbinol två gånger om dagen, med en dos på 200 mg för vuxna och viktbestämda doser för barn, i genomsnitt 50,2 månader, upplevde 70 % av försökspersonerna antingen ett fullständigt eller partiellt svar (17). Av de pediatriska patienterna upplevde en en fullständig respons, tre en partiell respons och fem ingen respons alls (17). Det är oklart varför vuxna patienter svarade bättre på indol-3-karbinol än pediatriska patienter. Den mindre aggressiva karaktären hos RRP hos vuxna kan vara en faktor. Med tanke på de föga lovande resultaten i den pediatriska populationen har det inte gjorts mycket mer forskning om behandling av juvenil begynnande RRP med av indol-3-karbinol.
Celecoxib
Celecoxib är ett antiinflammatoriskt läkemedel som hämmar cyklooxygenas-2 (COX-2), ett enzym som leder till inflammation och smärta, och används vanligtvis för att behandla artrit. In-vitro-studier har visat att papillomceller överuttrycker COX-2 som ett resultat av ökad signalering från den epidermala tillväxtfaktorreceptorn (EGFR) och att denna aktivitet är viktig för deras tillväxt (18). En kombinationsbehandling av celecoxib och erlotinib, en EGFR-kinashämmare, hjälpte till att kontrollera progressiv RRP hos en 58-årig man a genom att bromsa papillomtillväxten, vilket gjorde ytterligare kirurgi onödig (19). En pågående randomiserad kontrollstudie som sponsras av Northwell Health syftar till att fastställa om celecoxib kan minska återfallsfrekvensen av papillom hos både vuxna och pediatriska patienter (4).
Antirefluxmedicinering
Fallstudier har visat att behandling av gastroesofageal refluxsjukdom (GERD) med antirefluxmedicinering hos patienter med RRP av juvenil karaktär kan bidra till att bromsa återväxten av papillom (20, 21). I en studie fick patienter som inte följde GERD-behandlingen återfall (20). En retrospektiv journalgranskning visade också att barnpatienter som behandlades för RRP och som inte behandlades för reflux var betydligt mer benägna att utveckla larynxvävar efter det kirurgiska avlägsnandet av papillom (22). Även om det inte finns några entydiga bevis för att GERD förvärrar RRP, är det vettigt att hantera det för patienter som har klinisk presentation av GERD och komplicerade, progressiva fall av RRP (23).
Heat Shock Protein
Av de 700 barn med RRP som behandlades av 74 pediatriska otolaryngologer, som tillfrågades om deras användning av adjuvant behandling, fick 11 patienter HSP-E7, ett rekombinant fusionsprotein som består av heat shock protein 65 (Hsp65) och E7-proteinet från HPV typ 16 (1). HSP-E7 har undersökts som behandling vid flera sjukdomar som härrör från HPV, bland annat genitala vårtor och intraepitelial neoplasi (24). Det finns belägg för att det kan vara reaktivt mot fler HPV-stammar än bara HPV 16 (24). I en öppen studie med 27 pediatriska RRP-patienter förlängdes medianintervallet mellan operationerna efter behandling med HSP-E7 signifikant jämfört med medianintervallet före behandling (24). Det fanns få komplikationer, endast milda till måttliga reaktioner på injektionsstället. Även om det inte finns några pågående kliniska prövningar för att undersöka effekten av Hsp-E7 är det en lovande behandling.
HPV-vaccin
Ett fåtal fallrapporter och studier har dokumenterat användningen av HPV-vaccinet som adjuvantbehandling. Det finns för närvarande tre godkända HPV-vacciner: det bivalenta Cervarix, det tetravalenta Gardasil och det icke-avalenta Gardasil 9. Det tetravalenta vaccinet riktar sig mot HPV-6, HPV-11, HPV-16 och HPV-18. I en nyligen genomförd systematisk genomgång och metaanalys konstaterades att den genomsnittliga varaktigheten mellan operationerna hos 63 unga och vuxna RRP-patienter ökade signifikant efter HPV-vaccination, från 7 till 34 månader i genomsnitt (25). Studien fann inga signifikanta skillnader beroende på ålder när RRP uppstod (25). Andra fallstudier som inte ingick i metaanalysen har också visat på Gardasils effektivitet hos pediatriska patienter, eftersom den ökar tiden mellan operationerna avsevärt eller i vissa fall orsakar fullständig remission (26, 27).
Intramuskulär HPV-vaccination kan vara mer effektiv än tidigare identifierade, vanligare behandlingar som intralesionell cidofovir. I en retrospektiv fallstudie som följde unga och vuxna RRP-patienter i 22 år fann man att endast två av de 13 patienter som behandlades med kirurgi och Gardasil fick återfall, medan alla kontrollpatienter, som behandlades med kirurgi och Cidofovir, fick papillomåterväxt (28). Den genomsnittliga tiden till sjukdomsåterfall var också betydligt längre hos de behandlade patienterna än hos kontrollerna (28).
En av de mest lovande aspekterna av HPV som adjuvant behandling är att den inte har några allvarliga biverkningar. Dessutom kan förekomsten av juvenil RRP totalt sett minska med ökande vaccinationsfrekvens, eftersom denna form av sjukdomen vanligen förvärvas när ett barn utsätts för genitala vårtor orsakade av HPV 6- eller 11-virus under förlossningen (4).
Vaccin mot påssjuka
Det har gjorts mycket få studier om effekten av påssjukevaccinet som adjuvant terapi, även om den nuvarande forskningen är lovande. I en fallstudie konstaterades att remission inducerades hos nio av elva pediatriska patienter som behandlades med intralesionella injektioner av vaccinet med 3-12 veckors mellanrum tillsammans med laserkirurgi (29). I en retrospektiv studie som jämförde cidofovir och vaccinet mot mässling, påssjuka och röda hund (MMR) som adjuvansbehandlingar i en pediatrisk population fann man att det inte fanns några signifikanta skillnader mellan de barn som behandlades med intralesionella cidofovir- och MMR-injektioner efter debrideringar (30).
Bevacizumab
Bevacizumab är en human monoklonal antikropp som binder till och förhindrar interaktionen mellan vascular endothelial growth factor (VEGF) och receptorer. VEGF-aktivitet har en roll i RRP-utvecklingen, eftersom in vitro-studier har visat ett starkt uttryck av VEGF-A i papillomepitel och uttryck av VEGFR-1 och VEGFR-2 messenger RNA i underliggande vaskulära endotelceller (31).
De första studierna som tittade på bevacizumab som behandling av RRP undersökte nyttan av intralesionella injektioner som en adjuvant terapi till kirurgi. I en studie av tre patienter mellan 3 och 6 år med svår RRP (dvs. med minst fyra ingrepp per år) fann man att alla patienter upplevde ökad tid mellan kirurgisk debridering och pulsad KTP-laserbehandlingar och mindre svår RRP flera veckor efter avslutad bevacizumabbehandling jämfört med tidigare (32). De visade också förbättrad röstrelaterad livskvalitet (32).
Bortsett från fallrapporter har fallkontrollstudier också genomförts för att undersöka effekten av bevacizumab som adjuvant behandling. Efter 532 nm KTP-laserbehandling följt av sublesionella injektioner av bevacizumab i det mer sjuka stämlocket och injektioner av saltlösning i det andra locket hade 16 av 20 vuxna patienter med bilateral RRP i stämlocket färre papillom i det behandlade locket, vilket fastställdes genom endoskopisk avbildning (33). Tre av de 20 patienterna hade ingen sjukdom i båda vikarna och ingen av patienterna upplevde några komplikationer till följd av behandlingen (33).
Baserat på dessa lovande resultat genomfördes en större studie för att undersöka effekten av bevacizumab i en pediatrisk population. Hos 10 barn mellan 18 månader och 18 år med progressiv, icke-responsiv RRP ökade tre intralesionella bevacizumabinjektioner på 2,5 mg/ml med 2-3 veckors mellanrum, tillsammans med laserbehandling, medianlängden mellan kirurgiska ingrepp, minskade medianantalet ingrepp per år och förbättrade den röstrelaterade livskvaliteten (3). En av begränsningarna i studien är att doseringen är en uppskattning baserad på doser inom pediatrisk oftalmologi. Mängden som injicerades i paillomerna var inte heller densamma för varje patient, eftersom den varierade beroende på sjukdomens svårighetsgrad.
I vissa studier har man försökt fastställa optimala doser. I en annan studie där man undersökte nio pediatriska patienter med RRP med juvenil debut fann man också att efter en serie av fem subepiteliella injektioner som administrerades med 4-6 veckors mellanrum, med en genomsnittlig dos på 14,25 mg, tillsammans med KTP-laserablation, upplevde alla nio patienterna (med en medianålder på 8 år) att tidsintervallet mellan injektionerna ökade (34). Dessa resultat indikerar att visade att visade att högdosbehandling med bevacizumab inte har några komplikationer och kan vara mycket effektiv.
Efter bevis som visade effekten av intralesionellt bevacizumab vände sig forskningen till att behandla systemiskt bevacizumab, som är en särskilt lovande behandling för patienter med komplexa diagnoser. Den första rapporten om intravenös administrering visade att med en median på 6 kurer i doser på 5, 10, 15 mg/kg visade alla behandlade patienter med progressiv RRP papillomregression (35). Patienterna omfattade fyra fall av RRP med vuxen debut och ett fall med juvenil debut. De fem patienterna genomgick tillsammans 18 kirurgiska ingrepp året före bevacizumab, men endast det vuxna fallet krävde kirurgi efter behandlingen på grund av en malign omvandling året därpå (35).
Andra enstaka fallrapporter har bekräftat effekten av systemiskt bevacizumab utan att finna komplikationer, även om de flesta av dessa är hos vuxna patienter. Hos en 42-årig man med svår trakeal RRP bidrog en låg dos på 5 mg/kg, som med tiden ökades till 10 mg/kg bevacizumab, till att man uppnådde sjukdomsregression 3 månader efter det att behandlingen upphörde (36). En uppföljning efter 12 månader visade att patienten förblev sjukdomsfri. Sex kurer av systemisk bevacizumabbehandling med 5 mg/kg varannan vecka för en 87-årig patient som inte hade svarat på intralesionell cidofovir, en endobronchial stent eller HPV-vaccination, bidrog också till att uppnå en signifikant minskning av lobens massa och en patenterad bronk (37). Efter två kurer med 10 mg/kg intravenösa injektioner varannan vecka uppvisade en 63-åring med svår RRP mindre lunginvolvering och inga tecken på trakeal obstruktion (37).
Den enda publicerade fallrapporten om barn handlar om en 12-årig kvinna med progressiv laryngotrakeal papillomatos och lunginvolvering, som efter tre månaders påbörjad behandling med systemisk bevacizumab uppvisade ett partiellt svar i larynx och ett nästan fullständigt svar i trakea (38). Efter 5 månader uppvisade patienten inte längre någon lunginvolvering. Dessa resultat är ännu mer imponerande med tanke på att patienten under en tioårsperiod hade inlett Gardasil, interferon, celecoxib, antirefluxmedicin, zitromycin och propranolol och inte svarat på något av dessa (38).
Systemisk bevacizumabs potential som behandling av de mest aggressiva formerna av RRP sammanfattas bäst av resultaten av en elektronisk undersökning av RRP Task Force of the American Society of Pediatric Otolaryngology, American Broncho-Esophagological Association och läkare som har behandlat RRP med systemisk bevacizumab (39). De 11 ifyllda enkäterna från nio medicinska centra visade att de flesta av de patienter som behandlades med bevacizumab hade en lång historia av RRP med juvenil debut och hade misslyckats med att visa hållbara svar på cidofovir, interferon och celecoxib. Läkarna gav behandling i intervallet 5-10 mg/kg per dos. Sju av de åtta behandlade patienterna hade ett partiellt svar och en visade ett fullständigt svar på behandlingen (39). Alla patienter upplevde ökad tid mellan operationerna, nu i storleksordningen månader. Hos tre av de fyra patienterna med lunginblandning visade tre av dem förbättring eller upplösning av lungpapillom och en visade stabilisering av sjukdomen. Endast två patienter upplevde mindre komplikationer, hemoptys och proteinuri.
För att fastställa den kausala effekten av bevacizumab, bestämma lämpliga doser och identifiera eventuella komplikationer måste randomiserade kontrollstudier och större fallkontrollstudier genomföras. Dessutom måste protokoll för att definiera behandlingens varaktighet och samtidigt kontrollera eventuella rebound-effekter utarbetas.
Slutsatser
Och även om en optimal, universellt effektiv medicinsk adjuvant terapi för RRP ännu inte har hittats, ger lovande resultat från RRP-vaccinering som ett terapeutiskt tillvägagångssätt tillsammans med användningen av systemiskt bevacizumab hopp om förbättrade resultat för dessa barn under de kommande åren. Optimala protokoll för behandling bör utvecklas inom en nära framtid.
Författarbidrag
Alla författare som anges har gjort ett väsentligt, direkt och intellektuellt bidrag till arbetet och godkänt det för publicering.
Intressekonfliktutlåtande
Författarna förklarar att forskningen utfördes i avsaknad av kommersiella eller ekonomiska relationer som skulle kunna tolkas som en potentiell intressekonflikt.
Den behandlande redaktören förklarade ett tidigare medförfattarskap med en av författarna DP.
1. Schraff S, Derkay CS, Burke B, Lawson L. American Society of Pediatric Otolaryngology members’ experience with recurrent respiratory papillomatosis and the use of adjuvant therapy. Arch Otolaryngol Head Neck Surg. (2004) 130:1039-42. doi: 10.1001/archotol.130.9.1039
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Krstic M, Pavlović JM, Stanković P, Milenković MT. Etiopatogenes av återkommande laryngeal papillomatos och aktuella behandlingsstrategier. Acta Med Medianae. (2014) 53:64-74. doi: 10.5633/amm.2014.0411
CrossRef Full Text | Google Scholar
3. Rogers DJ, Ojha S, Maurer R, Hartnick CJ. Användning av adjuvant intralesionell bevacizumab vid aggressiv respiratorisk papillomatos hos barn. JAMA Otolaryngol Head Neck Surg. (2013) 139:496-501. doi: 10.1001/jamaoto.2013.1810
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Carifi M, Napolitano D, Morandi M, Dall’Olio D. Återkommande respiratorisk papillomatos: nuvarande och framtida perspektiv. Ther Clin Risk Manag. (2015) 11:731-8. doi: 10.2147/TCRM.S81825
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Nodarse-Cuní H, Iznaga-Marín N, Viera-Alvarez D, Rodríguez-Gómez H, Fernández-Fernández H, Blanco-López Y, et al. Interferon alfa-2b som adjuvant behandling av återkommande respiratorisk papillomatos på Kuba: nationellt program (rapport 1994-1999). J Laryngol Otol. (2004) 118:681-7. doi: 10.1258/0022215042244741
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Healy GB, Gelber RD, Trowbridge AL, Grundfast KM, Ruben RJ, Price KN. Behandling av återkommande respiratorisk papillomatos med humant leukocytinterferon. New Engl J Med. (1988) 319:401-7. doi: 10.1056/NEJM198808183190704
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gerein V, Rastorguev E, Gerein J, Jecker P, Pfister H. Användning av interferon-alfa vid recidiverande respiratorisk papillomatos: 20 års uppföljning. Ann Otol Rhinol Laryngol. (2005) 114:463-71. doi: 10.1177/000348940511400608
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Jackowska J, Piersiala K, Klimza H, Wierzbicka M. Outcomes of bevacizumab and cidofovir treatment in HPV-associated recurrent respiratory papillomatosis-review of the literature. Otolaryngol Pol. (2018) 72:1-8. doi: 10.5604/01.3001.0012.0484
PubMed Abstract | CrossRef Full Text | Google Scholar
9. McMurray JS, Connor N, Ford CN. Cidofovirs effekt vid återkommande respiratorisk papillomatos: en randomiserad, dubbelblind, placebokontrollerad studie. Ann Otol Rhinol Laryngol. (2008) 117:477-83. doi: 10.1177/000348940811700702
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Chadha NK. Intralesional cidofovir för återkommande respiratorisk papillomatos: systematisk genomgång av effekt och säkerhet. J Laryngol Voice. (2011) 1:22-6. doi: 10.4103/2230-9748.76133
CrossRef Full Text | Google Scholar
11. Broekema FI, Dikkers FG. Biverkningar av cidofovir vid behandling av återkommande respiratorisk papillomatos. Eur Arch Otorhinolaryngol. (2008) 265:871-9. doi: 10.1007/s00405-008-0658-0
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Dancey DR, Chamberlain DW, Krajden M, Palefsky J, Alberti PW, Downey GP. Framgångsrik behandling av juvenil laryngeal papillomatosrelaterad multicystisk lungsjukdom med cidofovir: fallrapport och litteraturgenomgång. Chest. (2000) 118:1210-4. doi: 10.1378/chest.118.4.1210
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Ksiazek J, Prager JD, Sun GH, Wood RE, Arjmand EM. Inhalerad cidofovir som adjuvant behandling av återkommande respiratorisk papillomatos. Otolaryngol Head Neck Surg. (2011) 144:639-41. doi: 10.1177/0194599810395353
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Abramson AL, Shikowitz MJ, Mullooly VM, Steinberg BM, Amella CA, Rothstein HR. Kliniska effekter av fotodynamisk terapi på återkommande larynxpapillom. Arch Otolaryngol Head Neck Surg. (1992) 118:25-9. doi: 10.1001/archotol.1992.01880010029011
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Feyh J, Kastenbauer E. Behandling av laryngeal papillomatos med fotodynamisk laserterapi. Laryngorhinootologi. (1992) 71:190-2.
PubMed Abstract | Google Scholar
16. Lieder A, Khan MK, Lippert BM. Fotodynamisk terapi för återkommande respiratorisk papillomatos. Cochrane Database Syst Rev. (2014) 5:CD009810. doi: 10.1002/14651858.CD009810.pub2
CrossRef Full Text | Google Scholar
17. Rosen CA, Bryson PC. Indol-3-karbinol för återkommande respiratorisk papillomatos: långtidsresultat. J Voice. (2004) 18:248-53. doi: 10.1016/j.jvoice.2003.05.005
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Wu R, Abramson AL, Shikowitz MJ, Dannenberg AJ, Steinberg BM. Epidermal tillväxtfaktor-inducerat uttryck av cyklooxygenas-2 medieras genom fosfatidylinositol-3 kinas, inte mitogenaktiverat protein/extracellulärt signalreglerat kinaskinas, i återkommande respiratoriska papillom. Clin. Cancer Res. (2005) 11:6155-61. doi: 10.1158/1078-0432.CCR-04-2664
CrossRef Full Text | Google Scholar
19. Limsukon A, Susanto I, Soo Hoo GW, Dubinett SM, Batra RK. Regression av återkommande respiratorisk papillomatos med kombinationsbehandling med celecoxib och erlotinib. Chest. (2009) 136:924-6. doi: 10.1378/chest.08-2639
PubMed Abstract | CrossRef Full Text | Google Scholar
20. McKenna M, Brodsky L. Extraesofageal acid reflux och återkommande respiratoriska papillom hos barn. Int. J. Pediatr. Otorhinolaryngol. (2005) 69:597-605. doi: 10.1016/j.ijporl.2004.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Borkowski G, Sommer P, Stark T, Sudhoff H, Luckhaupt H. Recurrent respiratory papillomatosis associated with gastroesophageal reflux disease in children. Eur Arch Otorhinolaryngol. (1999) 256:370-2. doi: 10.1007/s00404050050166
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Holland BW, Koufman JA, Postma GN, McGuirt WF Jr. Laryngopharyngeal reflux och larynxvävbildning hos patienter med pediatriska återkommande respiratoriska papillom. Laryngoscope. (2002) 112:1926-9. doi: 10.1097/00005537-200211000-00003
PubMed Abstract | CrossRef Full Text | Google Scholar
23. San Giorgi MRM, Helder HM, Lindeman RJS, de Bock GH, Dikkers FG. Sambandet mellan gastroesofageal refluxsjukdom och återkommande respiratorisk papillomatos: en systematisk översikt. Laryngoscope. (2016) 126:2330-9. doi: 10.1002/lary.25898
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Derkay CS, Smith RJH, McClay J, van Burik JAH, Wiatrak BJ, Arnold J, et al. HspE7-behandling av återkommande respiratorisk papillomatos hos barn: slutresultat av en öppen studie. Ann Otol Rhinol Laryngol. (2005) 114:730-7. doi: 10.1177/000348940511400913
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Rosenberg T, Philipsen BB, Mehlum CS, Dyrvig AK, Wehberg S, Chirilǎ M, et al. Therapeutic use of the human papillomavirus vaccine on recurrent respiratory papillomatosis: a systematic review and meta-analysis. J Infect Dis. (2019) 219:1016-25. doi: 10.1093/infdis/jiy616
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Mudry P, Vavrina M, Mazanek P, Machalova M, Litzman J, Sterba J. Recurrent laryngeal papillomatosis: framgångsrik behandling med vaccination mot humant papillomvirus. Arch Dis Child. (2011) 96:476-7. doi: 10.1136/adc.2010.198184
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Förster G, Boltze C, Seidel J, Pawlita M, Müller A. Juvenil laryngeal papillomatos-immunisering med det polyvalenta vaccinet gardasil. Laryngorhinootologie. (2008) 87:796-9. doi: 10.1055/s-2008-1077527
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Mauz PS, Schäfer FA, Iftner T, Gonser P. HPV-vaccination som förebyggande metod för återkommande respiratorisk papillomatos – en 22-årig retrospektiv klinisk analys. BMC Infect Dis. (2018) 18:343. doi: 10.1186/s12879-018-3260-0
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Pashley NRT. Kan vaccin mot påssjuka framkalla remission vid återkommande respiratoriskt papillom? Arch Otolaryngol Head Neck Surg. (2002) 128:783-6. doi: 10.1001/archotol.128.7.783
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Meacham RK, Thompson JW. Jämförelse av cidofovir och vaccin mot mässling, påssjuka och röda hund vid behandling av återkommande respiratorisk papillomatos. Ear Nose Throat J. (2017) 96:69-74. doi: 10.1177/014556131709600209
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Rahbar R, Vargas SO, Folkman J, McGill TJ, Healy GB, Tan X, et al. Roll för vascular endothelial growth factor-a vid återkommande respiratorisk papillomatos. Ann Otol Rhinol Laryngol. (2005) 114:289-95. doi: 10.1177/000348940511400407
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Maturo S, Hartnick CJ. Användning av 532-Nm pulsad kaliumtitanylfosfatlaser och adjuvant intralesionellt bevacizumab för aggressiv respiratorisk papillomatos hos barn: inledande erfarenhet. Arch Otolaryngol Head Neck Surg. (2010) 136:561-5. doi: 10.1001/archoto.2010.81
PubMed Abstract | CrossRef Full Text | Google Scholar
33. Zeitels SM, Barbu AM, Landau-Zemer T, Lopez-Guerra G, Burns JA, Friedman AD, et al. Lokal injektion av bevacizumab (Avastin) och angiolytisk KTP-laserbehandling av återkommande respiratorisk papillomatos i stämbanden: en prospektiv studie. Ann Otol Rhinol Laryngol. (2011) 120:627-34. doi: 10.1177/000348941112001001
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Sidell DR, Nassar M, Cotton RT, Zeitels SM, de Alarcon A. Högdos sublesionellt bevacizumab (Avastin) för återkommande respiratorisk papillomatos hos barn. Ann Otol Rhinol Laryngol. (2014) 123:214-21. doi: 10.1177/0003489414522977
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Mohr M, Schliemann C, Biermann C, Schmidt LH, Kessler T, Schmidt J, et al. Snabbt svar på systemisk bevacizumabbehandling vid återkommande respiratorisk papillomatos. Oncol Lett. (2014) 8:1912-8. doi: 10.3892/ol.2014.2486
PubMed Abstract | CrossRef Full Text | Google Scholar
36. Fernandez-Bussy S, Labarca G, Vial MR, Soto R, Mehta HJ, Jantz M, et al. Återkommande respiratorisk papillomatos och behandling med bevacizumab. Am J Respir Crit Care Med. (2017) 197:539-41. doi: 10.1164/rccm.201702-0279LE
PubMed Abstract | CrossRef Full Text | Google Scholar
37. Bedoya A, Glisinski K, Clarke J, Lind RN, Buckley CE, Shofer S. Systemisk bevacizumab för återkommande respiratorisk papillomatos: erfarenhet från ett enda center av två fall. Am J Case Rep. (2017) 18:842-6. doi: 10.12659/AJCR.904416
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Zur KB, Fox E. Bevacizumab kemoterapi för behandling av lung- och laryngotrakeal papillomatos hos ett barn. Laryngoscope. (2017) 127:1538-42. doi: 10.1002/lary.26450
PubMed Abstract | CrossRef Full Text | Google Scholar
39. Best SR, Mohr M, Zur KB. Systemisk bevacizumab för återkommande respiratorisk papillomatos: en nationell undersökning. Laryngoscope. (2017) 127:2225-9. doi: 10.1002/lary.26662
PubMed Abstract | CrossRef Full Text | Google Scholar
.