Bevezetés
A visszatérő légúti papillomatózis (RRP) egy krónikus betegség, amelyet a humán papillomavírus (HPV), általában a 6. és 11. típus okoz. Az RRP elváltozásai leggyakrabban a gégében jelennek meg (1. ábra), de megjelenhetnek a szájban, a légcsőben, a hörgőkben, a tüdőparenchimában és a nyelőcsőben is. Az RRP fiatalkori megjelenésű formája, amelyben a tünetek 12 éves kor előtt jelentkeznek, agresszívabb, mint a felnőttkori forma, és a tünetek súlyosabbak. A papillóma kiújulása különösen gyors a 3 év alatti gyermekeknél, akiknél rövidebb időközök telnek el a műtéti beavatkozások között, és így összességében több műtétre kerül sor. A fertőzés gégén túli terjedésének valószínűsége és a légcső nyitva tartását segítő légcsőmetszés előfordulása is nagyobb ebben a populációban (1). A fiatalkori kezdetű RRP-ben szenvedő betegek átlagosan 20 műtéti beavatkozáson esnek át, amelyek többsége gyermekkorban történik (2).
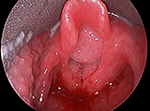
1. ábra. Közvetlen gégetükrözéses kép a gége bejáratát elzáró nagyméretű, terjedelmes légúti papillomatosisról.
A sebészi eltávolítás hagyományos sebészeti módszere klasszikusan KTP (kálium-titanilfoszfát) vagy szén-dioxid lézerrel történt (3). Tekintettel a lézeres abláció potenciálisan súlyos mellékhatásaira, beleértve a légúti égési sérüléseket és a gége hegesedését, a mikrodebriderek egyre népszerűbb műtéti eszközzé váltak, különösen a gyermek otolaryngológusok körében, a terjedelmes betegségek esetében (3). Ezzel a kézi eszközzel pontosabban lehet eltávolítani a beteg szövetet, csökkentve a környező szövetek károsodását (3). Tekintettel azonban a fiatalkori RRP agresszív jellegére, még mindig gyakoriak a tisztítások, és idővel még mindig jelentősen elhasználják a mögöttes szövetet, ami a hegképződés nagy gyakoriságával jár. Ezért számos orvosi terápiát vizsgáltak a műtétek eredményének javítására, a műtétek közötti idő meghosszabbításával vagy az RRP elváltozások kiújulásának minimalizálásával.
Interferon α
Az egyik első vizsgált lehetséges orvosi kezelés az interferon α volt, egy fehérje, amelyet a leukociták különböző ingerekre, többek között vírusfertőzésre reagálva termelnek (4). Adjuváns kezelésként való értéke ellentmondásos. Egy 85 gyermek és 84 felnőtt bevonásával végzett nagy vizsgálatban a gyermekek 58%-a fejezte be a hetente háromszor intramuszkuláris interferon α injekciót tartalmazó egyéves kezelési időszakot RRP bizonyítéka nélkül (5). A papillóma kiújulásának gyakorisága a kezelt gyermekek 74%-ánál csökkent (5). Egy 123 21 év alatti beteggel végzett randomizált kontrollvizsgálatban azonban az interferon α intramuszkuláris injekciókat kapó kísérleti csoportban a papillómák növekedési ütemének lassulása nem volt tartós az egyéves kezelés alatt (6). Hasonlóképpen egy másik vizsgálat azt találta, hogy 20 évvel az interferon α-kezelés befejezése után a betegeknek csak 42%-a mutatott hosszú távú választ, és mindazok, akik visszaestek, az RRP juvenilis kezdetű formáját mutatták (7). Az interferon α-t vizsgáló legtöbb tanulmány súlyos mellékhatásokról is beszámolt, például neurológiai zavarokról, leukopéniáról és trombocitopéniáról (5). Ezen okok miatt alkalmazása a gyermek fül-orr-gégészek körében visszaszorult, és általában nem ajánlott (1). 2014-ben az RRP-ben szenvedő gyermekek mindössze 4%-a kapott interferon α-t adjuváns terápiaként (1).
Cidofovir
Ez a széles spektrumú, vírusellenes gyógyszer, amely gátolja a vírus DNS-polimerázokat, ígéretesnek bizonyult az RRP műtétjének adjuváns intraléziós terápiájaként. Az intraléziós cidofovir-injekciók az RRP leggyakrabban alkalmazott gyógyszeres kezelése a gyermek fül-orr-gégészek körében (1). Az 1998 és 2011 között megjelent valamennyi, az intralezionális cidofovir hatékonyságát vizsgáló közlemény legalább egy esetben számolt be a betegség elmúlásáról (8). Mivel azonban e tanulmányok többsége nem kontrollált esettanulmány, nem világos, hogy az előnyöket a cidofovir okozta-e, vagy azok a betegség természetes lefolyásának részét képezik. Egy randomizált kontrollvizsgálat szerint 12 hónapos kezelés után nem volt statisztikailag szignifikáns különbség a papilloma súlyosságában vagy az egészséggel kapcsolatos életminőségben a szükség szerint sebészeti beavatkozásokkal és intraléziós sóoldat injekciókkal kezelt kontrollcsoport és a műtéttel és intraléziós Cidofovirral kezelt kísérleti csoport között (9). Mindkét csoportban a betegség súlyossága egy év alatt jelentősen csökkent, ami arra utal, hogy a betegség idővel magától is visszafejlődhet (9). Egy másik áttekintés, amely a cidofovir adagolásával kapcsolatos 27 tanulmányt vizsgált, amelyek mindegyike 2011 előtt jelent meg, azt találta, hogy a gyermekgyógyászati vizsgálatokban a cidofovirral elért átlagos teljes remissziós arány 37% volt (10). A cidofovirral kapcsolatban súlyos mellékhatások is előfordultak, mivel egy áttekintés szerint 447 RRP-s beteg 1,7, illetve 1%-ánál fordult elő rosszindulatú transzformáció, illetve nefrotoxicitás (8). Egyéb mellékhatások közé tartozik a bőrkiütés, a fejfájás és a hangszalagok hegesedése (11). Tekintettel ezekre a lehetséges szövődményekre és az adagolásra vagy a beadás gyakoriságára vonatkozó elfogadott protokoll hiányára, ez a gyógyszer nem megbízható adjuváns (4).
A cidofovirt szisztémás, nem pedig helyi kezelésként is alkalmazták a tüdőbetegséggel szövődményes RRP eseteiben. Négy egyedi esettanulmány kimutatta, hogy az intravénás cidofovir a betegség remissziójához vezetett, ami nem a betegség normális progressziója a tüdő érintettségével (11). Mindezekben a vizsgálatokban hyperhidrációt és probenecidet, húgysavcsökkentőt alkalmaztak a nefrotoxicitás esélyének csökkentése érdekében (11). A cidofovir és interferon kombinált terápiájának csak egy betegnél jelentkeztek mellékhatásai, részleges alopecia és leukopénia (12). Válaszul mindkét gyógyszer adagját csökkentették. Tizennyolc hónappal a kezelés befejezése után a betegnek csak egyszer volt szüksége műtétre RRP miatt, és tüdőbetegsége stabilizálódott (12).
A cidofovir beadásának újszerű módszere az inhaláció. Kevés tanulmány vizsgálta ennek a módszernek a hatékonyságát, de ígéretes lehet olyan betegek esetében, akik nem reagáltak más kezelési formákra, mint például egy 4 hónapos kisfiú, akinél a kéthetenkénti mikrodebridálás és az intraléziós Cidofovir- és intravénás interferon α-injekciók ellenére a tünetek súlyosbodtak (13). A napi 40 mg porlasztott Cidofovir 6 héten belül, 12 napon át és 2 napon át, a debridementek közötti idő megnövekedett (13). Hat hónappal később a beteg nem mutatott semmilyen tünetet (13). Összefoglalva, bár a Cidofovirt különböző alkalmazási formákban továbbra is széles körben alkalmazzák, kezelési eredményei a legjobb esetben is vegyesek, és a lehetséges mellékhatások némileg korlátozóak.
Fotodinamikai terápia
A fotodinamikai terápia (PDT) során egy fényérzékeny anyagot, úgynevezett fotoérzékenyítőt juttatnak szájon át vagy injekcióval a beteg szövetbe, és lézerfénnyel aktiválják az anyagot, hogy nekrózist idézzen elő. A PDT egyik fő előnye, hogy a környező szövetek érintése nélkül képes elpusztítani a daganatokat (4). Esettanulmányok azt mutatták, hogy az adjuváns vagy önálló terápiaként alkalmazott PDT-t követően a papillóma újranövekedése hamarosan jelentősen lelassult, és egyes esetekben a betegség néhány hét után már nem is jelentkezett (14, 15). A PDT hatását csak néhány randomizált kontrollvizsgálat vizsgálta, de a legutóbbi azt találta, hogy a betegség 3-5 év után kiújul, valószínűleg azért, mert hatását rövid távú immunválaszon keresztül fejti ki (16). További kutatásokat kell végezni a hatékonyságának és biztonságosságának megállapítására.
Indol-3-karbinol
A keresztesvirágú zöldségekben, például a brokkoliban és a káposztában nagy koncentrációban található indol-3-karbinol módosítja az ösztrogén anyagcserét, hogy megváltoztassa a sejtproliferációt és a DNS-szintézist. A legutóbbi klinikai vizsgálat megállapította, hogy az indol-3-karbinol napi kétszeri, felnőtteknél 200 mg-os, gyermekeknél súlytól függő dózisú, átlagosan 50,2 hónapig tartó szedése után az alanyok 70%-ánál teljes vagy részleges válasz lépett fel (17). A gyermekbetegek közül egy betegnél teljes, háromnál részleges, ötnél pedig egyáltalán nem volt válasz (17). Nem világos, hogy a felnőtt betegek miért reagáltak jobban az indol-3-karbinolra, mint a gyermekbetegek. A felnőttkori RRP kevésbé agresszív jellege lehet a tényező. Tekintettel a gyermekpopulációban elért nem túl biztató eredményekre, a fiatalkori RRP indol-3-karbinollal történő kezelésével kapcsolatban nem folytak további kutatások.
Celecoxib
A celecoxib egy gyulladáscsökkentő gyógyszer, amely gátolja a ciklooxigenáz-2 (COX-2) enzimet, amely gyulladáshoz és fájdalomhoz vezet, és általában ízületi gyulladás kezelésére használják. In-vitro vizsgálatok kimutatták, hogy a papillómasejtek a COX-2-t a fokozott epidermális növekedési faktor receptor (EGFR) jelátvitel következtében túlreprezentálják, és hogy ez az aktivitás fontos a növekedésükhöz (18). A celecoxib és az EGFR-kinázgátló erlotinib kombinált terápiája egy 58 éves férfi esetében a papillóma növekedésének lassításával segített kontrollálni a progresszív RRP-t, ami szükségtelenné tette a további műtétet (19). Egy folyamatban lévő, a Northwell Health által szponzorált randomizált kontrollvizsgálat célja annak meghatározása, hogy a celecoxib csökkenti-e a papillómák kiújulásának arányát felnőtt és gyermekbetegeknél egyaránt (4).
REFLUX-ellenes gyógyszeres kezelés
Egy esettanulmány kimutatta, hogy a gastrooesophagealis refluxbetegség (GERD) reflux-ellenes gyógyszeres kezelése fiatalkori RRP-ben szenvedő betegeknél segíthet a papillóma újranövekedésének lassításában (20, 21). Egy vizsgálatban azoknál a betegeknél, akik nem tartották be a GERD-kezelést, kiújulás következett be (20). Egy retrospektív kórlap-áttekintés azt is kimutatta, hogy azoknál az RRP miatt kezelt gyermekbetegeknél, akiket nem kezeltek reflux miatt, a papillómák műtéti eltávolítása után szignifikánsan nagyobb valószínűséggel alakultak ki gégehálózatok (22). Bár nincs meggyőző bizonyíték arra, hogy a GERD súlyosbítja az RRP-t, kezelésének van értelme azoknál a betegeknél, akiknél a GERD klinikai megjelenése és az RRP komplikált, progresszív esetei állnak fenn (23).
Hősokkfehérje
A 74 gyermek fül-orr-gégész által kezelt 700 RRP-s gyermek közül, akiket az adjuváns kezelés alkalmazásáról kérdeztek, 11 beteg kapott HSP-E7-et, egy rekombináns fúziós fehérjét, amely a 65-ös hősokkfehérjéből (Hsp65) és a HPV 16-os típusának E7 fehérjéjéből áll (1). A HSP-E7-et számos HPV-ből eredő betegség, köztük a genitális szemölcsök és az intraepiteliális neoplázia kezelésében vizsgálták (24). Bizonyítékok arra utalnak, hogy a HPV 16-os HPV-törzsnél több HPV-törzzsel szemben is reaktív lehet (24). Egy 27 gyermekkori RRP-s beteggel végzett nyílt vizsgálatban a HSP-E7 kezelését követően a műtétek közötti medián intervallum szignifikánsan meghosszabbodott a kezelés előtti mediánhoz képest (24). Kevés szövődmény fordult elő, csak enyhe vagy mérsékelt injekcióhelyi reakciók. Bár nincsenek folyamatban lévő klinikai vizsgálatok a Hsp-E7 hatékonyságának vizsgálatára, ez egy ígéretes kezelés.
HPV-vakcina
A HPV-vakcina adjuváns terápiaként való alkalmazását néhány esetjelentés és tanulmány dokumentálta. Jelenleg három engedélyezett HPV-vakcina létezik: a bivalens Cervarix, a tetravalens Gardasil és a nemavalens Gardasil 9. A tetravalens vakcina a HPV-6, HPV-11, HPV-16, HPV-18 ellen hat. Egy nemrégiben készült szisztematikus áttekintés és metaanalízis szerint 63 fiatalkorú és felnőtt RRP-s betegnél a műtétek közötti átlagos időtartam jelentősen, átlagosan 7-ről 34 hónapra nőtt a HPV-oltás után (25). A vizsgálat nem talált szignifikáns különbségeket az RRP kialakulásának életkora szerint (25). Más, a metaanalízisben nem szereplő esettanulmányok szintén kimutatták a Gardasil hatékonyságát gyermekbetegeknél, mivel jelentősen megnöveli a műtétek közötti időt, vagy egyes esetekben teljes remissziót okoz (26, 27).
A HPV-oltás hatékonyabb lehet, mint a korábban azonosított, elterjedtebb kezelések, például az intraléziós cidofovir. Egy retrospektív esettanulmány, amely 22 éven át követte a fiatalkori és felnőttkori RRP-s betegeket, azt találta, hogy a műtéttel és Gardasil-kezeléssel kezelt 13 beteg közül csak kettőnél alakult ki visszaesés, míg a műtéttel és cidofovirral kezelt kontrollbetegek mindegyikénél papilloma újranövekedést tapasztaltak (28). A betegség kiújulásáig eltelt átlagos idő is jelentősen hosszabb volt a kezelt betegeknél, mint a kontrolloknál (28).
A HPV mint adjuváns terápia egyik legígéretesebb aspektusa, hogy nincsenek súlyos mellékhatásai. Emellett az oltási arányok növekedésével a juvenilis RRP előfordulása összességében csökkenhet, mivel a betegségnek ezt a formáját általában akkor szerzik meg, amikor a csecsemő a szülés során a HPV 6 vagy 11 vírus által okozott genitális szemölcsökkel érintkezik (4).
Mumpszvakcina
A mumpszvakcina mint adjuváns terápia hatékonyságáról nagyon kevés tanulmány készült, bár a jelenlegi kutatások ígéretesek. Egy esettanulmány szerint 11 gyermekbetegből kilencnél sikerült remissziót előidézni, akiket a vakcina 3-12 hetes időközönkénti intraléziós injekcióival és lézeres műtéttel együtt kezeltek (29). Egy retrospektív tanulmány, amely a cidofovirt és a kanyaró, mumpsz és rubeola (MMR) vakcinát, mint adjuváns terápiát hasonlította össze egy gyermekpopulációban, azt találta, hogy nem volt jelentős különbség az intraléziós cidofovir- és MMR-injekciókkal kezelt gyermekek között a debriditumok után (30).
Bevacizumab
A bevacizumab humán monoklonális antitest, amely a vaszkuláris endoteliális növekedési faktor (VEGF) receptorokhoz kötődik és megakadályozza azok kölcsönhatását. A VEGF-aktivitásnak szerepe van az RRP kialakulásában, mivel in vitro vizsgálatok kimutatták a VEGF-A erős expresszióját a papilloma epitheliumában és a VEGFR-1 és VEGFR-2 hírvivő RNS-ek expresszióját a mögöttes érrendszeri endotélsejtekben (31).
A bevacizumabbal mint az RRP kezelésével foglalkozó első vizsgálatok az intraléziós injekciók előnyeit vizsgálták a műtétet kiegészítő terápiaként. Három, 3 és 6 év közötti, súlyos RRP-ben szenvedő (azaz évente legalább négy beavatkozással járó) beteg vizsgálatában azt találták, hogy valamennyi betegnél a bevacizumab-kezelés befejezése után néhány héttel a műtéti debridement és az impulzusos KTP-lézeres kezelések között hosszabb idő telt el, és a bevacizumab-kezelés befejezése után néhány héttel a korábbiakhoz képest kevésbé súlyos RRP-t tapasztaltak (32). A hanggal kapcsolatos életminőség javulását is kimutatták (32).
Az esetjelentések mellett esetkontrollvizsgálatokat is végeztek a bevacizumab mint adjuváns terápia hatékonyságának vizsgálatára. Az 532 nm-es KTP lézerkezelést, majd a betegebb hangszalagba szublézeres bevacizumab-injekciókat, illetve a másik hangszalagba sóoldatos injekciókat követően a 20 felnőtt, kétoldali hangszalag-RRP-ben szenvedő beteg közül 16-nál a kezelt hangszalagban kevesebb papilloma alakult ki, ahogy azt az endoszkópos képalkotás meghatározta (33). A 20 beteg közül háromnál nem volt betegség egyik hajtásban sem, és egyik betegnél sem lépett fel komplikáció a kezelés következtében (33).
Ezekre az ígéretes eredményekre alapozva egy nagyobb vizsgálatot végeztek a bevacizumab hatékonyságának vizsgálatára gyermekpopulációban. Tíz, 18 hónap és 18 év közötti, progresszív, nem reagáló RRP-ben szenvedő gyermeknél három, 2,5 mg/ml-es intraléziós bevacizumab-injekció 2-3 hét különbséggel, lézerterápiával együtt növelte a műtéti beavatkozások közötti medián időtartamot, csökkentette az évente elvégzendő beavatkozások medián számát, és javította a hanggal kapcsolatos életminőséget (3). A vizsgálat egyik korlátja, hogy az adagolás a gyermekszemészetben alkalmazott dózisok alapján becslés. A paillómákba beadott mennyiség sem volt minden betegnél azonos, mivel a betegség súlyossága alapján változott.
Egyes tanulmányok megpróbálták meghatározni az optimális adagokat. Egy másik vizsgálat, amely kilenc, fiatalkori kezdetű RRP-ben szenvedő gyermekbeteggel foglalkozott, szintén azt találta, hogy a 4-6 hetes időközönként beadott öt szubepithelialis injekció sorozatot követően, 14,25 mg átlagos dózis mellett, KTP lézer ablációval együtt, mind a kilenc betegnél (8 éves medián életkorral) megnőtt az injekciók közötti időintervallum (34). Ezek az eredmények azt mutatták, hogy a nagy dózisú bevacizumab-kezelésnek nincsenek szövődményei, és igen hatékony lehet.
Az intraléziós bevacizumab hatékonyságát bizonyító bizonyítékok után a kutatás a szisztémás bevacizumab felé fordult, amely különösen ígéretes kezelés a komplex diagnózisú betegek esetében. Az intravénás adagolásról szóló első beszámoló azt mutatta, hogy az 5, 10, 15 mg/kg dózisú 6 kúra mediánjával minden kezelt, progresszív RRP-ben szenvedő betegnél papilloma-regresszió következett be (35). A betegek között négy esetben felnőttkori, egy esetben pedig fiatalkori kezdetű RRP volt. Az öt beteg együttesen 18 sebészeti beavatkozáson esett át a bevacizumabot megelőző évben, de csak a felnőtt esetnél volt szükség műtétre a kezelés után, mert a következő évben rosszindulatú átalakulás következett be (35).
Más egyedi esetjelentések is alátámasztották a szisztémás bevacizumab hatékonyságát anélkül, hogy szövődményeket találtak volna, bár ezek többsége felnőtt betegeknél történt. Egy 42 éves, súlyos légcső-RRP-ben szenvedő férfinál a kezelés abbahagyása után 3 hónappal alacsony, 5 mg/kg-os dózisú, idővel 10 mg/kg bevacizumabra emelt adaggal sikerült elérni a betegség regresszióját (36). A 12 hónapos utánkövetés azt mutatta, hogy a beteg továbbra is betegségmentes maradt. Hat kúra szisztémás, kéthetente 5 mg/kg-os bevacizumab-kezelés egy 87 éves betegnél, aki nem reagált intraléziós cidofovirra, endobronchiális stentre vagy HPV-vakcinációra, szintén segített elérni a lebeny tömegének jelentős csökkenését és egy szabad hörgőt (37). Két, kéthetente 10 mg/kg intravénás injekciót követően egy 63 éves, súlyos RRP-ben szenvedő betegnél a tüdő érintettsége csökkent, és nem volt nyoma légcsőelzáródásnak (37).
Az egyetlen publikált gyermekkori esetleírás egy 12 éves, progresszív laryngotrachealis papillomatosisban és tüdőérintettségben szenvedő lányról szól, aki a szisztémás bevacizumab-kezelés megkezdése után 3 hónappal a gégében részleges, a légcsőben pedig csaknem teljes választ mutatott (38). A betegnél 5 hónap elteltével már nem volt tüdőérintettség. Ezek az eredmények még lenyűgözőbbek annak fényében, hogy a beteg 10 év alatt Gardasil, interferon, celecoxib, refluxellenes gyógyszer, zithromycin és propranolol kezelést kapott, és egyikre sem reagált (38).
A szisztémás bevacizumab potenciálját az RRP legagresszívebb formáinak kezelésében az Amerikai Gyermek-Otolaringológiai Társaság RRP munkacsoportja, az Amerikai Broncho-Esophagológiai Társaság és az RRP-t szisztémás bevacizumabbal kezelő orvosok elektronikus felmérésének eredményei foglalják össze a legjobban (39). A kilenc egészségügyi központból kapott 11 kitöltött felmérésből kiderült, hogy a bevacizumabbal kezelt betegek többsége régóta fiatalkori RRP-ben szenvedett, és nem mutatott tartós választ a cidofovirra, az interferonra és a celecoxibra. Az orvosok adagonként 5-10 mg/kg közötti kezelést adtak. A nyolc kezelt beteg közül hétnél részleges, egynél pedig teljes választ mutatott a kezelésre (39). Minden betegnél megnövekedett a műtétek közötti, immár hónapos nagyságrendű idő. A négy tüdőérintettségű beteg közül háromnál a tüdőpapillóma javulását vagy megszűnését, egynél pedig a betegség stabilizálódását mutatták ki. Csak két betegnél fordultak elő kisebb szövődmények, hemoptysis és proteinuria.
A bevacizumab okozati hatásának megállapításához, a megfelelő dózisok meghatározásához és az esetleges szövődmények azonosításához randomizált kontrollvizsgálatokat és nagyobb esetkontrollvizsgálatokat kell végezni. Ezenkívül ki kell dolgozni a kezelés időtartamát meghatározó protokollokat, miközben kontrollálni kell az esetleges visszaható hatásokat.
Következtetések
Noha az RRP optimális, általánosan hatékony gyógyszeres adjuváns terápiáját még nem találták meg, az RRP-vakcináció mint terápiás megközelítés ígéretes eredményei, valamint a szisztémás bevacizumab alkalmazása reményt adnak az elkövetkező években ezen gyermekek jobb kimenetelére. A közeljövőben optimális kezelési protokollokat kell kidolgozni.
A szerzők hozzájárulása
A felsorolt szerzők mindegyike jelentősen, közvetlenül és intellektuálisan hozzájárult a munkához, és jóváhagyta annak közzétételét.
Kérdések összeférhetetlenségi nyilatkozata
A szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségként értelmezhetők.
A kezelőszerkesztő a DP egyik szerzőjével való korábbi társszerzőségről nyilatkozott.
1. Schraff S, Derkay CS, Burke B, Lawson L. American Society of Pediatric Otolaryngology members’ experience with recurrent respiratory papillomatosis and the use of adjuvant therapy. Arch Otolaryngol Head Neck Surg. (2004) 130:1039-42. doi: 10.1001/archotol.130.9.1039
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Vizsgálatok a gyermekgyógyászatban és a gyermekgyógyászatban. Krstic M, Pavlović JM, Stanković P, Milenković MT. A recidiváló laryngealis papillomatosis etiopatogenezise és a kortárs kezelési stratégiák. Acta Med Medianae. (2014) 53:64-74. doi: 10.5633/amm.2014.0411
CrossRef Full Text | Google Scholar
3. Rogers DJ, Ojha S, Maurer R, Hartnick CJ. Adjuváns intralesionalis bevacizumab alkalmazása agresszív légúti papillomatosisban gyermekeknél. JAMA Otolaryngol Head Neck Surg. (2013) 139:496-501. doi: 10.1001/jamaoto.2013.1810
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Gyógyszerészi szakvélemény | CrossRef Full Text | Google Scholar
. Carifi M, Napolitano D, Morandi M, Dall’Olio D. Visszatérő légúti papillomatosis: jelenlegi és jövőbeli kilátások. Ther Clin Risk Manag. (2015) 11:731-8. doi: 10.2147/TCRM.S81825
PubMed Abstract | CrossRef Full Text | Google Scholar
5. 5. PubMed Abstract | CrossRef Full Text | Google Scholar
. Nodarse-Cuní H, Iznaga-Marín N, Viera-Alvarez D, Rodríguez-Gómez H, Fernández-Fernández H, Blanco-López Y, et al. Interferon alfa-2b mint a visszatérő légúti papillomatosis adjuváns kezelése Kubában: nemzeti program (1994-1999-es jelentés). J Laryngol Otol. (2004) 118:681-7. doi: 10.1258/0022215042244741
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Gyógyszerészi szakvélemény | CrossRef Full Text | Google Scholar
. Healy GB, Gelber RD, Trowbridge AL, Grundfast KM, Ruben RJ, Price KN. Visszatérő légúti papillomatosis kezelése humán leukocita interferonnal. New Engl J Med. (1988) 319:401-7. doi: 10.1056/NEJM198808183190704
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gerein V, Rastorguev E, Gerein J, Jecker P, Pfister H. Use of interferon-alpha in recurrent respiratory papillomatosis: 20-year follow-up. Ann Otol Rhinol Rhinol Laryngol. (2005) 114:463-71. doi: 10.1177/000348940511400608
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Gyógyszerészi szakvélemény | CrossRef Full Text | Google Scholar
. Jackowska J, Piersiala K, Klimza H, Wierzbicka M. A bevacizumab és cidofovir kezelés eredményei HPV-asszociált recidiváló légúti papillomatosisban – az irodalom áttekintése. Otolaryngol Pol. (2018) 72:1-8. doi: 10.5604/01.3001.0012.0484
PubMed Abstract | CrossRef Full Text | Google Scholar
9. PhD. McMurray JS, Connor N, Ford CN. A cidofovir hatékonysága visszatérő légúti papillomatosisban: randomizált, kettős vak, placebo-kontrollált vizsgálat. Ann Otol Rhinol Laryngol. (2008) 117:477-83. doi: 10.1177/000348940811700702
PubMed Abstract | CrossRef Full Text | Google Scholar
10. PubMed Abstract | CrossRef Full Text | Google Scholar
. Chadha NK. Intralesionalis cidofovir recidiváló légúti papillomatosis kezelésére: a hatékonyság és biztonságosság szisztematikus áttekintése. J Laryngol Voice. (2011) 1:22-6. doi: 10.4103/2230-9748.76133
CrossRef Full Text | Google Scholar
11. Google Scholar
11. Broekema FI, Dikkers FG. A cidofovir mellékhatásai a visszatérő légúti papillomatosis kezelésében. Eur Arch Otorhinolaryngol. (2008) 265:871-9. doi: 10.1007/s00405-008-0658-0
PubMed Abstract | CrossRef Full Text | Google Scholar
12. 12. Gyógyszerészi szakvizsga. Dancey DR, Chamberlain DW, Krajden M, Palefsky J, Alberti PW, Downey GP. A juvenilis gégepapillomatózissal összefüggő multicisztás tüdőbetegség sikeres kezelése cidofovirral: esetismertetés és az irodalom áttekintése. Chest. (2000) 118:1210-4. doi: 10.1378/chest.118.4.1210
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Ksiazek J, Prager JD, Sun GH, Wood RE, Arjmand EM. Inhalált cidofovir mint a visszatérő légúti papillomatosis adjuváns terápiája. Otolaryngol Head Neck Surg. (2011) 144:639-41. doi: 10.1177/0194599810395353
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Hosszú időn át tartó vizsgálat, amely során az érintettek a következő eredményeket kapták:
14. Abramson AL, Shikowitz MJ, Mullooly VM, Steinberg BM, Amella CA, Rothstein HR. A fotodinamikus terápia klinikai hatásai a recidiváló gégepapillómákon. Arch Otolaryngol Head Neck Surg. (1992) 118:25-9. doi: 10.1001/archotol.1992.01880010029011
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Orvosi és pszichiátriai tanulmányok és tanulmányok. Feyh J, Kastenbauer E. A gége papillomatosis kezelése fotodinamikus lézerterápiával. Laryngorhinootologie. (1992) 71:190-2.
PubMed Abstract | Google Scholar
16. Lieder A, Khan MK, Lippert BM. Fotodinamikus terápia a visszatérő légúti papillomatosisban. Cochrane Database Syst Rev. (2014) 5:CD009810. doi: 10.1002/14651858.CD009810.pub2
CrossRef Full Text | Google Scholar
17. Cochrane Database Syst Rev. (2014) 5:CD009810. dok. Rosen CA, Bryson PC. Indol-3-karbinol a visszatérő légúti papillomatózis kezelésére: hosszú távú eredmények. J Voice. (2004) 18:248-53. doi: 10.1016/j.jvoice.2003.05.005
PubMed Abstract | CrossRef Full Text | Google Scholar
18. PubMed Abstract | CrossRef Full Text | Google Scholar
. Wu R, Abramson AL, Shikowitz MJ, Dannenberg AJ, Steinberg BM. Az epidermális növekedési faktor által indukált ciklooxigenáz-2 expresszió a foszfatidil-inozitol-3-kinázon, nem pedig a mitogén-aktivált fehérje/extracelluláris jel-szabályozott kináz-kinázon keresztül mediálódik visszatérő légúti papillómákban. Clin. Cancer Res. (2005) 11:6155-61. doi: 10.1158/1078-0432.CCR-04-2664
CrossRef Full Text | Google Scholar
19. Cancer Res. Limsukon A, Susanto I, Soo Hoo GW, Dubinett SM, Batra RK. A recidiváló légúti papillomatosis regressziója celecoxib és erlotinib kombinációs terápiával. Chest. (2009) 136:924-6. doi: 10.1378/chest.08-2639
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Gyógyszerészi vizsgálat. McKenna M, Brodsky L. Extraoesophagealis savas reflux és recidiváló légúti papilloma gyermekeknél. Int. J. Pediatr. Otorhinolaryngol. (2005) 69:597-605. doi: 10.1016/j.ijporl.2004.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Hosszú időn át tartó interjúk a következő témakörökben készültek el: “Az oxigénhiányos gyomornyálkahártya-gyulladás”. Borkowski G, Sommer P, Stark T, Sudhoff H, Luckhaupt H. Gastrooesophagealis refluxbetegséggel társuló recidiváló légúti papillomatosis gyermekeknél. Eur Arch Otorhinolaryngol. (1999) 256:370-2. doi: 10.1007/s004050050166
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Google Scholar
22. Holland BW, Koufman JA, Postma GN, McGuirt WF Jr. Laryngopharyngealis reflux és laryngealis szövedékképződés gyermekkori recidiváló légúti papillómás betegeknél. Laryngoscope. (2002) 112:1926-9. doi: 10.1097/00005537-200211000-00003
PubMed Abstract | CrossRef Full Text | Google Scholar
23. A gégészeti szakfolyóiratok és a gégegyógyászati szakfolyóirat (2002) 112:1926-9. San Giorgi MRM, Helder HM, Lindeman RJS, de Bock GH, Dikkers FG. A gastrooesophagealis refluxbetegség és a visszatérő légúti papillomatosis közötti kapcsolat: szisztematikus áttekintés. Laryngoscope. (2016) 126:2330-9. doi: 10.1002/lary.25898
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Google Scholar
. Derkay CS, Smith RJH, McClay J, van Burik JAH, Wiatrak BJ, Arnold J, et al. HspE7 kezelés a gyermekkori visszatérő légúti papillomatosisban: egy nyílt vizsgálat végleges eredményei. Ann Otol Rhinol Laryngol. (2005) 114:730-7. doi: 10.1177/000348940511400913
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Keresés English (2005) 114:730-7. Rosenberg T, Philipsen BB, Mehlum CS, Dyrvig AK, Wehberg S, Chirilǎ M, et al. Therapeutic use of the human papillomavirus vaccine on recurrent respiratory papillomatosis: a systematic review and meta-analysis. J Infect Dis. (2019) 219:1016-25. doi: 10.1093/infdis/jiy616
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Infovírusos vírusfertőzés. Mudry P, Vavrina M, Mazanek P, Machalova M, Litzman J, Sterba J. Recidiváló laryngealis papillomatosis: sikeres kezelés humán papillomavírus vakcinációval. Arch Dis Child. (2011) 96:476-7. doi: 10.1136/adc.2010.198184
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Google Scholar
. Förster G, Boltze C, Seidel J, Pawlita M, Müller A. Juvenilis gégepapillomatózis-immunizáció a gardasil polivalens vakcinával. Laryngorhinootologie. (2008) 87:796-9. doi: 10.1055/s-2008-1077527
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Gyógyszerészi szakfolyóirat. Mauz PS, Schäfer FA, Iftner T, Gonser P. HPV-vakcináció mint prevenciós megközelítés a visszatérő légúti papillomatosis megelőzésére – egy 22 éves retrospektív klinikai elemzés. BMC Infect Dis. (2018) 18:343. doi: 10.1186/s12879-018-3260-0
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Vizsgálati eredmények. Pashley NRT. Indukálhat-e mumpszvakcina remissziót a visszatérő légúti papillómában? Arch Otolaryngol Head Neck Surg. (2002) 128:783-6. doi: 10.1001/archotol.128.7. doi: 10.1001/archotol.128.7.783
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Meacham RK, Thompson JW. A cidofovir és a kanyaró, mumpsz és rubeola vakcina összehasonlítása a visszatérő légúti papillomatosis kezelésében. Ear Nose Throat J. (2017) 96:69-74. doi: 10.1177/014556131709600209
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Ear Nose Throat J (2017) 96:69-74. Rahbar R, Vargas SO, Folkman J, McGill TJ, Healy GB, Tan X, et al. Vascular endothelial growth factor-a szerepe a visszatérő légúti papillomatosisban. Ann Otol Rhinol Rhinol Laryngol. (2005) 114:289-95. doi: 10.1177/000348940511400407
PubMed Abstract | CrossRef Full Text | Google Scholar
32. PhD. Maturo S, Hartnick CJ. 532-Nm-es impulzusú kálium-titanilfoszfát lézer és adjuváns intraléziós bevacizumab alkalmazása agresszív légúti papillomatosisban gyermekeknél: kezdeti tapasztalatok. Arch Otolaryngol Head Neck Surg. (2010) 136:561-5. doi: 10.1001/archoto.2010.81
PubMed Abstract | CrossRef Full Text | Google Scholar
33. Google Scholar
. Zeitels SM, Barbu AM, Landau-Zemer T, Lopez-Guerra G, Burns JA, Friedman AD, et al. Bevacizumab (Avastin) helyi injekciója és angiolitikus KTP lézeres kezelés a hangszalagok visszatérő légúti papillomatózisában: prospektív vizsgálat. Ann Otol Rhinol Rhinol Laryngol. (2011) 120:627-34. doi: 10.1177/000348941112001001
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Gyógyszerészi szakvélemény | CrossRef Full Text | Google Scholar
. Sidell DR, Nassar M, Cotton RT, Zeitels SM, de Alarcon A. Nagy dózisú szubléziós bevacizumab (Avastin) gyermekkori recidiváló légúti papillomatosis kezelésére. Ann Otol Rhinol Laryngol. (2014) 123:214-21. doi: 10.1177/0003489414522977
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Mohr M, Schliemann C, Biermann C, Schmidt LH, Kessler T, Schmidt J, et al. Rapid response to systemic bevacizumab therapy in recurrent respiratory papillomatosis. Oncol Lett. (2014) 8:1912-8. doi: 10.3892/ol.2014.2486
PubMed Abstract | CrossRef Full Text | Google Scholar
36. Fernandez-Bussy S, Labarca G, Vial MR, Soto R, Mehta HJ, Jantz M, et al. Recurrent respiratory papillomatosis and bevacizumab treatment. Am J Respir Crit Care Med. (2017) 197:539-41. doi: 10.1164/rccm.201702-0279LE
PubMed Abstract | CrossRef Full Text | Google Scholar
37. PhD. Bedoya A, Glisinski K, Clarke J, Lind RN, Buckley CE, Shofer S. Szisztémás bevacizumab a visszatérő légúti papillomatosis kezelésére: két eset egyközpontú tapasztalata. Am J Case Rep. (2017) 18:842-6. doi: 10.12659/AJCR.904416
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Az Am J Case Rep. Zur KB, Fox E. Bevacizumab kemoterápia a pulmonális és laryngotrachealis papillomatosis kezelésére egy gyermeknél. Laryngoscope. (2017) 127:1538-42. doi: 10.1002/lary.26450
PubMed Abstract | CrossRef Full Text | Google Scholar
39. A Laryngaryngoszkópia és a Laryngoszkópia és a Laryngoszkópia és a Laryngoszkópia. Best SR, Mohr M, Zur KB. Szisztémás bevacizumab a recidiváló légúti papillomatosis kezelésére: országos felmérés. Laryngoscope. (2017) 127:2225-9. doi: 10.1002/lary.26662
PubMed Abstract | CrossRef Full Text | Google Scholar