Introduction
La papillomatose respiratoire récurrente (PRR) est une maladie chronique causée par le papillomavirus humain (HPV), généralement les types 6 et 11. Les lésions de la PRR apparaissent le plus souvent dans le larynx (figure 1), mais peuvent également apparaître dans la bouche, la trachée, les bronches, le parenchyme pulmonaire et l’œsophage. La forme juvénile du PRR, dans laquelle les symptômes apparaissent avant 12 ans, est plus agressive que la forme adulte, et les symptômes sont plus sévères. La récurrence des papillomes est particulièrement rapide chez les enfants de moins de 3 ans, chez qui les intervalles entre les interventions chirurgicales sont plus courts et qui subissent donc globalement plus d’interventions chirurgicales. La probabilité que l’infection se propage au-delà du larynx et l’incidence d’une trachéotomie, pour aider à maintenir la trachée ouverte, sont également plus grandes dans cette population (1). Les patients atteints de PRR à début juvénile subissent en moyenne 20 interventions chirurgicales, dont la plupart pendant l’enfance (2).
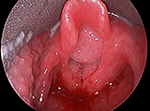
Figure 1. Image laryngoscopique directe d’une grande papillomatose volumineuse des voies aériennes obstruant l’entrée du larynx.
La méthode traditionnelle d’extirpation chirurgicale faisait classiquement appel aux lasers KTP (phosphate de titanyle de potassium) ou au dioxyde de carbone (3). Compte tenu des effets secondaires potentiellement graves de l’ablation au laser, notamment les brûlures des voies respiratoires et les cicatrices laryngées, les microdébrideurs sont devenus un outil chirurgical de plus en plus populaire, notamment chez les otolaryngologistes pédiatriques, pour les maladies volumineuses (3). Ce dispositif à main permet d’enlever le tissu malade avec plus de précision, réduisant ainsi les dommages aux tissus environnants (3). Cependant, étant donné la nature agressive du PRR juvénile, les débridements sont encore fréquents et, avec le temps, ils usent considérablement les tissus sous-jacents, avec une incidence élevée de formation de cicatrices. À ce titre, plusieurs traitements médicaux ont été étudiés pour améliorer les résultats de la chirurgie, en augmentant la durée entre les opérations, ou en minimisant la récurrence des lésions de PRR.
Interféron α
L’interféron α, une protéine produite par les leucocytes en réaction à divers stimuli, notamment une infection virale, a été l’un des premiers traitements médicaux potentiels étudiés (4). Sa valeur en tant que traitement adjuvant est controversée. Dans une vaste étude portant sur 85 enfants et 84 adultes, 58 % des enfants ont terminé la période de traitement d’un an d’injections intramusculaires d’interféron α trois fois par semaine sans preuve de PRR (5). La fréquence de récidive des papillomes a diminué chez 74 % des enfants traités (5). Cependant, dans un essai contrôlé randomisé portant sur 123 patients de moins de 21 ans, le ralentissement de la croissance des papillomes dans le groupe expérimental ayant reçu des injections intramusculaires d’interféron α ne s’est pas maintenu au cours de l’année de traitement (6). De même, une autre étude a révélé que, 20 ans après la fin du traitement par l’interféron α, seuls 42 % des patients présentaient une réponse à long terme, et tous ceux qui ont rechuté présentaient la forme juvénile du PRR (7). La plupart des études portant sur l’interféron α ont également fait état d’effets secondaires graves, comme des troubles neurologiques, une leucopénie et une thrombocytopénie (5). Pour ces raisons, son utilisation par les otolaryngologistes pédiatriques a diminué et n’est généralement pas recommandée (1). En 2014, seulement 4 % des enfants atteints de PRR ont reçu de l’interféron α comme traitement adjuvant (1).
Cidofovir
Ce médicament antiviral à large spectre qui inhibe les ADN polymérases virales s’est révélé prometteur comme traitement intralésionnel adjuvant à la chirurgie pour le PRR. Les injections intralésionnelles de cidofovir sont le traitement médical le plus couramment administré pour le PRR par les otolaryngologistes pédiatriques (1). Tous les articles publiés entre 1998 et 2011 qui ont étudié l’efficacité du cidofovir intralésionnel ont rapporté au moins un cas de rémission de la maladie (8). Cependant, comme la plupart de ces études sont des études de cas non contrôlées, on ne sait pas si les bénéfices sont causés par le cidofovir ou s’ils font partie de l’évolution naturelle de la maladie. Un essai contrôlé randomisé a révélé qu’il n’y avait pas de différences statistiquement significatives dans la gravité des papillomes ou la qualité de vie liée à la santé entre un groupe témoin, traité par des interventions chirurgicales selon les besoins et des injections intralésionnelles de solution saline, et le groupe expérimental, traité par chirurgie et Cidofovir intralésionnel, après 12 mois de traitement (9). Les deux groupes ont connu une diminution significative de la gravité de la maladie au cours de l’année, ce qui indique que la maladie peut régresser d’elle-même avec le temps (9). Une autre revue qui a examiné 27 études sur l’administration de cidofovir, toutes publiées avant 2011, a révélé que le taux moyen de rémission complète avec le cidofovir était de 37 % dans les études pédiatriques (10). Certains effets secondaires graves ont également été associés au cidofovir, car une revue a révélé que 1,7 et 1 % des 447 patients atteints de PRR ont subi une transformation maligne et une néphrotoxicité, respectivement (8). Parmi les autres effets secondaires, citons les éruptions cutanées, les céphalées et les cicatrices des cordes vocales (11). Compte tenu de ces complications potentielles et de l’absence de protocole accepté pour le dosage ou la fréquence d’administration, ce médicament n’est pas un adjuvant fiable (4).
Le ciclofovir a également été administré comme traitement systémique plutôt que local pour les cas de PRR compliqués par une maladie pulmonaire. Quatre études de cas uniques ont montré que le cidofovir intraveineux a conduit à une rémission de la maladie, ce qui n’est pas la progression normale de la maladie avec une atteinte pulmonaire (11). Toutes ces études ont eu recours à l’hyperhydratation et au probénécide, un réducteur d’acide urique, pour réduire les risques de néphrotoxicité (11). Un seul patient a présenté des effets secondaires, une alopécie partielle et une leucopénie, suite à une thérapie combinée de cidofovir et d’interféron (12). Les doses des deux médicaments ont été réduites en réponse. Dix-huit mois après la fin du traitement, la patiente n’avait dû subir qu’une seule fois une intervention chirurgicale pour le PRR et sa maladie pulmonaire s’était stabilisée (12).
Une nouvelle méthode d’administration du Cidofovir est l’inhalation. Peu d’études ont examiné l’efficacité de cette méthode, mais elle peut être prometteuse pour les patients qui n’ont pas répondu aux autres formes de traitement, comme un garçon de 4 mois qui, malgré des microdébridements bihebdomadaires et des injections intralésionnelles de Cidofovir et d’interféron α par voie intraveineuse, a vu ses symptômes s’aggraver (13). Après 6 semaines de traitement par 40 mg de Cidofovir nébulisé par jour, 12 jours de suite et 2 jours de repos, le délai entre les débridements a augmenté (13). Six mois plus tard, le patient ne présentait plus aucun symptôme (13). En résumé, bien que le Cidofovir sous diverses formes d’administration reste largement utilisé, ses résultats thérapeutiques sont au mieux mitigés, et son potentiel d’effets secondaires est quelque peu limité.
Traitement photodynamique
La thérapie photodynamique (TPD) consiste à introduire une substance sensible à la lumière, appelée photo-sensibilisateur, par voie orale ou par injection, dans le tissu malade et à activer la substance avec une lumière laser pour induire une nécrose. L’un des principaux avantages de la PDT est sa capacité à détruire les tumeurs sans affecter les tissus environnants (4). Des études de cas ont montré des taux de repousse des papillomes nettement plus faibles peu après une TPD, administrée en tant que traitement adjuvant ou autonome, et dans certains cas, l’absence de maladie après plusieurs semaines (14, 15). Il n’y a eu que quelques essais contrôlés randomisés pour étudier l’impact de la TPD, mais le plus récent a révélé que la maladie réapparaissait après 3 à 5 ans, probablement parce qu’elle génère son impact par une réponse immunitaire à court terme (16). Des recherches supplémentaires devraient être menées pour vérifier son efficacité et sa sécurité.
Indole-3-Carbinol
Trouvé en forte concentration dans les légumes crucifères comme le brocoli et le chou, l’indole-3-carbinol modifie le métabolisme des œstrogènes pour altérer la prolifération cellulaire et la synthèse de l’ADN. L’essai clinique le plus récent a révélé qu’après avoir pris de l’indole-3-carbinol deux fois par jour, avec une dose de 200 mg pour les adultes et des doses déterminées en fonction du poids pour les enfants, pendant une moyenne de 50,2 mois, 70 % des sujets ont présenté une réponse complète ou partielle (17). Parmi les patients pédiatriques, un a présenté une réponse complète, trois une réponse partielle et cinq aucune réponse (17). La raison pour laquelle les patients adultes ont mieux répondu à l’indole-3-carbinol que les patients pédiatriques n’est pas claire. La nature moins agressive du PRR à l’âge adulte pourrait être un facteur. Compte tenu des résultats peu prometteurs dans la population pédiatrique, il n’y a pas eu beaucoup plus de recherches sur le traitement du PRR d’apparition juvénile avec de l’indole-3-carbinol.
Celecoxib
Le célécoxib est un médicament anti-inflammatoire qui inhibe la cyclo-oxygénase-2 (COX-2), une enzyme qui conduit à l’inflammation et à la douleur, et est couramment utilisé pour traiter l’arthrite. Des études in vitro ont montré que les cellules de papillome surexpriment la COX-2 en raison d’une signalisation accrue du récepteur du facteur de croissance épidermique (EGFR), et que cette activité est importante pour leur croissance (18). Une thérapie combinant le célécoxib et l’erlotinib, un inhibiteur de la kinase de l’EGFR, a permis de contrôler le PRR progressif chez un homme de 58 ans en ralentissant la croissance des papillomes, rendant ainsi inutile une nouvelle intervention chirurgicale (19). Un essai de contrôle randomisé en cours parrainé par Northwell Health vise à déterminer si le célécoxib peut diminuer le taux de récurrence des papillomes chez les patients adultes et pédiatriques (4).
Médicaments anti-reflux
Des études de cas ont montré que le traitement du reflux gastro-œsophagien (RGO) par des médicaments anti-reflux chez les patients atteints de PRR à début juvénile peut aider à ralentir le taux de repousse des papillomes (20, 21). Dans une étude, les patients qui n’ont pas respecté le traitement RGO ont connu une récidive (20). Une analyse rétrospective des dossiers a également montré que les patients pédiatriques traités pour un PRR qui n’étaient pas traités pour le reflux étaient significativement plus susceptibles de développer des toiles laryngées après l’ablation chirurgicale des papillomes (22). Bien qu’il n’y ait pas de preuves concluantes que le RGO aggrave le PRR, sa prise en charge est logique pour les patients qui ont une présentation clinique de RGO et des cas compliqués et progressifs de PRR (23).
Heat Shock Protein
Parmi les 700 enfants atteints de PRR pris en charge par 74 oto-rhino-laryngologistes pédiatriques, qui ont été interrogés sur leur utilisation du traitement adjuvant, 11 patients ont reçu HSP-E7, une protéine de fusion recombinante composée de la protéine de choc thermique 65 (Hsp65) et de la protéine E7 du HPV de type 16 (1). La HSP-E7 a été étudiée en tant que traitement de plusieurs maladies issues du VPH, notamment les verrues génitales et les néoplasies intra-épithéliales (24). Des données suggèrent qu’elle pourrait être réactive contre plus de souches de VPH que le seul VPH 16 (24). Dans un essai ouvert portant sur 27 patients pédiatriques atteints de PRR, l’intervalle médian entre les interventions chirurgicales après traitement par HSP-E7 a été significativement prolongé par rapport à l’intervalle médian avant traitement (24). Il y a eu peu de complications, seulement des réactions légères à modérées au site d’injection. Bien qu’il n’y ait pas d’essais cliniques en cours pour étudier l’efficacité de Hsp-E7, il s’agit d’un traitement prometteur.
Vaccin HPV
Quelques rapports de cas et études ont documenté l’utilisation du vaccin HPV comme thérapie adjuvante. Il existe actuellement trois vaccins anti-HPV approuvés : le bivalent Cervarix, le tétravalent Gardasil et le nonavalent Gardasil 9. Le vaccin tétravalent agit sur les HPV-6, HPV-11, HPV-16, HPV-18. Une récente étude systématique et une méta-analyse ont révélé que la durée moyenne entre les interventions chirurgicales chez 63 patients juvéniles et adultes atteints de PRR augmentait de manière significative après la vaccination contre le VPH, passant de 7 à 34 mois en moyenne (25). L’étude n’a trouvé aucune différence significative en fonction de l’âge d’apparition du PRR (25). D’autres études de cas non incluses dans la méta-analyse ont également montré l’efficacité de Gardasil chez les patients pédiatriques, car il augmente significativement le temps entre les chirurgies ou, dans certains cas, provoque une rémission complète (26, 27).
La vaccination HPV intramusculaire pourrait être plus efficace que les traitements précédemment identifiés et plus courants comme le cidofovir intralésionnel. Une étude de cas rétrospective qui a suivi des patients atteints de PRR juvéniles et adultes pendant 22 ans a révélé que seuls deux des 13 patients traités par chirurgie et Gardasil ont rechuté, alors que tous les patients témoins, traités par chirurgie et Cidofovir, ont connu une repousse des papillomes (28). La durée moyenne du délai avant la récidive de la maladie était également significativement plus longue chez les patients traités que chez les témoins (28).
L’un des aspects les plus prometteurs du VPH comme thérapie adjuvante est qu’il ne présente pas d’effets secondaires graves. De plus, avec l’augmentation des taux de vaccination, l’incidence du PRR juvénile pourrait diminuer globalement, car cette forme de la maladie est couramment acquise lorsqu’un bébé est exposé à des verrues génitales causées par le virus HPV 6 ou 11 pendant l’accouchement (4).
Vaccin contre les oreillons
Il y a eu très peu d’études sur l’efficacité du vaccin contre les oreillons en tant que thérapie adjuvante, bien que les recherches actuelles soient prometteuses. Une étude de cas a révélé qu’une rémission a été induite chez neuf des 11 patients pédiatriques traités par des injections intralésionnelles du vaccin à des intervalles de 3 à 12 semaines en même temps que la chirurgie au laser (29). Une étude rétrospective comparant le Cidofovir et le vaccin contre la rougeole, les oreillons et la rubéole (ROR) en tant que thérapies adjuvantes dans une population pédiatrique a révélé qu’il n’y avait pas de différences significatives entre les enfants traités par des injections intralésionnelles de cidofovir et de ROR après des débridements (30).
Bevacizumab
Le bevacizumab est un anticorps monoclonal humain qui se lie au facteur de croissance endothélial vasculaire (VEGF) et empêche son interaction avec les récepteurs. L’activité du VEGF joue un rôle dans le développement du PRR, car des études in vitro ont montré une forte expression du VEGF-A dans l’épithélium du papillome et l’expression des ARN messagers VEGFR-1 et VEGFR-2 dans les cellules endothéliales vasculaires sous-jacentes (31).
Les premières études portant sur le bevacizumab en tant que traitement du PRR ont examiné les avantages des injections intralésionnelles en tant que thérapie adjuvante à la chirurgie. Une étude portant sur trois patients âgés de 3 à 6 ans présentant un PRR sévère (c’est-à-dire avec au moins quatre interventions par an) a révélé que tous les patients ont vu s’allonger le délai entre le débridement chirurgical et les traitements au laser KTP pulsé et que le PRR était moins sévère plusieurs semaines après la fin du traitement au bévacizumab qu’avant (32). Ils ont également montré une amélioration de la qualité de vie liée à la voix (32).
En dehors des rapports de cas, des études cas-témoins ont également été menées pour étudier l’efficacité du bevacizumab en tant que thérapie adjuvante. Après un traitement au laser KTP de 532 nm suivi d’injections sub-lésionnelles de bevacizumab dans le pli vocal le plus malade, et d’injections de solution saline dans l’autre pli, 16 des 20 patients adultes atteints de PRR bilatéral des plis vocaux présentaient moins de papillomes dans le pli traité, comme l’a déterminé l’imagerie endoscopique (33). Trois des 20 patients n’avaient aucune maladie dans l’un ou l’autre des deux plis, et aucun des patients n’a connu de complications liées au traitement (33).
Sur la base de ces résultats prometteurs, une étude plus large portant sur l’efficacité du bevacizumab a été menée dans une population pédiatrique. Chez 10 enfants âgés de 18 mois à 18 ans présentant une PRR progressive et non réactive, trois injections intralésionnelles de bevacizumab de 2,5 mg/ml espacées de 2 à 3 semaines, associées à une thérapie au laser, ont permis d’augmenter la durée médiane entre les interventions chirurgicales, de diminuer le nombre médian d’interventions par an et d’améliorer la qualité de vie liée à la voix (3). L’une des limites de l’étude est que le dosage est une estimation basée sur les doses en ophtalmologie pédiatrique. La quantité injectée dans les paillomes n’était également pas la même pour chaque patient, car elle variait en fonction de la gravité de la maladie.
Certaines études ont tenté de déterminer les doses optimales. Une autre étude portant sur neuf patients pédiatriques atteints de PRR d’apparition juvénile a également constaté qu’après une série de cinq injections sous-épithéliales administrées à des intervalles de 4 à 6 semaines, avec une dose moyenne de 14,25 mg, associée à une ablation au laser KTP, les neuf patients (dont l’âge médian était de 8 ans) ont connu une augmentation de l’intervalle entre les injections (34). Ces résultats indiquent que le traitement au bevacizumab à haute dose ne présente pas de complications et peut être très efficace.
Après avoir démontré l’efficacité du bevacizumab intralésionnel, la recherche s’est tournée vers le bevacizumab systémique, qui est un traitement particulièrement prometteur pour les patients présentant des diagnostics complexes. Le premier rapport sur l’administration intraveineuse a montré qu’avec une médiane de 6 traitements à des doses de 5, 10, 15 mg/kg, tous les patients traités avec un PRR progressif ont montré une régression des papillomes (35). Les patients comprenaient quatre cas de PRR d’âge adulte et un cas d’âge juvénile. Les cinq patients ont collectivement subi 18 interventions chirurgicales l’année précédant le bevacizumab, mais seul le cas adulte a dû être opéré après le traitement en raison d’une transformation maligne l’année suivante (35).
D’autres rapports de cas uniques ont corroboré l’efficacité du bevacizumab systémique sans trouver de complications, bien que la plupart d’entre eux concernent des patients adultes. Chez un homme de 42 ans présentant un PRR trachéal sévère, une faible dose de 5 mg/kg, augmentée à 10 mg/kg de bevacizumab au fil du temps, a permis d’obtenir une régression de la maladie 3 mois après l’arrêt du traitement (36). Un suivi de 12 mois a révélé que le patient était toujours indemne de la maladie. Six traitements par bevacizumab systémique à raison de 5 mg/kg toutes les 2 semaines chez un patient de 87 ans qui n’avait pas répondu au cidofovir intralésionnel, à une endoprothèse endobronchique ou à la vaccination contre le VPH, ont également permis d’obtenir une diminution significative de la masse du lobe et une bronche perméable (37). Après deux cures d’injections intraveineuses de 10 mg/kg toutes les 2 semaines, une personne de 63 ans présentant un PRR sévère a montré une moindre atteinte pulmonaire et aucun signe d’obstruction trachéale (37).
Le seul rapport de cas publié chez l’enfant concerne une jeune fille de 12 ans présentant une papillomatose laryngotrachéale progressive et une atteinte pulmonaire qui, après 3 mois d’initiation du traitement systémique par bevacizumab, a montré une réponse partielle au niveau du larynx et une réponse presque complète au niveau de la trachée (38). Après 5 mois, le patient ne présentait plus d’atteinte pulmonaire. Ces résultats sont d’autant plus impressionnants que, sur une période de 10 ans, la patiente avait été initiée au Gardasil, à l’interféron, au célécoxib, aux médicaments anti-reflux, à la zithromycine et au propranolol, et n’avait répondu à aucun (38).
Le potentiel du bevacizumab systémique comme traitement des formes les plus agressives de PRR est le mieux résumé par les résultats d’un sondage électronique de la RRP Task Force de l’American Society of Pediatric Otolaryngology, de l’American Broncho-Esophagological Association et des médecins qui ont traité le PRR avec du bevacizumab systémique (39). Les 11 questionnaires remplis provenant de neuf centres médicaux ont montré que la plupart des patients traités par le bevacizumab avaient de longs antécédents de PRR d’apparition juvénile et n’avaient pas présenté de réponses durables au cidofovir, à l’interféron et au célécoxib. Les médecins ont administré le traitement à raison de 5 à 10 mg/kg par dose. Sept des huit patients traités ont eu une réponse partielle et un a montré une réponse complète au traitement (39). Tous les patients ont vu s’allonger le délai entre les interventions chirurgicales, désormais de l’ordre de plusieurs mois. Chez trois des quatre patients présentant une atteinte pulmonaire, trois ont montré une amélioration ou une résolution du papillome pulmonaire et un a montré une stabilisation de la maladie. Seuls deux patients ont présenté des complications mineures, une hémoptysie et une protéinurie.
Pour vérifier l’effet causal du bevacizumab, déterminer les doses appropriées et identifier toute complication potentielle, des essais contrôlés randomisés et des études cas-témoins de plus grande envergure doivent être menés. De plus, des protocoles pour définir la durée du traitement, tout en contrôlant tout effet rebond potentiel, doivent être élaborés.
Conclusions
Bien qu’un traitement médical adjuvant optimal et universellement efficace pour le PRR n’ait pas encore été trouvé, les résultats prometteurs de la vaccination contre le PRR comme approche thérapeutique ainsi que l’utilisation du bevacizumab systémique offrent l’espoir d’une amélioration des résultats pour ces enfants dans les années à venir. Des protocoles optimaux de traitement devraient être développés dans un avenir proche.
Contributions des auteurs
Tous les auteurs listés ont apporté une contribution substantielle, directe et intellectuelle au travail, et l’ont approuvé pour publication.
Déclaration de conflit d’intérêts
Les auteurs déclarent que la recherche a été menée en l’absence de toute relation commerciale ou financière qui pourrait être interprétée comme un conflit d’intérêts potentiel.
Le rédacteur en chef de traitement a déclaré une co-audition passée avec l’un des auteurs DP.
1. Schraff S, Derkay CS, Burke B, Lawson L. American Society of Pediatric Otolaryngology members’ experience with recurrent respiratory papillomatosis and the use of adjuvant therapy. Arch Otolaryngol Head Neck Surg. (2004) 130:1039-42. doi : 10.1001/archotol.130.9.1039
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Krstic M, Pavlović JM, Stanković P, Milenković MT. Etiopathogénie de la papillomatose laryngée récurrente et stratégies de traitement contemporaines. Acta Med Medianae. (2014) 53:64-74. doi : 10.5633/amm.2014.0411
CrossRef Full Text | Google Scholar
3. Rogers DJ, Ojha S, Maurer R, Hartnick CJ. Utilisation du bevacizumab intralésionnel adjuvant pour la papillomatose respiratoire agressive chez les enfants. JAMA Otolaryngol Head Neck Surg. (2013) 139:496-501. doi : 10.1001/jamaoto.2013.1810
PubMed Abstract | CrossRef Full Text | Google Scholar
4. Carifi M, Napolitano D, Morandi M, Dall’Olio D. Papillomatose respiratoire récurrente : perspectives actuelles et futures. Ther Clin Risk Manag. (2015) 11:731-8. doi : 10.2147/TCRM.S81825
PubMed Abstract | CrossRef Full Text | Google Scholar
5. Nodarse-Cuní H, Iznaga-Marín N, Viera-Alvarez D, Rodríguez-Gómez H, Fernández-Fernández H, Blanco-López Y, et al. Interféron alpha-2b comme traitement adjuvant de la papillomatose respiratoire récurrente à Cuba : programme national (Rapport 1994-1999). J Laryngol Otol. (2004) 118:681-7. doi : 10.1258/0022215042244741
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Healy GB, Gelber RD, Trowbridge AL, Grundfast KM, Ruben RJ, Price KN. Traitement de la papillomatose respiratoire récurrente avec l’interféron leucocytaire humain. New Engl J Med. (1988) 319:401-7. doi : 10.1056/NEJM198808183190704
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gerein V, Rastorguev E, Gerein J, Jecker P, Pfister H. Use of interferon-alpha in recurrent respiratory papillomatosis : 20-year follow-up. Ann Otol Rhinol Laryngol. (2005) 114:463-71. doi : 10.1177/000348940511400608
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Jackowska J, Piersiala K, Klimza H, Wierzbicka M. Résultats du traitement par bevacizumab et cidofovir dans la papillomatose respiratoire récurrente associée au HPV-revue de la littérature. Otolaryngol Pol. (2018) 72:1-8. doi : 10.5604/01.3001.0012.0484
PubMed Abstract | CrossRef Full Text | Google Scholar
9. McMurray JS, Connor N, Ford CN. Efficacité du cidofovir dans la papillomatose respiratoire récurrente : une étude randomisée, en double aveugle, contrôlée par placebo. Ann Otol Rhinol Laryngol. (2008) 117:477-83. doi : 10.1177/000348940811700702
PubMed Abstract | CrossRef Full Text | Google Scholar
10. Chadha NK. Cidofovir intralésionnel pour la papillomatose respiratoire récurrente : examen systématique de l’efficacité et de la sécurité. J Laryngol Voice. (2011) 1:22-6. doi : 10.4103/2230-9748.76133
CrossRef Full Text | Google Scholar
11. Broekema FI, Dikkers FG. Effets secondaires du cidofovir dans le traitement de la papillomatose respiratoire récurrente. Eur Arch Otorhinolaryngol. (2008) 265:871-9. doi : 10.1007/s00405-008-0658-0
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Dancey DR, Chamberlain DW, Krajden M, Palefsky J, Alberti PW, Downey GP. Successful treatment of juvenile laryngeal papillomatosis-related multicystic lung disease with cidofovir : case report and review of the literature. Chest. (2000) 118:1210-4. doi : 10.1378/chest.118.4.1210
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Ksiazek J, Prager JD, Sun GH, Wood RE, Arjmand EM. Le cidofovir inhalé comme thérapie adjuvante pour la papillomatose respiratoire récurrente. Otolaryngol Head Neck Surg. (2011) 144:639-41. doi : 10.1177/0194599810395353
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Abramson AL, Shikowitz MJ, Mullooly VM, Steinberg BM, Amella CA, Rothstein HR. Effets cliniques de la thérapie photodynamique sur les papillomes laryngés récurrents. Arch Otolaryngol Head Neck Surg. (1992) 118:25-9. doi : 10.1001/archotol.1992.01880010029011
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Feyh J, Kastenbauer E. Traitement de la papillomatose laryngée par thérapie laser photodynamique. Laryngorhinootologie. (1992) 71:190-2.
PubMed Abstract | Google Scholar
16. Lieder A, Khan MK, Lippert BM. Thérapie photodynamique pour la papillomatose respiratoire récurrente. Cochrane Database Syst Rev. (2014) 5:CD009810. doi : 10.1002/14651858.CD009810.pub2
CrossRef Full Text | Google Scholar
17. Rosen CA, Bryson PC. Indole-3-carbinol pour la papillomatose respiratoire récurrente : résultats à long terme. J Voice. (2004) 18:248-53. doi : 10.1016/j.jvoice.2003.05.005
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Wu R, Abramson AL, Shikowitz MJ, Dannenberg AJ, Steinberg BM. Epidermal growth factor-induced cyclooxygenase-2 expression is mediated through phosphatidylinositol-3 kinase, not mitogen-activated protein/extracellular signal-regulated kinase kinase, in recurrent respiratory papillomas. Clin. Cancer Res. (2005) 11:6155-61. doi : 10.1158/1078-0432.CCR-04-2664
CrossRef Full Text | Google Scholar
19. Limsukon A, Susanto I, Soo Hoo GW, Dubinett SM, Batra RK. Régression de la papillomatose respiratoire récurrente avec la thérapie combinée de célécoxib et d’erlotinib. Chest. (2009) 136:924-6. doi : 10.1378/chest.08-2639
PubMed Abstract | CrossRef Full Text | Google Scholar
20. McKenna M, Brodsky L. Extraesophageal acid reflux and recurrent respiratory papilloma in children. Int. J. Pediatr. Otorhinolaryngol. (2005) 69:597-605. doi : 10.1016/j.ijporl.2004.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Borkowski G, Sommer P, Stark T, Sudhoff H, Luckhaupt H. Recurrent respiratory papillomatosis associated with gastroesophageal reflux disease in children. Eur Arch Otorhinolaryngol. (1999) 256:370-2. doi : 10.1007/s004050050166
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Holland BW, Koufman JA, Postma GN, McGuirt WF Jr. Reflux laryngopharyngé et formation de toile laryngée chez les patients atteints de papillomes respiratoires récurrents pédiatriques. Laryngoscope. (2002) 112:1926-9. doi : 10.1097/00005537-200211000-00003
PubMed Abstract | CrossRef Full Text | Google Scholar
23. San Giorgi MRM, Helder HM, Lindeman RJS, de Bock GH, Dikkers FG. L’association entre le reflux gastro-œsophagien et la papillomatose respiratoire récurrente : une revue systématique. Laryngoscope. (2016) 126:2330-9. doi : 10.1002/lary.25898
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Derkay CS, Smith RJH, McClay J, van Burik JAH, Wiatrak BJ, Arnold J, et al. HspE7 treatment of pediatric recurrent respiratory papillomatosis : final results of an open-label trial. Ann Otol Rhinol Laryngol. (2005) 114:730-7. doi : 10.1177/000348940511400913
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Rosenberg T, Philipsen BB, Mehlum CS, Dyrvig AK, Wehberg S, Chirilǎ M, et al. Utilisation thérapeutique du vaccin contre le papillomavirus humain sur la papillomatose respiratoire récurrente : une revue systématique et une méta-analyse. J Infect Dis. (2019) 219:1016-25. doi : 10.1093/infdis/jiy616
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Mudry P, Vavrina M, Mazanek P, Machalova M, Litzman J, Sterba J. Recurrent laryngeal papillomatosis : successful treatment with human papillomavirus vaccination. Arch Dis Child. (2011) 96:476-7. doi : 10.1136/adc.2010.198184
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Förster G, Boltze C, Seidel J, Pawlita M, Müller A. Juvenile laryngeal papillomatosis-immunisation avec le vaccin polyvalent gardasil. Laryngorhinootologie. (2008) 87:796-9. doi : 10.1055/s-2008-1077527
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Mauz PS, Schäfer FA, Iftner T, Gonser P. HPV vaccination as preventive approach for recurrent respiratory papillomatosis-a 22-year retrospective clinical analysis. BMC Infect Dis. (2018) 18:343. doi : 10.1186/s12879-018-3260-0
PubMed Abstract | CrossRef Full Text | Google Scholar
29. Pashley NRT. Le vaccin contre les oreillons peut-il induire une rémission du papillome respiratoire récurrent ? Arch Otolaryngol Head Neck Surg. (2002) 128:783-6. doi : 10.1001/archotol.128.7.783
PubMed Abstract | CrossRef Full Text | Google Scholar
30. Meacham RK, Thompson JW. Comparaison du cidofovir et du vaccin contre la rougeole, les oreillons et la rubéole dans le traitement de la papillomatose respiratoire récurrente. Ear Nose Throat J. (2017) 96:69-74. doi : 10.1177/014556131709600209
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Rahbar R, Vargas SO, Folkman J, McGill TJ, Healy GB, Tan X, et al. Role of vascular endothelial growth factor-a in recurrent respiratory papillomatosis. Ann Otol Rhinol Laryngol. (2005) 114:289-95. doi : 10.1177/000348940511400407
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Maturo S, Hartnick CJ. Utilisation du laser 532-Nm pulsé potassium titanyl phosphate et du bevacizumab intralésionnel adjuvant pour la papillomatose respiratoire agressive chez les enfants : expérience initiale. Arch Otolaryngol Head Neck Surg. (2010) 136:561-5. doi : 10.1001/archoto.2010.81
PubMed Abstract | CrossRef Full Text | Google Scholar
33. Zeitels SM, Barbu AM, Landau-Zemer T, Lopez-Guerra G, Burns JA, Friedman AD, et al. Injection locale de bevacizumab (Avastin) et traitement angiolytique au laser KTP de la papillomatose respiratoire récurrente des plis vocaux : une étude prospective. Ann Otol Rhinol Laryngol. (2011) 120:627-34. doi : 10.1177/000348941112001001
PubMed Abstract | CrossRef Full Text | Google Scholar
34. Sidell DR, Nassar M, Cotton RT, Zeitels SM, de Alarcon A. High-dose sublesional bevacizumab (Avastin) for pediatric recurrent respiratory papillomatosis. Ann Otol Rhinol Laryngol. (2014) 123:214-21. doi : 10.1177/0003489414522977
PubMed Abstract | CrossRef Full Text | Google Scholar
35. Mohr M, Schliemann C, Biermann C, Schmidt LH, Kessler T, Schmidt J, et al. Réponse rapide au traitement systémique par bevacizumab dans la papillomatose respiratoire récurrente. Oncol Lett. (2014) 8:1912-8. doi : 10.3892/ol.2014.2486
PubMed Abstract | CrossRef Full Text | Google Scholar
36. Fernandez-Bussy S, Labarca G, Vial MR, Soto R, Mehta HJ, Jantz M, et al. Papillomatose respiratoire récurrente et traitement au bevacizumab. Am J Respir Crit Care Med. (2017) 197:539-41. doi : 10.1164/rccm.201702-0279LE
PubMed Abstract | CrossRef Full Text | Google Scholar
37. Bedoya A, Glisinski K, Clarke J, Lind RN, Buckley CE, Shofer S. Bevacizumab systémique pour la papillomatose respiratoire récurrente : une expérience de centre unique de deux cas. Am J Case Rep. (2017) 18:842-6. doi : 10.12659/AJCR.904416
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Zur KB, Fox E. Chimiothérapie au bevacizumab pour la prise en charge de la papillomatose pulmonaire et laryngotrachéale chez un enfant. Laryngoscope. (2017) 127:1538-42. doi : 10.1002/lary.26450
PubMed Abstract | CrossRef Full Text | Google Scholar
39. Best SR, Mohr M, Zur KB. Bevacizumab systémique pour la papillomatose respiratoire récurrente : une enquête nationale. Laryngoscope. (2017) 127:2225-9. doi : 10.1002/lary.26662
PubMed Abstract | CrossRef Full Text | Google Scholar
.