Zaak
Een 63-jarige man met hypertensie, diabetes en onlangs gediagnosticeerde squameuze-cellige longkanker presenteert zich met diffuse buikpijn en verwardheid die twee dagen duurt. Hij weegt 105 Kg, zijn bloeddruk is 105/65 mm/Hg, zijn hartslag is 105 slagen per minuut en zijn temperatuur is 99,0 graden Fahrenheit. Zijn ademhaling is 18 ademhalingen per minuut, zuurstofverzadiging is 95% op kamerlucht, en zijn orthostatica zijn positief. Bij lichamelijk onderzoek worden droge slijmvliezen met een verminderde turgor van de huid waargenomen. Laboratoriumonderzoek toont een calciumgehalte van 15,5 mg/dL, creatininegehalte van 1,2 mg/dL, albuminegehalte van 4,3 g/dL, en een fosforgehalte van 2,9 mg/dL.
Wat is de beste behandeling van deze aandoening?
Overzicht
Calcium homeostase impliceert complexe interacties tussen de nieren, het maagdarmkanaal (GI), en het skeletstelsel via hormonale invloeden. Hoewel 99% van het calcium in het lichaam wordt opgeslagen in de botten, is 50% van het serumcalcium in de actieve geïoniseerde vorm, 40% is gebonden aan albumine, en 10% is gecomplexeerd met anionen.1 Het is belangrijk om deze percentages te onthouden bij het evalueren van het serumcalcium van een patiënt; verhoogd serumcalcium kan worden gevalideerd met behulp van een correctieformule (gecorrigeerd calcium=gemeten totaal calcium + ) of door directe meting van het geïoniseerde calcium, dat de fysiologisch actieve vorm is.
Hypercalciëmie van maligniteit is de meest voorkomende oorzaak van hypercalciëmie bij de gehospitaliseerde patiënt. Twintig tot 30% van de kankerpatiënten zal op een bepaald moment in hun ziekteverloop hypercalciëmie ontwikkelen.2 Over het algemeen voorspelt dit een slechte prognose met een mediane overleving van drie tot vier maanden.3
Vier algemene mechanismen zijn betrokken bij de pathogenese van maligne hypercalciëmie; deze mechanismen vormen de basis voor de beschikbare behandelingsstrategieën:
- Osteolytische tumoren, zoals multipel myeloom, kunnen direct inwerken op het bot, wat leidt tot activering van osteoclasten en afgifte van calcium;
- Humorale mediatoren die door kwaadaardige cellen worden aangemaakt, zoals parathyroïdhormoon-gerelateerd peptide (PTH-RP), kunnen activering van osteoclasten bewerkstelligen en de renale eliminatie van calcium verminderen, waardoor humorale hypercalciëmie van maligniteit ontstaat;
- Sommige maligniteiten (meestal lymfomen) kunnen direct 1,25 (OH)2 vitamine D synthetiseren, wat leidt tot verhoogde luminale absorptie van zowel calcium als fosfor uit het maagdarmkanaal; en
- Directe productie van parathyroïdhormoon (PTH) door de maligne cellen is zeldzaam, maar is gerapporteerd.2
Andere factoren, waaronder verminderde mobiliteit, kunnen leiden tot verdere botresorptie en een verergering van de hypercalcemische toestand.
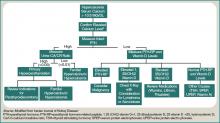
Een patiënt met hypercalciëmie moet een systematische workup hebben, met kennis van andere oorzaken van hypercalciëmie die aanwezig zouden kunnen zijn, ongeacht de maligniteit. Voorbeelden hiervan zijn primaire hyperparathyroïdie, medicijneffecten en genetische etiologie. Hoewel verdere discussie buiten het bestek van dit artikel valt, wordt een brede diagnostische benadering weergegeven in figuur 1 (rechts).
Effectieve behandeling van hypercalciëmie vereist overweging van zowel de onmiddellijke als de klinische situatie van de patiënt op langere termijn, in het licht van de prognose van de patiënt. Het primaire doel bij de acute behandeling van hypercalciëmie is het normaliseren van de serumwaarden en het verminderen van de symptomen. Dit moet echter gebeuren met in het achterhoofd dat de metabole stoornis werd veroorzaakt door een onderliggende maligniteit. De klinische therapie moet zich vooral hierop richten.
 klik voor grote versie
klik voor grote versie
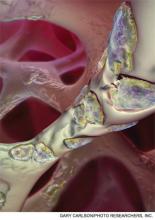
Een door de computer gegenereerd beeld van multinucleaire osteoclasten die het trabeculaire bot wegvreten in een proces dat botresorptie wordt genoemd. De bisfosfonaten remmen dit proces bij door maligniteit veroorzaakte hypercalciëmie.
Review of the Data
Intraveneuze (IV) vloeistoffen. IV-hydratatie met isotone zoutoplossing is de meest directe en kritische interventie bij de acute behandeling van maligne hypercalciëmie. Deze aandoening heeft meerdere, potentieel schadelijke effecten op de nier, waaronder vasoconstrictie, remming van de zoutabsorptie distaal, en antagonisme van het anti-diuretisch hormoon (ADH), wat leidt tot zowel zout- als waterverlies. De afname van het intravasculaire volume versterkt vervolgens de verhoogde natriumreabsorptie proximaal in de nier.
Isotone zoutoplossing herstelt de volumedepletie die steevast optreedt in het kader van door hypercalciëmie veroorzaakte zoutverspilling in de urine. Het herstel van het intravasculaire volume resulteert in een toename van de glomerulaire filtratiesnelheid en daarmee in een toename van de calciumfiltratie. Bovendien neemt de proximale tubulaire natrium- en calciumreabsorptie af naarmate de glomerulaire filtratiesnelheid toeneemt. Bovendien lokt een toename van de natrium- en waterpresentie aan de distale tubulaire plaatsen van de nieren een verdere calciurese uit.
Geschat wordt dat met zouthydratatie de calciumconcentratie zou moeten dalen, ten minste met de mate waarin de dehydratie deze heeft verhoogd, gewoonlijk in het bereik van 1,6 mg tot 2,4 mg per deciliter.4 Hydratatie alleen leidt echter zelden tot normalisatie van de serumcalciumconcentratie bij patiënten met ernstige hypercalciëmie.
De infusiesnelheid is gebaseerd op de ernst van de hypercalciëmie, en de leeftijd en comorbiditeiten van de patiënt, met bijzondere aandacht voor hart- of nieraandoeningen. Een standaard aanpak voor de meeste patiënten zonder oedeem en zonder hart- of nierinsufficiëntie is om te beginnen met een zoutinfusie met een beginsnelheid tussen 200 mL/h tot 300 mL/h. Het doel is om de urineproductie op 100 mL/h tot 150 mL/h te houden.
Furosemide. Na het toedienen van intraveneuze vloeistoffen om een euvolemische toestand te herstellen, wordt van oudsher furosemide gebruikt omdat het een calcinurisch effect heeft met geforceerde diurese. Het is ook nuttig voor het beheersen en voorkomen van de overbelasting van vocht die optreedt bij zoutoplossing. Gegevens ondersteunen echter niet het routinematige gebruik ervan om calciumspiegels te verlagen bij hypercalcemische patiënten.
De meeste artikelen die het gebruik van furosemide bestudeerden, werden gepubliceerd in de jaren ’70 en ’80, en zij betreffen een verscheidenheid aan doses en toedieningsschema’s variërend van 40 mg oraal per dag tot 100 mg IV per uur met variabele verbetering van serum calciumspiegels en effecten die van korte duur waren. Hoewel sommige studies hebben aangetoond dat deze hoge doses (2.400 mg/24 uur) furosemide de calciumspiegels kunnen verlagen, werden als gevolg daarvan ernstige metabolische afwijkingen in andere elektrolyten aangetroffen. Deze aanpak vereiste frequente en invasieve monitoring om dergelijke afwijkingen te voorkomen.5 De klinische toepassing van deze studies heeft geleid tot gepubliceerde aanbevelingen die even variabel zijn als de doses die meer dan 30 jaar geleden in de oorspronkelijke studies werden gebruikt.
Dit omvat de overweging dat, in het licht van de beschikbaarheid en werkzaamheid van bisfosfonaten, furosemide klinisch niet langer nuttig zou kunnen zijn bij dit streven.6 De huidige rol van furosemide in de behandeling van patiënten met hypercalciëmie blijft op basis van noodzaak voor de behandeling van een toestand van overbelasting van vloeistof na agressieve IV vloeistofresuscitatie.
 klik voor grote versie
klik voor grote versie
Figuur 1: Diagnostische benadering van hypercalciëmie.
Bisfosfonaten. Bisfosfonaten kwamen in het begin van de jaren negentig voor het eerst beschikbaar voor de behandeling van hypercalciëmie en hebben de acute interventie ingrijpend veranderd en het klinische beloop op lange termijn van patiënten met maligne hypercalciëmie verbeterd. Hoewel ze voor het eerst werden ontwikkeld in de 19e eeuw met industriële toepassingen, werd hun rol in het botmetabolisme pas in de jaren 1960 gewaardeerd.
Hoewel hun complexe werkingsmechanisme een kwestie van lopend onderzoek blijft, is het bekend dat bisfosfonaten naar de botten worden geleid, waar ze een enzym in de HMG-CoA-reductase route remmen en apoptotische celdood van osteoclasten bevorderen.7 Door osteoclast-gemedieerde botresorptie te blokkeren, zijn bisfosfonaten doeltreffend bij de behandeling van de hypercalciëmie die optreedt bij een aantal botresorberende ziekteprocessen, waaronder maligne hypercalciëmie. Als betrekkelijk niet-toxische verbindingen, die in staat zijn een diepgaande en aanhoudende verlaging van het serumcalcium te bewerkstelligen, hebben deze middelen de voorkeur gekregen bij de behandeling van acute en chronische hypercalciëmie als gevolg van maligniteit.
Er zijn vijf parenterale bisfosfonaten beschikbaar voor de behandeling van maligne hypercalciëmie: pamidronaat, zoledroninezuur, ibandronaat, etidronaat, en clodronaat. Etidronaat en clodronaat zijn middelen van de eerste generatie, die minder krachtig zijn en meer bijwerkingen hebben dan andere middelen en niet zo vaak worden gebruikt. Ibandronaat is een nuttig middel met een lange halfwaardetijd waarvan is aangetoond dat het even effectief is als pamidronaat, hoewel het niet zo uitgebreid is bestudeerd als de andere middelen.
Pamidronaat is grondig bestudeerd in meerdere observationele en gerandomiseerde onderzoeken, en er is aangetoond dat het zeer effectief en minimaal toxisch is bij de behandeling van hypercalciëmie door meerdere oorzaken, waaronder kwaadaardige hypercalciëmie.8,9 Een maximaal calciumverlagend effect treedt op bij een dosis van 90 mg, en de dosis wordt vaak getitreerd op basis van het gemeten serumcalcium. Het wordt gedurende twee tot vier uur toegediend, heeft binnen één tot twee dagen een verlagend effect op het serumcalcium en heeft een aanhoudend effect dat tot twee weken of langer aanhoudt.
Als het krachtigste en gemakkelijkst toe te dienen bisfosfonaat wordt zoledroninezuur door velen beschouwd als het middel bij uitstek voor de behandeling van maligne hypercalciëmie. Het kan worden toegediend als een dosis van 4 mg-8 mg intraveneus in 15 minuten (vergeleken met twee uur voor pamidronaat). Twee fase III-studies met 275 patiënten hebben de superieure doeltreffendheid van zoledroninezuur in vergelijking met pamidronaat aangetoond, waarbij 88% van de patiënten een genormaliseerd serumcalcium bereikte (vergeleken met 70% van de patiënten die een dosis pamidronaat van 90 mg kregen).10
Ondanks het feit dat deze middelen betrekkelijk niet toxisch zijn, kunnen zij bij de ontvangers een milde, voorbijgaande flulachtige ziekte veroorzaken. Nierdisfunctie is zelden waargenomen. Deze middelen moeten renaal worden gedoseerd en met voorzichtigheid worden gebruikt bij patiënten met gevorderde nierinsufficiëntie (serumcreatinine >2,5). Osteonecrose van de kaak is waargenomen bij minder dan 2% van de patiënten die IV bisfosfonaten kregen. Daarom wordt aanbevolen dat patiënten een tandheelkundig onderzoek ondergaan voordat zij het middel krijgen toegediend (indien mogelijk) en invasieve tandheelkundige ingrepen vermijden rond de tijd dat zij het middel krijgen toegediend.11
 klik voor grote versie
klik voor grote versie
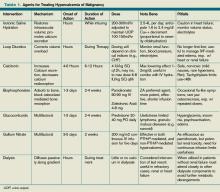
Tabel 1. Agents for Treating Hypercalcemia of Malignancy
Andere therapeutische interventies. De bisfosfonaten zijn de best bestudeerde en meest effectieve farmaceutische middelen die beschikbaar zijn om hypercalciëmie te behandelen. Van deze middelen mag alleen worden afgeweken wanneer zij gecontra-indiceerd zijn, in ernstige omstandigheden, of nadat de patiënt niet heeft gereageerd.
Calcitonine is al lang door de FDA goedgekeurd voor de behandeling van hypercalciëmie bij volwassenen. Het is aangetoond in kleine, niet-gerandomiseerde studies uit de jaren ’70 en ’80 om snel (binnen twee uur) calciumspiegels te verlagen bij hypercalcemische patiënten.12,13,14 Deze verlagingen zijn echter klein (<10%) en van voorbijgaande aard (meestal aanhoudend tot 72 tot 96 uur) als gevolg van de tachyphylaxsis die met deze medicatie is opgemerkt. Desalniettemin kan calcitonine worden gebruikt als een adjuvante overbrugging om calciumspiegels te verlagen bij ernstig hypercalcemische patiënten gedurende de eerste paar dagen voordat andere middelen effect beginnen te krijgen.
Glucocorticoïden worden sinds de jaren 1950 gebruikt om hypercalciëmie te behandelen. Prednison, dexamethason en methylprednisolon hebben alle een FDA-indicatie voor hypercalciëmie, maar gegevens ontbreken en zijn tegenstrijdig. Een kleine (n=28) gerandomiseerde gecontroleerde trial (RCT) uitgevoerd in 1984 toonde geen extra werkzaamheid van glucocorticoïden met IV-vloeistoffen in vergelijking met IV-vloeistoffen alleen.15 Een andere kleine (n=30) RCT uitgevoerd in 1992 bij vrouwen met uitgezaaide borstkanker toonde een significante verbetering bij patiënten die werden behandeld met prednisolon, IV-vloeistoffen en furosemide in vergelijking met IV-vloeistoffen en furosemide.16 Andere niet-gerandomiseerde trials toonden aan dat de respons op zijn best onvoorspelbaar is.17 Desondanks blijven glucocorticoïden waarschijnlijk een beperkte rol spelen voor behandeling in specifieke gevallen, waaronder hypercalciëmie geïnduceerd door lymfomen die de niveaus van 1,25(OH)2 vitamine D verhogen (aangezien dit interageert met een steroïdgereguleerde receptor), of multipele myelomen waar ze mogelijk de ziekteprogressie beïnvloeden.
Galliumnitraat, een watervrij zout van een zwaar metaal, is in verschillende gerandomiseerde onderzoeken een effectief therapeutisch middel gebleken bij het verlagen van calciumspiegels bij hypercalcemische patiënten.18,19 Bovendien heeft een dubbelblind onderzoek bij 64 patiënten met hypercalciëmie als gevolg van een maligniteit aangetoond dat galliumnitraat ten minste even effectief is als pamidronaat voor de acute controle van kankergerelateerde hypercalciëmie.20 De noodzaak van continue infusie gedurende een periode van vijf dagen heeft de toepassing van dit middel echter beperkt.
Hemodialyse met een calciumarm dialysaat is in kleine, niet-gerandomiseerde studies een tijdelijk effectieve methode gebleken om de serumcalciumspiegel te verlagen.21,22 Deze behandelmethode kan echter het beste worden gereserveerd voor patiënten met ernstige hypercalciëmie, bij wie agressieve intravasculaire volumeaanvulling en bisfosfonaten niet raadzaam zijn (bijvoorbeeld patiënten met ernstig hart- of nierfalen) en met een onderliggende etiologie die waarschijnlijk wel op andere behandelingen reageert. Bovendien moet worden overwogen of dergelijke invasieve temporiserende procedures wel geschikt zijn bij patiënten met uitgezaaide kanker.
Terug naar de casus
Deze patiënt had een geïoniseerd calciumgehalte van 1,9 mmol/L (normaal 1,1-1,4 mmol/L). Hij werd gestart met agressieve IV hydratatie met normale zoutoplossing en zoledroninezuur. Zijn thuismedicatie werd bekeken, en er werd bevestigd dat hij geen gecontra-indiceerde medicatie nam zoals thiaziden of calcium/vitamine D-supplementen.
Verder onderzoek naar de etiologie van zijn hypercalcemie toonde een juist onderdrukt, intact PTH en normale 25 (OH) vitamine D- en 1,25 (OH)2 vitamine D-spiegels. Zijn intacte PTH-RP was verhoogd met 10 pmol/L, en consistent met hypercalciëmie van maligniteit.
Oncologie en palliatieve zorg consulten werden aangevraagd om te helpen met de coördinatie van de behandeling van de onderliggende longkanker van de patiënt; plannen werden gemaakt voor systemische chemotherapie. Zijn symptomen verbeterden langzaam, en 72 uur na opname was zijn serumcalcium genormaliseerd. Hij werd ontslagen met een plan om chemotherapie te starten en verdere follow-up met oncologie.
Bottom Line
Acute behandeling van hypercalciëmie van maligniteit richt zich op het verlagen van het serumcalcium door middel van een verscheidenheid aan farmacologische middelen. Echter, langetermijnkwesties zoals behandeling van de onderliggende maligniteit en discussies over de doelen van zorg in deze patiëntenpopulatie met hoge mortaliteit zijn van het grootste belang. TH
Dr. Hartley en Dr. Repaskey zijn klinisch instructeurs in interne geneeskunde aan de University of Michigan Health System. Dr. Rohde is een klinisch assistent-professor interne geneeskunde aan UMHS.
- Assadi F. Hypercalcemia: een evidence-based benadering van klinische gevallen. Iran J Kidney Dis. 2009;3:(2):71-79.
- Stewart A. Hypercalcemia associated with cancer. N Engl J Med. 2005;542(4):373-379.
- Seccareccia D. Kanker-gerelateerde hypercalciëmie. Can Fam Physician. 2010;56:(3):244-246.
- Bilezikian JP. Beheer van acute hypercalciëmie. N Engl J Med. 1992; 326(18):1196-1203.
- Suki WN, Yium JJ, VonMinden M, et al. Acute behandeling van hypercalciëmie met furosemide. N Engl J Med. 1970;283:836-840.
- LeGrand SB, Leskuski D, Zama I. Narrative review: furosemide for hypercalcemia: an unproven yet common practice. Ann Intern Med. 2008;149:259-263.
- Drake MT, Bart LC, Khosla S. Bisphosphonates: mechanism of action and role in clinical practice. Mayo Clinic Proc. 2008;83(9):1032-1045.
- Nussbaum SR, Younger J, Vandepol CJ, et al. Single-dose intravenous therapy with pamidronate for the treatment of hypercalcemia of malignancy: comparison of 30-, 60-, and 90-mg dosages. Am J Med. 1993; 95(3):297-304.
- Gucalp R, Ritch P, Riernik PH, et al. Comparative study of pamidronate disodium and etidronate disodium in the treatment of cancer-related hypercalcemia. J Clin Oncol. 1992;10(1):134-142.
- Major P, Lortholary A, Hon J, et al. Zoledroninezuur is superieur aan pamidronaat bij de behandeling van hypercalciëmie van maligniteit: een gepoolde analyse van twee gerandomiseerde, gecontroleerde klinische trials. J Clin Oncol. 2001;19(2): 558-567.
- Tanvetyanon T. Management of the adverse effects associated with intravenous bisphosphonates. Ann Oncol. 2006;17(6):897-907.
- Wisneski LA, Croom WP, Silva OL, et al. Salmon calcitonin in hypercalcemia. Clin Pharmacol Ther. 1978; 24:219-222.
- Binstock ML, Mundy GR. Effect of calcitonin and glucocorticoids in combination on the hypercalcemia of malignancy. Ann Intern Med. 1980;93(2):269-272.
- Nilsson O, Almqvist S, Karlberg BE. Salmon calcitonin in the acute treatment of moderate and severe hypercalcemia in man. Acta Med Scand. 1978;204(4): 249-252.
- Percival RC, Yates AJ, Gray RE, et al. Role of glucocorticoids in management of malignant hypercalcemia. Br Med J. 1984;289(6440):287.
- Kristensen B, Ejlertsen B, Holmegaard SN, et al. Prednisolone in the treatment of severe malignant hypercalcemia in metastatic breast cancer: a randomized study. J Intern Med. 1992;232(3):237-245.
- Thalassinos NC, Joplin GF. Failure of corticosteroid therapy to correct the hypercalcemia of malignant disease. Lancet. 1970;2(7672):537-538.
- Warrell RP Jr, Murphy WK, Schulman P, et al. A randomized double-blind study of gallium nitrate compared with etidronate for acute control of cancer-related hypercalcemia. J Clin Oncol. 1991;9(8):1467-1475.
- Warrell RP Jr, Israel R, Frisone M, et al. Gallium nitrate for acute treatment of cancer-related hypercalcemia: a randomized, double-blinded comparison to calcitonin. Ann Intern Med. 1988;108:669-674.
- Cvitkovic F, Armand JP, Tubiana-Hulin M, et al. Randomized, double-blind, phase II trial of galliumnitraat compared with pamidronate for acute control of cancer-related hypercalcemia. Cancer J. 2006;12 (1):47-53.
- Cardella CJ, Birkin BL, Rapoport A. Role of dialysis in the treatment of severe hypercalcemia: report of two cases successfully treated with hemodialysis and review of the literature. Clin Nephrol. 1979; 12(6):285-290.
- Koo WS, Jeon DS, Ahn SJ, et al. Calciumvrije hemodialyse voor de behandeling van hypercalciëmie. Nephron. 1996;72(3):424-428.