Cahn-Ingold-Prelog-prioriteringar (2): Determining R/S On Rings, Chains, And More
Detta inlägg är skrivet tillsammans med Matt Pierce från Organic Chemistry Solutions. Fråga Matt om att schemalägga en handledningssession online här.
I det här inlägget utökar vi Cahn-Ingold-Prelog-reglerna (CIP) och visar hur man tilldelar R/S i några knepigare fall som involverar ringar, flera chirala centra, flera bindningar och isotoper. Vi kommer att se att ”prickmetoden” är mycket värdefull för att bryta olikheter vid fastställandet av CIP-prioriteringar!
Innehållsförteckning
- Sammanfattning:
- Hur tilldelar vi CIP-prioriteringar i knepigare fall med ringar, flera kirala centra, flera bindningar och isotoper?
- Hänvisning: Cahn-Ingold-Prelog-prioriteringar bestäms vid den första skillnaden
- Ansättning av CIP-prioriteringar:
- Hur bestämmer vi R/S-konfiguration i ringar?
- Bestämning av R/S-konfiguration i ringar: En vanlig ”knepfråga”
- Ansättning av R/S-konfigurationer för molekyler med flera chirala centra
- Ansättning av Cahn-Ingold-Prelog (CIP)-prioriteringar med multipla bindningar
- Utvidgning av multipla bindningar med ”fantomatomer”
- Cahn-Ingold-Prelog-prioriteringar med isotoper
- Slutsats: Tilldelning av R/S-konfigurationer med ”The Method Of Dots”
- Anteckningar
- 1. Recap: I vårt första inlägg om Cahn-Ingold-Prelog-reglerna (CIP) gav vi en bred översikt över hur man tilldelar R eller S till chirala centra i en molekyl. Vi följde upp detta med ett efterföljande inlägg om hur man använder CIP-reglerna för att bestämma prioriteringar i alkener för att avgöra om de är E eller Z.
- 2. Hur tilldelar vi CIP-prioriteringar i knepigare fall som involverar ringar, flera kirala centra, flera bindningar och isotoper?
- 3. Påminnelse: Cahn-Ingold-Prelog Prioriteterna bestäms vid den första differenspunkten
- 4. Tilldelning av CIP-prioriteringar: An Application Of The ”Method Of Dots”
- 5. Hur bestämmer vi R/S-konfiguration i ringar?
- 6. Bestämning av R/S-konfiguration i ringar: Det finns faktiskt ett fall där det kan verka konstigt för den oinvigde att bestämma R/S i en ring.
- Att tilldela R/S-konfigurationer till molekyler med flera kirala centra
- Att tilldela Cahn-Ingold-Prelog (CIP)-prioriteringar (CIP) med flera bindningar
- 9. Expanding Out Multiple Bonds With ”Phantom Atoms”
- Cahn-Ingold-Prelog Priorities With Isotopes
- Slutsats: För de flesta fall kan man med hjälp av ”The Method Of Dots”
- Anteckningar
1. Recap: I vårt första inlägg om Cahn-Ingold-Prelog-reglerna (CIP) gav vi en bred översikt över hur man tilldelar R eller S till chirala centra i en molekyl. Vi följde upp detta med ett efterföljande inlägg om hur man använder CIP-reglerna för att bestämma prioriteringar i alkener för att avgöra om de är E eller Z.
Som med de flesta introducerande inlägg var de valda exemplen ganska enkla. Det är ganska enkelt att tilldela prioriteringar i en molekyl som molekylerna nedan där det centrala kolet är knutet till fyra atomer med olika atomvikter. Och som vi diskuterade tidigare är det, när man väl lärt sig regeln om enkel byte, tillräckligt enkelt att bestämma R/S i de fall då substituenten med prioritet nr 4 inte pekar bakom sidans plan.
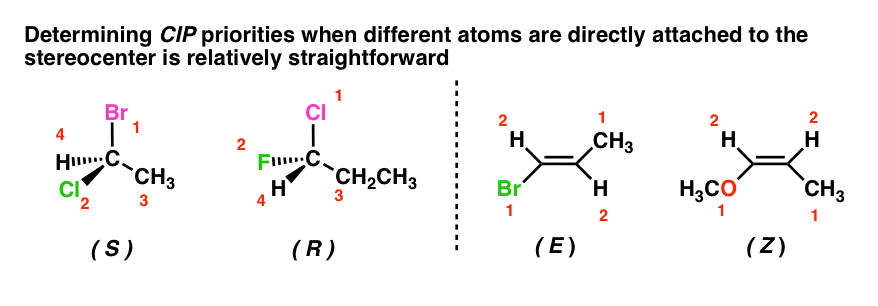
I de fall där stereocentrarna är knutna till identiska atomer såg vi att det också är ganska okomplicerat att använda ”prickmetoden” för att bryta band och förflytta sig nedåt i kedjan. Mer om det om en stund: här finns några övningar som du kan öva på om du vill.
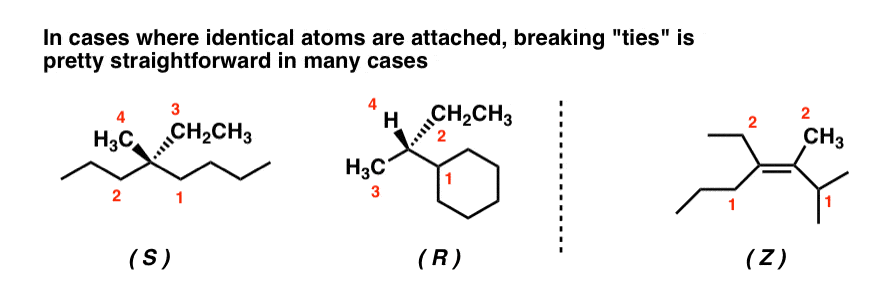
2. Hur tilldelar vi CIP-prioriteringar i knepigare fall som involverar ringar, flera kirala centra, flera bindningar och isotoper?
Detta inlägg handlar om några av de ytterligare komplikationer som vi ser vid tilldelningen av prioriteringar. Hur tilldelar man till exempel prioriteringar i följande fall:
- Ringar
- Multipla chirala centra
- Hantering av flera bindningar
- Hur är det med isotoper?
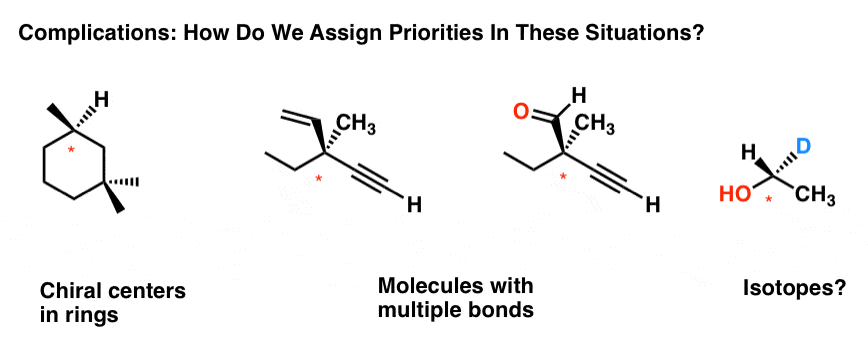
Detta inlägg är ägnat åt att reda ut dessa lite knepigare fall. Vi kommer uteslutande att fokusera på att bestämma R/S men samma prioriteringsregler gäller även för att bestämma (E/Z).
3. Påminnelse: Cahn-Ingold-Prelog Prioriteterna bestäms vid den första differenspunkten
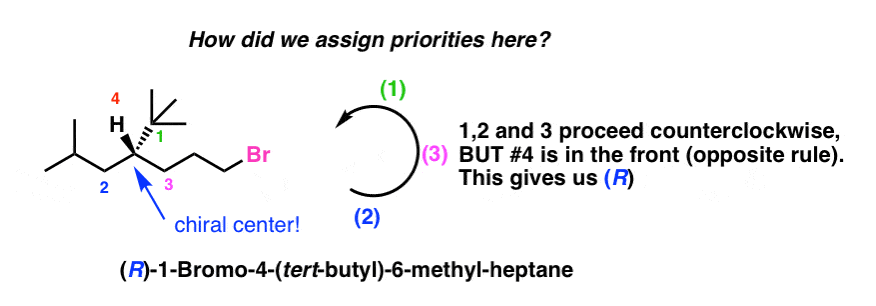
Låt oss börja med en vanlig knepfråga. Vilken är den högst prioriterade ”gruppen” som är knuten till det chirala centret i molekylen nedan? Tilldela R/S .
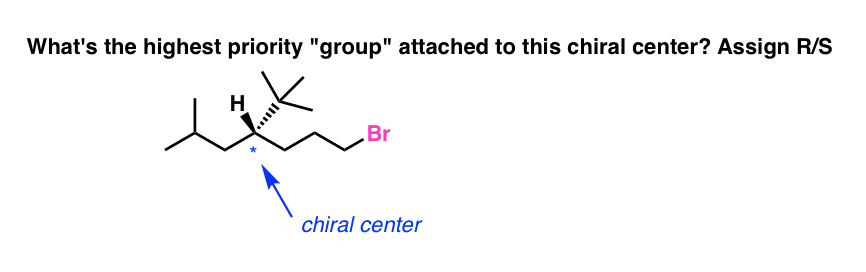
Din första instinkt kanske är att säga ”kolkedjan som innehåller brom”, eftersom brom har det högsta atomnumret av alla atomer i molekylen.
I själva verket är kolkedjan som innehåller brom den tredje prioriterade gruppen (endast väte är lägre!), vilket ger det kirala centret en R-konfiguration.
Detta beror på det sätt som prioriteringarna tilldelas: vi rör oss utåt från det kirala centret, ett kol i taget, och bestämmer prioriteringarna vid den första skillnaden.
4. Tilldelning av CIP-prioriteringar: An Application Of The ”Method Of Dots”
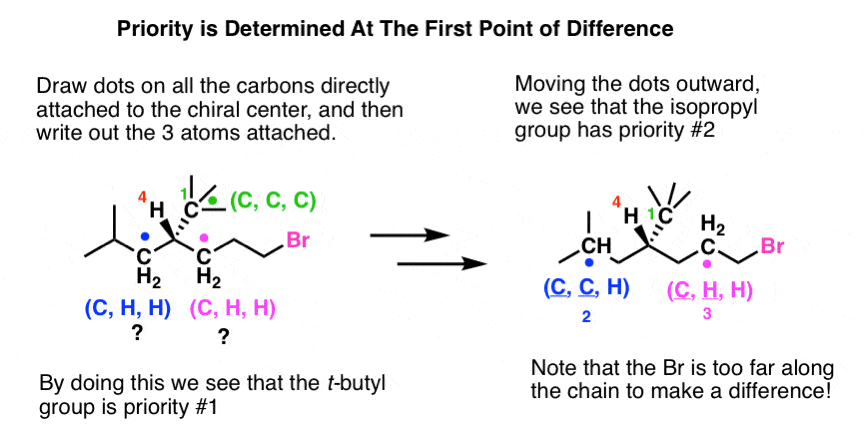
Processen för att tilldela prioriteringar här är i huvudsak identisk med vad vi visade tidigare:
- Först jämför du de fyra atomer som är direkt bundna till det chirala kolet och rangordnar dem baserat på atomnummer. I vårt exempel är H helt klart prioritet nr 4.
- Om det är oavgjort, lista alla tre atomer som är direkt bundna till de oavgjorda atomerna i fallande ordning efter atomnummer. Jag tycker att det är bra att sätta prickar på varje atom som jag jämför, vilket är anledningen till att jag kallar denna metod för ”The Method of Dots”).
- Genomför varje lista, atom för atom. Gruppen t-butyl (C(CH3)3) har högst prioritet . men vi kan fortfarande inte skilja isobutylgruppen eller bromopropylgruppen åt.
- Då det fortfarande är oavgjort flyttar vi prickarna ett steg längre ner i kedjan, närmare bestämt till nästa kolatom eftersom den har det högsta atomnumret (prickarna hjälper oss att hålla reda på var vi är). Detta gör att vi nu kan tilldela prioriteringarna #2 och #3 .
- Med alla prioriteringar tilldelade är vi redo att tilldela R och S genom att spåra vägen för 1 → 3. Eftersom #4 ligger på en kil innebär rotationen moturs en R-konfiguration (”motsatt regel”).
Om detta fortfarande är oklart kan du hålla muspekaren här för att få en popup-visning eller klicka här för att få upp en bild med en fullständig steg-för-steg-behandling.
5. Hur bestämmer vi R/S-konfiguration i ringar?
Det krävs faktiskt inga nya regler för att bestämma prioriteringar i ringar, men många elever berättar för mig att de har svårt att bestämma R/S om ett chiralt centrum finns på en ring. Låt oss därför gå igenom ett exempel och försöka göra detta så tydligt som möjligt.
Bestämma R/S på en ring är bara metoden med prickar om och om igen. Vi rör oss bara längs kedjan bort från det chirala centret tills vi hittar en skillnadspunkt. Nedan måste vi flytta två kolväten bort från det kirala centret för att prioritera (C,C,C) framför (C,H,H):
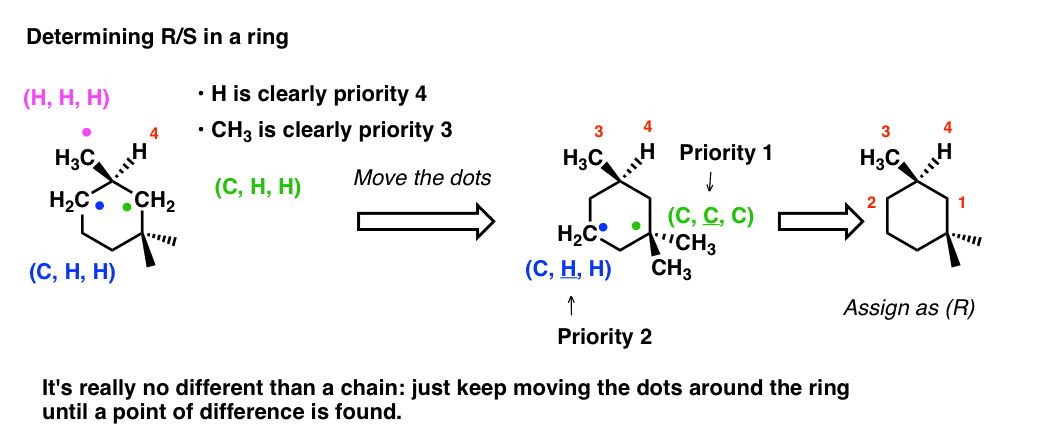
6. Bestämning av R/S-konfiguration i ringar: Det finns faktiskt ett fall där det kan verka konstigt för den oinvigde att bestämma R/S i en ring.
Molekylen nedan har kilar och streck som anger stereokemin för två kolväten. Vad skulle hända om du ombads att bestämma R/S för det kol som står i stjärnan?
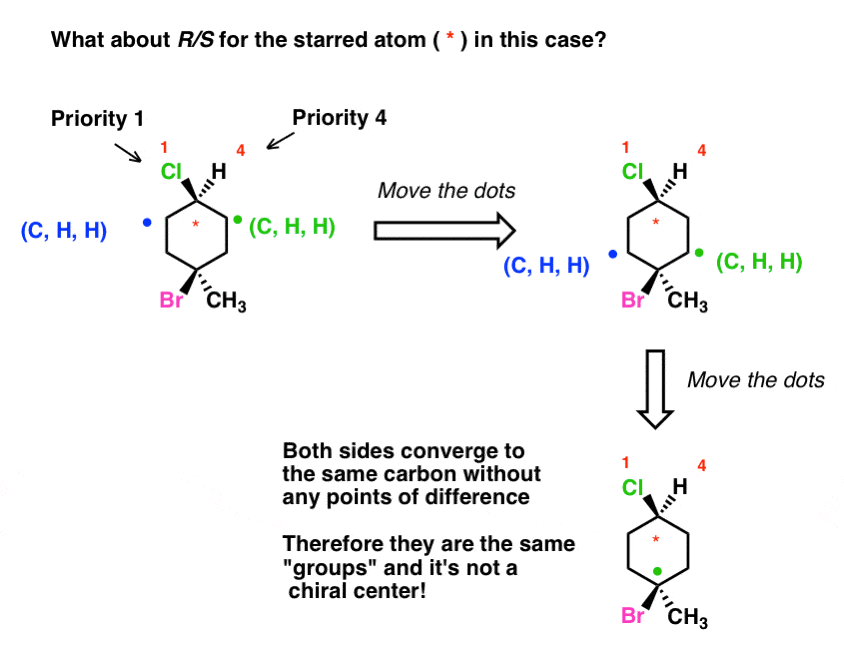
Förhoppningsvis ser du att detta faktiskt är en ”trickfråga”. När vi försöker bestämma en skillnadspunkt slutar det med att vi konvergerar tillbaka till det nedersta kolet utan att hitta en enda skillnad. Vad detta betyder är att dessa två ”grupper” faktiskt är desamma och att det ”stjärniga” kolet inte är ett kiralt centrum.
Att tilldela R/S-konfigurationer till molekyler med flera kirala centra
Molekyler med flera kirala centra kräver faktiskt inte heller några nya begrepp. Vi behöver bara identifiera varje chiralt centrum och bestämma R eller S för vart och ett. När vi sätter ihop det slutliga namnet måste vi sedan ange konfigurationen för varje kol i början av namnet.

Härav följer att molekylen ovan är (1R, 3R, 4S)-3-bromo-4-etyl-1-metyl-1-propylcyclopentan.
Om du vill se exakt hur tilldelningen för (S)-konfigurationen gjordes, håll muspekaren här för att få en popup-visning eller följ den här länken till en bild.
Att tilldela Cahn-Ingold-Prelog (CIP)-prioriteringar (CIP) med flera bindningar
Exemplen hittills har egentligen inte krävt några nya begrepp. De regler vi har sett hittills börjar dock bryta samman när flera bindningar kommer in i bilden.
Till exempel är det inte intuitivt logiskt att en metylgrupp skulle ha högre prioritet än en alken.
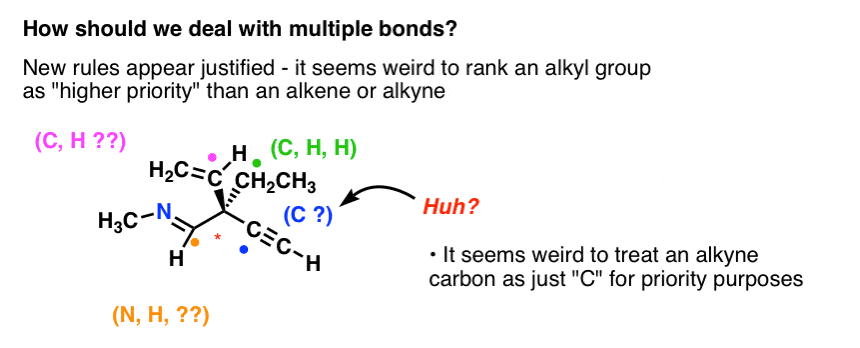
Det är tydligt att det behövs en ny regel för att hantera flera bindningar.
9. Expanding Out Multiple Bonds With ”Phantom Atoms”
Lösningen är att ”expandera” varje multipelbindning som en enda bindning knuten till en ”fantomatom” (i blått).
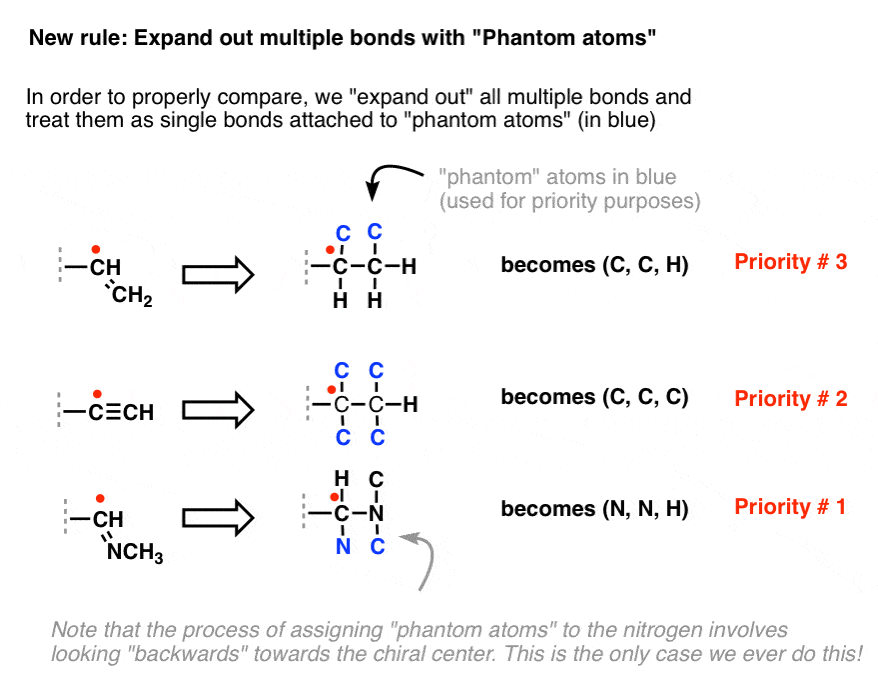
Dessa ”fantomatomer” används enbart i syfte att fastställa CIP-prioritet – de har ingen kemisk betydelse.
Bemärk att i processen för att tilldela fantomatomer till båda atomer i en multipelbindning innebär att den mer avlägsna atomen ”tittar bakåt” mot det chirala centret. Detta är den enda gången som vi någonsin får göra detta!
Om vi tillämpar metoden med ”fantomatomer” på flerbindningarna i denna molekyl ser vi då att alken faktiskt har högre prioritet än alken, som har högre prioritet än etyl.

Om processen med att tilldela prioriteter till denna molekyl verkade otydlig, kan du hålla muspekaren över den här för att få en popup-visning eller klicka på den här för att se en bild som går igenom tilldelningen.
För en god stund kan du försöka använda vår nya metod för att bestämma prioriteringen av vinyl-, isopropyl- och s-butylgrupper (nedan).

Processen beskrivs ganska tätt här.
Cahn-Ingold-Prelog Priorities With Isotopes
finns det en punkt där vi slutar bry oss om skillnader? Låt oss till exempel säga att vi förbereder en molekyl med deuterium i stället för väte som i molekylen nedan. Räknas detta fortfarande som ett chiralt centrum?

Ja, detta räknas absolut som ett chiralt centrum. (Huruvida det skulle ha en betydande optisk rotation är en annan sak).
Att tilldela prioritet här är faktiskt ganska okomplicerat. I fall där atomnumren är desamma bryter vi band genom att tilldela högsta prioritet till högre atomvikter.
För väte innebär det att tritium (3H) prioriteras framför deuterium (2H) som prioriteras framför protium (1H).

Givetvis är detta inte den typ av situation som man troligen stöter på i introduktionskursen i organiska ämnen. Men den dyker upp! Och förresten, att förbereda chirala molekyler som innehåller deuterium är inte bara en teoretisk övning – det har varit enormt fördelaktigt för att bestämma enzymernas verkningsmekanism. Se till exempel här.
Slutsats: För de flesta fall kan man med hjälp av ”The Method Of Dots”
För de flesta fall kan man med hjälp av ”The Method Of Dots” komma dit man behöver komma för att bestämma prioriteringarna för ett chiralt centrum. En viktig sak från det här inlägget att komma ihåg är begreppet ”fantomatomer” för att bestämma prioriteringar i alkener och andra multipla bindningar.
Är det något som saknas och som du vill prata om? Lämna en kommentar!
Tack återigen till Matt för hans hjälp med det här inlägget. Anlita Matt som din handledare!
Anteckningar
- Här är ett riktigt intressant exempel på fantomatomer i aktion. Att ändra en grupp på kväve från H till CH3 resulterar i ett byte av konfiguration från (S) till (R). Big Hat Tip to r/dennisdcao
http://imgur.com/WLmmDNM - Detta inlägg tog inte heller upp den kiralitet som finns i allener och andra arter med en kiralitetsaxel. I dessa fall använder vi inte R/S utan P/M. CIP:s prioritetsregler fungerar dock fortfarande.
- Det här har inte tagits upp, men… är det mittersta kolet här ett kiralt centrum?
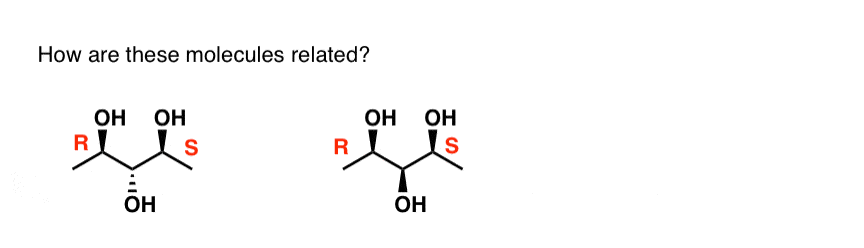
Inte helt och hållet. Det mittersta kolet är ett så kallat pseudoasymmetriskt centrum. Det har fyra olika substituenter – det chirala centret (R) skiljer sig från det chirala centret (S). IUPAC-regeln är att (R) har företräde framför (S). De små bokstäverna (r) och (s) används i detta fall. Mer om detta ämne här.
4. Farbror Al har ett (teoretiskt) exempel på en molekyl där CIP-reglerna inte fungerar. Farbror Al har också några ganska starka åsikter om kiralitet.