Cahn-Ingold-Prelog prioriteettien määrittäminen (2): Determining R/S On Rings, Chains, And More
Tämä postaus on kirjoitettu yhdessä Matt Piercen kanssa Organic Chemistry Solutionsista. Kysy Mattilta verkko-opetussession sopimisesta täältä.
Tässä postauksessa laajennamme Cahn-Ingold-Prelog (CIP) -sääntöjä ja näytämme, miten R/S määritetään joissakin hankalammissa tapauksissa, joihin liittyy renkaita, useita kiraalisia keskuksia, useita sidoksia ja isotooppeja. Näemme, että ”pistemenetelmä” on erittäin arvokas keino ratkaista tasapelejä CIP-prioriteettien määrittämisessä!
Sisällysluettelo
- Kokoelma: CIP-prioriteettien määrittäminen suoraviivaisissa tapauksissa
- Miten määrittelemme CIP-prioriteetteja hankalammissa tapauksissa, joihin liittyy renkaita, useita kiraalisia keskuksia, useita sidoksia ja isotooppeja?
- Muistutus: Cahn-Ingold-Prelog-prioriteetit määritetään ensimmäisessä erotuskohdassa
- CIP-prioriteettien määrittäminen: An Application Of The ”Method Of Dots”
- How Do We Determine R/S Configuration In Rings?
- R/S-konfiguraation määrittäminen renkaissa: A Common ”Trick Question”
- Assigning R/S Configurations To Molecules With Multiple Chiral Centers
- Assigning Cahn-Ingold-Prelog (CIP) Priorities With Multiple Bonds
- Expanding Out Multiple Bonds With ”Phantom Atoms”
- Cahn-Ingold-Prelog Priorities With Isotopes
- Conclusion:
- Huomautuksia
- 1. Yhteenveto: CIP-prioriteettien määrittäminen suoraviivaisissa tapauksissa
- 2. Miten osoitamme CIP-prioriteetteja hankalammissa tapauksissa, joissa on mukana renkaita, useita kiraalisia keskuksia, useita sidoksia ja isotooppeja?
- 3. Muistutus: Cahn-Ingold-Prelog Prioriteetit määräytyvät ensimmäisessä eropisteessä
- 4. CIP-prioriteettien osoittaminen: An Application Of The ”Method Of Dots”
- 5. Miten määrittelemme R/S-konfiguraation renkaissa?
- 6. Determining R/S Configuration In Rings: Yleinen ”temppukysymys”
- R/S-konfiguraatioiden osoittaminen molekyyleille, joilla on useita kiraalisia keskuksia
- Cahn-Ingold-Prelog (CIP) -prioriteettien määrittäminen useilla sidoksilla
- 9. JOHTOPÄÄTÖKSET. Moninkertaisten sidosten laajentaminen ”fantomiatomien” avulla
- Cahn-Ingold-Prelog Prioriteetit isotooppeja käytettäessä
- Johtopäätös: R/S-konfiguraatioiden määrittäminen ”pistemenetelmällä”
- Huomautuksia
1. Yhteenveto: CIP-prioriteettien määrittäminen suoraviivaisissa tapauksissa
Ensimmäisessä Cahn-Ingold-Prelog (CIP) -sääntöjä käsittelevässä kirjoituksessamme annoimme laajan yleiskatsauksen siitä, miten R- tai S-konfiguraatioita osoitetaan molekyylin kiraalikeskuksille. Jatkoimme tätä seuraavalla postauksella siitä, miten CIP-sääntöjä käytetään alkeenien prioriteettien määrittämiseen sen määrittämiseksi, ovatko ne E:tä vai Z:tä.
Kuten useimmissa johdantopostauksissa, valitut esimerkit olivat melko yksinkertaisia. On melko suoraviivaista määrittää prioriteetit alla olevien molekyylien kaltaisessa molekyylissä, jossa keskushiili on kiinnittynyt neljään atomiin, joilla on eri atomipainot. Ja kuten aiemmin keskustelimme, kun opit yhden vaihdon säännön, R/S:n määrittäminen on riittävän helppoa tapauksissa, joissa prioriteettisubstituentti #4 ei osoita sivun tason taakse.
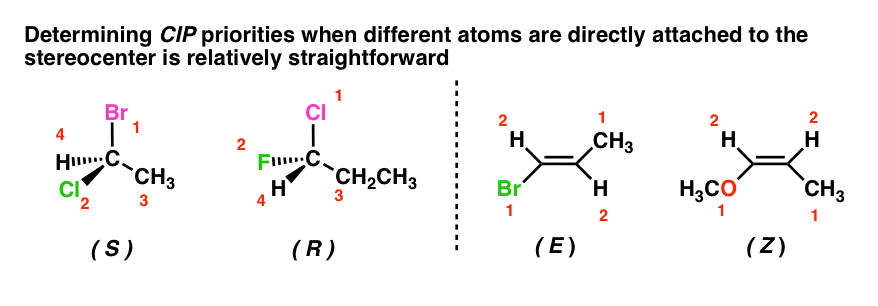
Tapauksissa, joissa stereosentriset hiilet ovat kiinnittyneet identtisiin atomeihin, näimme, että ”pistemenetelmän” käyttäminen tasapisteiden katkaisemiseen ja ketjussa alaspäin etenemiseen on myös melko suoraviivaista. Tästä lisää hetken kuluttua: tässä on muutamia harjoituksia, joita voit halutessasi harjoitella.
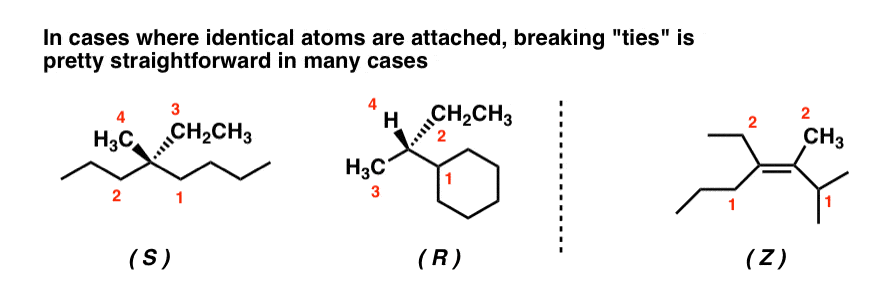
2. Miten osoitamme CIP-prioriteetteja hankalammissa tapauksissa, joissa on mukana renkaita, useita kiraalisia keskuksia, useita sidoksia ja isotooppeja?
Tässä postauksessa käsittelemme joitain lisäkomplikaatioita prioriteettien osoittamisessa. Miten esimerkiksi asetat prioriteetit seuraavissa tapauksissa:
- Renkaat
- Moninkertaiset kiraaliset keskukset
- Moninkertaisten sidosten käsittely
- Entä isotoopit?
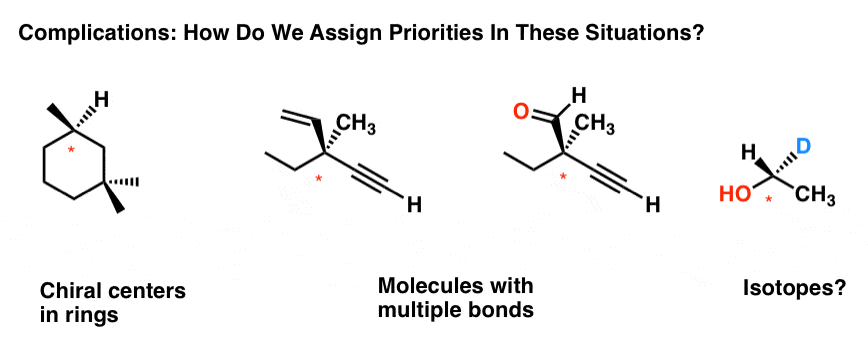
Tämä postaus on omistettu näiden hiukan hankalampien tapausten selvittämiselle. Keskitymme yksinomaan R/S:n määrittämiseen, mutta samat prioriteettisäännöt pätevät myös (E/Z:n) määrittämiseen.
3. Muistutus: Cahn-Ingold-Prelog Prioriteetit määräytyvät ensimmäisessä eropisteessä
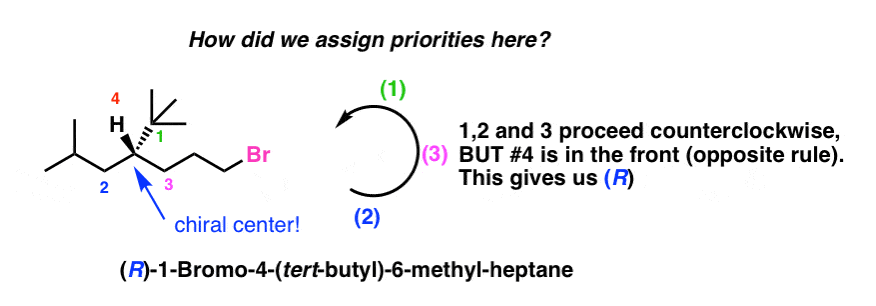
Aloitetaan yleisestä temppukysymyksestä. Mikä on korkeimman prioriteetin ”ryhmä”, joka on liitetty alla olevan molekyylin kiraaliseen keskukseen? Määritä R/S .
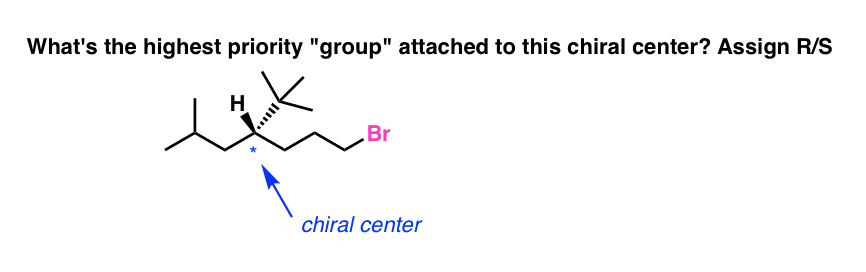
Ensimmäinen vaistosi saattaa olla sanoa: ”bromia sisältävä hiiliketju”, koska bromilla on molekyylin kaikista atomeista korkein järjestysluku.
Tosiasiassa bromia sisältävä hiiliketju on kolmanneksi ensisijainen ryhmä (vain vety on alempana)!), mikä antaa kiraalikeskukselle R-konfiguraation.
Tämä johtuu tavasta, jolla prioriteetit määritetään: siirrymme ulospäin kiraalisesta keskuksesta hiili kerrallaan ja määrittelemme prioriteetit ensimmäisessä eripisteessä.
4. CIP-prioriteettien osoittaminen: An Application Of The ”Method Of Dots”
Tämä prioriteettien määritysprosessi on tässä olennaisesti samanlainen kuin aiemmin osoittamamme:
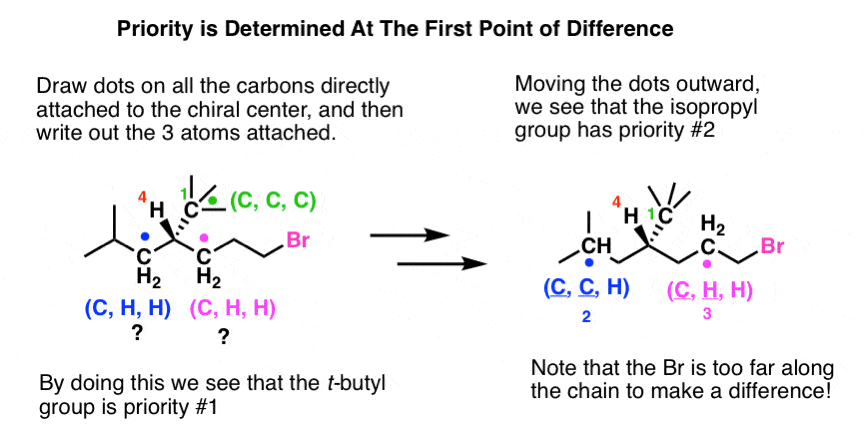
- Vertaillaan ensin neljää suoraan kiraaliseen hiileen sitoutunutta atomia ja asetetaan ne paremmuusjärjestykseen atominumeron perusteella. Esimerkissämme H on selvästi prioriteetti nro 4.
- Jos on tasapeli, luetellaan kaikki kolme atomia, jotka ovat suoraan sidoksissa tasapelissä oleviin atomeihin, atomiluvun mukaisessa laskevassa järjestyksessä. Minusta on hyödyllistä laittaa pisteitä jokaisen vertailemani atomin kohdalle, minkä vuoksi kutsun tätä menetelmää pisteiden menetelmäksi.)
- Vertaile jokaista listaa atomi atomilta. T-butyyli (C(CH3)3)-ryhmällä on korkein prioriteetti . mutta emme silti pysty erottamaan isobutyyli- tai bromipropyyliryhmää.
- Koska on edelleen tasapeli, siirretään pisteet yhden askeleen alemmas ketjussa, tarkemmin sanottuna seuraavaan hiileen, koska sillä on korkein järjestysluku (pisteet auttavat meitä pitämään kirjaa siitä, missä olemme). Näin voimme nyt määrittää prioriteetit #2 ja #3 .
- Kun kaikki prioriteetit on määritetty, olemme valmiita määrittämään R:n ja S:n jäljittämällä polun 1 → 3. Koska #4 on kiilan päällä, kierto vastapäivään merkitsee R-konfiguraatiota (”päinvastainen sääntö”).
- Tässä on todella mielenkiintoinen esimerkki haamuatomeista toiminnassa. Typen ryhmän vaihtaminen H:sta CH3:ksi johtaa konfiguraation vaihtumiseen (S):stä (R):ksi. Big Hat Tip to r/dennisdcao
http://imgur.com/WLmmDNM - Tässä postauksessa ei myöskään käsitelty alleeneissa ja muissa akselilla kiraalisuutta omaavissa lajeissa esiintyvää kiraalisuutta. Näissä tapauksissa ei käytetä R/S, vaan P/M. CIP:n prioriteettisäännöt toimivat kuitenkin edelleen.
- Ei ole käsitelty tätä, mutta… onko tässä keskimmäinen hiili kiraalinen keskus?
Jos tämä on vielä epäselvää, siirrä hiiren leijailua tästä ponnahdusikkunanäkymään tai napsauta tästä saadaksesi näkyviin kuvan täydellisestä vaiheittaisesta käsittelystä.
5. Miten määrittelemme R/S-konfiguraation renkaissa?
Renkaiden prioriteettien määrittämiseen ei oikeastaan tarvita uusia sääntöjä, mutta monet opiskelijat kertovat minulle, että heillä on vaikeuksia määrittää R/S, jos kiraalinen keskus on renkaassa. Tästä syystä käydään läpi esimerkki ja yritetään tehdä asia mahdollisimman selväksi.
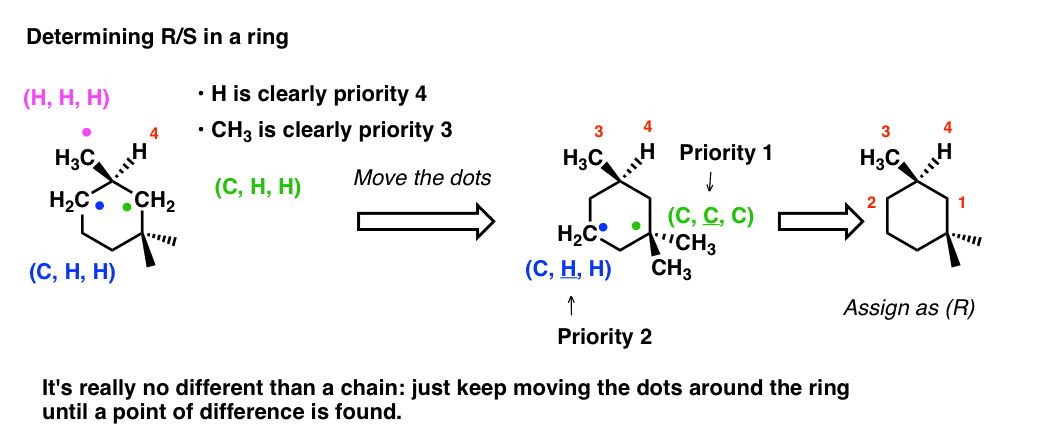
R/S:n määrittäminen renkaalla on vain pistemenetelmä uudestaan. Siirrymme vain ketjua pitkin poispäin kiraalisesta keskuksesta, kunnes löydämme eripisteen. Alla meidän on siirryttävä kaksi hiiltä poispäin kiraalisesta keskuksesta, jotta (C,C,C) asetetaan etusijalle (C,C,C) ennen (C,H,H):
6. Determining R/S Configuration In Rings: Yleinen ”temppukysymys”
On itse asiassa yksi tapaus, jossa R/S-konfiguraation määrittäminen renkaassa saattaa tuntua asiaan vihkiytymättömistä oudolta.
Alhaalla olevassa molekyylissä on kiiloja ja katkoviivoja, jotka osoittavat kahden hiilen stereokemian. Entä jos sinua pyydettäisiin määrittämään R/S tähtihiilen osalta?
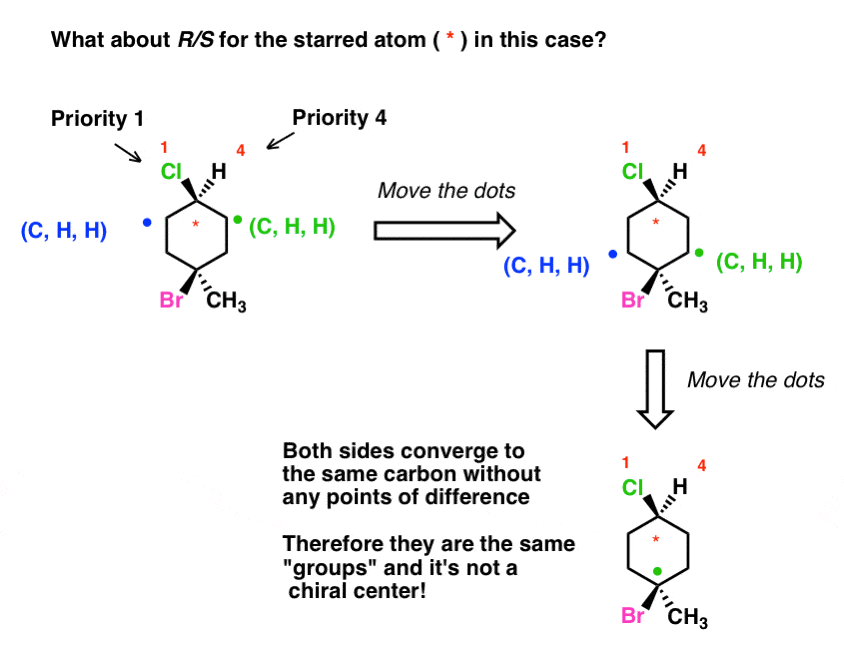
Toivottavasti huomaat, että tämä on itse asiassa ”temppukysymys”. Kun yritämme määrittää eropistettä, päädymme konvergoimaan takaisin pohjahiileen löytämättä yhtään eroa. Tämä tarkoittaa sitä, että nämä kaksi ”ryhmää” ovat itse asiassa samoja ja ”tähtihiili” ei ole kiraalinen keskus.
R/S-konfiguraatioiden osoittaminen molekyyleille, joilla on useita kiraalisia keskuksia
Molekyylit, joilla on useita kiraalisia keskuksia, eivät oikeastaan vaadi myöskään uusia käsitteitä. Meidän on vain tunnistettava jokainen kiraalinen keskus ja määritettävä R tai S kullekin. Kun kokoamme lopullisen nimen, meidän on sitten määritettävä kunkin hiilen konfiguraatio nimen alussa.

Yllä oleva molekyyli on siis (1R, 3R, 4S)-3-bromi-4-etyyli-1-metyyli-1-propyylisyklopentaani.
Jos haluat nähdä tarkalleen, miten (S)-konfiguraation määritys tehtiin, siirry tästä ponnahdusikkunaan tai seuraa tätä linkkiä kuvaan.
Cahn-Ingold-Prelog (CIP) -prioriteettien määrittäminen useilla sidoksilla
Esimerkit tähän mennessä eivät oikeastaan ole vaatineet mitään uusia käsitteitä. Tähän mennessä näkemämme säännöt alkavat kuitenkin hajota, kun kuvaan tulee useita sidoksia.
Esimerkiksi ei ole intuitiivisesti järkevää, että metyyliryhmällä olisi korkeampi prioriteetti kuin alkyynillä.
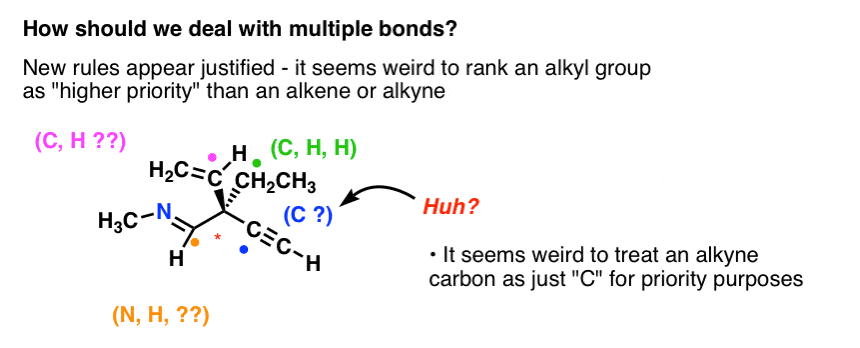
Yksiselitteisesti tarvitaan uusi sääntö useiden sidosten käsittelemiseksi.
9. JOHTOPÄÄTÖKSET. Moninkertaisten sidosten laajentaminen ”fantomiatomien” avulla
Ratkaisu on ”laajentaa” jokainen moninkertainen sidos yhdeksi sidokseksi, joka on kiinnittynyt ”fantomiatomiin” (sinisellä).
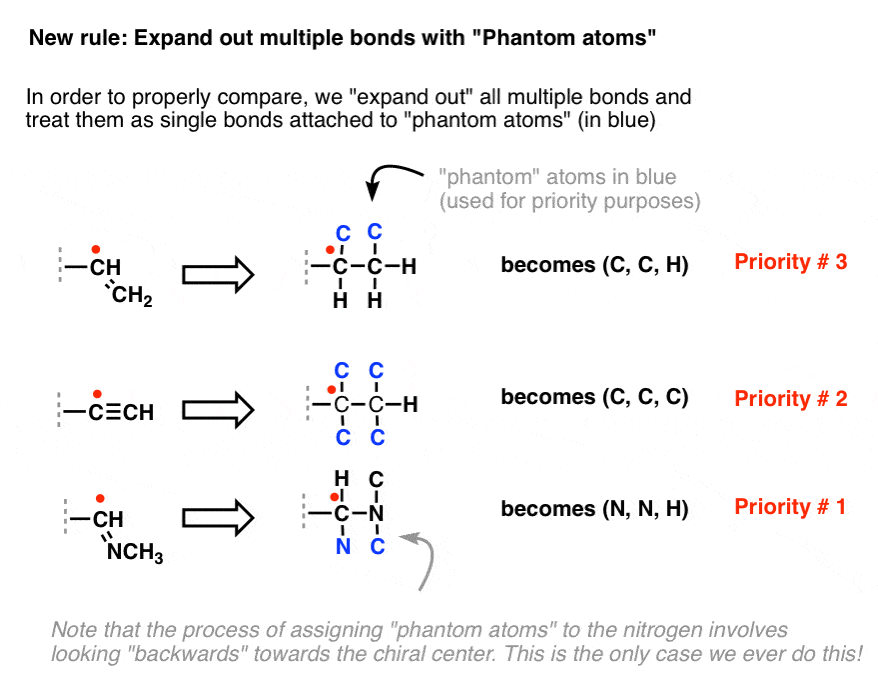
Näitä ”fantomiatomeja” käytetään ainoastaan CIP-prioriteettien määrittämiseksi – niillä ei ole mitään kemiallista merkitystä.
Huomaa, että määrittäessä phantom-atomeja molemmille monisidoksen atomeille etäisempi atomi ”katsoo taaksepäin” kohti kiraalista keskusta. Tämä on ainoa kerta, kun saamme tehdä näin!
Jos sovellamme ”fantomiatomi”-menetelmää tämän molekyylin moninkertaisiin sidoksiin, näemme, että alkyni on tosiaankin korkeammalla prioriteetilla kuin alkeeni, joka on korkeammalla prioriteetilla kuin etyyli.

Jos prioriteettien määrittämisprosessi tälle molekyylille vaikutti epäselvältä, siirrä leijailevasti tänne, niin saat ponnahdusikkunanäkymän näkyviin, tai napsauta tätä, niin saat näkyviin kuvassa, jossa käydään läpi prioriteettien määrittely.
Kokeile huviksesi käyttää uutta menetelmäämme vinyyli-, isopropyyli- ja s-butyyliryhmien prioriteettien määrittämiseen (alla).

Prosessi on kuvattu melko tiiviisti täällä.
Cahn-Ingold-Prelog Prioriteetit isotooppeja käytettäessä
Onkohan olemassa piste, jossa lakkaamme välittämästä eroista? Sanotaan esimerkiksi, että valmistamme molekyylin, jossa on vedyn sijasta deuteriumia, kuten alla olevassa molekyylissä. Lasketaanko tämä silti kiraaliseksi keskukseksi?

Kyllä, tämä lasketaan ehdottomasti kiraaliseksi keskukseksi. (Se, olisiko sillä merkittävä optinen rotaatio, on toinen juttu).
Prioriteettien määrittäminen tässä on itse asiassa melko suoraviivaista. Tapauksissa, joissa atomiluvut ovat samat, katkaisemme tasapelit antamalla korkeimman prioriteetin korkeammille atomipainoille.
Vedyn kohdalla tämä tarkoittaa, että tritium (3H) on etusijalla deuteriumiin (2H) nähden, joka on etusijalla protiumiin (1H) nähden.

Todennäköisesti tällaiseen tilanteeseen ei todennäköisesti törmää orgaanisen aineen johdantokurssilla. Mutta kyllä se tulee vastaan! Ja muuten, deuteriumia sisältävien kiraalisten molekyylien valmistaminen ei ole pelkästään teoreettinen harjoitus – siitä on ollut valtavasti hyötyä entsyymien toimintamekanismien selvittämisessä. Katso esimerkiksi täältä.
Johtopäätös: R/S-konfiguraatioiden määrittäminen ”pistemenetelmällä”
Useimmissa tapauksissa ”pistemenetelmällä” pääsee sinne, minne on mentävä määrittämään kiraalisen keskuksen prioriteetit. Yksi keskeinen asia tästä viestistä, joka on hyvä muistaa, on ”fantomiatomien” käsite prioriteettien määrittämiseksi alkeenien ja muiden moninkertaisten sidosten kohdalla.
Puuttuuko jotain, josta haluaisit puhua? Jätä kommentti!
Kiitos vielä kerran Mattille avusta tässä postauksessa. Palkkaa Matt tutoriksesi!
Huomautuksia
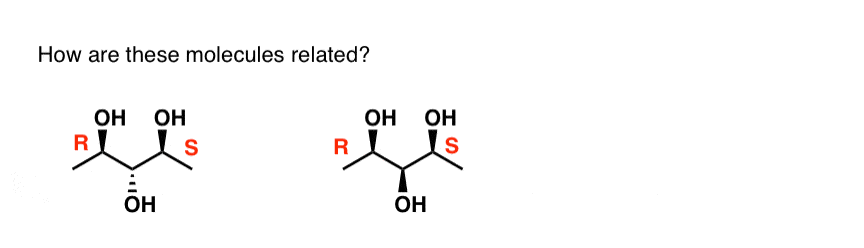
Ei aivan. Tuo keskimmäinen hiili on ns. pseudoasymmetrinen keskus. Sillä on tosin 4 eri substituenttia – (R) kiraalinen keskus on erilainen kuin (S). IUPACin sääntö on, että (R) on etusijalla (S):ään nähden. Tässä tapauksessa käytetään pieniä kirjaimia (r) ja (s). Lisää tästä aiheesta täällä.
4. Al-sedällä on (teoreettinen) esimerkki molekyylistä, jossa CIP-säännöt eivät toimi. Al-sedällä on myös melko vahvoja mielipiteitä kiraalisuudesta.