Priorità Cahn Ingold Prelog (2): Determinazione di R/S su anelli, catene e altro
Questo post è stato scritto insieme a Matt Pierce di Organic Chemistry Solutions. Chiedi a Matt di programmare una sessione di tutoraggio online qui.
In questo post ci espanderemo sulle regole di Cahn-Ingold-Prelog (CIP) e mostreremo come assegnare R/S in alcuni casi più difficili che coinvolgono anelli, centri chirali multipli, legami multipli e isotopi. Vedremo che il “metodo dei punti” è estremamente prezioso per rompere i legami nella determinazione delle priorità CIP!
Tabella dei contenuti
- Ricapitolazione: Determinazione delle priorità CIP in casi semplici
- Come assegnare le priorità CIP in casi più complicati che coinvolgono anelli, centri chirali multipli, legami multipli e isotopi?
- Ricordo: Le priorità Cahn-Ingold-Prelog sono determinate al primo punto di differenza
- Assegnare le priorità CIP: Un’applicazione del “metodo dei punti”
- Come si determina la configurazione R/S negli anelli?
- Determinare la configurazione R/S negli anelli: Una comune “domanda trabocchetto”
- Assegnare le configurazioni R/S alle molecole con più centri chirali
- Assegnare le priorità Cahn-Ingold-Prelog (CIP) con legami multipli
- Espandere i legami multipli con “atomi fantasma”
- Priorità Cahn-Ingold-Prelog con isotopi
- Conclusione: Assegnazione di configurazioni R/S con “Il metodo dei punti”
- Note
- 1. Recap: Determinazione delle priorità CIP in casi semplici
- 2. Come assegnare le priorità CIP nei casi più difficili che coinvolgono anelli, centri chirali multipli, legami multipli e isotopi?
- 3. Promemoria: Le priorità di Cahn-Ingold-Prelog sono determinate al primo punto di differenza
- 4. Assegnazione delle priorità CIP: Un’applicazione del “metodo dei punti”
- 5. Come determiniamo la configurazione R/S negli anelli?
- 6. Determinazione della configurazione R/S negli anelli: Una comune “domanda a trabocchetto”
- Assegnare le configurazioni R/S alle molecole con centri chirali multipli
- Assegnare le priorità Cahn-Ingold-Prelog (CIP) con legami multipli
- 9. Espandere i legami multipli con “atomi fantasma”
- Cahn-Ingold-Prelog Priorities With Isotopes
- Conclusione: Assegnare le configurazioni R/S con il “metodo dei punti”
- Note
1. Recap: Determinazione delle priorità CIP in casi semplici
Nel nostro primo post sulle regole Cahn-Ingold-Prelog (CIP), abbiamo dato un’ampia panoramica su come assegnare R o S ai centri chirali in una molecola. Abbiamo seguito questo con un post successivo su come utilizzare le regole CIP per determinare le priorità negli alcheni al fine di determinare se sono E o Z.
Come per la maggior parte dei post introduttivi, gli esempi scelti erano piuttosto semplici. È abbastanza semplice assegnare le priorità in una molecola come le molecole qui sotto dove il carbonio centrale è attaccato a quattro atomi con diversi pesi atomici. E come abbiamo discusso in precedenza, una volta imparata la regola dello scambio singolo, è abbastanza facile determinare R/S nei casi in cui il sostituente prioritario #4 non punta dietro il piano della pagina.
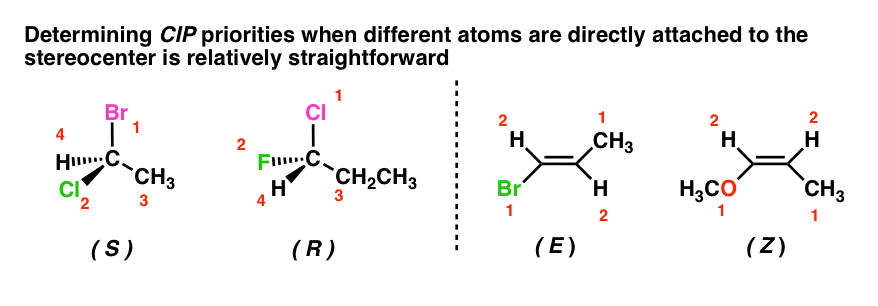
Nei casi di stereocentri che sono attaccati ad atomi identici, abbiamo visto che è anche abbastanza semplice usare il “metodo dei punti” per rompere i legami e muoversi lungo la catena. Più avanti, ecco alcuni esercizi su cui potete fare pratica, se volete.
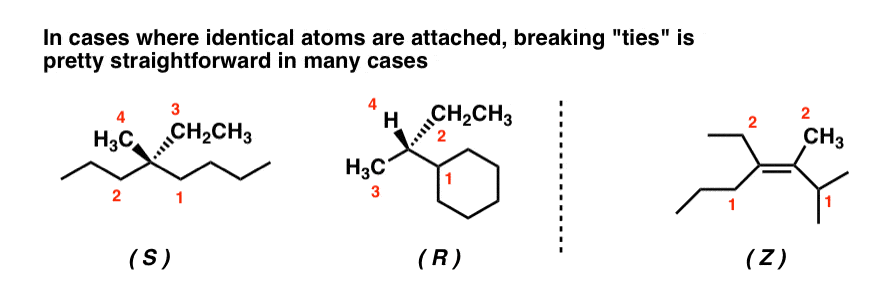
2. Come assegnare le priorità CIP nei casi più difficili che coinvolgono anelli, centri chirali multipli, legami multipli e isotopi?
Questo post riguarda alcune delle ulteriori complicazioni che vediamo nell’assegnazione delle priorità. Per esempio, come si assegnano le priorità nei seguenti casi:
- Anelli
- Centri chirali multipli
- Gestione di legami multipli
- E gli isotopi?
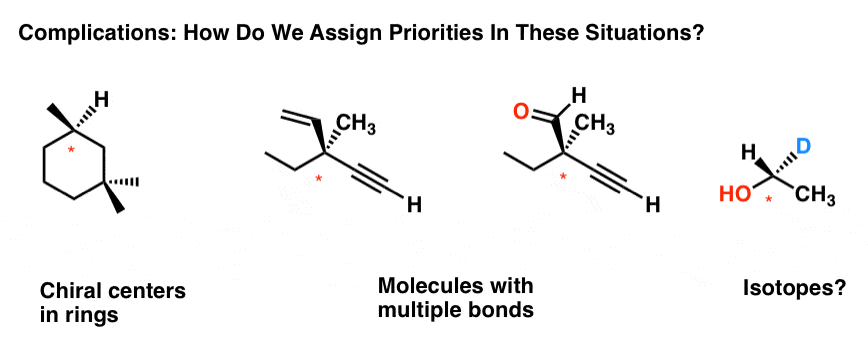
Questo post è dedicato alla risoluzione di questi casi leggermente più complicati. Ci concentreremo esclusivamente sulla determinazione di R/S, ma le stesse regole di priorità valgono anche per la determinazione di (E/Z).
3. Promemoria: Le priorità di Cahn-Ingold-Prelog sono determinate al primo punto di differenza
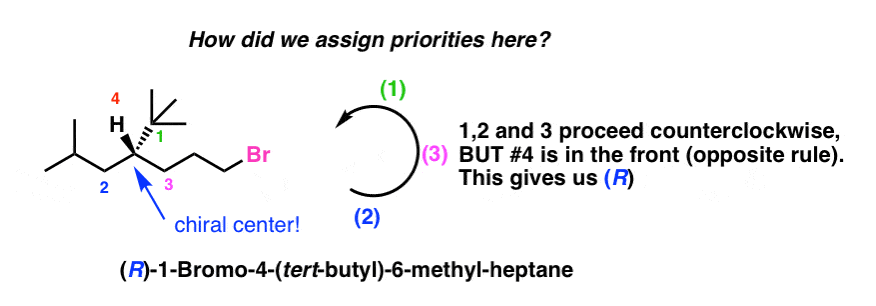
Iniziamo con una comune domanda trabocchetto. Qual è il “gruppo” a più alta priorità attaccato al centro chirale nella molecola qui sotto? Assegna R/S .
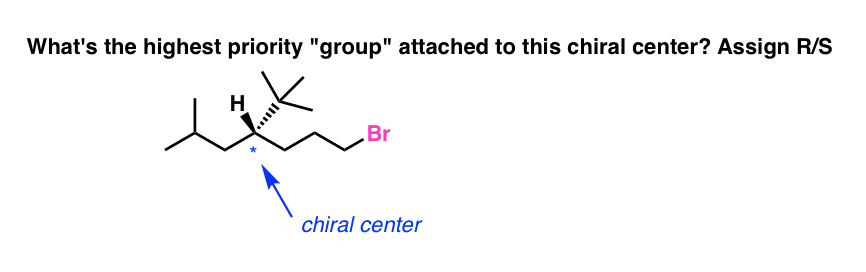
Il tuo primo istinto potrebbe essere quello di dire, “la catena di carbonio contenente il bromo”, dato che il bromo ha il numero atomico più alto di tutti gli atomi della molecola.
In realtà, la catena di carbonio contenente il bromo è il terzo gruppo prioritario (solo l’idrogeno è inferiore!), dando al centro chirale una configurazione R.
Questo è dovuto al modo in cui vengono assegnate le priorità: ci muoviamo verso l’esterno del centro chirale, un carbonio alla volta, e determiniamo le priorità al primo punto di differenza.
4. Assegnazione delle priorità CIP: Un’applicazione del “metodo dei punti”
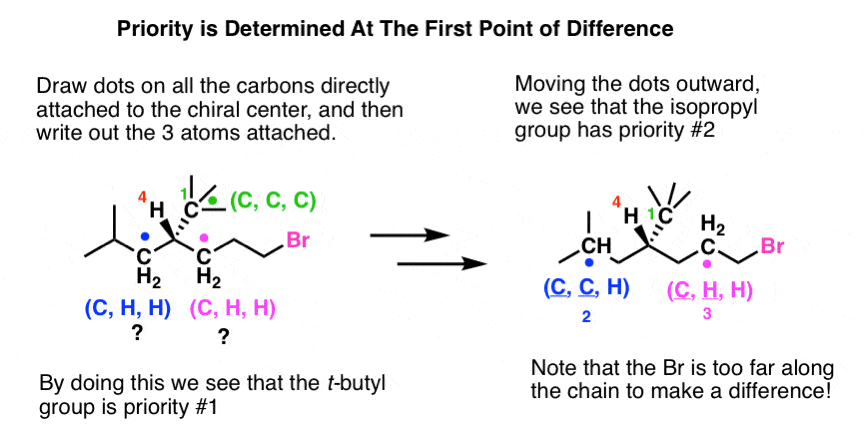
Questo processo di assegnazione delle priorità è essenzialmente identico a quello che abbiamo mostrato in precedenza:
- Primo, confrontare i quattro atomi direttamente legati al carbonio chirale e classificarli in base al numero atomico. Nel nostro esempio, H è chiaramente la priorità #4.
- Se c’è un pareggio, elencate tutti e tre gli atomi direttamente legati agli atomi legati in ordine decrescente di numero atomico. Trovo utile mettere dei puntini su ogni atomo che sto confrontando, ecco perché chiamo questo Il metodo dei puntini).
- Confrontate ogni lista, atomo per atomo. Il gruppo t-butilico (C(CH3)3) ha la priorità più alta. ma non possiamo ancora differenziare il gruppo isobutilico o il gruppo bromopropilico.
- Perché c’è ancora un pareggio, spostiamo i puntini un passo più in basso nella catena, in particolare al carbonio successivo perché quello ha il numero atomico più alto (i puntini ci aiutano a tenere traccia di dove siamo). Questo ci permette ora di assegnare le priorità #2 e #3 .
- Con tutte le priorità assegnate, siamo pronti ad assegnare R e S tracciando il percorso di 1 → 3. Dato che #4 è su un cuneo, la rotazione in senso antiorario significa una configurazione R (“regola opposta”).
Se questo non è ancora chiaro, passa il mouse qui per una visualizzazione pop-up o clicca qui per far apparire un’immagine di un trattamento completo passo-passo.
5. Come determiniamo la configurazione R/S negli anelli?
In realtà non ci sono nuove regole necessarie per determinare le priorità negli anelli, ma molti studenti mi dicono che hanno difficoltà a determinare R/S se un centro chirale è su un anello. Per questo motivo facciamo un esempio e cerchiamo di rendere questo il più chiaro possibile.
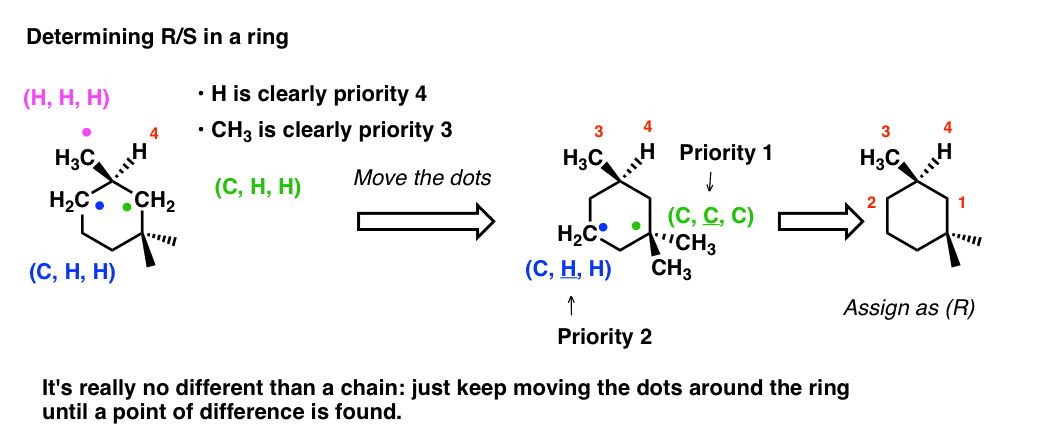
Determinare R/S su un anello è solo il metodo dei punti da capo. Ci muoviamo semplicemente lungo la catena allontanandoci dal centro chirale finché non troviamo un punto di differenza. Di seguito, dobbiamo allontanarci di due carboni dal centro chirale per dare la priorità a (C,C,C) rispetto a (C,H,H):
6. Determinazione della configurazione R/S negli anelli: Una comune “domanda a trabocchetto”
C’è in effetti un caso in cui determinare la R/S su un anello potrebbe sembrare strano ai non addetti ai lavori.
La molecola qui sotto ha cunei e trattini che indicano la stereochimica di due carboni. E se ti chiedessero di determinare l’R/S per il carbonio stellato?
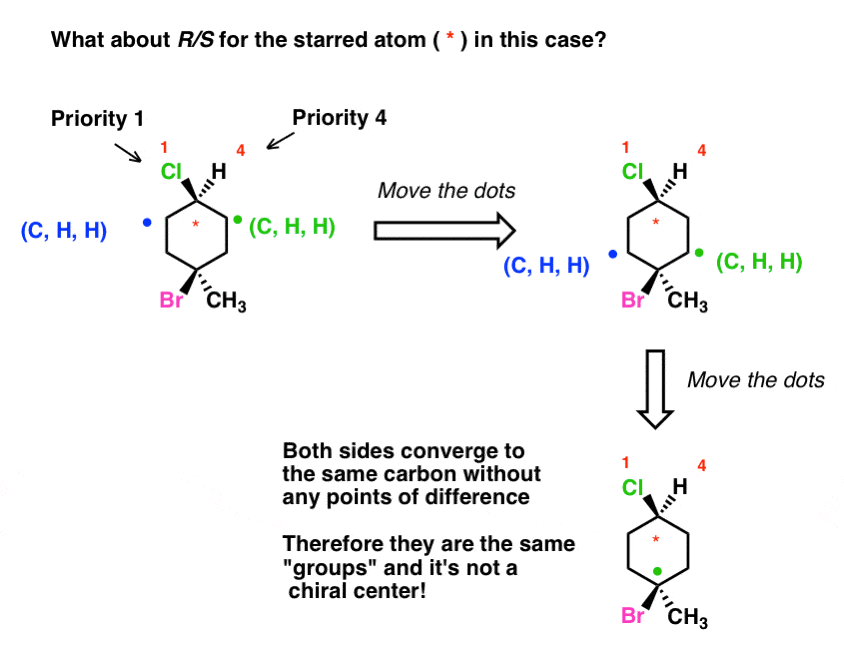
Spero che tu veda che questa è in realtà una “domanda trabocchetto”. Quando cerchiamo di determinare un punto di differenza, finiamo per convergere di nuovo verso il carbonio inferiore senza trovare alcuna differenza. Ciò significa che questi due “gruppi” sono in realtà gli stessi e che il carbonio “stellato” non è un centro chirale.
Assegnare le configurazioni R/S alle molecole con centri chirali multipli
Anche le molecole con centri chirali multipli non richiedono nuovi concetti. Dobbiamo semplicemente identificare ogni centro chirale e determinare R o S per ognuno. Quando mettiamo insieme il nome finale, dobbiamo poi specificare la configurazione di ogni carbonio all’inizio del nome.

Quindi la molecola sopra è (1R, 3R, 4S)-3-bromo-4-etil-1-metil-1-propylcyclopentane.
Se vuoi vedere esattamente come è stata fatta l’assegnazione della configurazione (S), passa il mouse qui per una visualizzazione pop-up o segui questo link per un’immagine.
Assegnare le priorità Cahn-Ingold-Prelog (CIP) con legami multipli
Gli esempi finora non hanno effettivamente richiesto nuovi concetti. Tuttavia, le regole che abbiamo visto finora iniziano a rompersi una volta che entrano in gioco i legami multipli.
Per esempio, non ha senso intuitivo che un gruppo metile debba avere una priorità più alta di un alchene.
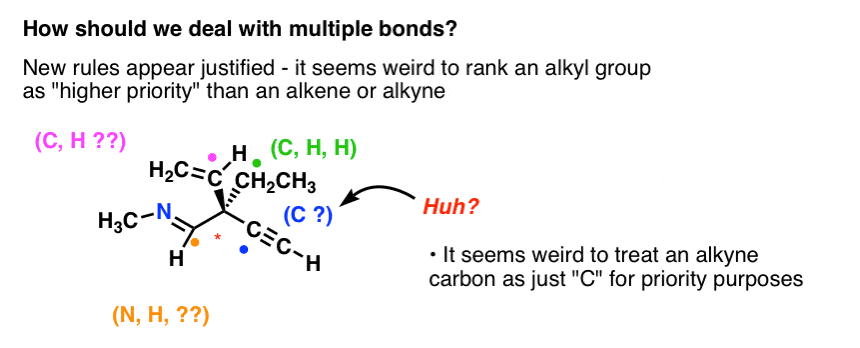
E’ chiaro che è necessaria una nuova regola per trattare i legami multipli.
9. Espandere i legami multipli con “atomi fantasma”
La soluzione è quella di “espandere” ogni legame multiplo come un singolo legame attaccato ad un “atomo fantasma” (in blu).
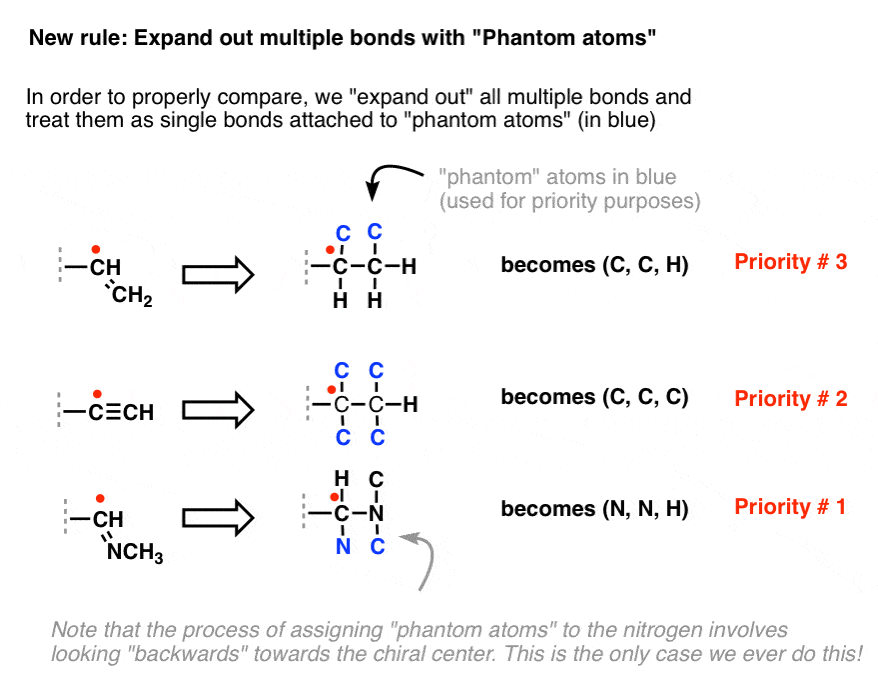
Questi “atomi fantasma” sono usati al solo scopo di determinare la priorità CIP – non hanno alcun significato chimico.
Nota che nel processo di assegnazione degli atomi fantasma ad entrambi gli atomi in un legame multiplo, l’atomo più lontano “guarda indietro” verso il centro chirale. Questa è l’unica volta che ci è permesso di farlo!
Se applichiamo il metodo dell'”atomo fantasma” ai legami multipli in questa molecola, vediamo che l’alchene è effettivamente più prioritario dell’alchene, che è più prioritario dell’etile.

Se il processo di assegnazione delle priorità a questa molecola sembra poco chiaro, passa il mouse qui per una visualizzazione pop-up o clicca qui per vedere un’immagine dell’assegnazione.
Per divertirvi, provate ad usare il nostro nuovo metodo per determinare la priorità dei gruppi vinile, isopropile e s-butile (sotto).

Il processo è descritto piuttosto densamente qui.
Cahn-Ingold-Prelog Priorities With Isotopes
C’è un punto dove smettiamo di preoccuparci delle differenze? Per esempio, diciamo che prepariamo una molecola con deuterio al posto dell’idrogeno, come nella molecola qui sotto. Questo conta ancora come centro chirale?

Sì, questo conta assolutamente come centro chirale. (Che abbia una rotazione ottica significativa è un’altra storia).
Assegnare la priorità qui è in realtà abbastanza semplice. Nei casi in cui i numeri atomici sono gli stessi, rompiamo i legami assegnando la massima priorità ai pesi atomici più alti.
Per l’idrogeno, ciò significa che il trizio (3H) ha la priorità sul deuterio (2H) che ha la priorità sul protio (1H).

Concesso, questo non è il tipo di situazione che si incontra nell’introduzione all’organico. Ma viene fuori! E comunque, preparare molecole chirali contenenti deuterio non è solo un esercizio teorico – è stato enormemente utile per determinare il meccanismo d’azione degli enzimi. Vedi qui per esempio.
Conclusione: Assegnare le configurazioni R/S con il “metodo dei punti”
Per la maggior parte dei casi, il “metodo dei punti” vi porterà dove avete bisogno di andare per determinare le priorità per un centro chirale. L’unica cosa chiave di questo post da ricordare è il concetto di “atomi fantasma” per determinare le priorità negli alcheni e altri legami multipli.
C’è qualcosa che manca e di cui vuoi parlare? Lascia un commento!
Grazie ancora a Matt per averci aiutato con questo post. Assumete Matt come vostro tutor!
Note
- Ecco un esempio davvero interessante di atomi fantasma in azione. Cambiando un gruppo sull’azoto da H a CH3 si ottiene un cambio di configurazione da (S) a (R). Big Hat Tip to r/dennisdcao
http://imgur.com/WLmmDNM - Questo post inoltre non ha affrontato la chiralità presente negli alleni e altre specie con un asse di chiralità. In questi casi non usiamo R/S, ma P/M. Le regole di priorità CIP funzionano ancora però.
- Non mi sono addentrato in questo, ma… il carbonio centrale qui è un centro chirale?
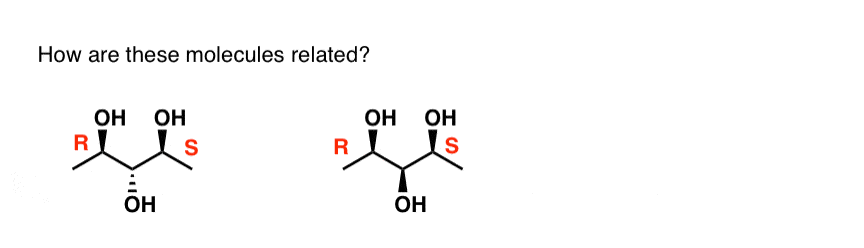
Non proprio. Quel carbonio centrale è quello che si chiama un centro pseudo asimmetrico. Ha 4 diversi sostituenti – il centro chirale (R) è diverso da quello (S). La regola IUPAC è che (R) ha la priorità su (S). Le lettere minuscole (r) e (s) sono usate in questo caso. Maggiori informazioni su questo argomento qui.
4. Lo zio Al ha un esempio (teorico) di una molecola dove le regole CIP falliscono. Lo zio Al ha anche delle opinioni piuttosto forti riguardo alla chiralità.
Sono stati fatti degli esempi.