Introducere
Papilomatoza respiratorie recurentă (RRP) este o boală cronică cauzată de papilomavirusul uman (HPV), de obicei tipurile 6 și 11. Leziunile de RRP apar cel mai frecvent în laringe (figura 1), dar pot apărea și în gură, trahee, bronhii, parenchim pulmonar și esofag. Forma de RRP cu debut juvenil, în care simptomele apar înainte de 12 ani, este mai agresivă decât forma cu debut la adult, iar simptomele sunt mai severe. Recurența papilomului este deosebit de rapidă la copiii sub 3 ani, care se confruntă cu intervale mai scurte între intervențiile chirurgicale și, prin urmare, cu mai multe intervenții chirurgicale în general. Probabilitatea ca infecția să se răspândească dincolo de laringe și incidența unei traheostomii, pentru a ajuta la menținerea traheei deschise, sunt, de asemenea, mai mari la această populație (1). Pacienții cu PRR cu debut juvenil sunt supuși în medie la 20 de intervenții chirurgicale, dintre care cele mai multe în copilărie (2).
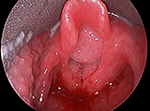
Figura 1. Imagine laringoscopică directă a papilomatozei mari și voluminoase a căilor respiratorii care obstrucționează intrarea laringiană.
Metoda chirurgicală tradițională pentru extirparea chirurgicală a implicat în mod clasic laserul KTP (potasiu titanil fosfat) sau laserul cu dioxid de carbon (3). Având în vedere efectele secundare potențial severe ale ablației cu laser, inclusiv arsuri ale tractului respirator și cicatrizare laringiană, microdebriderele au devenit un instrument chirurgical din ce în ce mai popular, în special în rândul otorinolaringologilor pediatri, pentru boala voluminoasă (3). Acest dispozitiv portabil poate îndepărta mai precis țesutul bolnav, reducând deteriorarea țesuturilor înconjurătoare (3). Cu toate acestea, având în vedere natura agresivă a PRR juvenilă, debridările sunt încă frecvente și, în timp, continuă să uzeze semnificativ țesutul subiacent, cu o incidență ridicată a formării de cicatrici. Ca atare, au fost studiate mai multe terapii medicale pentru a îmbunătăți rezultatul intervenției chirurgicale, prin creșterea duratei de timp între operații sau prin minimizarea recurenței leziunilor RRP.
Interferon α
Interferonul α, o proteină produsă de leucocite ca reacție la diverși stimuli, inclusiv la infecții virale, a fost unul dintre primele tratamente medicale potențiale studiate (4). Valoarea sa ca tratament adjuvant este controversată. Într-un studiu amplu efectuat pe 85 de copii și 84 de adulți, 58% dintre copii au încheiat perioada de tratament de un an cu injecții intramusculare de interferon α de trei ori pe săptămână fără a prezenta semne de PRR (5). Frecvența recurenței papilomului a scăzut la 74% din toți copiii tratați (5). Cu toate acestea, într-un studiu randomizat de control efectuat pe 123 de pacienți sub 21 de ani, rata de creștere încetinită a papiloamelor în grupul experimental care a primit injecții intramusculare cu interferon α nu s-a menținut pe parcursul tratamentului de un an (6). În mod similar, un alt studiu a constatat că, la 20 de ani de la încheierea tratamentului cu interferon α, doar 42% dintre pacienți au indicat un răspuns pe termen lung, iar toți cei care au recidivat au avut forma juvenilă de apariție a RRP (7). Majoritatea studiilor care au investigat interferonul α au raportat, de asemenea, efecte secundare grave, precum tulburări neurologice, leucopenie și trombocitopenie (5). Din aceste motive, utilizarea sa de către otolaringologii pediatri a scăzut și, în general, nu este recomandată (1). În 2014, doar 4% dintre copiii cu RRP au primit interferon α ca terapie adjuvantă (1).
Cidofovir
Acest medicament antiviral cu spectru larg, care inhibă polimerazele ADN virale, s-a dovedit a fi promițător ca terapie intralesională adjuvantă la intervenția chirurgicală pentru RRP. Injecțiile intralesionale de cidofovir sunt cel mai frecvent administrat tratament medical pentru RRP în rândul otolaringologilor pediatri (1). Toate lucrările publicate între 1998 și 2011 care au investigat eficacitatea cidofovirului intralesional au raportat cel puțin un caz de remisiune a bolii (8). Cu toate acestea, deoarece majoritatea acestor studii sunt studii de caz necontrolate, nu este clar dacă beneficiile sunt cauzate de cidofovir sau fac parte din evoluția naturală a bolii. Un studiu randomizat de control a constatat că nu au existat diferențe semnificative din punct de vedere statistic în ceea ce privește severitatea papilomului sau calitatea vieții legată de sănătate între un grup de control, tratat cu intervenții chirurgicale la nevoie și injecții intralesionale de soluție salină, și grupul experimental, tratat cu chirurgie și Cidofovir intralesional, după 12 luni de tratament (9). Ambele grupuri au înregistrat o scădere semnificativă a severității bolii pe parcursul anului, ceea ce indică faptul că boala poate regresa de la sine în timp (9). O altă analiză care a analizat 27 de studii privind administrarea de Cidofovir, toate publicate înainte de 2011, a constatat că rata medie de remisiune completă cu Cidofovir a fost de 37% în studiile pediatrice (10). Au existat, de asemenea, unele efecte secundare severe asociate cu cidofovirul, deoarece o analiză a constatat că 1,7 și 1% din 447 de pacienți cu RRP au prezentat transformare malignă și, respectiv, nefrotoxicitate (8). Alte efecte secundare includ erupții cutanate, cefalee și cicatrizarea corzilor vocale (11). Având în vedere aceste complicații potențiale și lipsa unui protocol acceptat pentru dozaj sau frecvența administrării, acest medicament nu este un adjuvant de încredere (4).
Cidofovirul a fost, de asemenea, administrat ca tratament sistemic mai degrabă decât local pentru cazurile de PRR care sunt complicate de afecțiuni pulmonare. Patru studii pe un singur caz au arătat că cidofovirul intravenos a dus la remisiunea bolii, ceea ce nu reprezintă evoluția normală a bolii cu implicare pulmonară (11). Toate aceste studii au utilizat hiperhidratarea și probenecidul, un reductor de acid uric, pentru a reduce șansele de nefrotoxicitate (11). Un singur pacient a prezentat efecte secundare, alopecie parțială și leucopenie, în urma unei terapii combinate de cidofovir și interferon (12). Dozele ambelor medicamente au fost reduse ca răspuns. La optsprezece luni de la încheierea tratamentului, pacienta a necesitat o singură dată o intervenție chirurgicală pentru PRR, iar boala sa pulmonară s-a stabilizat (12).
O nouă metodă de administrare a cidofovirului este inhalarea. Puține studii au investigat eficacitatea acestei metode, dar ea poate fi promițătoare pentru pacienții care nu au răspuns la alte forme de tratament, cum ar fi un băiețel de 4 luni care, în ciuda microdefrișărilor bisăptămânale și a injecțiilor intralesionale de Cidofovir și interferon α intravenos, a prezentat o agravare a simptomelor (13). În termen de 6 săptămâni de 40 mg de Cidofovir nebulizat zilnic, 12 zile da și 2 zile nu, timpul dintre debridări a crescut (13). Șase luni mai târziu, pacientul nu a prezentat niciun simptom (13). În concluzie, deși Cidofovirul sub diferite forme de administrare rămâne utilizat pe scară largă, rezultatele tratamentului său sunt, în cel mai bun caz, mixte, iar potențialul său de efecte secundare este oarecum limitativ.
Terapie fotodinamică
Terapia fotodinamică (PDT) presupune introducerea unei substanțe sensibile la lumină, numită fotosensibilizator, pe cale orală sau prin injectare, în țesutul bolnav și activarea substanței cu lumină laser pentru a induce necroza. Unul dintre beneficiile majore ale PDT este capacitatea de a distruge tumorile fără a afecta țesuturile înconjurătoare (4). Studiile de caz au arătat rate semnificativ mai lente de reapariție a papilomului la scurt timp după PDT, administrată ca terapie adjuvantă sau de sine stătătoare și, în unele cazuri, absența bolii după câteva săptămâni (14, 15). Au existat doar câteva studii randomizate de control pentru a investiga impactul PDT, dar cel mai recent a constatat că boala a recidivat după 3-5 ani, probabil pentru că își generează impactul printr-un răspuns imunitar pe termen scurt (16). Ar trebui efectuate cercetări suplimentare pentru a se stabili eficacitatea și siguranța acesteia.
Indole-3-Carbinol
Găsit în concentrații ridicate în legumele crucifere, cum ar fi broccoli și varza, indolul-3-carbinolul modifică metabolismul estrogenilor pentru a modifica proliferarea celulară și sinteza ADN. Cel mai recent studiu clinic a constatat că, după administrarea de indol-3-carbinol de două ori pe zi, cu o doză de 200 mg pentru adulți și doze determinate în funcție de greutate pentru copii, timp de 50,2 luni în medie, 70% dintre subiecți au prezentat un răspuns complet sau parțial (17). Dintre pacienții pediatrici, unul a prezentat un răspuns complet, trei un răspuns parțial, iar cinci nu au prezentat niciun răspuns (17). Nu este clar de ce pacienții adulți au răspuns mai bine la indol-3-carbinol decât pacienții pediatrici. Natura mai puțin agresivă a RRP cu debut la adulți poate fi un factor. Având în vedere rezultatele nepromițătoare la populația pediatrică, nu au existat mai multe cercetări privind tratarea PRR cu debut juvenil cu de indol-3-carbinol.
Celecoxib
Celecoxib este un medicament antiinflamator care inhibă ciclooxigenază-2 (COX-2), o enzimă care duce la inflamație și durere, și este utilizat în mod obișnuit pentru tratarea artritei. Studiile in vitro au arătat că celulele de papilom supraexprimă COX-2 ca urmare a intensificării semnalizării receptorului factorului de creștere epidermică (EGFR) și că această activitate este importantă pentru creșterea lor (18). O terapie combinată de celecoxib și erlotinib, un inhibitor al kinazei EGFR, a ajutat la controlul RRP progresiv la un bărbat de 58 de ani a prin încetinirea creșterii papilomului, făcând inutilă o intervenție chirurgicală suplimentară (19). Un studiu de control randomizat în curs de desfășurare, sponsorizat de Northwell Health, urmărește să determine dacă celecoxibul poate scădea rata de recurență a papiloamelor atât la pacienții adulți, cât și la cei pediatrici (4).
Medicamente antireflux
Studii de caz au arătat că tratarea bolii de reflux gastroesofagian (GERD) cu medicamente antireflux la pacienții cu RRP cu debut juvenil poate ajuta la încetinirea ratei de recreștere a papilomului (20, 21). Într-un studiu, pacienții care nu au respectat tratamentul GERD au prezentat recidivă (20). O analiză retrospectivă a fișelor a arătat, de asemenea, că pacienții pediatrici tratați pentru PRR care nu au fost tratați pentru reflux au avut o probabilitate semnificativ mai mare de a dezvolta pânze laringiene după îndepărtarea chirurgicală a papiloamelor (22). Deși există dovezi neconcludente că BRGE agravează RRP, gestionarea acestuia are sens pentru pacienții care au o prezentare clinică de BRGE și cazuri complicate, progresive de RRP (23).
Heat Shock Protein
Printre cei 700 de copii cu RRP gestionați de 74 de otorinolaringologi pediatri, care au fost chestionați cu privire la utilizarea tratamentului adjuvant, 11 pacienți au primit HSP-E7, o proteină de fuziune recombinantă compusă din proteina 65 a șocului termic (Hsp65) și proteina E7 a HPV tip 16 (1). HSP-E7 a fost investigată ca tratament în mai multe boli care derivă din HPV, inclusiv verucile genitale și neoplazia intraepitelială (24). Dovezile sugerează că ar putea fi reactivă împotriva mai multor tulpini HPV decât doar împotriva HPV 16 (24). Într-un studiu deschis efectuat pe 27 de pacienți pediatrici cu RRP, intervalul median dintre intervenții chirurgicale în urma tratamentului cu HSP-E7 a fost semnificativ prelungit în comparație cu mediana de dinaintea tratamentului (24). Au existat puține complicații, doar reacții ușoare spre moderate la locul injecției. Deși nu există studii clinice în curs de desfășurare pentru a investiga eficacitatea Hsp-E7, acesta este un tratament promițător.
Vaccinul HPV
Câteva rapoarte de caz și studii au documentat utilizarea vaccinului HPV ca terapie adjuvantă. În prezent, există trei vaccinuri HPV aprobate: Cervarix bivalent, Gardasil tetravalent și Gardasil 9 nonavalent. Vaccinul tetravalent acționează vizează HPV-6, HPV-11, HPV-16, HPV-18. O recenzie sistematică și o meta-analiză recentă a constatat că durata medie între intervenții chirurgicale la 63 de pacienți RRP juvenili și adulți a crescut semnificativ după vaccinarea HPV, de la 7 la 34 de luni în medie (25). Studiul nu a constatat diferențe semnificative în funcție de vârsta de debut a RRP (25). Alte studii de caz care nu au fost incluse în metaanaliză au arătat, de asemenea, eficacitatea Gardasil la pacienții pediatrici, deoarece crește semnificativ timpul dintre intervenții chirurgicale sau, în unele cazuri, determină o remisiune completă (26, 27).
Vaccinarea HPV intramusculară ar putea fi mai eficientă decât tratamentele identificate anterior, mai comune, cum ar fi cidofovirul intralesional. Un studiu de caz retrospectiv care a urmărit timp de 22 de ani pacienți RRP juvenili și adulți cu debut la vârsta adultă a constatat că doar doi dintre cei 13 pacienți tratați cu intervenție chirurgicală și Gardasil au recidivat, în timp ce toți pacienții de control, tratați cu intervenție chirurgicală și Cidofovir, au prezentat o recreștere a papilomului (28). Durata medie de timp până la recidiva bolii a fost, de asemenea, semnificativ mai mare la pacienții tratați decât la cei de control (28).
Unul dintre cele mai promițătoare aspecte ale HPV ca terapie adjuvantă este faptul că nu are efecte secundare severe. În plus, odată cu creșterea ratelor de vaccinare, incidența PRR juvenilă ar putea scădea în general, deoarece această formă a bolii este dobândită în mod obișnuit atunci când un copil este expus la verucile genitale cauzate de virusul HPV 6 sau 11 în timpul nașterii (4).
Vaccinul împotriva oreionului
Au existat foarte puține studii privind eficacitatea vaccinului împotriva oreionului ca terapie adjuvantă, deși cercetările actuale sunt promițătoare. Un studiu de caz a constatat că remisiunea a fost indusă la nouă din 11 pacienți pediatrici tratați cu injecții intralesionale ale vaccinului la intervale de 3 până la 12 săptămâni, împreună cu o intervenție chirurgicală cu laser (29). Un studiu retrospectiv care a comparat Cidofovirul și vaccinul împotriva rujeolei, oreionului și rubeolei (ROR) ca terapii adjuvante la o populație pediatrică a constatat că nu au existat diferențe semnificative între acei copii tratați cu injecții intralesionale de cidofovir și ROR după debridări (30).
Bevacizumab
Bevacizumab este un anticorp monoclonal uman care se leagă și previne interacțiunea factorului de creștere a endoteliului vascular (VEGF) cu receptorii. Activitatea VEGF are un rol în dezvoltarea RRP, deoarece studiile in vitro au arătat o expresie puternică a VEGF-A în epiteliul papilomatic și expresia ARN mesager al VEGFR-1 și VEGFR-2 în celulele endoteliale vasculare subiacente (31).
Primile studii care au analizat bevacizumab ca tratament pentru RRP au investigat beneficiul injecțiilor intralesionale ca terapie adjuvantă la intervenția chirurgicală. Un studiu efectuat pe trei pacienți cu vârste cuprinse între 3 și 6 ani cu RRP severă (adică cu cel puțin patru intervenții pe an) a constatat că toți pacienții au prezentat un timp mai mare între debridarea chirurgicală și tratamentele cu laser KTP pulsat și RRP mai puțin severă la câteva săptămâni după terminarea tratamentului cu bevacizumab, comparativ cu perioada anterioară (32). Aceștia au prezentat, de asemenea, o îmbunătățire a calității vieții legate de voce (32).
În afară de rapoartele de caz, au fost efectuate și studii de control de caz pentru a investiga eficacitatea bevacizumabului ca terapie adjuvantă. După un tratament cu laser KTP de 532 nm urmat de injecții sublesionale cu bevacizumab în pliul vocal mai bolnav și de injecții saline în celălalt pliu, 16 din cei 20 de pacienți adulți cu RRP bilateral al pliului vocal au avut mai puține papilomuri în pliul tratat, așa cum s-a determinat prin imagistică endoscopică (33). Trei dintre cei 20 de pacienți nu au avut nicio boală în niciunul dintre cele două pliuri și niciunul dintre pacienți nu a prezentat complicații în urma tratamentului (33).
Pe baza acestor rezultate promițătoare, a fost efectuat un studiu mai amplu care a analizat eficacitatea bevacizumabului la o populație pediatrică. La 10 copii cu vârste cuprinse între 18 luni și 18 ani cu RRP progresivă, fără răspuns, trei injecții intralesionale de bevacizumab de 2,5 mg/ml la 2-3 săptămâni distanță, împreună cu terapia cu laser, au crescut durata mediană de timp între intervențiile chirurgicale, au scăzut numărul median de intervenții pe an și au îmbunătățit calitatea vieții legate de voce (3). Una dintre limitările studiului este că dozajul este o estimare bazată pe dozele din oftalmologia pediatrică. De asemenea, cantitatea injectată în pailoame nu a fost aceeași pentru fiecare pacient, deoarece a variat în funcție de severitatea bolii.
Câteva studii au încercat să determine dozele optime. Un alt studiu care a analizat nouă pacienți pediatrici cu RRP cu debut juvenil a constatat, de asemenea, că, după o serie de cinci injecții subepiteliale administrate la intervale de 4-6 săptămâni, cu o doză medie de 14,25 mg, împreună cu ablația cu laser KTP, toți cei nouă pacienți (cu o vârstă medie de 8 ani) au prezentat o creștere a intervalului de timp între injecții (34). Aceste rezultate indică faptul că au arătat că tratamentul cu doze mari de bevacizumab nu prezintă complicații și poate fi foarte eficient.
După dovezile care au arătat eficacitatea bevacizumabului intralesional, cercetarea s-a îndreptat spre abordarea bevacizumabului sistemic, care este un tratament deosebit de promițător pentru pacienții cu diagnostice complexe. Primul raport privind administrarea intravenoasă a arătat că, cu o medie de 6 cure în doze de 5, 10, 15 mg/kg, toți pacienții tratați cu RRP progresivă au prezentat regresie a papilomului (35). Pacienții au inclus patru cazuri de RRP cu debut la adulți și unul cu debut juvenil. Cei cinci pacienți au fost supuși colectiv la 18 intervenții chirurgicale în anul anterior tratamentului cu bevacizumab, dar numai cazul adultului a necesitat intervenție chirurgicală după tratament din cauza unei transformări maligne în anul următor (35).
Alte rapoarte de cazuri unice au coroborat eficacitatea bevacizumabului sistemic fără a găsi complicații, deși majoritatea dintre acestea sunt la pacienți adulți. La un bărbat în vârstă de 42 de ani cu RRP traheală severă, o doză mică de 5 mg/kg, crescută în timp la 10 mg/kg de bevacizumab, a ajutat la obținerea regresiei bolii la 3 luni după încetarea tratamentului (36). O urmărire la 12 luni a arătat că pacientul a rămas liber de boală. Șase cure de tratament sistemic cu bevacizumab de 5 mg/kg la fiecare 2 săptămâni pentru un pacient în vârstă de 87 de ani care nu a răspuns la cidofovir intralesional, la un stent endobronșic sau la vaccinarea împotriva HPV, a ajutat, de asemenea, la obținerea unei scăderi semnificative a masei lobului și a unei bronhii permeabile (37). După două serii de injecții intravenoase de 10 mg/kg la fiecare 2 săptămâni, o persoană în vârstă de 63 de ani cu RRP severă a prezentat mai puțină afectare pulmonară și nicio dovadă de obstrucție traheală (37).
Singurul raport de caz publicat la copii este cel al unei fetițe de 12 ani cu papilomatoză laringotraheală progresivă și afectare pulmonară care, după 3 luni de la inițierea tratamentului sistemic cu bevacizumab, a prezentat un răspuns parțial la nivelul laringelui și un răspuns aproape complet la nivelul traheei (38). După 5 luni, pacientul nu mai prezenta afectare pulmonară. Aceste rezultate sunt cu atât mai impresionante cu cât, pe o perioadă de 10 ani, pacientul fusese inițiat cu Gardasil, interferon, celecoxib, medicație antireflux, zitromicină și propranolol și nu a răspuns la niciunul (38).
Potențialul bevacizumabului sistemic ca tratament pentru cele mai agresive forme de RRP este cel mai bine sintetizat de rezultatele unui sondaj electronic al RRP Task Force al Societății Americane de Otorinolaringologie Pediatrică, al Asociației Americane de Bronho-Esofagologie și al medicilor care au tratat RRP cu bevacizumab sistemic (39). Cele 11 sondaje completate, obținute de la nouă centre medicale, au arătat că majoritatea pacienților tratați cu bevacizumab aveau un istoric îndelungat de RRP cu debut juvenil și nu au reușit să prezinte răspunsuri susținute la cidofovir, interferon și celecoxib. Medicii au administrat tratamentul în intervalul de 5-10 mg/kg pe doză. Șapte dintre cei opt pacienți tratați au avut un răspuns parțial și unul a prezentat un răspuns complet la tratament (39). Toți pacienții au prezentat o creștere a timpului dintre operații, acum de ordinul lunilor. La trei dintre cei patru pacienți cu afectare pulmonară, trei au prezentat ameliorarea sau rezolvarea papilomului pulmonar și unul a prezentat stabilizarea bolii. Doar doi pacienți au prezentat complicații minore, hemoptizie și proteinurie.
Pentru a stabili efectul cauzal al bevacizumabului, pentru a determina dozele adecvate și pentru a identifica orice complicații potențiale, trebuie efectuate studii randomizate de control și studii de control de caz mai mari. Mai mult, trebuie elaborate protocoale pentru a defini durata tratamentului, controlând în același timp orice efecte potențiale de ricoșeu.
Concluzii
Deși nu s-a găsit încă o terapie medicală adjuvantă optimă, universal eficientă pentru RRP, rezultatele promițătoare ale vaccinării împotriva RRP ca abordare terapeutică, împreună cu utilizarea bevacizumabului sistemic, oferă speranța unor rezultate îmbunătățite pentru acești copii în următorii ani. Protocoale optime de tratament ar trebui să fie dezvoltate în viitorul apropiat.
Contribuții ale autorilor
Toți autorii enumerați au avut o contribuție substanțială, directă și intelectuală la această lucrare și au aprobat-o pentru publicare.
Declarație privind conflictul de interese
Autorii declară că cercetarea a fost efectuată în absența oricăror relații comerciale sau financiare care ar putea fi interpretate ca un potențial conflict de interese.
Editorul care se ocupă de manipulare a declarat o coautorat în trecut cu unul dintre autorii DP.
1. Schraff S, Derkay CS, Burke B, Lawson L. Experiența membrilor Societății Americane de Otorinolaringologie Pediatrică în ceea ce privește papilomatoza respiratorie recurentă și utilizarea terapiei adjuvante. Arch Otolaryngol Head Neck Surg. (2004) 130:1039-42. doi: 10.1001/archotol.130.9.1039
PubMed Abstract | Refef Full Text | Google Scholar
2. Krstic M, Pavlović JM, Stanković P, Milenković MT. Etiopatogenia papilomatozei laringiene recurente și strategiile de tratament contemporane. Acta Med Medianae. (2014) 53:64-74. doi: 10.5633/amm.2014.0411
CrossRef Full Text | Google Scholar
3. Rogers DJ, Ojha S, Maurer R, Hartnick CJ. Utilizarea bevacizumabului intralesional adjuvant pentru papilomatoza respiratorie agresivă la copii. JAMA Otolaryngol Head Neck Surg. (2013) 139:496-501. doi: 10.1001/jamaoto.2013.1810
PubMed Abstract | Full CrossRef Text | Google Scholar
4. Carifi M, Napolitano D, Morandi M, Dall’Olio D. Papilomatoza respiratorie recurentă: perspective actuale și viitoare. Ther Clin Risk Manag. (2015) 11:731-8. doi: 10.2147/TCRM.S81825
PubMed Abstract | Refef Full Text | Google Scholar
5. Nodarse-Cuní H, Iznaga-Marín N, Viera-Alvarez D, Rodríguez-Gómez H, Fernández-Fernández H, Blanco-López Y, et al. Interferon alfa-2b ca tratament adjuvant al papilomatozei respiratorii recurente în Cuba: program național (Raport 1994-1999). J Laryngol Otol. (2004) 118:681-7. doi: 10.1258/0022215042244741
PubMed Abstract | Reflect Full Text | Google Scholar
6. Healy GB, Gelber RD, Trowbridge AL, Grundfast KM, Ruben RJ, Price KN. Tratamentul papilomatozei respiratorii recurente cu interferon leucocitar uman. New Engl J Med. (1988) 319:401-7. doi: 10.1056/NEJM198808183190704
PubMed Abstract | CrossRef Full Text | Google Scholar
7. Gerein V, Rastorguev E, Gerein J, Jecker P, Pfister H. Utilizarea interferonului-alfa în papilomatoza respiratorie recurentă: urmărire pe 20 de ani. Ann Otol Rhinol Laryngol. (2005) 114:463-71. doi: 10.1177/000348940511400608
PubMed Abstract |Ref Full Text | Google Scholar
8. Jackowska J, Piersiala K, Klimza H, Wierzbicka M. Rezultatele tratamentului cu bevacizumab și cidofovir în papilomatoza respiratorie recurentă asociată cu HPV-revizuirea literaturii. Otolaryngol Pol. (2018) 72:1-8. doi: 10.5604/01.3001.0012.0484
PubMed Abstract | Full CrossRef Text | Google Scholar
9. McMurray JS, Connor N, Ford CN. Eficacitatea cidofovirului în papilomatoza respiratorie recurentă: un studiu randomizat, dublu-orb, controlat cu placebo. Ann Otol Rhinol Laryngol. (2008) 117:477-83. doi: 10.1177/000348940811700702
PubMed Abstract |Ref Full Text | Google Scholar
10. Chadha NK. Cidofovir intralesional pentru papilomatoza respiratorie recurentă: revizuire sistematică a eficacității și siguranței. J Laryngol Voice. (2011) 1:22-6. doi: 10.4103/2230-9748.76133
CrossRef Full Text | Google Scholar
11. Broekema FI, Dikkers FG. Efecte secundare ale cidofovirului în tratamentul papilomatozei respiratorii recurente. Eur Arch Otorhinolaryngol. (2008) 265:871-9. doi: 10.1007/s00405-008-0658-0
PubMed Abstract | Refef Full Text | Google Scholar
12. Dancey DR, Chamberlain DW, Krajden M, Palefsky J, Alberti PW, Downey GP. Tratamentul cu succes al bolii pulmonare multichistice legate de papilomatoza laringiană juvenilă cu cidofovir: raport de caz și revizuire a literaturii. Chest. (2000) 118:1210-4. doi: 10.1378/chest.118.4.1210
PubMed Abstract | Textul integral | Google Scholar
13. Ksiazek J, Prager JD, Sun GH, Wood RE, Arjmand EM. Cidofovir inhalat ca terapie adjuvantă pentru papilomatoza respiratorie recurentă. Otolaryngol Head Neck Surg. (2011) 144:639-41. doi: 10.1177/0194599810395353
PubMed Abstract | Refef Full Text | Google Scholar
14. Abramson AL, Shikowitz MJ, Mullooly VM, Steinberg BM, Amella CA, Rothstein HR. Efectele clinice ale terapiei fotodinamice asupra papiloamelor laringiene recurente. Arch Otolaryngol Head Neck Surg. (1992) 118:25-9. doi: 10.1001/archotol.1992.01880010029011
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Feyh J, Kastenbauer E. Tratamentul papilomatozei laringiene cu terapie laser fotodinamică. Laryngorhinootologie. (1992) 71:190-2.
PubMed Abstract | Google Scholar
16. Lieder A, Khan MK, Khan MK, Lippert BM. Terapia fotodinamică pentru papilomatoza respiratorie recurentă. Cochrane Database Syst Rev. (2014) 5:CD009810. doi: 10.1002/14651858.CD009810.pub2
CrossRef Full Text | Google Scholar
17. Rosen CA, Bryson PC. Indole-3-carbinol pentru papilomatoza respiratorie recurentă: rezultate pe termen lung. J Voice. (2004) 18:248-53. doi: 10.1016/j.jvoice.2003.05.005
PubMed Abstract | Refef Full Text | Google Scholar
18. Wu R, Abramson AL, Shikowitz MJ, Dannenberg AJ, Steinberg BM. Expresia ciclooxigenazei-2 indusă de factorul de creștere epidermică este mediată prin fosfatidilinositol-3 kinaza, nu prin proteina kinaza proteinelor activate de mitogen / kinaza kinazei reglate de semnalul extracelular, în papiloamele respiratorii recurente. Clin. Cancer Res. (2005) 11:6155-61. doi: 10.1158/1078-0432.CCR-04-2664
CrossRef Full Text | Google Scholar
19. Limsukon A, Susanto I, Soo Hoo GW, Dubinett SM, Batra RK. Regresia papilomatozei respiratorii recurente cu terapia combinată cu celecoxib și erlotinib. Chest. (2009) 136:924-6. doi: 10.1378/chest.08-2639
PubMed Abstract | Refef Full Text | Google Scholar
20. McKenna M, Brodsky L. Refluxul acid extraesofagian și papilomul respirator recurent la copii. Int. J. Pediatr. Otorhinolaryngol. (2005) 69:597-605. doi: 10.1016/j.ijporl.2004.11.021
PubMed Abstract | CrossRef Full Text | Google Scholar
21.
21.
. Borkowski G, Sommer P, Stark T, Sudhoff H, Luckhaupt H. Papilomatoza respiratorie recurentă asociată cu boala de reflux gastroesofagian la copii. Eur Arch Otorhinolaryngol. (1999) 256:370-2. doi: 10.1007/s004050050166
PubMed Abstract | Text integral | Google Scholar
22. Holland BW, Koufman JA, Postma GN, McGuirt WF Jr. Refluxul laringofaringian și formarea pânzei laringiene la pacienții cu papiloame respiratorii recurente pediatrice. Laryngoscop. (2002) 112:1926-9. doi: 10.1097/00005537-200211000-00003
PubMed Abstract | CrossRef Full Text | Google Scholar
23. San Giorgi MRM, Helder HM, Lindeman RJS, de Bock GH, Dikkers FG. Asocierea dintre boala de reflux gastroesofagian și papilomatoza respiratorie recurentă: o revizuire sistematică. Laryngoscop. (2016) 126:2330-9. doi: 10.1002/lary.25898
PubMed Abstract | Textul integral | Google Scholar
24. Derkay CS, Smith RJH, McClay J, van Burik JAH, Wiatrak BJ, Arnold J, et al. Tratamentul HspE7 al papilomatozei respiratorii recurente pediatrice: rezultatele finale ale unui studiu deschis. Ann Otol Rhinol Laryngol. (2005) 114:730-7. doi: 10.1177/000348940511400913
PubMed Abstract | Refef Full Text | Google Scholar
25. Rosenberg T, Philipsen BB, Mehlum CS, Dyrvig AK, Wehberg S, Chirilǎ M, et al. Therapeutic use of the human papillomavirus vaccine on recurrent respiratory papillomatosis: a systematic review and meta-analysis. J Infect Dis. (2019) 219:1016-25. doi: 10.1093/infdis/jiy616
PubMed Abstract | Refef Cross Full Text | Google Scholar
26. Mudry P, Vavrina M, Mazanek P, Machalova M, Litzman J, Sterba J. Papilomatoza laringiană recurentă: tratament de succes cu vaccinarea împotriva papilomavirusului uman. Arch Dis Child. (2011) 96:476-7. doi: 10.1136/adc.2010.198184
PubMed Abstract | Refef Cross Full Text | Google Scholar
27. Förster G, Boltze C, Seidel J, Pawlita M, Müller A. Juvenile laryngeal papillomatosis-imunizarea cu vaccinul polivalent gardasil. Laryngorhinootologie. (2008) 87:796-9. doi: 10.1055/s-2008-1077527
PubMed Abstract | Full Text | Google Scholar
28. Mauz PS, Schäfer FA, Iftner T, Gonser P. Vaccinarea HPV ca abordare preventivă pentru papilomatoza respiratorie recurentă – o analiză clinică retrospectivă de 22 de ani. BMC Infect Dis. (2018) 18:343. doi: 10.1186/s12879-018-3260-0
PubMed Abstract | Full Text | Google Scholar
29. Pashley NRT. Poate vaccinul împotriva oreionului să inducă remisiune în papilomul respirator recurent? Arch Otolaryngol Head Neck Surg. (2002) 128:783-6. doi: 10.1001/archotol.128.7.783
PubMed Abstract | Textul integral | Google Scholar
30. Meacham RK, Thompson JW. Compararea cidofovirului și a vaccinului împotriva rujeolei, oreionului și rubeolei în tratamentul papilomatozei respiratorii recurente. Ear Nose Throat J. (2017) 96:69-74. doi: 10.1177/014556131709600209
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Rahbar R, Vargas SO, Folkman J, McGill TJ, Healy GB, Tan X, et al. Rolul factorului de creștere endotelială vasculară-a în papilomatoza respiratorie recurentă. Ann Otol Rhinol Laryngol. (2005) 114:289-95. doi: 10.1177/000348940511400407
PubMed Abstract | Refef Full Text | Google Scholar
32. Maturo S, Hartnick CJ. Utilizarea laserului cu titanil fosfat de potasiu pulsat de 532-Nm și a bevacizumabului intralesional adjuvant pentru papilomatoza respiratorie agresivă la copii: experiență inițială. Arch Otolaryngol Head Neck Surg. (2010) 136:561-5. doi: 10.1001/archoto.2010.81
PubMed Abstract | Text integral | Google Scholar
33. Zeitels SM, Barbu AM, Landau-Zemer T, Lopez-Guerra G, Burns JA, Friedman AD, et al. Injectarea locală de bevacizumab (Avastin) și tratamentul angiolitic cu laser KTP al papilomatozei respiratorii recurente a pliurilor vocale: un studiu prospectiv. Ann Otol Rhinol Laryngol. (2011) 120:627-34. doi: 10.1177/000348941112001001
PubMed Abstract | Refef Full Text | Google Scholar
34. Sidell DR, Nassar M, Cotton RT, Zeitels SM, de Alarcon A. High-dose sublesional bevacizumab (Avastin) pentru papilomatoza respiratorie pediatrică recurentă. Ann Otol Rhinol Laryngol. (2014) 123:214-21. doi: 10.1177/0003489414522977
PubMed Abstract | Refef Full Text | Google Scholar
35. Mohr M, Schliemann C, Biermann C, Schmidt LH, Kessler T, Schmidt J, et al. Răspuns rapid la terapia sistemică cu bevacizumab în papilomatoza respiratorie recurentă. Oncol Lett. (2014) 8:1912-8. doi: 10.3892/ol.2014.2486
PubMed Abstract | Full Text | Google Scholar
36. Fernandez-Bussy S, Labarca G, Vial MR, Soto R, Mehta HJ, Jantz M, et al. Papilomatoza respiratorie recurentă și tratamentul cu bevacizumab. Am J Respir Crit Care Med. (2017) 197:539-41. doi: 10.1164/rccm.201702-0279LE
PubMed Abstract | Refef Full Text | Google Scholar
37. Bedoya A, Glisinski K, Clarke J, Lind RN, Buckley CE, Shofer S. Bevacizumab sistemic pentru papilomatoza respiratorie recurentă: experiența unui singur centru cu două cazuri. Am J Case Rep. (2017) 18:842-6. doi: 10.12659/AJCR.904416
PubMed Abstract | CrossRef Full Text | Google Scholar
38. Zur KB, Fox E. Chimioterapia cu bevacizumab pentru gestionarea papilomatozei pulmonare și laringotraheale la un copil. Laryngoscop. (2017) 127:1538-42. doi: 10.1002/lary.26450
PubMed Abstract | Refef Full Text | Google Scholar
39. Best SR, Mohr M, Zur KB. Bevacizumab sistemic pentru papilomatoza respiratorie recurentă: un studiu național. Laryngoscop. (2017) 127:2225-9. doi: 10.1002/lary.26662
PubMed Abstract | Full Text | Google Scholar
.