Case
Um homem de 63 anos com hipertensão, diabetes e cancro do pulmão de células escamosas recentemente diagnosticado apresenta dor abdominal difusa e confusão de dois dias de duração. Ele pesa 105 Kg, sua pressão arterial é 105/65 mm/Hg, freqüência cardíaca 105 batimentos por minuto e temperatura de 99,0 graus Fahrenheit. Sua respiração é de 18 respirações por minuto, a saturação de oxigênio é de 95% no ar ambiente, e sua ortostática é positiva. As membranas mucosas secas com diminuição do turgor da pele são notadas no exame físico. A avaliação laboratorial revela um nível de cálcio de 15,5 mg/dL, nível de creatinina de 1,2 mg/dL, nível de albumina de 4,3 g/dL, e um nível de fósforo de 2,9 mg/dL.
Qual o melhor tratamento para esta condição?
Over visão
A homeostase do cálcio envolve interacções complexas entre o rim, o tracto gastrointestinal (GI), e o sistema esquelético através de influências hormonais. Embora 99% do cálcio do organismo esteja armazenado nos ossos, 50% do cálcio sérico está na forma ionizada ativa, 40% está ligado à albumina e 10% é complexado com ânions.1 É importante lembrar estas porcentagens ao avaliar o cálcio sérico de um paciente; o cálcio sérico elevado pode ser validado através de uma fórmula de correção (cálcio corrigido=cálcio total medido + ) ou através da medição direta do cálcio ionizado, que é a forma fisiologicamente ativa.
Hipercalcemia de malignidade é a causa mais comum de hipercalcemia no paciente hospitalizado. Vinte a 30% dos pacientes com câncer desenvolverão hipercalcemia em algum momento do curso da doença.2 Em geral, isso retrata um prognóstico ruim com uma sobrevida mediana de três a quatro meses.3
Quatro mecanismos gerais estão envolvidos na patogênese da hipercalcemia maligna; estes mecanismos formam a base para as estratégias de tratamento disponíveis:
- Tumores osteolíticos, como o mieloma múltiplo, podem atuar diretamente sobre o osso, levando à ativação osteoclasta e liberação de cálcio;
- Medicadores tumorais elaborados por células malignas, como o peptídeo relacionado ao hormônio paratireo (PTH-RP), podem efetuar ativação dos osteoclastos e diminuir a eliminação renal do cálcio, causando hipercalcemia humoral da malignidade;
- algumas neoplasias malignas (mais comumente linfomas) podem sintetizar diretamente 1,25 (OH)2 vitamina D, levando ao aumento da absorção luminal tanto de cálcio quanto de fósforo do trato gastrointestinal; e
- Produção direta de hormônio paratireoidiano (PTH) pelas células malignas é rara, mas tem sido relatada.2
Outros fatores, incluindo mobilidade reduzida, podem levar a uma maior reabsorção óssea e ao agravamento do estado hipercalcêmico.
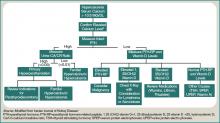
Um paciente com hipercalcemia deve ter um trabalho sistemático, com conhecimento de outras causas de hipercalcemia que possam estar presentes, independentemente da malignidade. Exemplos incluem hiperparatireoidismo primário, efeito medicamentário e etiologias genéticas. Embora uma discussão mais aprofundada esteja além do escopo deste artigo, uma abordagem diagnóstica ampla está representada na Figura 1 (à direita).
O tratamento eficaz da hipercalcemia exige a consideração tanto da situação clínica imediata do paciente, quanto da situação clínica a longo prazo, à luz do prognóstico do paciente. O objetivo primário no manejo agudo da hipercalcemia é normalizar os valores séricos e diminuir os sintomas. No entanto, isto deve ser feito com a apreciação de que o desarranjo metabólico foi gerado por uma malignidade subjacente. O foco principal da terapêutica clínica deve ser direcionado para isso.
 clique para versão grande
clique para versão grande
Uma imagem gerada por computador de osteoclastos multinucleados gravando o osso trabecular em um processo chamado reabsorção óssea. Os bisfosfonatos inibem este processo em hipercalcemia induzida por malignidade.
Revisão dos dados
Fluidos intravenosos (IV). A hidratação intravenosa com soro isotônico representa a intervenção mais imediata e crítica no manejo agudo da hipercalcemia maligna. Esta condição tem múltiplos efeitos potencialmente deletérios no rim, incluindo vasoconstrição, inibição da absorção distal do sal e antagonismo do hormônio anti-diurético (ADH), levando à perda tanto de sal como de água. A diminuição do volume intravascular então potencia o aumento da reabsorção de sódio proximalmente no rim.
Soro isotônico restaura o esgotamento do volume que invariavelmente ocorre no ajuste do desgaste do sal urinário provocado pela hipercalcemia. A restauração do volume intravascular resulta em um aumento na taxa de filtração glomerular e, portanto, um aumento da filtração de cálcio. Além disso, a reabsorção tubular proximal de sódio e cálcio diminui à medida que a taxa de filtração glomerular aumenta. Além disso, um aumento na apresentação de sódio e água nos sítios tubulares renais distais provoca uma calcificação adicional.
Estima-se que com a hidratação salina, a concentração de cálcio deve diminuir, pelo menos pelo grau em que a desidratação a elevou, tipicamente na faixa de 1,6 mg a 2,4 mg por decilitro.4 A hidratação por si só, no entanto, raramente leva à normalização da concentração sérica de cálcio em pacientes com hipercalcemia grave.
A taxa de infusão é baseada na gravidade da hipercalcemia, e na idade e comorbidades do paciente, com especial atenção às doenças cardíacas ou renais. Uma abordagem padrão para a maioria dos pacientes sem edema e sem insuficiência cardíaca ou renal é iniciar uma infusão salina a uma taxa inicial entre 200 mL/h a 300 mL/h. O objetivo é manter o débito urinário em 100 mL/h a 150 mL/h.
Furosemida. Após a administração de líquidos intravenosos para restabelecer o estado eurovolêmico, a furosemida tem sido usada historicamente porque tem um efeito calcinúrico com diurese forçada. Também é útil para gerir e prevenir a sobrecarga de fluidos que ocorre com a hidratação salina. Entretanto, os dados não suportam seu uso rotineiro para baixar os níveis de cálcio em pacientes hipercalcemicos.
A maioria dos artigos estudando o uso da furosemida foram publicados nos anos 70 e 80, e envolvem uma variedade de doses e horários de administração que variam de 40 mg por via oral diariamente a 100 mg IV por hora com melhora variável nos níveis séricos de cálcio e efeitos de curta duração. Embora alguns estudos tenham mostrado que essas altas doses (2.400 mg/24 horas) de furosemida podem diminuir os níveis de cálcio, foram encontrados desarranjos metabólicos graves em outros eletrólitos. Esta abordagem exigiu uma monitorização frequente e invasiva para prevenir tais desarranjos.5 A aplicação clínica destes estudos levou a recomendações publicadas que são tão variáveis quanto as doses utilizadas nos estudos iniciais há mais de 30 anos.
Isto inclui a consideração de que, à luz da disponibilidade e eficácia dos bifosfonatos, a furosemida pode não ser mais clinicamente útil neste esforço.6 O papel atual da furosemida no manejo de pacientes hipercalcemicos permanece na base do necessário para o manejo dos estados de sobrecarga de fluidos provocados após a reanimação agressiva do fluido intravenoso.
 clique para versão grande
clique para versão grande
Figura 1: Abordagem diagnóstica da hipercalcemia.
Bisfosfonatos. Os bisfosfonatos tornaram-se disponíveis pela primeira vez para o tratamento da hipercalcemia no início dos anos 90 e mudaram drasticamente a intervenção aguda e melhoraram o curso clínico a longo prazo dos pacientes com hipercalcemia maligna. Embora desenvolvidos pela primeira vez no século XIX com aplicações industriais, só nos anos 60 é que o seu papel no metabolismo ósseo foi apreciado.
Embora o seu complexo mecanismo de acção continue a ser uma questão de investigações em curso, sabe-se que os bisfosfonatos são dirigidos para os ossos, onde inibem uma enzima na via redutase HMG-CoA e promovem a morte das células apoptóticas dos osteoclastos.7 Ao bloquear a reabsorção óssea mediada por osteoclastos, os bisfosfonatos são eficazes no tratamento da hipercalcemia que ocorre com uma variedade de processos de doença reabsorvente óssea, incluindo a hipercalcemia maligna. Como compostos relativamente atóxicos capazes de conferir uma diminuição profunda e sustentada no cálcio sérico, estes agentes tornaram-se preferidos no tratamento da hipercalcemia maligna aguda e crônica.
Existem cinco bisfosfonatos parenterais disponíveis para o tratamento da hipercalcemia maligna: pamidronato, ácido zoledrônico, ibandronato, etidronato e clodronato. O etidronato e o clodronato são agentes de primeira geração, que são menos potentes e têm mais efeitos colaterais que outros agentes e não são tão comumente usados. O candronato é um agente útil com uma longa meia-vida mostrada ser tão eficaz quanto o pamidronato, embora não tenha sido tão amplamente estudado quanto os outros agentes.
Pamidronato tem sido estudado exaustivamente em múltiplos ensaios observacionais e randomizados, e tem se mostrado altamente eficaz e minimamente tóxico no tratamento da hipercalcemia devido a múltiplas causas, incluindo a hipercalcemia maligna.8,9 Um efeito máximo de diminuição do cálcio ocorre com uma dose de 90 mg, e a dose é frequentemente titulada com base no soro de cálcio medido. Ele é infundido durante duas a quatro horas, produz uma redução do cálcio sérico dentro de um a dois dias, e tem um efeito sustentado que dura até duas semanas ou mais.
Como o bisfosfonato mais potente e de mais fácil administração, o ácido zoledrônico é considerado por muitos o agente de escolha no tratamento da hipercalcemia maligna. Pode ser administrado como uma dose de 4 mg-8 mg por via intravenosa durante 15 minutos (em comparação com duas horas para o pamidronato). Dois ensaios Fase III, compreendendo 275 pacientes, demonstraram a eficácia superior do ácido zoledrônico em comparação com o pamidronato, com 88% dos pacientes realizando um soro de cálcio normalizado (comparado com 70% dos pacientes recebendo uma dose de 90 mg de pamidronato).10
Even, embora estes agentes sejam relativamente atóxicos, cada um pode provocar uma doença flulike leve e transitória nos receptores. A disfunção renal tem sido notada raramente. Estes agentes devem ser renalmente dosados e utilizados com cautela em pacientes com insuficiência renal avançada (creatinina sérica >2,5). Osteonecrose da mandíbula tem sido observada em menos de 2% dos pacientes que recebem bifosfonatos intravenosos. Assim, recomenda-se que os pacientes sejam submetidos a avaliação dentária antes de receberem o agente (se possível) e evitar procedimentos dentários invasivos em torno do momento em que recebem o agente.11
 clique para versão grande
clique para versão grande
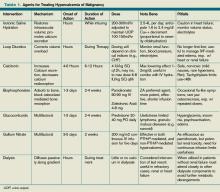
Tabela 1. Agentes de Tratamento da Hipercalcemia da Malignidade
Outras intervenções terapêuticas. Os bisfosfonatos representam os agentes farmacêuticos mais estudados e eficazes disponíveis para tratar a hipercalcemia. O afastamento destes agentes deve ser considerado apenas quando estão contra-indicados, em circunstâncias graves, ou após o paciente não responder.
Calcitonina há muito tempo tem a aprovação do FDA para o tratamento da hipercalcemia em adultos. Tem sido demonstrado em pequenos estudos não randomizados dos anos 70 e 80, que diminui rapidamente (em duas horas) os níveis de cálcio em pacientes hipercalcemicos.12,13,14 No entanto, essas reduções são pequenas (<10%) e transitórias (geralmente persistindo até 72 a 96 horas) devido à taquifilaxia observada com essa medicação. No entanto, a calcitonina pode ser usada como ponte adjuvante para baixar os níveis de cálcio em pacientes com hipercalcemia grave durante os primeiros dias antes que outros agentes comecem a fazer efeito.
Glucocorticoides têm sido usados para tratar a hipercalcemia desde a década de 1950. A prednisona, dexametasona e metilprednisolona têm todas indicações da FDA para hipercalcemia, mas faltam dados e são contraditórios. Um pequeno (n=28) ensaio randomizado controlado (TCR) realizado em 1984 não mostrou eficácia adicional de glicocorticóides com fluidos intravenosos quando comparado apenas com fluidos intravenosos.15 Outro pequeno (n=30) TCR realizado em 1992 em mulheres com câncer de mama metastático mostrou uma melhora significativa em pacientes tratadas com prednisolona, fluidos intravenosos e furosemida quando comparado com fluidos intravenosos e furosemida.16 Outros ensaios não randomizados mostraram uma resposta imprevisível na melhor das hipóteses.17 Apesar disso, os glicocorticoides provavelmente retêm um papel limitado para tratamento em casos específicos, incluindo hipercalcemia induzida por linfomas que elevam os níveis de vitamina D 1,25(OH)2 (uma vez que interage com um receptor regulado por esteróides), ou mielomas múltiplos onde eles potencialmente impactam a progressão da doença.
Nitrato de gálio, um sal anidro de um metal pesado, demonstrou em vários ensaios aleatórios ser um agente terapêutico eficaz na redução dos níveis de cálcio em pacientes hipercalcemicos.18,19 Além disso, um estudo duplo-cego de 64 pacientes com hipercalcemia de malignidade mostrou que o nitrato de gálio é pelo menos tão eficaz quanto o pamidronato no controle agudo da hipercalcemia relacionada ao câncer.20 No entanto, a necessidade de infusão contínua durante um período de cinco dias limitou a aplicação deste agente.
Hemodialysis with a calcium-lacking dialysate has been shown in small, nonrandomized studies to be a temporarily effective method of reducing sérico calcium levels.21,22 No entanto, esta modalidade de tratamento seria melhor reservada para pacientes com hipercalcemia grave, nos quais a repleção agressiva do volume intravascular e os bisfosfonatos não são aconselháveis (por exemplo, aqueles com insuficiência cardíaca ou renal significativa) e têm uma etiologia subjacente que provavelmente será responsiva a outros tratamentos. Além disso, deve-se levar em consideração a adequação de tais procedimentos invasivos temporizadores em pacientes com câncer metastático.
Voltar ao caso
Este paciente tinha um nível de cálcio ionizado de 1,9 mmol/L (normal 1,1-1,4 mmol/L). Ele foi iniciado com hidratação IV agressiva com soro fisiológico normal e ácido zoledrônico. Seus medicamentos caseiros foram revistos, e foi confirmado que ele não estava tomando medicamentos contra-indicados como tiazidas ou suplementação com cálcio/vitamina D.
Outros trabalhos para a etiologia de sua hipercalcemia revelaram um PTH adequadamente suprimido, intacto e normal 25 (OH) níveis de vitamina D e 1,25 (OH)2 vitamina D. Seu PTH-RP intacto foi elevado às 10pmol/L, e consistente com hipercalcemia de malignidade.
Oncologia e consultas de cuidados paliativos foram solicitadas para auxiliar na coordenação do tratamento do câncer de pulmão subjacente do paciente; planos foram feitos para quimioterapia sistêmica. Seus sintomas melhoraram lentamente, e 72 horas após a admissão, seu soro de cálcio normalizou. Recebeu alta com um plano para iniciar quimioterapia e acompanhamento continuado com oncologia.
Bottom Line
A gestão aguda da hipercalcemia da malignidade centra-se na redução do cálcio sérico através de uma variedade de agentes farmacológicos. Entretanto, questões de longo prazo como o tratamento da malignidade subjacente e discussões sobre os objetivos dos cuidados nesta população de pacientes de alta mortalidade são primordiais. TH
Dr. Hartley e Dr. Repaskey são instrutores clínicos em medicina interna no Sistema de Saúde da Universidade de Michigan. O Dr. Rohde é professor assistente clínico de medicina interna na UMHS.
- Assadi F. Hypercalcemia: uma abordagem baseada em evidências para casos clínicos. Iran J Kidney Dis. 2009;3:(2):71-79.
- Stewart A. Hipercalcemia associada ao câncer. N Engl J Med. 2005;542(4):373-379.
- Seccareccia D. Hipercalcemia associada ao câncer. Can Fam Physician. 2010;56:(3):244-246.
- Bilezikian JP. Manejo de hipercalcemia aguda. N Engl J Med. 1992; 326(18):1196-1203.
- Suki WN, Yium JJ, VonMinden M, et al. Tratamento agudo da hipercalcemia com furosemida. N Engl J Med. 1970;283:836-840.
- LeGrand SB, Leskuski D, Zama I. Revisão narrativa: furosemida para hipercalcemia: uma prática ainda não comprovada e comum. Ann Intern Med. 2008;149:259-263.
- Drake MT, Bart LC, Khosla S. Bisphosphonates: mecanismo de ação e papel na prática clínica. Mayo Clinic Proc. 2008;83(9):1032-1045.
- Nussbaum SR, Younger J, Vandepol CJ, et al. Terapia intravenosa de dose única com pamidronato para o tratamento da hipercalcemia de malignidade: comparação das dosagens de 30-, 60- e 90-mg. Am J Med. 1993; 95(3):297-304.
- Gucalp R, Ritch P, Riernik PH, et al. Estudo comparativo de pamidronato dissódico e etidronato dissódico no tratamento da hipercalcemia relacionada ao câncer. J Clin Oncol. 1992;10(1):134-142.
- Major P, Lortholary A, Hon J, et al. Zoledronic acid is superior to pamidronate in the treatment of hypercalcemia of malignancy: a pooled analysis of two randomized, controlled clinical trials. J Clin Oncol. 2001;19(2): 558-567.
- Tanvetyanon T. Manejo dos efeitos adversos associados aos bifosfonatos intravenosos. Ann Oncol. 2006;17(6):897-907.
- Wisneski LA, Croom WP, Silva OL, et al. Salmon calcitonin em hipercalcemia. Clin Pharmacol Ther. 1978; 24:219-222.
- Binstock ML, Mundy GR. Effect of calcitonin and glucocorticoids in combination on the hypercalcemia of malignancy. Ann Intern Med. 1980;93(2):269-272.
- Nilsson O, Almqvist S, Karlberg BE. Salmon calcitonina no tratamento agudo da hipercalcemia moderada e grave no homem. Acta Med Scand. 1978;204(4): 249-252.
- Percival RC, Yates AJ, Gray RE, et al. Role of glucocorticoids in management of malignant hypercalcemia. Br Med J. 1984;289(6440):287.
- Kristensen B, Ejlertsen B, Holmegaard SN, et al. Prednisolone no tratamento da hipercalcemia maligna grave no câncer de mama metastático: um estudo randomizado. J Intern Med. 1992;232(3):237-245.
- Thalassinos NC, Joplin GF. Failure of corticosteroid therapy to correct the hypercalcemia of malignant disease. Lanceta. 1970;2(7672):537-538.
- Warrell RP Jr, Murphy WK, Schulman P, et al. Um estudo randomizado duplo-cego de nitrato de gálio comparado com etidronato para controle agudo da hipercalcemia relacionada ao câncer. J Clin Oncol. 1991;9(8):1467-1475.
- Warrell RP Jr, Israel R, Frisone M, et al. Gallium nitrate for acute treatment of cancer-related hypercalcemia: a randomized, double-blinded comparison to calcitonin. Ann Intern Med. 1988;108:669-674.
- Cvitkovic F, Armand JP, Tubiana-Hulin M, et al. Estudo randomizado, duplo-cego, fase II de nitrato de gálio comparado com pamidronato para o controle agudo da hipercalcemia relacionada ao câncer. Cancer J. 2006;12 (1):47-53.
- Cardella CJ, Birkin BL, Rapoport A. Role of dialysis in the treatment of severe hypercalcemia: relato de dois casos tratados com sucesso com hemodiálise e revisão da literatura. Clin Nephrol. 1979; 12(6):285-290.
- Koo WS, Jeon DS, Ahn SJ, et al. Hemodiálise sem cálcio para o tratamento da hipercalcemia. Nephron. 1996;72(3):424-428.