Le tableau périodique est le tableau qui range les éléments chimiques sous une forme systématique qui est une forme tabulaire. Les éléments sont classés de gauche à droite dans l’ordre croissant de leur numéro atomique. Le numéro atomique est le nombre de protons et de neutrons présents dans les noyaux d’un élément.
Vérifiez ici aussi les électrons de valence :-
- Electrons de valence de l’hydrogène
- Electrons de valence de l’hélium
- Electrons de valence du lithium
- Electrons de valence du béryllium
- Electrons de valence du bore
- Electrons de valence du carbone.
- Electrons de valence d’azote
- Electrons de valence d’oxygène
- Electrons de valence de fluor
- Electrons de valence de néon
- Electrons de valence de sodium
- Electrons de valence de magnésium
- Aluminium Electrons de valence
- Silicium Electrons de valence
- Phosphore Electrons de valence
- Soufre Electrons de valence
- Chlore Electrons de valence
- Argon Electrons de valence
- Potassium Electrons de valence Électrons de valence du potassium
- Électrons de valence du calcium
- Électrons de valence du scandium
- Électrons de valence du titane
- Électrons de valence du vanadium
- Électrons de valence du chrome
- Électrons de valence du manganèse
- .
- Électrons de valence de fer
- Électrons de valence de cobalt
- Électrons de valence de nickel
- Électrons de valence de cuivre
- Électrons de valence de zinc
- Électrons de valence de gallium
- Électrons de valence de germanium Electrons de valence
- Arsenic électrons de valence
- Sélénium électrons de valence
- Brome électrons de valence
- Krypton électrons de valence
- Rubidium électrons de valence
- Strontium électrons de valence
- YttriumÉlectrons de valence
- Zirconium Électrons de valence
- Niobium Électrons de valence
- Molybdène Électrons de valence
- Technetium Électrons de valence
- Ruthénium Électrons de valence
- Rhodium Electrons de valence
- Palladium Electrons de valence
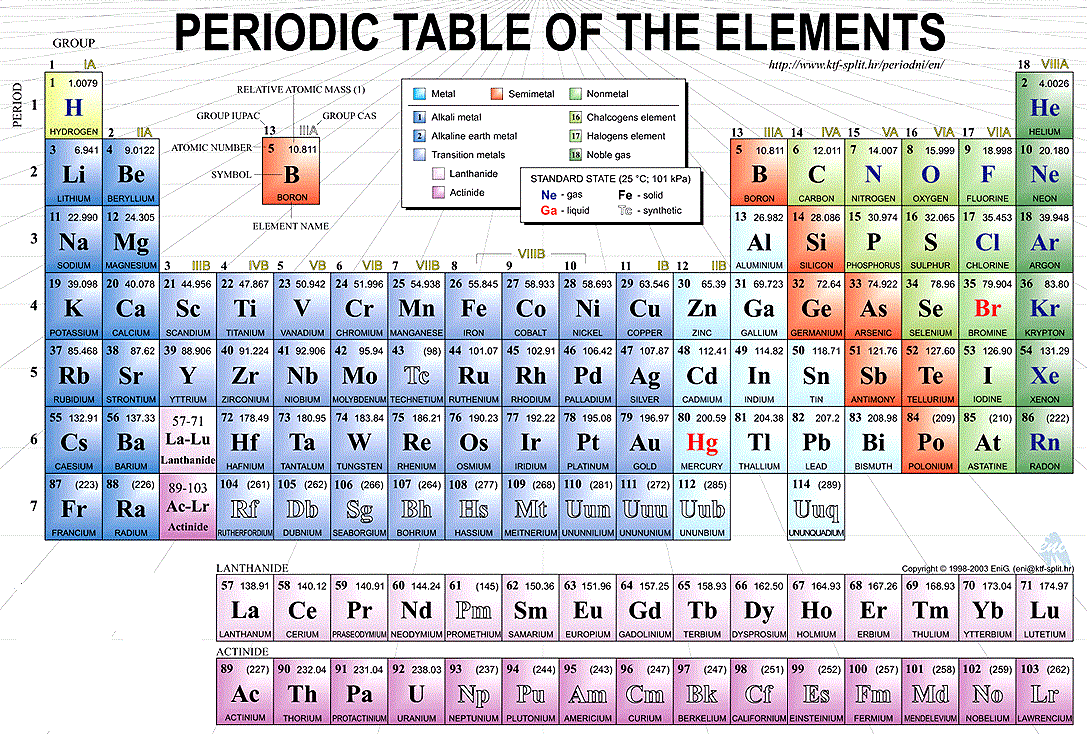

Les rangées horizontales du tableau périodique sont appelées périodes tandis que les colonnes verticales sont appelées groupes. Les éléments sont classés dans différents groupes en fonction de leurs propres caractéristiques de propriétés physiques et chimiques
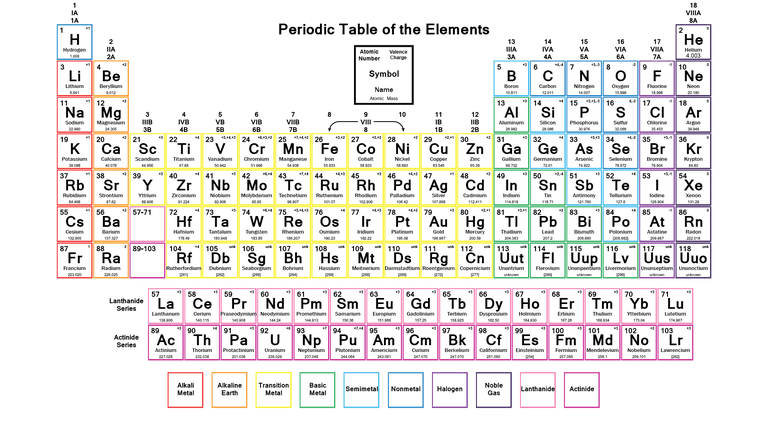
Tableau périodique des éléments étiquetés
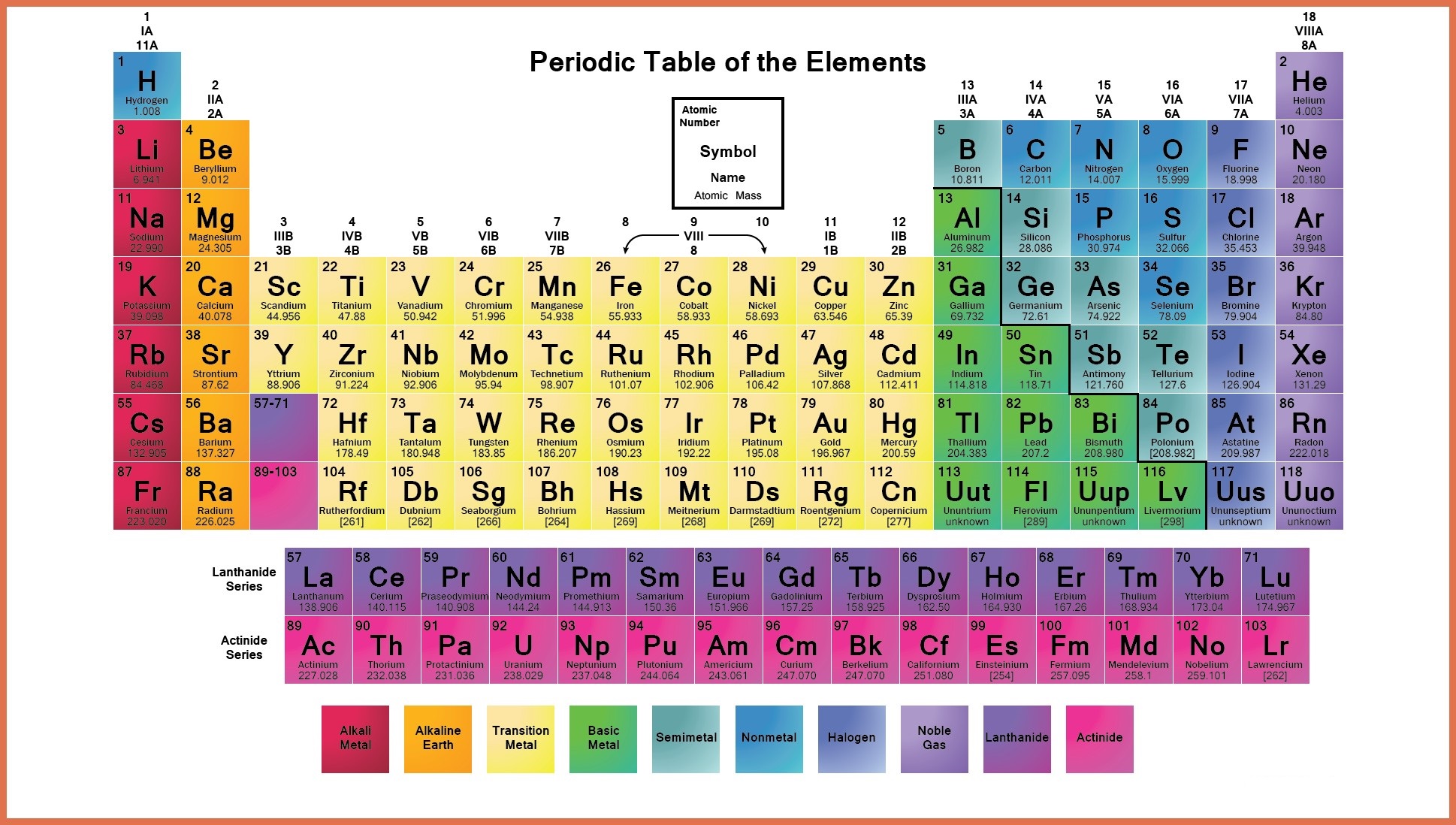
Il existe différents types d’éléments dans un tableau périodique;
- Métalloïdes : Les éléments qui relèvent de ce groupe ont la caractéristique d’être à la fois des métaux et des non-métaux. Par exemple l’Antimoine, le Bore, le Germanium, le Silicium, l’Arsenic, le Tellure et le Polonium
- Métaux alcalins : Ils sont placés dans le premier groupe du tableau et comprennent les éléments Lithium, Sodium, Potassium, Rubidium, Césium, Francium.
- Métaux alcalino-terreux : Ce type de métaux est placé dans le deuxième groupe du tableau périodique, par exemple, le Magnésium, le Béryllium, le Strontium, le Calcium, le Baryum et le Radium
- Métaux de transition : Ce sont les métaux de transition. La malléabilité, la ductilité et la conductivité de l’électricité sont quelques-unes des caractéristiques de base de ces éléments, par exemple, le cuivre, le nickel, le chrome, le mercure, l’or et l’argent
- Éléments des terres rares : De tels éléments sont situés dans les 3e, 6e et 7e périodes du tableau. Ils sont principalement fabriqués par l’homme, par exemple le curium, le cérium, l’uranium, l’europium, etc.
- Non-métaux : Ces métaux comprennent l’hydrogène, le carbone, l’azote, l’oxygène, le phosphore, le soufre et le sélénium
- Gaz nobles : Les gaz nobles peuvent être trouvés dans un 18e groupe du tableau périodique par exemple le Néon, l’Argon, l’Hélium, le Krypton, le Xénon et le Radon.
Trouver la valence des éléments ici
Métaux étiquetés du tableau périodique
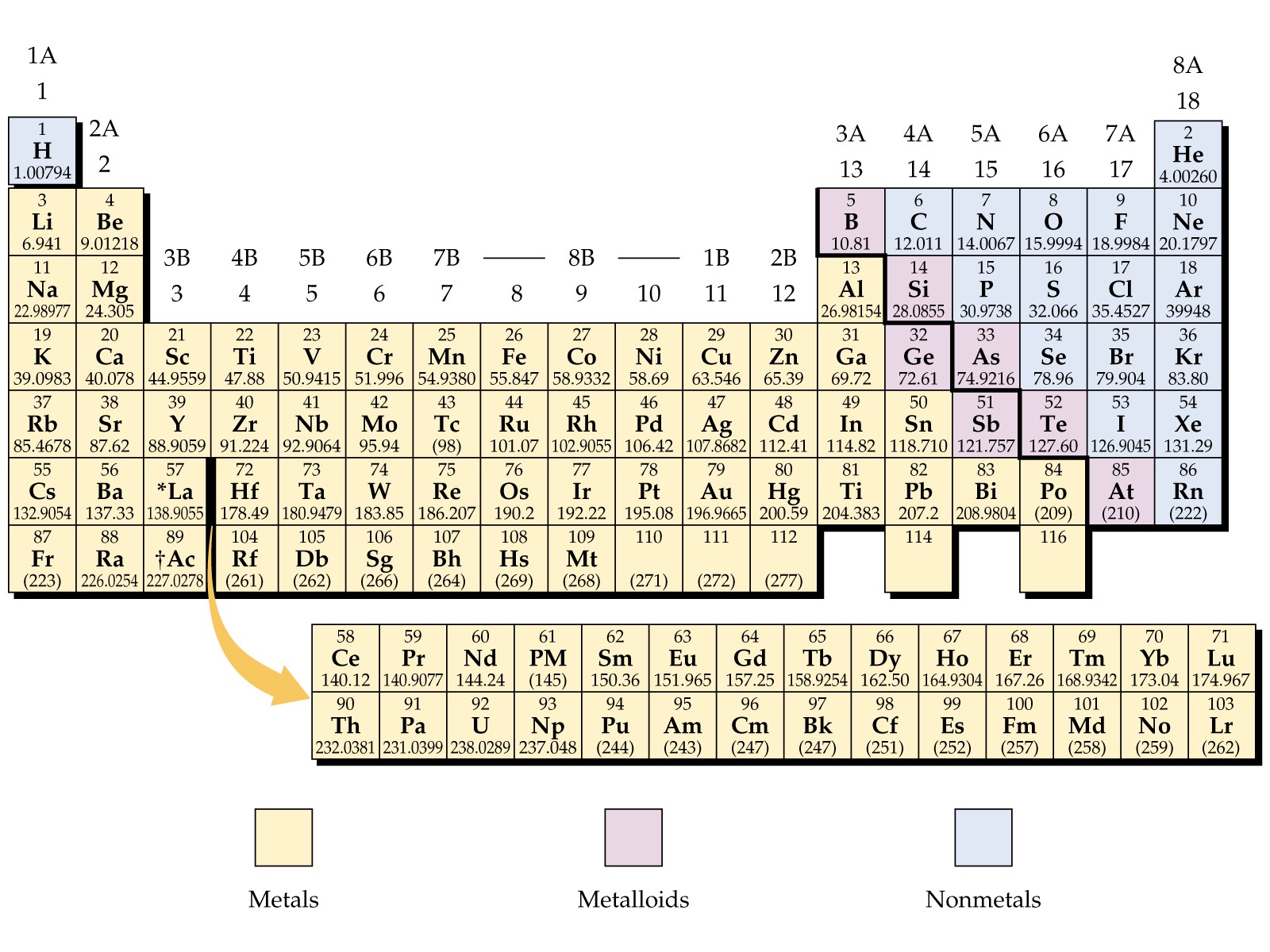

Les éléments qui sont classés comme métaux dans le tableau périodique partagent un certain nombre de propriétés. Tous les métaux sont solides à température ambiante, sauf le mercure, qui est liquide à température ambiante. Tous les métaux ont la propriété de conduire la chaleur et l’électricité, et ils sont brillants en apparence. Tous les métaux peuvent être transformés en fils et feuilles minces, cette propriété est appelée ductilité et malléabilité. En dehors de ces propriétés, les métaux peuvent également être caractérisés par leur capacité à perdre facilement des électrons.
Pour le tableau d’électronégativité et le tableau vierge du tableau périodique, visitez ici.
Tableau périodique étiqueté groupes
Le tableau périodique étiqueté groupes est joint ci-dessous;
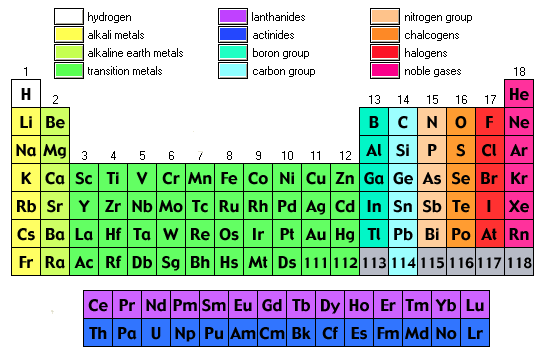

Tableau périodique étiqueté charges
Le tableau périodique fourni ci-dessous est étiqueté charges, si vous le voulez vous pouvez le télécharger ci-dessous ;
Trouver les charges des éléments ici

Les dernières tendances du tableau périodique.