US Pharm. 2016;41(6):HS14-HS18.
ABSTRACT : La maladie de Basedow est un trouble auto-immun qui se produit lorsque le système immunitaire attaque la glande thyroïde et l’amène à produire trop d’hormones thyroïdiennes (hyperthyroïdie). La cause exacte de la maladie de Graves n’est pas connue. Cette maladie peut toucher n’importe qui à n’importe quel âge, mais elle est plus fréquente chez les femmes. Si elle n’est pas traitée, la maladie de Graves peut provoquer une crise grave, potentiellement mortelle (c’est-à-dire une crise thyroïdienne). Les principaux objectifs du traitement sont d’éliminer l’excès d’hormones thyroïdiennes et de minimiser les conséquences à long terme de la maladie. Les traitements comprennent l’iode radioactif, les médicaments antithyroïdiens (propylthiouracile, méthimazole) et la chirurgie. Les bêta-bloquants peuvent être utilisés pour soulager les symptômes.
La maladie de Graves doit son nom au médecin qui l’a décrite pour la première fois en Irlande en 1835 – Robert J. Graves.1 Elle est également appelée maladie de Basedow – du nom d’un médecin allemand, Karl Adolph von Basedow, qui a également décrit cette affection en 1840. Il ne savait pas que Graves avait décrit la même maladie quelques années auparavant. Le terme de maladie de Basedow est plus couramment utilisé en Europe continentale ; aux États-Unis, on l’appelle maladie de Graves.1
La thyroïde, une glande en forme de papillon située à l’avant du cou, est un organe important du système endocrinien2. Cette glande libère les hormones thyroxine (T4) et triiodothyronine (T3), qui contrôlent le métabolisme du corps.3-6 L’hormone thyroïdienne aide le corps à utiliser l’énergie, à rester au chaud et à assurer le bon fonctionnement du cerveau, du cœur, des muscles et des autres organes. Le contrôle du métabolisme est important pour réguler l’humeur, le poids et les niveaux d’énergie mentale et physique. Lorsque l’organisme produit trop d’hormones thyroïdiennes, on parle d’hyperthyroïdie. Une glande thyroïde sous-active entraîne une hypothyroïdie.
Parce que les hormones thyroïdiennes affectent divers systèmes corporels, les signes et les symptômes associés à la maladie de Basedow peuvent être très variés et influencer de manière significative le bien-être général d’une personne. Les signes courants de l’hypothyroïdie sont la léthargie, la peau sèche, les cheveux et les ongles cassants et la sensibilité au froid.3,4 Les signes typiques de l’hyperthyroïdie sont souvent tout le contraire et comprennent la tachycardie, la sensibilité à la chaleur et une peau humide et grasse.3-7 Bien qu’un certain nombre de troubles puissent entraîner une hyperthyroïdie, la maladie de Basedow en est une cause fréquente.
Bien que la maladie de Basedow puisse toucher n’importe qui, elle est plus fréquente chez les femmes et se manifeste avant l’âge de 40 ans.1,7-9 L’incidence est d’environ 1 personne sur 2 000 (0,05 %). Les facteurs qui augmentent le risque de maladie de Graves sont décrits dans le TABLEAU 1.4,8,10,11

Pathophysiologie
La maladie de Graves est un trouble auto-immun qui peut survenir lorsque le système immunitaire attaque par erreur le tissu thyroïdien sain, ce qui entraîne une suractivité de la glande thyroïde. Normalement, la fonction thyroïdienne est régulée par une hormone libérée par l’hypophyse. En cas de besoin, le système immunitaire de l’organisme produit des anticorps conçus pour cibler un virus, une bactérie ou une autre substance étrangère spécifique. Dans la maladie de Basedow, l’organisme produit un anticorps dirigé contre certaines cellules de la glande thyroïde. L’anticorps associé à la maladie de Basedow, l’anticorps récepteur de la thyrotropine, imite l’hormone hypophysaire régulatrice et prend le pas sur la régulation normale de la thyroïde par l’organisme, provoquant une surproduction d’hormones thyroïdiennes.2,6,8,9
Ces anticorps, appelés immunoglobulines stimulant la thyroïde (IST), provoquent la croissance de la thyroïde et la fabrication d’une quantité d’hormones thyroïdiennes supérieure aux besoins de l’organisme. Les IST se lient aux récepteurs des cellules thyroïdiennes, qui sont normalement des « stations d’accueil » pour la thyréostimuline (TSH). Les IAC incitent alors la thyroïde à se développer et à produire trop d’hormones thyroïdiennes, ce qui entraîne une hyperthyroïdie. La glande thyroïde peut s’hypertrophier lorsque le régime alimentaire du patient ne contient pas suffisamment d’iode ou lorsque les taux de TSH s’élèvent en réponse à un défaut de synthèse normale des hormones par la glande thyroïde. Dans la maladie de Basedow, on sait que l’auto-immunité médiée par les lymphocytes B et T est dirigée contre des antigènes thyroïdiens familiers : la thyroglobuline, la peroxydase thyroïdienne, le symporteur sodium-iodure et le récepteur de la thyrotropine. Le récepteur de la thyrotropine est le principal auto-antigène de la maladie de Basedow et est responsable de la manifestation de l’hyperthyroïdie. Les principaux symptômes de l’hyperthyroïdie sont les suivants : yeux exorbités (exophtalmie), intolérance à la chaleur, énergie accrue, tachycardie, troubles du sommeil, diarrhée et anxiété. Les signes et symptômes spécifiques à la maladie de Basedow sont énumérés dans le TABLEAU 2.4,10,11 Si elle n’est pas traitée, la maladie de Basedow peut provoquer une thyrotoxicose grave ou une crise thyroïdienne9,10,12,13.

Les manifestations peu fréquentes de la maladie de Basedow comprennent la dermopathie de Basedow (un rougissement et un épaississement de la peau, souvent sur les tibias ou le dessus des pieds) et l’ophtalmopathie de Basedow (une accumulation de certains glucides dans la peau).2,8
Complications de la maladie de Basedow
Il existe de nombreuses complications associées à la maladie de Basedow, notamment les problèmes de grossesse, les troubles cardiaques, l’ostéoporose et la tempête thyroïdienne. Les complications possibles pendant la grossesse comprennent une fausse couche, une naissance prématurée, un dysfonctionnement thyroïdien fœtal, une mauvaise croissance fœtale, une insuffisance cardiaque maternelle et une prééclampsie.4,5,8 Si elle n’est pas traitée, la maladie de Basedow peut entraîner des troubles du rythme cardiaque, des modifications de la structure et de la fonction des muscles cardiaques et l’incapacité du cœur à pomper suffisamment de sang dans l’organisme5,8,10. L’hyperthyroïdie non traitée peut également entraîner une faiblesse et une fragilité des os.5,8
La crise thyroïdienne est une complication rare, potentiellement mortelle, également connue sous le nom d’hyperthyroïdie accélérée ou de crise thyrotoxique.2,9,13-16 Elle est plus probable lorsque l’hyperthyroïdie sévère n’est pas traitée ou traitée de manière inadéquate. Les effets indésirables graves comprennent la fièvre, la transpiration abondante, les vomissements, la diarrhée, le délire, la faiblesse grave, les convulsions, l’irrégularité marquée du rythme cardiaque, la jaunisse, l’hypotension artérielle grave et le coma. La tempête thyroïdienne nécessite souvent des soins d’urgence immédiats.5,8,15
Tests et diagnostic
Le diagnostic de la maladie de Basedow comprend plusieurs étapes. Lors d’un examen physique, les yeux seront examinés pour voir s’ils sont irrités ou saillants, et si la glande thyroïde est hypertrophiée.8 La fréquence cardiaque, la pression artérielle et tout signe de tremblements seront surveillés. Les analyses sanguines indiquent que les taux de TSH et de thyroïde sont généralement élevés dans la maladie de Basedow8. La quantité et le taux d’iode radioactif absorbé par la thyroïde permettent de déterminer si la maladie de Basedow ou une autre affection est à l’origine de l’hyperthyroïdie. L’échographie peut montrer si la glande thyroïde est hypertrophiée, et elle est surtout utile chez les personnes qui ne peuvent pas subir de captation d’iode radioactif, comme les femmes enceintes. Les tests d’imagerie (tomodensitométrie ou IRM) peuvent aider à identifier et à diagnostiquer l’ophtalmopathie de Graves.5
Traitement
Les principaux objectifs du traitement de l’hyperthyroïdie sont d’éliminer l’excès d’hormones thyroïdiennes et de minimiser les conséquences à long terme9. Les traitements comprennent l’iode radioactif, les médicaments antithyroïdiens (propylthiouracile , méthimazole ) et la chirurgie.2,8-10 Des bêta-bloquants sont parfois ajoutés pour apporter un soulagement symptomatique.9,13,15
Traitement par iode radioactif (TIR) : La dose habituelle pour la RIT varie de 5 à 15 mCi de 131I. En général, des doses plus élevées sont nécessaires pour les patients qui ont de gros goitres ou une faible captation d’iode radioactif, ou qui ont été prétraités avec des médicaments antithyroïdiens.15,16
Comme la thyroïde a besoin d’iode pour produire des hormones, l’iode radioactif va dans les cellules thyroïdiennes et, avec le temps, les cellules thyroïdiennes hyperactives sont détruites. La glande thyroïde rétrécit et, après plusieurs semaines ou mois, les symptômes de l’hyperthyroïdie diminuent progressivement.16 L’ITR peut augmenter le risque d’apparition ou d’aggravation des symptômes de l’ophtalmopathie de Basedow. Cet effet indésirable est généralement léger et temporaire, mais le traitement ne doit pas être utilisé si la personne souffre déjà de problèmes oculaires modérés à graves. Parmi les autres effets secondaires de ce traitement figurent une sensibilité du cou et une augmentation temporaire du taux d’hormones thyroïdiennes. Comme ce traitement peut entraîner un déclin de la fonction thyroïdienne globale, l’ITR n’est généralement pas utilisé chez les femmes enceintes ou allaitantes. D’autres traitements visant à fournir à l’organisme des quantités normales d’hormones thyroïdiennes peuvent être nécessaires. Les patients qui prennent actuellement des médicaments antithyroïdiens doivent interrompre leur traitement au moins 2 jours avant de prendre le produit radiopharmaceutique.11,16 Avec l’iode radioactif, l’objectif du traitement est de provoquer un état hypothyroïdien dû à la destruction de la glande thyroïde, qui se produit généralement 2 à 3 mois après l’administration du médicament. La contre-indication absolue de l’iode radioactif est la grossesse.14,16,17
Médicaments antithyroïdiens (ATM) : Les ATM agissent en bloquant l’utilisation de l’iode par la thyroïde pour produire des hormones.5,11 Ces médicaments comprennent le PTU oral et la MMI. Le PTU peut être utilisé lorsque les patients ne peuvent pas tolérer la MMI, l’iode radioactif ou la chirurgie. Lorsque ces médicaments sont utilisés, une rechute de l’hyperthyroïdie peut survenir au fil du temps. Les ATM bloquent la réaction de couplage de la monoiodotyrosine et de la diiodotyrosine pour produire la T4 et la T3, empêchant ainsi efficacement la synthèse des hormones thyroïdiennes.9,11 De plus, le PTU, mais pas la MMI, inhibe la conversion périphérique de la T4 en T3.9 Les doses orales initiales de PTU varient entre 300 et 600 mg par jour (dose quotidienne maximale = 1 200 mg). Les doses orales initiales de MMI, qui est 10 fois plus puissant que le PTU, varient entre 30 et 60 mg par jour (dose quotidienne maximale = 120 mg).9,11,13 Bien que ces médicaments soient traditionnellement divisés en trois ou quatre doses quotidiennes, ils peuvent être administrés en doses uniques.9 Une amélioration clinique est généralement observée après 4 à 8 semaines, après quoi la dose doit être diminuée selon un calendrier mensuel.9 Les doses d’entretien orales typiques pour chaque agent sont de 50 à 300 mg pour le PTU et de 5 à 30 mg pour le MMI. Le traitement doit être poursuivi pendant 12 à 24 mois si l’objectif est d’obtenir une rémission à vie.9,11,13
Les MTA peuvent être utilisés avant ou après la RIT comme traitement complémentaire. Les effets indésirables des deux médicaments comprennent des éruptions cutanées, des douleurs articulaires, une insuffisance hépatique et une diminution des globules blancs qui combattent la maladie. En raison du risque de malformations congénitales, la MMI n’est généralement pas utilisée pour traiter les femmes enceintes au cours du premier trimestre. Le PTU peut être considéré comme le médicament de choix juste avant et pendant le premier trimestre de la grossesse. La FDA a émis un avertissement boîte noire sur le PTU indiquant sa capacité à provoquer des lésions hépatiques potentiellement fatales ou graves et une insuffisance hépatique aiguë chez les adultes et les enfants.18
Bêta-bloquants : Ces médicaments n’inhibent pas la production d’hormones thyroïdiennes, mais ils bloquent l’effet des hormones sur le corps. Ils peuvent être utilisés pour soulager les battements cardiaques irréguliers, les tremblements, l’anxiété ou l’irritabilité, l’intolérance à la chaleur, la transpiration, la diarrhée et la faiblesse musculaire. Les bêta-bloquants couramment utilisés sont le propranolol, l’aténolol, le métoprolol, le lopressor et le nadolol. Comme les bêta-bloquants peuvent compliquer la gestion de l’asthme et du diabète, ces patients doivent utiliser ces médicaments avec prudence.5,11
Chirurgie : La chirurgie visant à retirer tout ou partie de la glande thyroïde (thyroïdectomie ou thyroïdectomie subtotale) est également une option pour le traitement de la maladie de Basedow. Après l’intervention, les patients devront probablement suivre un traitement pour fournir à l’organisme des quantités normales d’hormones thyroïdiennes. Les risques de l’opération comprennent des dommages potentiels aux cordes vocales et aux glandes parathyroïdes. Les glandes parathyroïdes produisent une hormone qui contrôle le niveau de calcium dans le sang. Les complications sont rares sous les soins d’un chirurgien expérimenté en chirurgie thyroïdienne.5,11
Traitement de l’ophtalmopathie de Graves
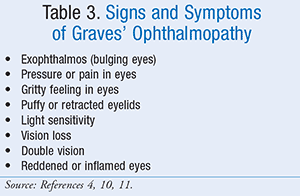
L’ophtalmopathie de Graves peut être divisée en deux phases cliniques : le stade inflammatoire et le stade fibrotique.5 Le stade inflammatoire est marqué par un œdème et un dépôt de glycosaminoglycane dans les muscles extra-oculaires. Le stade inflammatoire est marqué par un œdème et un dépôt de glycosaminoglycane dans les muscles extra-oculaires, ce qui entraîne les manifestations cliniques suivantes : gonflement orbitaire, regard fixe, diplopie, œdème périorbitaire et, parfois, douleur. L’ophtalmopathie de Graves ne s’améliore pas toujours avec le traitement de la maladie de Graves. Les symptômes de l’ophtalmopathie de Graves (TABLEAU 3) peuvent même s’aggraver pendant 3 à 6 mois. Ensuite, les signes et les symptômes se stabilisent généralement pendant un an environ, puis commencent à s’améliorer, souvent de manière autonome. Les symptômes légers de l’ophtalmopathie de Graves peuvent être gérés en utilisant des larmes artificielles en vente libre pendant la journée et des gels lubrifiants la nuit.5
Si les symptômes sont plus sévères, le médecin peut recommander plusieurs traitements, notamment des corticostéroïdes, une chirurgie de décompression orbitale, une radiothérapie orbitale et des thérapies non pharmacologiques. Un traitement à la prednisone peut être nécessaire pour réduire le gonflement derrière les globes oculaires.11 Les effets indésirables des corticostéroïdes comprennent la rétention d’eau, la prise de poids, l’élévation de la glycémie, l’augmentation de la pression artérielle et les sautes d’humeur. La chirurgie de décompression orbitaire est une intervention qui consiste à retirer l’os situé entre l’orbite et les sinus, c’est-à-dire les espaces aériens situés à côté de l’orbite.11 Cela permet aux yeux de retrouver leur position initiale. Ce traitement est généralement utilisé si la pression exercée sur le nerf optique menace la perte de la vision. Les complications possibles sont la vision double. La radiothérapie orbitale utilise des rayons X ciblés pendant plusieurs jours pour détruire une partie des tissus situés derrière les yeux.2,11
Mode de vie et remèdes maison : Bien manger et faire de l’exercice peut améliorer l’amélioration de certains symptômes pendant le traitement. Comme la thyroïde contrôle le métabolisme, le patient peut avoir tendance à prendre du poids lorsque l’hyperthyroïdie est corrigée. La maladie de Basedow peut également entraîner une fragilité osseuse, et les exercices de port de poids peuvent aider à maintenir la densité osseuse.2,4,6
Les patients peuvent appliquer des compresses froides sur leurs yeux, car l’humidité ajoutée peut être apaisante. Il faut également conseiller aux patients de porter des lunettes de soleil pour diminuer la sensibilité aux rayons ultraviolets (UV) et à la lumière vive. Les gouttes ophtalmiques lubrifiantes peuvent soulager la sensation de sécheresse et de démangeaison à la surface des yeux. Un gel à base de paraffine, tel que Refresh Lacri-Lube, peut être appliqué la nuit. Les patients doivent surélever la tête de leur lit. Le fait de garder la tête plus haute que le reste du corps réduit l’accumulation de liquide dans la tête et peut soulager la pression sur les yeux. Enfin, il faut conseiller aux patients de ne pas fumer, car le tabagisme aggrave l’ophtalmopathie de Graves.
Traitement de la dermopathie de Graves
L’utilisation de crèmes ou de pommades en vente libre contenant de l’hydro-cortisone peut aider à soulager le gonflement et les rougeurs. En outre, l’utilisation d’enveloppes de compression sur les jambes peut être bénéfique.5,11
Conclusion
La pharmacothérapie de la maladie de Basedow est complexe mais gérable. Comme le résultat souhaité des médicaments antithyroïdiens est de détruire la glande thyroïde et de provoquer un état hypothyroïdien, les patients devront faire l’objet d’une surveillance clinique continue, de conseils (TABLEAU 4) et d’une substitution thyroïdienne à vie par des hormones thyroïdiennes.

1. Ellis H. Robert Graves : 1796-1852. Br J Hosp Med (Lond). 2006;67(6):313.
2. Yeung SJ. La maladie de Graves. Overview. Medcape. 18 novembre 2015. http://emedicine.medscape.com/article/120619-overview. Consulté le 8 mars 2016.
3. Garber JR, Cobin RH, Gharib H, et al. Directives de pratique clinique pour l’hypothyroïdie chez les adultes : coparrainées par l’Association américaine des endocrinologues cliniques et l’Association américaine de la thyroïde. Endocr Pract. 2012;18(6):988-1028.
4. maladie de Graves. MedlinePlus. 21 avril 2015. www.nlm.nih.gov/medlineplus/ency/article/000358.htm. Consulté le 8 mars 2016.
5. Cockerham KP, Chan SS. La maladie oculaire thyroïdienne. Neurol Clin. 2010;28:729-755.
6. Yeung SJ. La maladie de Graves. Epidemiology. Medcape. 18 novembre 2015. http://emedicine.medscape.com/article/120619-overview#a6. Consulté le 8 mars 2016.
7. Woeber KA. Mise à jour sur la gestion de l’hyperthyroïdie et de l’hypothyroïdie. Arch Fam Med. 2007;9(8):743-747.
8. maladie de Graves. Risk factors. Clinique Mayo. www.mayoclinic.org/diseases-conditions/graves-disease/basics/risk-factors/con-20025811. Consulté le 8 mars 2016.
9. Yeung SJ. La maladie de Basedow. Background. Medcape. 18 novembre 2015. http://emedicine.medscape.com/article/120619-overview#a4. Consulté le 8 mars 2016.
10. Yeung SJ. La maladie de Graves. Pathophysiologie. Medcape. 18 novembre 2015. http://emedicine.medscape.com/article/120619-overview#a5. Consulté le 8 mars 2016.
11. Yeung SJ. Traitement de la maladie de Basedow & gestion. 18 novembre 2015. http://emedicine.medscape.com/article/120619-treatment. Consulté le 8 mars 2016.
12. Nayak B, Burman K. Thyrotoxicose et tempête thyroïdienne. Endcrinol Metab Clin North Am. 2006;35(4):663-686.
13. Mandel SJ, Larsen PR, Davies TF. Thyrotoxicosis. In : Melmed S, Polonsky KS, Larsen PR, Kronenberg HM, eds. Williams Textbook of Endocrinology. 12th ed. Philadelphie, PA : Elsevier Saunders ; 2011:362-405.
14. Bhattacharyya A, Wiles PG. Crise thyrotoxique se présentant comme un abdomen aigu. 1997;90(12):681-682.
15. Bahn RS, Burch HB, Cooper DS, et al. Hyperthyroïdie et autres causes de thyrotoxicose : directives de gestion de l’American Thyroid Association et de l’American Association of Clinical Endocrinologists. Endocr Pract. 2011;17(3):456-520.
16. McDermott MT, Kidd GS, Dodson LE, et al. Radioiodine-induced thyroid storm. Rapport de cas et revue de la littérature. Am J Med. 1983;75(2):353-359.
17. Read CH Jr, Tansey MJ, Menda Y. Analyse rétrospective sur 36 ans de l’efficacité et de la sécurité de l’iode radioactif dans le traitement des jeunes patients atteints du syndrome de Graves. J Clin Endocrinol Metab. 2004;89(9):4229-4233.
18. Communication sur la sécurité des médicaments de la FDA. Nouvelle mise en garde encadrée sur les lésions hépatiques graves avec le propylthiouracile. 21 avril 2010. www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationforPatientsandProviders/ucm209023.htm. Consulté le 8 mars 2016.