La Ligue internationale contre l’épilepsie (ILAE) a révisé sa définition de l’épilepsie en 2014 afin de maximiser l’identification et le traitement précoces des patients épileptiques1. La définition conceptuelle de l’épilepsie par la LICE, formulée pour la première fois en 2005, est » un trouble du cerveau caractérisé par une prédisposition durable à générer des crises d’épilepsie. » En pratique, cette définition correspondait aux patients présentant au moins deux crises non provoquées à plus de 24 heures d’intervalle. Nous savons toutefois que tous les patients ayant subi une seule crise non provoquée n’ont pas la même probabilité d’en subir une deuxième. Selon la nouvelle définition de l’ILAE, les patients présentant une seule crise non provoquée et une probabilité de récurrence des crises supérieure à 60 % répondent désormais aux critères de diagnostic de l’épilepsie.
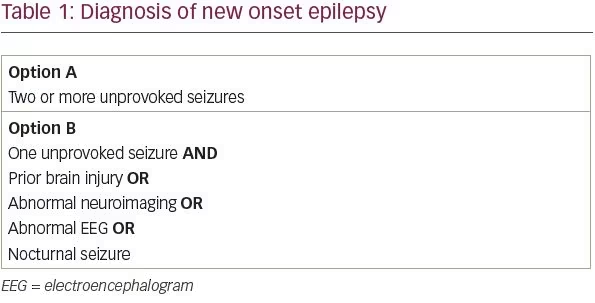
Dans une revue systématique des études évaluant le risque de récurrence des crises après une seule crise non provoquée, entre 21 et 45 % des patients ont eu une autre crise non provoquée dans les 2 premières années2. D’un point de vue pratique, on a identifié quatre facteurs de risque qui doublent approximativement le risque de récurrence des crises chez un patient : une lésion cérébrale antérieure, un résultat anormal de neuro-imagerie correspondant au foyer de crise présumé, des décharges épileptiformes focales ou généralisées à l’électroencéphalogramme (EEG), ou une crise nocturne3.-Ainsi, les patients présentant une seule crise non provoquée et au moins l’un de ces quatre facteurs de risque ont probablement plus de 60 % de chances de subir une crise récurrente et peuvent être diagnostiqués comme épileptiques (tableau 1).
Bien qu’une première étude importante ait suggéré qu’un examen neurologique anormal était associé à un risque accru de récurrence des crises, une étude de suivi du même groupe n’a trouvé aucune augmentation du risque.3,7 La même étude de suivi a révélé que le fait d’avoir un frère ou une sœur épileptique augmente le risque de récurrence chez les patients atteints d’épilepsie idiopathique, mais même chez ces patients, le risque de récurrence n’est que de 46 % à 5 ans. Ainsi, les résultats de l’examen neurologique et les antécédents familiaux d’épilepsie doivent être pris en considération lors de l’évaluation d’un patient présentant une première crise, mais ces caractéristiques ne suffisent pas à elles seules à poser un diagnostic d’épilepsie.
Envisagement du traitement par antiépileptique dans l’épilepsie nouvelle
La plupart des premières études sur la récurrence des crises après une crise initiale non provoquée incluaient à la fois des patients traités par antiépileptique (AED) et des patients non traités, ce qui rend difficile l’estimation du risque réel de crise récurrente. L’étude FIRST a révélé que 51% des patients qui n’ont pas commencé un traitement par AED après une première crise en ont eu une autre dans les 2 ans, alors que seulement 25% de ceux qui ont commencé un AED ont eu une autre crise dans la même période.8 Cependant, des études ultérieures ont montré que bien que le traitement par AED réduise le risque de récurrence des crises dans les 2 ans suivant une première crise, il n’affecte pas la probabilité de rémission des crises à long terme ou la qualité de vie.9,10 Comme le traitement précoce par les AED n’est pas garanti pour changer le résultat global du patient, et que les AED ne sont pas des médicaments entièrement bénins, tous les patients qui reçoivent un diagnostic d’épilepsie ne choisissent pas de commencer le traitement tout de suite.
Toutes les décisions concernant le traitement par AED doivent être prises en collaboration avec le patient après une discussion approfondie des risques et des avantages, en pesant le risque de préjudice dû aux crises contre les effets indésirables potentiels des AED. La présence d’un type de crise associé à un risque plus élevé de blessure ou de décès, comme les crises tonico-cloniques ou l’état de mal épileptique, peut être un facteur influençant la décision du patient et du médecin de commencer ou non les DEA.11-13
Caractérisation du type d’épilepsie
La détermination du type d’épilepsie du patient – focale ou généralisée – au moment du diagnostic initial est importante car elle permet de prédire le pronostic et de guider la sélection d’un DEA approprié. Cette détermination est généralement effectuée sur la base de la sémiologie des crises et des résultats de l’imagerie par résonance magnétique (IRM) et de l’EEG. Des symptômes moteurs ou sensoriels latéralisés, une déviation forcée des yeux ou une rotation de la tête, des automatismes, des troubles du langage et des phénomènes expérientiels suggèrent un début focal, tandis que des secousses myocloniques bilatérales ou une activité tonique bilatérale initiale suggèrent un début généralisé.
Cependant, la sémiologie seule peut être trompeuse : les crises focales peuvent ne pas présenter de caractéristiques de latéralisation au début, et plus de la moitié des patients atteints d’épilepsie généralisée présentent des symptômes de crises focales.14 De plus, les trois quarts des patients atteints d’épilepsie focale sont amnésiques pour au moins certaines de leurs crises, et 30 % sont amnésiques pour toutes les crises.15 En outre, jusqu’à 60 % des patients ne présentent pas d’aura précédant leurs crises.16 Ces facteurs rendent le diagnostic et la caractérisation de l’épilepsie difficiles chez de nombreux patients.
La plupart des patients ayant une première crise devraient subir une IRM, sauf contre-indication. L’IRM a un rendement plus élevé que la tomodensitométrie (TDM) pour la détection des lésions épileptogènes focales.17-19 La présence d’une lésion focale peut confirmer un début focal si la localisation de la lésion correspond à la sémiologie du patient. Pour les patients présentant un syndrome d’épilepsie généralisée primaire électroclinique clair, comme l’épilepsie myoclonique juvénile, la neuro-imagerie peut ne pas être nécessaire.
Si une IRM est obtenue, les séquences recommandées comprennent une séquence T1 3D avec des tranches isotropes de 1 mm (par ex, écho de gradient rapide préparé par magnétisation ), des séquences T2 et FLAIR axiales et coronales avec des coupes ≤3 mm, et une séquence T2* axiale pour l’hémosidérine et la calcification (par exemple, imagerie pondérée par la susceptibilité ou écho de gradient ).20 Le contraste n’est pas nécessaire pour tous les patients, mais doit être envisagé pour les patients de plus de 50 ans, en raison de la probabilité plus élevée de tumeur cérébrale métastatique ou primaire dans ce groupe d’âge. Lorsque cela est possible, l’IRM à 3 Tesla est préférée à celle à 1,5 Tesla car elle est plus sensible aux lésions épileptogènes.21,22 Récemment, les scanners IRM à 7 Tesla ont encore augmenté la sensibilité, mais ils ne sont généralement disponibles que dans le cadre de protocoles de recherche.23
L’EEG est l’autre modalité essentielle pour le diagnostic et la caractérisation de l’épilepsie nouvelle. Un seul EEG de routine peut être insuffisant pour la détection des anomalies épileptiformes ; une méta-analyse récente de 15 études a montré que la sensibilité d’un EEG de routine était de 17 %.24 Afin d’augmenter ce rendement, les médecins doivent envisager de réaliser un EEG prolongé de 60 minutes, un EEG avec privation de sommeil ou jusqu’à trois EEG de routine en série.25-Les enregistrements EEG ambulatoires augmentent également la probabilité de détecter des anomalies épileptiformes ; les avantages d’un enregistrement prolongé diminuent après 48 heures, puisque 95 % des anomalies sont détectées dans ce délai28. Une étude vidéo EEG pour patients hospitalisés peut être envisagée dans des scénarios spécifiques, tels que la différenciation des crises épileptiques des attaques psychogènes non épileptiques.29
Choisir un médicament antiépileptique-épilepsie focale
L’essai SANAD-traitement de première intention de l’épilepsie focale nouvellement apparue
L’objectif du traitement AED dans l’épilepsie nouvellement apparue est de contrôler les crises avec un seul AED tout en minimisant les effets indésirables. Bien que de nombreux médicaments soient disponibles pour le traitement de l’épilepsie focale, il existe peu d’études contrôlées comparant leur efficacité et leur tolérance. L’essai SANAD, publié en 2007, est une étude fondamentale portant sur 1 721 patients souffrant d’épilepsie focale et randomisés pour recevoir un traitement à base de carbamazépine, de gabapentine, de lamotrigine, d’oxcarbazépine ou de topiramate.30 Le principal résultat était le délai avant l’échec du traitement, défini comme l’arrêt du médicament en raison de crises non contrôlées ou d’effets indésirables. La lamotrigine était significativement meilleure que la carbamazépine, la gabapentine et le topiramate, et non significativement meilleure que l’oxcarbazépine. Pour le temps de rémission à 12 mois, cependant, la carbamazépine était significativement meilleure que la gabapentine et non significativement meilleure que la lamotrigine, le topiramate et l’oxcarbazépine30.
Les résultats de l’essai SANAD suggèrent que la lamotrigine est le meilleur traitement de première intention pour l’épilepsie focale en raison de sa combinaison d’efficacité et de tolérance, la carbamazépine étant une alternative raisonnable chez les patients qui peuvent la tolérer.
Nouveaux antiépileptiques pour le traitement de première intention de l’épilepsie focale
Depuis la publication de l’essai SANAD, plusieurs nouveaux médicaments pour l’épilepsie focale sont entrés sur le marché. Si tous ces médicaments ont été initialement étudiés en tant que traitements d’appoint, beaucoup sont maintenant utilisés en monothérapie, et certains, en particulier le lévétiracétam, sont maintenant couramment utilisés en première intention. Un avantage majeur de ces nouveaux médicaments est que les doses peuvent être augmentées rapidement chez les patients présentant des crises fréquentes, sans risque de syndrome de Stevens-Johnson, un effet indésirable connu de la lamotrigine et, dans une moindre mesure, de la carbamazépine.
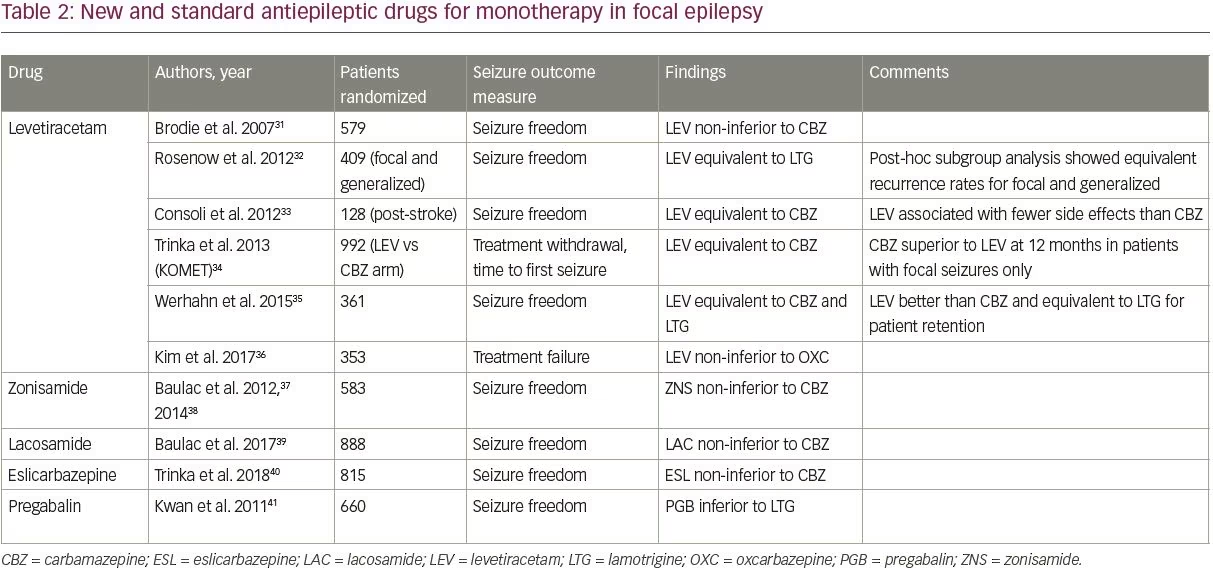
Parmi les nouveaux DEA, quatre – le lévétiracétam, le zonisamide, le lacosamide et l’eslicarbazépine – ont été comparés aux DEA plus anciens dans des essais contrôlés randomisés, comme le montre le tableau 2.31-41 Les essais ont été identifiés à l’aide du filtre des essais cliniques de PubMed et des termes de recherche » monothérapie, » et » « , et ont été inclus s’ils étudiaient des patients adultes atteints d’épilepsie focale en comparant un DEA plus récent à l’un des DEA standard (ceux inclus dans l’essai SANAD).
Parmi les quatre nouveaux AED, le levetiracetam est le mieux étudié et le plus largement prescrit ; il est largement devenu l’AED de première ligne par défaut pour les épilepsies nouvelles en raison de sa facilité de titration et de son profil d’effets secondaires favorable. Le lévétiracetam est maintenant le DEA de première intention le plus couramment prescrit chez les adultes plus âgés, représentant 45,5 % des ordonnances42. Des études ont montré que le lévétiracétam a une efficacité similaire à celle des anciens DEA, bien qu’il ait été inférieur à la carbamazépine dans une analyse de sous-groupe d’une étude (tableau 2).
Important, seules deux études ont comparé le lévétiracétam à la lamotrigine ; les deux études ont trouvé une efficacité similaire pour les deux médicaments32,35. Le volet épilepsie focale de l’essai SANAD II, qui sera la plus grande étude visant à comparer l’efficacité et la tolérance à long terme du lévétiracétam et de la lamotrigine, est actuellement en cours (ISRCTN30294119).
En dehors du lévétiracétam, les données de haute qualité évaluant les nouveaux DEA en monothérapie sont limitées. Le zonisamide, le lacosamide et l’eslicarbazépine se sont tous révélés non inférieurs à la carbamazépine dans une seule étude chacun (tableau 2) ; le zonisamide est également étudié dans le bras focal de l’essai SANAD II. Ces trois agents peuvent être considérés comme des options pour le traitement de première ligne en fonction des comorbidités et des contre-indications du patient. La prégabaline a également été étudiée en comparaison avec la lamotrigine et s’est avérée inférieure,41 et n’est donc pas recommandée comme
traitement de première intention.
La brivaracetam a été bien tolérée dans deux études randomisées de conversion de la polythérapie à la monothérapie, mais le nombre de patients restant sous brivaracetam à la fin de ces études était trop faible pour déterminer son efficacité en monothérapie;43 elle n’a pas non plus été étudiée en comparaison directe avec les anciens AED. Ainsi, les données probantes sont insuffisantes pour recommander le brivaracétam en monothérapie comme traitement de première intention à l’heure actuelle.
Le clobazam, le perampanel et le cénobamate sont de nouveaux DEA qui peuvent être utilisés en monothérapie. Le clobazam et le perampanel ont tous deux été efficaces et bien tolérés dans de petites études rétrospectives incluant des patients atteints d’épilepsie focale et généralisée.44,45 Le clobazam s’est également révélé supérieur à la carbamazépine et à la phénytoïne dans un essai randomisé mené auprès de patients pédiatriques, mais n’a pas été directement comparé aux anciens AED dans une population adulte.46 Le cénobamate, un exhausteur de l’inactivation des canaux sodiques rapides et lents à posologie uniquotidienne, a récemment démontré son efficacité en tant qu’agent d’appoint pour les patients atteints d’épilepsie focale, mais n’a pas encore été étudié en monothérapie47.
Résumé du traitement de première intention de l’épilepsie focale
Levetiracetam a donné des résultats aussi bons, voire légèrement moins bons, que les anciens AED dans les essais tête-à-tête,31-36 et constitue un traitement de première intention raisonnable chez les patients sans antécédents de problèmes psychiatriques, en particulier si les crises sont fréquentes ou si les patients ont des difficultés avec le calendrier de titration de la lamotrigine. Chez les patients présentant des comorbidités psychiatriques, nous recommandons la lamotrigine comme traitement de première intention. L’étude SANAD II, qui est en cours, apportera une réponse plus définitive à la question de savoir lequel de ces deux AED est supérieur en termes d’efficacité et de tolérance. Selon les comorbidités du patient et sa tolérance aux effets secondaires, plusieurs des anciens DEA (carbamazépine, oxcarbazépine, topiramate) et des nouveaux DEA (zonisamide, lacosamide, eslicarbazépine) peuvent constituer des alternatives raisonnables. Le brivaracetam, le clobazam, le perampanel et le cenobamate pourraient être des options viables à l’avenir, mais les preuves sont insuffisantes pour le moment. La gabapentine et la prégabaline ne devraient pas être utilisées comme traitements de première intention.
Choisir un médicament antiépileptique-épilepsie généralisée ou non classée
L’essai SANAD-traitement de première intention de l’épilepsie généralisée nouvellement apparue
L’essai SANAD 2007 comprenait un deuxième bras, qui étudiait les patients atteints d’épilepsie généralisée ou d’épilepsie qui ne pouvait pas être définitivement classée au moment de l’initiation du traitement48. Le valproate était significativement meilleur que le topiramate pour le délai avant l’échec du traitement dans l’analyse globale, et significativement meilleur que le topiramate et la lamotrigine chez les patients ayant un diagnostic confirmé d’épilepsie généralisée. Pour le délai de rémission à 12 mois, le valproate était significativement meilleur que la lamotrigine dans les deux groupes, mais pas significativement différent du topiramate dans les deux groupes. Ainsi, le valproate semblait présenter la meilleure combinaison d’efficacité et de tolérance des trois médicaments étudiés.
Malgré le succès du valproate dans la SANAD, son utilisation en dehors du cadre des essais est problématique en raison de ses effets indésirables. Chez les femmes en âge de procréer, le valproate est contre-indiqué en raison de sa tératogénicité, car il augmente significativement le risque de malformations congénitales et de déficits neurocognitifs à long terme.49-52 Depuis 2018, l’Union européenne a interdit l’utilisation du valproate chez les femmes en âge de procréer, sauf si elles sont inscrites à un programme de prévention de la grossesse53. Le valproate a également plusieurs autres effets secondaires indésirables, notamment la prise de poids, la perte de cheveux, le syndrome des ovaires polykystiques et l’encéphalopathie hépatique.54-57 Des traitements alternatifs de première intention sont nécessaires, en particulier pour les femmes en âge de procréer.
Nouvelles alternatives au valproate pour le traitement de l’épilepsie généralisée
Levetiracetam est le nouvel AED le plus étudié pour l’épilepsie généralisée. Deux des essais de monothérapie décrits ci-dessus incluaient également des patients atteints d’épilepsie généralisée.32,34 Dans l’étude KOMET, le lévétiracétam était équivalent au valproate tant pour le taux d’abandon du traitement que pour le délai avant la première crise.34 Il a également été démontré que le lévétiracétam était équivalent à la lamotrigine pour le taux d’absence de crise dans un échantillon hétérogène ; une analyse post-hoc des sous-groupes a montré que cela était vrai pour l’épilepsie focale et généralisée32.
Récemment, Marson et ses collègues ont présenté les résultats du bras d’épilepsie généralisée de l’essai SANAD II.58 Le valproate était supérieur au levetiracetam pour le temps jusqu’à l’échec du traitement, le temps jusqu’à la première crise, et le temps jusqu’à la rémission à 24 mois. Il est intéressant de noter que la différence de temps jusqu’à l’échec du traitement était attribuable à un contrôle inadéquat des crises, plutôt qu’à des effets indésirables, ce qui suggère que le valproate n’était pas plus mal toléré que le lévétiracétam dans cet échantillon.
Comme nous l’avons mentionné plus haut, le clobazam et le perampanel se sont avérés avoir une bonne efficacité et une bonne tolérance dans des études d’observation rétrospectives qui incluaient des patients atteints d’épilepsie généralisée, mais aucun des deux médicaments n’a été comparé à l’un des médicaments plus anciens dans un essai randomisé.44,45 À notre connaissance, aucun des autres nouveaux DEA n’a été étudié en monothérapie chez les patients atteints d’épilepsie généralisée.
Résumé du traitement de première intention pour l’épilepsie généralisée et non classée
Bien que les résultats de SANAD II suggèrent que le valproate demeure le DEA le plus efficace pour l’épilepsie généralisée ou non classée, nous ne le recommandons pas comme traitement de première intention en raison de ses effets indésirables. La lamotrigine est un bon choix si la fréquence des crises est suffisamment faible pour permettre une augmentation lente de la dose. Si une action rapide est nécessaire, le levetiracetam peut être utilisé. Si les crises sont réfractaires à ces deux agents, le valproate peut être utilisé après une discussion attentive des risques et des avantages.
Counseling des patients avec une épilepsie nouvelle
Les patients avec un nouveau diagnostic d’épilepsie ont généralement de nombreuses questions sur la maladie et son impact sur leur vie. Les questions les plus fréquentes portent sur le pronostic à long terme de l’épilepsie, sur l’opportunité de commencer un traitement AED et sur le fait de savoir si le traitement AED sera à vie. Comme nous l’avons vu plus haut, les patients doivent être informés que le traitement AED immédiat réduit le risque de récidive précoce des crises, mais ne change pas le pronostic global de l’épilepsie, et que la décision de commencer un AED doit être prise sur une base individuelle. Les patients doivent être informés qu’environ la moitié d’entre eux parviendront à contrôler leurs crises avec leur premier AED, tandis que 20 % supplémentaires répondront à un deuxième ou un troisième médicament.59 En outre, ils doivent savoir que toute tentative d’interruption du traitement AED ne doit pas être entreprise avant au moins deux ans d’absence de crises, et que près de la moitié des patients auront une récurrence des crises après l’arrêt de l’AED.60
En dehors du contrôle des crises, les questions pratiques les plus courantes concernent la conduite automobile. Toute crise avec altération de la conscience – absente, tonico-clonique ou focale inconsciente – peut causer des dommages importants si elle se produit pendant que le patient conduit. La plupart des États exigent un intervalle d’absence de crise avant que le patient puisse reprendre la conduite. Les médecins doivent s’assurer que les patients connaissent les lois de leur État. Certains États exigent des médecins qu’ils signalent leurs patients épileptiques ou ayant des crises au Department of Motor Vehicles, tandis que d’autres ne le font pas.61 Il est important de noter que dans les États où la déclaration n’est pas obligatoire, les médecins peuvent ne pas bénéficier d’une protection juridique lorsqu’ils divulguent un diagnostic d’épilepsie sans le consentement du patient. Dans ces cas, les médecins devront peser les risques que le patient continue à conduire (en particulier dans le cas des conducteurs professionnels) par rapport aux risques de ramifications juridiques liées à la violation de la confidentialité du patient. Toutes les conversations sur la conduite automobile doivent être documentées dans le dossier médical du patient.
Les femmes en âge de procréer doivent en outre être conseillées sur les implications de l’épilepsie et des AED sur la grossesse. Les patientes doivent savoir que les crises, en particulier les crises tonico-cloniques généralisées, et certains DEA, peuvent avoir des effets indésirables sur le développement du fœtus. Chez les femmes qui ne prévoient pas de grossesse, il est préférable d’opter pour une contraception à action prolongée au moyen d’un dispositif intra-utérin ou d’une injection de dépôt, car ceux-ci minimisent les risques d’erreur de manipulation. Les patientes doivent également savoir que le traitement par des DEA inducteurs enzymatiques peut réduire l’efficacité de la contraception hormonale.62 Toutes les femmes épileptiques qui planifient une grossesse doivent en informer leur neurologue à l’avance ; si la grossesse n’est pas planifiée, le neurologue doit être informé dès que possible. De plus, toutes les femmes épileptiques en âge de procréer devraient prendre de l’acide folique, qu’une grossesse soit prévue ou non, car cela réduit le risque d’anomalies du tube neural qui se développent au début du premier trimestre, souvent avant que la grossesse ne soit connue.63
Le sujet le plus difficile à aborder avec les patients nouvellement diagnostiqués est la mort subite inattendue en épilepsie (SUDEP). Les facteurs de risque de MSIE comprennent une fréquence élevée des crises, un âge précoce d’apparition de la maladie, une longue durée de la maladie, des crises tonico-cloniques généralisées, des crises nocturnes, le fait de vivre seul, le sexe masculin, la dépendance à l’alcool et la toxicomanie.64-66 La plupart des neurologues pensent que tous les patients épileptiques devraient être informés sur la MSIE, tandis que certains soutiennent que les conseils sur la MSIE ne sont nécessaires que pour les patients à haut risque.67 Nous recommandons de discuter de la MSIE avec tous les patients souffrant d’épilepsie nouvelle dans le cadre d’une discussion initiale sur l’importance de l’observance du traitement, et de fournir des conseils plus fréquents et plus approfondis aux patients à haut risque.