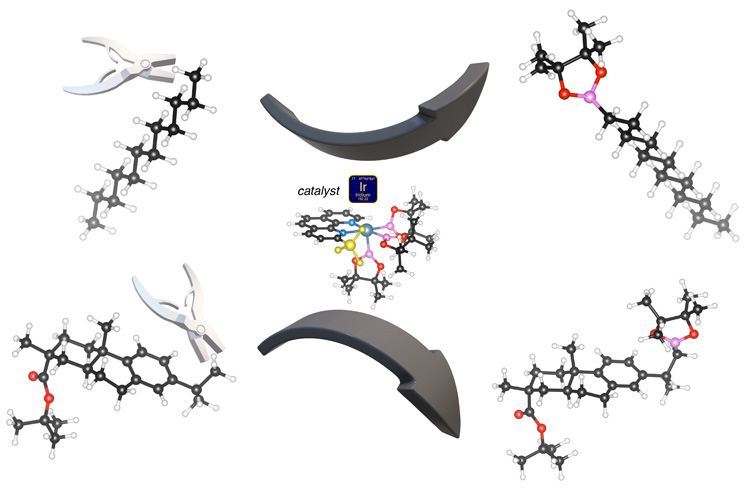
Un catalyseur (au centre) à base d’iridium (boule bleue) peut arracher un atome d’hydrogène (boules blanches) à un groupe méthyle terminal (en haut et en bas à gauche) pour ajouter un composé bore-oxygène (rose et rouge) qui peut facilement être échangé contre des groupes chimiques plus compliqués. La réaction fonctionne sur des chaînes d’hydrocarbures simples (réaction du haut) ou des composés carbonés plus complexes (réaction du bas). La sélectivité exquise de cette réaction catalytique est due au groupe méthyle (jaune) qui a été ajouté au catalyseur d’iridium. Les boules noires sont des atomes de carbone, les rouges des atomes d’oxygène et les roses des atomes de bore. (Image de l’UC Berkeley par John Hartwig)
La liaison chimique la plus courante dans le monde vivant – celle entre le carbone et l’hydrogène – a longtemps résisté aux tentatives des chimistes de l’ouvrir, contrecarrant les efforts pour ajouter de nouvelles cloches et des sifflets aux anciennes molécules à base de carbone.
Maintenant, après près de 25 ans de travail par les chimistes de l’Université de Californie, Berkeley, ces liaisons hydrocarbures – deux tiers de toutes les liaisons chimiques dans le pétrole et les plastiques – ont entièrement cédé, ouvrant la porte à la synthèse d’une large gamme de nouvelles molécules organiques, y compris des médicaments basés sur des composés naturels.
« Les liaisons carbone-hydrogène font généralement partie du cadre, la partie inerte d’une molécule », a déclaré John Hartwig, titulaire de la chaire Henry Rapoport de chimie organique à UC Berkeley. « Cela a été un défi et un graal de la synthèse de pouvoir faire des réactions à ces positions parce que, jusqu’à présent, il n’y avait pas de réactif ou de catalyseur qui vous permette d’ajouter quoi que ce soit à la plus forte de ces liaisons. »
Hartwig et d’autres chercheurs avaient déjà montré comment ajouter de nouveaux groupes chimiques aux liaisons C-H qui sont plus faciles à rompre, mais ils ne pouvaient les ajouter qu’aux positions les plus fortes de simples chaînes d’hydrocarbures.
Dans le numéro du 15 mai de la revue Science, Hartwig et ses collègues de l’UC Berkeley ont décrit comment utiliser un catalyseur nouvellement conçu pour ajouter des groupes chimiques fonctionnels aux plus difficiles des liaisons carbone-hydrogène à briser : les liaisons, généralement à la tête ou à la queue d’une molécule, où un carbone a trois atomes d’hydrogène attachés, ce qu’on appelle un groupe méthyle (CH3).
« Les liaisons C-H primaires, celles sur un groupe méthyle à la fin d’une chaîne, sont les moins riches en électrons et les plus fortes », a-t-il dit. « Elles ont tendance à être les moins réactives des liaisons C-H. »
Le postdoctorant Raphael Oeschger de l’Université de Berkeley a découvert une nouvelle version d’un catalyseur basé sur le métal iridium qui ouvre l’une des trois liaisons C-H sur un groupe méthyle terminal et insère un composé de bore, qui peut être facilement remplacé par des groupes chimiques plus complexes. Le nouveau catalyseur était plus de 50 fois plus efficace que les catalyseurs précédents et tout aussi facile à travailler.
« Nous avons maintenant la capacité de faire ces types de réactions, ce qui devrait permettre aux gens de faire rapidement des molécules qu’ils n’auraient pas faites auparavant », a déclaré Hartwig. « Je ne dirais pas que ce sont des molécules qui n’auraient pas pu être fabriquées auparavant, mais les gens ne les feraient pas parce que cela prendrait trop de temps, trop de temps et d’efforts de recherche, pour les fabriquer. »
Les retombées pourraient être énormes. Chaque année, près d’un milliard de livres d’hydrocarbures sont utilisées par l’industrie pour fabriquer des solvants, des réfrigérants, des retardateurs de feu et d’autres produits chimiques et constituent le point de départ typique pour la synthèse de médicaments.
Une « chirurgie experte » sur les hydrocarbures
Pour prouver l’utilité de la réaction catalytique, le postdoctorant Bo Su de l’UC Berkeley et ses collègues du laboratoire l’ont utilisée pour ajouter un composé du bore, ou borane, à un atome de carbone terminal, ou primaire, dans 63 structures moléculaires différentes. Le borane peut ensuite être remplacé par un nombre quelconque de groupes chimiques. La réaction cible spécifiquement les liaisons C-H terminales, mais fonctionne sur d’autres liaisons C-H lorsqu’une molécule ne possède pas de C-H terminal.

John Hartwig dans son bureau de UC Berkeley. (Photo UC Berkeley avec l’aimable autorisation du Collège de chimie)
« Nous faisons une liaison carbone-bore en utilisant des boranes comme réactifs – ils sont à deux pas du poison pour fourmis, l’acide borique – et cette liaison carbone-bore peut être convertie en beaucoup de choses différentes », a déclaré Hartwig. « Classiquement, vous pouvez créer une liaison carbone-oxygène à partir de cette liaison, mais vous pouvez également créer une liaison carbone-azote, une liaison carbone-carbone, une liaison carbone-fluor ou d’autres liaisons carbone-halogène. Donc, une fois que vous faites cette liaison carbone-bore, il y a beaucoup de composés différents qui peuvent être faits. »
Le chimiste organique Varinder Aggarwal de l’Université de Bristol a qualifié la réaction catalytique de « chirurgie experte » et a caractérisé la nouvelle technique de l’UC Berkeley de « sophistiquée et intelligente », selon le magazine Chemical and Engineering News
Une application potentielle, a déclaré Hartwig, est la modification des composés naturels – des produits chimiques provenant de plantes ou d’animaux qui ont des propriétés utiles, comme l’activité antibiotique – pour les rendre meilleurs. De nombreuses sociétés pharmaceutiques se concentrent aujourd’hui sur les produits biologiques – des molécules organiques, telles que les protéines, utilisées comme médicaments – qui pourraient également être modifiées par cette réaction pour améliorer leur efficacité.
« Dans le cours normal des choses, il faudrait revenir en arrière et refaire toutes ces molécules depuis le début, mais cette réaction pourrait vous permettre de simplement les fabriquer directement », a déclaré Hartwig. « C’est un type de chimie qui vous permettrait de prendre ces structures complexes que la nature fabrique et qui ont une activité biologique inhérente et d’améliorer ou de modifier cette activité biologique en apportant de petits changements à la structure. »
Il a ajouté que les chimistes pourraient également ajouter de nouveaux groupes chimiques aux extrémités des molécules organiques pour les préparer à la polymérisation en longues chaînes jamais synthétisées auparavant.
« Cela pourrait vous permettre de prendre des molécules qui seraient naturellement abondantes, des molécules biosourcées comme les acides gras, et être en mesure de les dériver à l’autre extrémité à des fins de polymérisation », a-t-il déclaré.
La longue histoire de l’UC Berkeley avec les liaisons C-H
Les chimistes ont longtemps essayé de faire des ajouts ciblés aux liaisons carbone-hydrogène, une réaction appelée activation C-H. Un rêve encore inachevé est de convertir le méthane – un sous-produit abondant, mais souvent gaspillé, de l’extraction du pétrole et un puissant gaz à effet de serre – en un alcool appelé méthanol qui peut être utilisé comme point de départ dans de nombreuses synthèses chimiques dans l’industrie.

Robert Bergman, le professeur émérite Gerald E. K. Branch Distinguished Professor, émérite, au département de chimie.
En 1982, Robert Bergman, aujourd’hui professeur émérite de chimie à l’UC Berkeley, a montré pour la première fois qu’un atome d’iridium pouvait rompre une liaison C-H dans une molécule organique et s’insérer, avec un ligand attaché, entre le carbone et l’hydrogène. Bien qu’il s’agisse d’une avancée majeure en chimie organique et inorganique, la technique n’était pas pratique – il fallait un atome d’iridium par liaison C-H. Dix ans plus tard, d’autres chercheurs ont trouvé un moyen d’utiliser l’iridium et d’autres métaux dits de transition, comme le tungstène, comme catalyseur, où un seul atome pouvait briser et fonctionnaliser des millions de liaisons C-H.
Hartwig, qui était étudiant diplômé avec Bergman à la fin des années 1980, a continué à frapper sur les liaisons C-H non réactives et, en 2000, a publié un article dans Science décrivant comment utiliser un catalyseur à base de rhodium pour insérer du bore aux liaisons C-H terminales. Une fois le bore inséré, les chimistes pouvaient facilement le remplacer par d’autres composés. Grâce à des améliorations ultérieures de la réaction et au remplacement du rhodium par de l’iridium, certains fabricants ont utilisé cette réaction catalytique pour synthétiser des médicaments en modifiant différents types de liaisons C-H. Mais l’efficacité des réactions au niveau du méthylmercure n’a pas été démontrée. Mais l’efficacité pour les réactions aux liaisons C-H méthyliques aux extrémités des chaînes de carbone est restée faible, car la technique exigeait que les produits chimiques réactifs soient également le solvant.
Avec l’ajout de la nouvelle réaction catalytique, les chimistes peuvent maintenant coller des produits chimiques dans presque tous les types de liaison carbone-hydrogène. Dans la réaction, l’iridium coupe un atome d’hydrogène terminal, et le bore le remplace ; un autre composé du bore s’éloigne avec l’atome d’hydrogène libéré. L’équipe a attaché un nouveau ligand à l’iridium – un groupe méthyle appelé 2-méthylphénanthroline – qui a accéléré la réaction de 50 à 80 fois par rapport aux résultats précédents.
Hartwig reconnaît que ces expériences sont une première étape. Les réactions varient de 29% à 85% dans leur rendement du produit final. Mais il travaille à des améliorations.
« Pour nous, cela montre, oui, vous pouvez le faire, mais nous devrons fabriquer des catalyseurs encore meilleurs. Nous savons que le but ultime est atteignable si nous pouvons encore augmenter nos taux d’un facteur 10, disons. Ensuite, nous devrions être en mesure d’accroître la complexité des molécules pour cette réaction et d’obtenir des rendements plus élevés », a déclaré Hartwig. « C’est un peu comme un mile en quatre minutes. Une fois que vous savez que quelque chose peut être accompli, beaucoup de gens sont capables de le faire, et la prochaine chose que vous savez, nous courons un mile de trois minutes et quart. »
Les autres coauteurs de l’article sont Isaac Yu, un étudiant diplômé de première année ; l’ancien étudiant invité Christian Ehinger, maintenant à l’ETH Zürich, une université de recherche publique en Suisse ; le boursier postdoctoral Erik Romero et Sam He, étudiant de premier cycle.