La fibrillation auriculaire (FA) est la tachyarythmie soutenue la plus fréquente, survenant chez 1 à 2 % de la population générale. L’isolation de la veine pulmonaire (PVI) est le pilier de l’ablation de la FA.1 Bien que cette procédure soit efficace pour prévenir la récurrence de l’arythmie chez les patients souffrant de FA paroxystique, si elle est réalisée seule, elle n’a qu’un succès limité dans la FA persistante.1,2 Les données initiales suggéraient que la récurrence de l’arythmie pouvait être diminuée par une ablation supplémentaire de la ligne ou par une ablation complexe fractionnée de l’électrogramme auriculaire. Cependant, le bénéfice d’une ablation supplémentaire au-delà de la PVI n’a pas été confirmé par les résultats récents des méta-analyses3 et des essais contrôlés randomisés,4 soulignant l’importance d’une PVI durable, même dans la FA persistante.
Au cours des dernières années, l’ablation par cryoballon est devenue une approche alternative viable à l’ablation par radiofréquence (RF) et s’est avérée au moins aussi efficace que la PVI chez les patients atteints de FA paroxystique. Les résultats récents de l’essai FIRE & ICE ont définitivement tranché le débat dans ce domaine.5 De plus, en raison de la simplicité relative, de la courbe d’apprentissage plus rapide – et peut-être encore plus important – de la remarquable reproductibilité6 de cette procédure, elle a été largement adoptée dans la pratique clinique.6
En revanche, le traitement interventionnel de la FA persistante reste un défi : cette approche n’a pas été standardisée ou perfectionnée et il y a de la place pour l’innovation. Dans ce contexte, la question d’un rôle possible de la cryoablation est intéressante.
ÉVIDENCES CLINIQUES
Bien que l’efficacité de l’ablation de la FA chez les patients souffrant de FA persistante suscite un intérêt croissant, les données de suivi après l’utilisation du nouveau cathéter à cryoballon de 28 mm de deuxième génération (Arctic Front Advance, Medtronic Inc., Minneapolis, MN) sont encore limitées. Jusqu’à présent, les résultats de l’ablation par cryoballon dans la FA persistante ont été évalués indirectement par des méta-analyses, des comparaisons non randomisées7 et des études d’observation8-10
Ciconte et al.9 ont signalé que 60 % des patients souffrant de FA persistante n’avaient plus de tachyarythmie auriculaire après le traitement par le nouveau cathéter à cryoballon. La durée de la FA persistante, qui était un prédicteur indépendant de la récurrence de l’arythmie au cours du suivi, fournit un soutien clair pour l’ablation à des stades plus précoces de la maladie.
Dans une étude rétrospective de 48 patients atteints de FA persistante, le taux de succès clinique à 1 an était de 69%.10
Une autre étude à un seul bras a évalué l’efficacité de la cryoablation de deuxième génération dans un groupe de 100 patients souffrant de FA persistante en tant que procédure d’indexation (durée moyenne de 5,5 ± 3,7 mois).8 Après un suivi moyen de 10,6 ± 6,3 mois, aucune récurrence de tachyarythmie auriculaire n’a été observée chez 67 % des patients après une période de suppression de 3 mois. Le seul facteur prédictif indépendant significatif de récurrence était l’apparition d’une tachyarythmie auriculaire pendant la période de suppression.
Une étude monocentrique, non prospective et non randomisée a également évalué la RF en comparaison avec la cryoablation chez les patients souffrant de FA persistante uniquement.7 Dans cette étude, le résultat procédural de l’ablation par radiofréquence (à l’aide d’un cathéter d’ablation à force de contact) par rapport à la cryoablation (à l’aide d’un cryoballon de 28 mm de deuxième génération) a été évalué dans une cohorte de 100 patients souffrant de FA persistante réfractaire aux médicaments (la durée moyenne de la FA était de 7,2 et 7,6 mois, respectivement, dans les groupes d’ablation par radiofréquence et de cryoablation). Les temps de procédure et de fluoroscopie étaient significativement plus courts dans le groupe cryoablation, mais le taux de patients exempts d’arythmies auriculaires était similaire entre les deux groupes après 12 mois de suivi (60 % dans le groupe cryoablation contre 56 % dans le groupe ablation par radiofréquence, P = 0,71). Lors de l’analyse multivariée, les seuls facteurs prédictifs indépendants d’échec se sont avérés être la durée de la FA persistante et les récidives pendant la période de suppression.
Enfin, un essai prospectif, multicentrique et non randomisé a comparé les résultats après une seule procédure d’ablation, en utilisant l’ablation par cryoballon de première génération pour la PVI uniquement par rapport à l’ablation par radiofréquence à iris ouvert par une approche progressive dans une cohorte de patients appariés en fonction de la propension et présentant une FA persistante11. Les résultats, montrant une absence d’arythmies auriculaires d’environ 55 % au cours d’un suivi moyen de 15,6 ± 11,5 mois après une seule ablation, à la fois avec le cryoballon et la RF, étaient similaires aux données disponibles. Plusieurs résultats sont à noter :
- –
Premièrement, les résultats cliniques étaient similaires dans les 2 bras de traitement, même si le groupe RF a subi une ablation supplémentaire et plus étendue au-delà de la PVI.
- –
Deuxièmement, le taux de complications était similaire avec les 2 techniques.
- –
Troisièmement, la durée de la procédure était plus courte avec la cryoablation.
La physiopathologie et la stratégie optimale pour l’ablation de la FA persistante sont encore incertaines, et par conséquent, le pilier de cette thérapie reste l’obtention d’une PVI durable4. Pour y parvenir, la cryoablation semble être une approche thérapeutique alternative valable à la RF. Comme l’approche de l’ablation par radiofréquence n’a pas été normalisée (la plupart des patients du groupe RF ont développé des lésions supplémentaires), on ne sait pas si les résultats sont dus à la source d’énergie ou à la stratégie d’ablation. De plus, les résultats à moyen terme ne semblent pas être significativement améliorés par des lésions biatriales supplémentaires au-delà de la PVI chez les patients souffrant de FA persistante.4
TIRER SUR LA BONNE CIBLE ?
Les raisons de l’absence d’un bénéfice accru de l’ablation supplémentaire restent à élucider. Une possibilité est le potentiel iatrogène d’une approche de substrat avec une ablation plus étendue, qui peut favoriser le développement de nouvelles zones d’arythmogénèse en raison de tissus incomplètement ablatés ou de lignes incomplètes de bloc de conduction. Une autre possibilité est que la zone coupable ne soit pas systématiquement identifiée et que ni les électrogrammes auriculaires fractionnés complexes ni les lésions linéaires ne constituent des cibles complémentaires optimales pour l’ablation.12 Dans cette hypothèse, il reste nécessaire de localiser l’œil du cyclone (en ciblant les rotors ou les ganglions),13 éventuellement en utilisant de nouveaux algorithmes de cartographie. Les données disponibles appuient également le rôle de la durée de la FA et, par conséquent, du remodelage électrique de la FA (la FA engendre la FA), car seule la durée de la FA était un prédicteur indépendant de la récurrence de l’arythmie dans la comparaison par score de propension11, comme l’ont indiqué précédemment Tilz et al.2
Plusieurs essais en cours contribueront à élucider l’innocuité et l’efficacité de la cryoablation chez les patients atteints de FA persistante. L’essai Cryoballoon Ablation for Early Persistent Atrial Fibrillation (Cryo4 Persistent AF – NCT02213731) est une étude pilote européenne multicentrique, prospective, à un seul bras, visant à évaluer le taux de réussite de la PVI uniquement par cryoablation à un an chez les patients présentant une FA persistante depuis moins de 12 mois. Cet essai est encore en phase de recrutement et les premiers résultats sont attendus pour la fin 2017. L’objectif suivant sera de comparer les résultats dans une étude randomisée entre l’approche progressive par RF et la cryoablation par PVI dans un groupe homogène de patients présentant une FA persistante. Les résultats de cet essai randomisé à grande échelle sont attendus avec impatience.
ARGUMENTS ET LIMITES
Chez les patients atteints de FA persistante, même les diamètres PV maximaux les plus élevés (entre 20 mm et 23 mm) sont sensiblement inférieurs à la valeur critique de 28 mm (le diamètre maximal du cryoballon utilisé dans la pratique clinique courante).14 En raison de ce décalage entre les diamètres du ballon et des PV, lorsque ce dispositif est positionné contre l’antre du PV, sa partie réfrigérante est en contact à la fois avec l’antre du PV et le tissu auriculaire adjacent, ce qui semble être un avantage important de cette procédure. Kenigsberg et al,15 ont calculé la surface du tissu cardiaque ablaté après cryoablation du PV par cartographie électroanatomique tridimensionnelle du voltage de l’oreillette gauche après cryoablation. Grâce à cette méthode, ces auteurs ont joliment démontré qu’après cryoablation avec le dispositif de cryoballon de 28 mm, le pourcentage de la surface de la paroi postérieure de l’oreillette gauche qui restait électriquement intacte n’était que de 27 %.
À noter que, bien que le cryoballon ne cible conceptuellement que les PV, il effectue également un débulking électrique substantiel de la paroi postérieure de l’oreillette gauche (figure). En étendant la circonférence de la zone de refroidissement, ce dispositif peut conférer un avantage collatéral en effectuant l’ablation de contributeurs locaux aux structures qui contribuent au déclenchement et au maintien de la FA, comme les plexi et les rotors ganglionnaires, ce qui pourrait avoir des implications thérapeutiques majeures pour les patients atteints de FA persistante13. Cette caractéristique pourrait également expliquer, au moins partiellement, les résultats des essais susmentionnés.
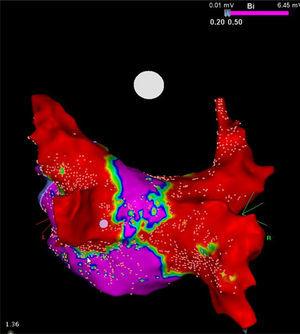
Carte de tension à haute densité de la paroi postérieure après une procédure de cryoablation chez un patient présentant une fibrillation auriculaire persistante. Notez le couloir étroit (violet) restant entre les deux grandes cicatrices (rouges) obtenues avec le cryoballon Artic Front Advance de 28 mm (Medtronic, Minneapolis, MN, États-Unis). Courtoisie du Prof. Mario Oliveira, Hôpital Santa Marta, Lisbonne, Portugal.
Bien que les taux de réussite du cryoballon soient comparables à ceux de la RF dans des études non randomisées de patients souffrant de FA persistante, le taux relativement élevé de récidive de l’arythmie dans les deux groupes reste inexpliqué et pourrait ne pas être uniquement attribuable à la récupération de la conduction des PV. Cette possibilité a été mentionnée dans des études soulevant des inquiétudes quant au rôle des sources non PV fournissant le mécanisme de la récidive.9
Dans la FA persistante, le traitement invasif reste difficile en raison de sa pathophysiologie diverse. De nouvelles connaissances mécanistiques sont nécessaires pour permettre une approche personnalisée de la FA persistante mais, jusqu’à ce que de telles connaissances soient disponibles, l’IPV autonome de première intention peut être suffisante, au moins pour les patients présentant une FA persistante moins sévère. Sur la base de cette approche » moins, c’est plus « , la PVI par cryoballon pourrait s’avérer être une stratégie d’ablation adéquate dans la FA persistante, permettant une PVI fiable avec un débulking complémentaire du myocarde auriculaire voisin. Une modification supplémentaire du substrat ne semble pas apporter de bénéfice supplémentaire. Cette procédure « minimaliste » est une première option acceptable chez les patients présentant des antécédents relativement récents de FA persistante symptomatique, c’est-à-dire avec « plus de déclencheur que de substrat » (ou avec un substrat concentré autour des ostia PVs…). En effet, le grand (28mm) cryoballon de deuxième génération fournit des résultats similaires à ceux de procédures plus complexes utilisant l’énergie RF et des méthodes sophistiquées. Il est à noter que la courbe d’apprentissage, la reproductibilité et la sécurité semblent être en faveur du dispositif de cryoballon dans des mains moins expérimentées. Dans ce contexte, et dans le sous-groupe de patients susmentionné, la PVI avec le grand cryoballon de deuxième génération semble être une approche initiale raisonnable, apportant une amélioration significative pour plus de la moitié des candidats. Pour les patients présentant des récidives de FA, cette première procédure ne sera pas inutile. En effet, dans une quantité considérable de substrat (entourant les antra PV droite et gauche) qui a déjà été traité, la seconde procédure, par RF cette fois, se concentrera principalement sur les foyers extra-PVs, les potentiels fragmentés, les circuits micro- ou macro-réentrants, etc.
À notre avis, cette stratégie en 2 étapes est compatible avec le déploiement de centres à faible ou moyen volume se concentrant principalement sur les PVIs, et travaillant main dans la main avec des centres de référence tertiaires réalisant les procédures plus complexes. Ces derniers devront faire face aux quelque 40% de patients présentant des récidives après le premier « cryo-débullage ».
« Less is more », mais encore, ce n’est pas suffisant…
CONFLITS D’INTÉRÊTS
S. Boveda reçoit des honoraires de consultant de Medtronic, Boston Scientific et Livanova.