Atrieflimren (AF) er den hyppigste vedvarende takyarytmi, der forekommer hos 1 % til 2 % af den almindelige befolkning. Pulmonalveneisolation (PVI) er hovedhjørnestenen i AF-ablation.1 Selv om denne procedure er effektiv til at forhindre recidiv af arytmi hos patienter med paroxysmal AF, har den, hvis den udføres alene, kun begrænset succes ved vedvarende AF.1,2 Indledende data antydede, at recidiv af arytmi kunne mindskes ved yderligere linieablation eller kompleks fraktioneret atrielektrogramablation. Fordelen ved yderligere ablation ud over PVI er imidlertid ikke blevet bekræftet af de seneste resultater af metaanalyser3 og randomiserede kontrollerede forsøg4 , hvilket understreger betydningen af varig PVI, selv ved vedvarende AF.
I løbet af de sidste par år er cryoballonablation blevet et levedygtigt alternativ til radiofrekvens (RF)-ablation og har vist sig at være mindst lige så effektiv som PVI hos patienter med paroxysmal AF. De nylige resultater af FIRE & ICE-forsøget har definitivt afgjort debatten på dette område.5 På grund af den relative enkelhed, den hurtigere indlæringskurve – og måske endnu vigtigere – den bemærkelsesværdige reproducerbarhed6 af denne procedure er den desuden blevet bredt anvendt i klinisk praksis.6
På den anden side er interventionsbehandlingen af vedvarende AF fortsat en udfordring: denne fremgangsmåde er ikke blevet standardiseret eller perfektioneret, og der er plads til innovation. I denne sammenhæng er spørgsmålet om en mulig rolle for cryoablation interessant.
KLINISK EVIDENS
Selv om der er stigende interesse for effektiviteten af AF-ablation hos patienter med vedvarende AF, er opfølgningsdata efter anvendelse af det nye 28 mm andengenerations cryoballonkateter af anden generation (Arctic Front Advance, Medtronic Inc., Minneapolis, MN) stadig begrænset. Hidtil er resultaterne af postkryoballonablation ved vedvarende AF blevet vurderet indirekte ved metaanalyser, ikke-randomiserede sammenligninger7 og observationsstudier.8-10
Ciconte et al.9 rapporterede, at 60 % af patienterne med vedvarende AF var fri for atrietisk takyarytmi efter behandling med det nye cryoballon-kateter. Varigheden af persisterende AF, som var en uafhængig prædiktor for arytmierecidiv under opfølgningen, giver klar støtte til ablation i tidligere stadier af sygdommen.
I en retrospektiv undersøgelse af 48 patienter med persisterende AF var den kliniske succesrate efter 1 år 69 %.10
En anden enarmet undersøgelse vurderede effektiviteten af andengenerations-kryoablation i en gruppe på 100 persisterende AF-patienter som en indeksprocedure (gennemsnitlig varighed 5,5 ± 3,7 måneder).8 Efter en gennemsnitlig opfølgning på 10,6 ± 6,3 måneder var der ingen recidiv af atriel takyarytmi hos 67 % af patienterne efter en 3-måneders blanking-periode. Den eneste signifikante uafhængige prædiktor for recidiv var forekomsten af atriel takyarytmi i løbet af blankingperioden.
Et enkeltcenter, ikke-prospektivt, ikke-randomiseret studie evaluerede også RF i sammenligning med kryoablation udelukkende hos persisterende AF-patienter.7 I denne undersøgelse blev det proceduremæssige resultat af RF-ablation (ved hjælp af et kontaktkraft-ablationskateter) sammenlignet med kryoablation (ved hjælp af 28 mm andengenerations-kryoballon) evalueret i en kohorte på 100 patienter med lægemiddelrefraktær vedvarende AF (den gennemsnitlige varighed af AF var henholdsvis 7,2 og 7,6 måneder i RF-ablations- og kryoablationsgrupperne). Både procedure- og fluoroskopitider var signifikant kortere i kryoablationsgruppen, men andelen af patienter uden atrielle arytmier var ens mellem de 2 grupper efter 12 måneders opfølgning (60 % i kryoablations- mod 56 % i RF-ablationsgrupper, P = .71). Ved multivariat analyse blev de eneste uafhængige prædiktorer for fiasko igen fundet at være varigheden af persisterende AF og recidiv i løbet af blankingperioden.
Finalt sammenlignede et prospektivt, multicenter, ikke-randomiseret forsøg resultaterne efter en enkelt ablationsprocedure ved hjælp af første generations kryoballonablation kun til PVI vs. åbenirrigeret RF-ablation gennem en trinvis tilgang i en kohorte af propensitetsmatchede patienter med persisterende AF.11 Resultaterne, der viste ca. 55 % frihed fra atrielle arytmier i løbet af en gennemsnitlig opfølgning på 15,6 ± 11,5 måneder efter en enkelt ablation, både med kryoballon og RF, svarede til de tilgængelige data. Flere resultater var bemærkelsesværdige:
- –
For det første var de kliniske resultater ens i de 2 behandlingsarme, selv om RF-gruppen gennemgik yderligere og mere omfattende ablation ud over PVI.
- –
For det andet var komplikationsraten ens med de 2 teknikker.
- –
For det tredje var procedurens varighed kortere med kryoablation.
Der er stadig usikkerhed om patofysiologien og den optimale strategi for vedvarende AF-ablation, og derfor er hovedhjørnestenen i denne behandling fortsat opnåelse af en varig PVI.4 For at opnå dette synes kryoablation at være et gyldigt alternativ til RF som behandlingsmetode. Udførelse af yderligere ablation oven på PVI er forbundet med længere proceduretid.4 Da RF-ablationstilgangen ikke er blevet standardiseret (de fleste patienter i RF-armen udviklede yderligere læsioner), er det uklart, om resultaterne skyldes energikilden eller ablationsstrategien. Desuden synes resultaterne på mellemlang sigt ikke at være signifikant forbedrede ved yderligere biatriale læsioner ud over PVI hos persisterende AF-patienter.4
SHOOTING AT THE RIGHT TARGET?
Der mangler stadig at blive belyst, hvorfor der ikke er en øget fordel ved yderligere ablation. En mulighed er det iatrogene potentiale ved en substrattilgang med mere omfattende ablation, som kan fremme udviklingen af nye områder med arytmogenese på grund af ufuldstændigt ableret væv eller ufuldstændige linjer af ledningsblokering. En anden mulighed er, at det skyldige område ikke rutinemæssigt identificeres, og at hverken komplekse fraktionerede atrielle elektrogrammer eller lineære læsioner er de optimale komplementære mål for ablation.12 I denne hypotese er der fortsat behov for at lokalisere stormens øje (ved at målrette mod rotorer eller ganglier)13 , eventuelt ved hjælp af nyere kortlægningsalgoritmer. De foreliggende data giver også støtte til den rolle, som AF-varighed og dermed elektrisk AF-remodellering (AF avler AF) spiller, fordi kun AF-varighed var en uafhængig prædiktor for arytmierecidiv i propensity-score-sammenligningen,11 som tidligere rapporteret af Tilz et al.2
Flere igangværende forsøg vil bidrage til at belyse sikkerheden og virkningen af kryoablation hos vedvarende AF-patienter. Cryoballoon Ablation for Early Persistent Atrial Fibrillation trial (Cryo4 Persistent AF – NCT02213731) er en europæisk multicenter, prospektiv, enarmet pilotundersøgelse, der har til formål at evaluere succesraten for PVI udelukkende ved hjælp af cryoablation efter 1 år hos patienter med en mindre end 12 måneders historie med vedvarende AF. Dette forsøg er stadig i rekrutteringsfasen, og de første resultater forventes at foreligge i slutningen af 2017. Det næste mål vil være at sammenligne resultaterne i en randomiseret undersøgelse mellem den trinvise RF-tilgang og PVI-kryoablation i en homogen gruppe af patienter med vedvarende AF. Resultaterne af dette storstilede randomiserede forsøg forventes med spænding.
STYRKER OG BEGRÆNSNINGER
I persisterende AF-patienter er selv de højeste maksimale PV-diametre (mellem 20 mm og 23 mm) væsentligt lavere end den kritiske værdi på 28 mm (den maksimale diameter af den cryoballon, der anvendes i klinisk rutinepraksis).14 På grund af denne uoverensstemmelse mellem ballonens og PV’ernes diametre, når denne anordning placeres mod PV-antrummet, er dens kølende del i kontakt med både PV-antrummet og det tilstødende atriale væv, hvilket synes at være en vigtig fordel ved denne procedure. Kenigsberg et al.15 beregnede arealet af det ablerede hjertevæv efter PV-kryoablation ved hjælp af 3-dimensionel elektroanatomisk spændingskortlægning af venstre atrium efter kryoablation. Ved hjælp af denne metode påviste disse forfattere flot, at efter kryoablation med 28 mm cryoballon-enheden var procentdelen af venstre atriums bagvægsoverflade, der forblev elektrisk intakt, kun 27 %.
Det skal bemærkes, at selv om cryoballonen konceptuelt set kun er rettet mod PV’erne, udfører den også en betydelig elektrisk debulking af venstre atriums bagvæg (Figur). Ved at udvide omkredsen af køleområdet kan denne anordning give en kollateral fordel ved at ablede lokale bidragydere til strukturer, der bidrager til at udløse og opretholde AF, såsom ganglionære plexi og rotorer, hvilket muligvis har store terapeutiske implikationer for patienter med vedvarende AF.13 Denne funktion kunne også, i det mindste delvist, forklare resultaterne af de ovennævnte forsøg.
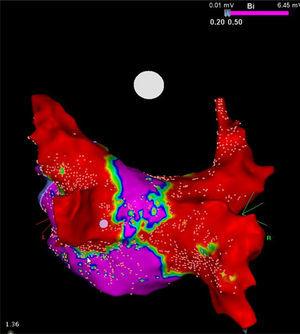
Spændingskort med høj tæthedsgrad af den bageste væg efter en kryoablationsprocedure hos en patient med vedvarende atrieflimren. Bemærk den smalle korridor (lilla), der er tilbage mellem de to store ar (røde), der er opnået med 28 mm Artic Front Advance-kryoballonen (Medtronic, Minneapolis, MN, USA). Med venlig hilsen af Prof. Mario Oliveira, Santa Marta Hospital, Lissabon, Portugal.
Og selv om cryoballon-succesraten er sammenlignelig med RF-succesraten i ikke-randomiserede undersøgelser af patienter med vedvarende AF, er den relativt høje arytmi-recidivrate i begge grupper fortsat uforklarlig og kan muligvis ikke kun tilskrives ledningsgenopretning af PV’erne. Denne mulighed er blevet nævnt i undersøgelser, der giver anledning til bekymring om den rolle, som ikke-PVI-kilder spiller som mekanisme for tilbagefald.9
I persisterende AF er invasiv behandling fortsat en udfordring på grund af dens forskelligartede patofysiologi. Der er behov for ny mekanistisk indsigt for at muliggøre en individuelt skræddersyet tilgang til vedvarende AF, men indtil en sådan viden bliver tilgængelig, kan det være tilstrækkeligt med en standalone PVI i første omgang, i det mindste for patienter med mindre alvorlig vedvarende AF. Baseret på denne “mindre er mere”-tilgang kan cryoballon PVI vise sig at være en passende ablationsstrategi ved vedvarende AF, der muliggør pålidelig PVI med supplerende debulking af det tilstødende atriale myokardie. Yderligere substratmodifikation synes ikke at give ekstra fordele. Denne “minimalistiske” procedure er en acceptabel første mulighed hos patienter med en relativt nyere historie med symptomatisk vedvarende AF, dvs. med “mere trigger end substrat” (eller med et substrat koncentreret omkring PV-ostierne …). Den store (28 mm) andengenerations-kryoballon af anden generation giver faktisk lignende resultater som mere komplekse procedurer, der anvender RF-energi og sofistikerede metoder. Det skal bemærkes, at indlæringskurven, reproducerbarheden og sikkerheden synes at være til fordel for kryoballonanordningen i mindre erfarne hænder. I disse omgivelser og i den ovennævnte patientundergruppe synes PVI med den store andengenerations-kryoballon at være en fornuftig indledende metode, der giver en betydelig forbedring for mere end halvdelen af kandidaterne. For patienter med AF-recidiv vil denne første procedure ikke være ubrugelig. I en betydelig mængde substrat (omkring højre og venstre PV antra), der allerede er blevet behandlet, vil den anden procedure, denne gang med RF, nemlig primært fokusere på ekstra PV-foki, fragmenterede potentialer, mikro- eller makrorentrantkredsløb osv.
Denne totrinsstrategi er efter vores mening forenelig med indsættelsen af centre med lav til mellemstor volumen, der primært fokuserer på PVI, og som arbejder hånd i hånd med tertiære henvisningscentre, der udfører de mere komplekse procedurer. Sidstnævnte vil skulle tage sig af de ca. 40 % af patienterne, der har recidiv efter den første “cryo-debulking”.
“Less is more”, men det er stadig ikke nok…
INTERESSEKONFLIKTER
S. Boveda modtager konsulenthonorarer fra Medtronic, Boston Scientific og Livanova.