Knogler er en specialiseret type bindevæv. Det har et unikt histologisk udseende, som gør det muligt for det at udføre sine mange funktioner:
- Hæmatopoiese – dannelse af blodceller fra hæmatopoietiske stamceller, der findes i knoglemarven.
- Lipid- og mineralopbevaring – knogle er et reservoir, der indeholder fedtvæv i knoglemarven og kalcium i hydroxyapatitkrystallerne.
- Støtte – knogler danner kroppens ramme og form.
- Beskyttelse – især det aksiale skelet, som omgiver kroppens vigtigste organer.
I denne artikel skal vi se på knoglens ultrastruktur – dens bestanddele, struktur og udvikling. Vi skal også se på, hvordan sygdom kan påvirke dens struktur.
Knoglens bestanddele
Knoglen er en specialiseret form for bindevæv. Som ethvert andet bindevæv kan dets komponenter opdeles i cellulære komponenter og den ekstracellulære matrix.
Cellulære komponenter
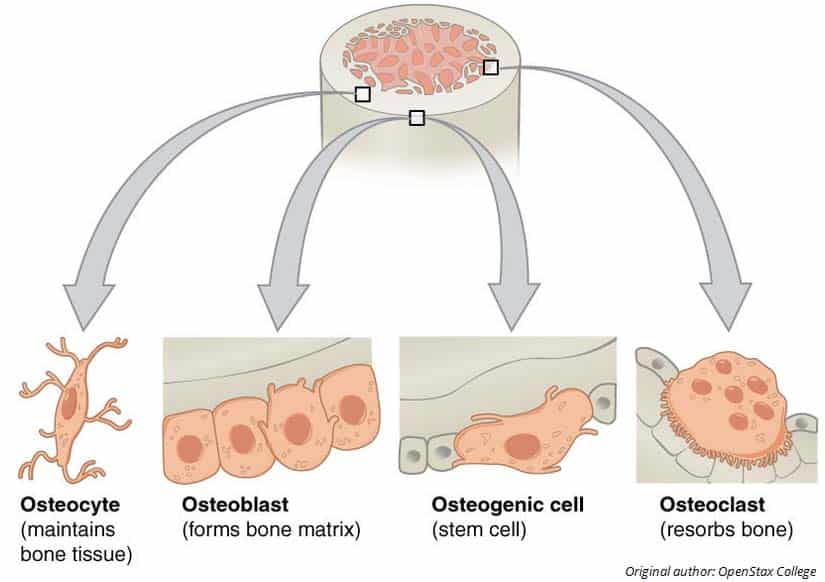 Fig 1.0 – Knoglens cellulære komponenter og deres funktioner.
Fig 1.0 – Knoglens cellulære komponenter og deres funktioner.Der er tre typer celler i knoglen:
- Osteoblaster – Syntese af ukalket/umineraliseret ekstracellulær matrix kaldet osteoid. Dette bliver senere kalcificeret/mineraliseret og danner knogle.
- Osteocytter – Efterhånden som osteoidet mineraliseres, bliver osteoblasterne indlejret mellem lamellerne i lacunae, hvor de modnes til osteocytter. De overvåger derefter mineraler og proteiner for at regulere knoglemassen.
- Osteoklaster – Stammer fra monocytter og resorberer knogle ved at frigive H+-ioner og lysosomale enzymer. De er store og flerkernede celler.
Balancen mellem osteoblast- og osteoklastaktivitet er afgørende for opretholdelsen af vævets strukturelle integritet. Den spiller også en rolle ved tilstande som osteoporose.
Extracellulær matrix
Den ekstracellulære matrix (ECM) henviser til de molekyler, der yder biokemisk og strukturel støtte til cellerne.
Knoglens ECM er højt specialiseret. Ud over kollagen og de tilknyttede proteiner, der normalt findes i bindevæv, er knoglen imprægneret med mineralsalte, især calciumhydroxyapatitkrystaller. Disse krystaller forbinder sig med kollagenfibrene og gør knoglen hård og stærk. Denne matrix er organiseret i talrige tynde lag, kaldet lameller.
Knoglens struktur
Under mikroskopet kan knogle opdeles i to typer:
- Vævet knogle (primær knogle) – Optræder i embryonal udvikling og ved reparation af brud, da den hurtigt kan lægges op. Den består af osteoid (umineraliseret ECM), hvor kollagenfibrene er anbragt tilfældigt. Det er en midlertidig struktur, som hurtigt erstattes af moden lamelknogle.
- Lamelknogle (sekundær knogle) – Knoglen i det voksne skelet. Den består af stærkt organiserede plader af mineraliseret osteoid. Denne organiserede struktur gør den meget stærkere end vævet knogle. Selve lamelknoglen kan opdeles i to typer – kompakt og svampet.
I begge typer knogle er den ydre overflade dækket af et lag bindevæv, kendt som periost. Et lignende lag, endosteum, beklæder hulrummene i knoglen (såsom marvkanalen, Volkmanns kanal og svampede knoglerum).
Lamellær knogle kan opdeles i to typer. Den yderste er kendt som kompakt knogle – denne er tæt og stiv. De indre lag af knogle er præget af mange indbyrdes forbundne hulrum og kaldes svampet knogle.
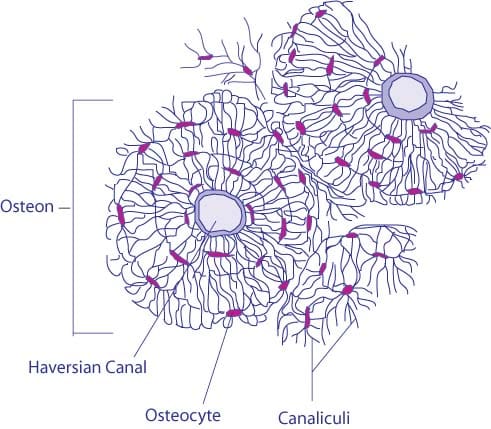 Fig 1.1 – Mikroskopisk billede af kompakt knogle. Bemærk arrangementet omkring en enkelt haversiansk kanal.
Fig 1.1 – Mikroskopisk billede af kompakt knogle. Bemærk arrangementet omkring en enkelt haversiansk kanal.Kompakt knogle
Kompakt knogle danner den ydre “skal” af knogle. I denne type knogle er lamellerne organiseret i koncentriske cirkler, som omgiver en lodret Haversian-kanal (som leder små neurovaskulære og lymfekarrene videre). Hele denne struktur kaldes en osteon og er knoglens funktionelle enhed.
De haversianske kanaler er forbundet af vandrette Volkmann-kanaler – disse indeholder små kar, der anastomoserer (slutter sig til) med arterierne i de haversianske kanaler. Volkmanns kanalerne sender også blodkar fra periostet.
Osteocytter er placeret mellem lamellerne, i små hulrum (kendt som lacunae). Lakunaerne er forbundet med hinanden af en række indbyrdes forbundne tunneller, kaldet canaliculi.
Svampet knogle
Svampet knogle udgør det indre af de fleste knogler og er placeret dybt inde i den kompakte knogle. Den indeholder mange store rum – det giver den et honeycombed-udseende.
Knoglematrixen består af et 3D-netværk af fine søjler, som krydsforbindes til uregelmæssige trabekler. Dette giver en let, porøs knogle, der er stærk over for multidirektionelle kraftlinjer. Den lethed, som den svampede knogle har, er afgørende for, at kroppen kan bevæge sig. Hvis den eneste type knogle var kompakt, ville de være for tunge til at kunne mobiliseres.
Rummene mellem trabeklerne er ofte fyldt med knoglemarv. Gul knoglemarv indeholder adipocytter, og rød knoglemarv består af hæmatopoietiske stamceller.
Denne type knogle indeholder ingen Volkmann- eller Haversian-kanaler.
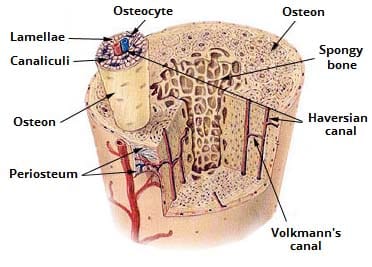 Fig 1.2 – Strukturen af moden knogle. Bemærk den forskellige struktur af kompakte og svampede knogletyper.
Fig 1.2 – Strukturen af moden knogle. Bemærk den forskellige struktur af kompakte og svampede knogletyper.Ossifikation og remodellering
Ossifikation er den proces, hvor der dannes ny knogle. Den sker via en af to mekanismer:
- Endokondral ossifikation – Hvor hyalinbrusk erstattes af osteoblaster, der udskiller osteoid. Lårbenet er et eksempel på en knogle, der gennemgår endochondral ossifikation.
- Intramembranøs ossifikation – Hvor mesenkymalt (embryonalt) væv kondenseres til knogle. Denne type ossifikation danner flade knogler som f.eks. tindingebenet og skulderbladet.
I begge mekanismer dannes der i første omgang primær knogle. Det erstattes senere af moden sekundær knogle.
Remodellering
Knoglen er et levende væv og undergår som sådan konstant en remodellering. Det er den proces, hvorved modent knoglevæv reabsorberes, og der dannes nyt knoglevæv. Den udføres af knoglens cellulære komponent.
Osteoklaster nedbryder knogle via en skærekegle. Næringsstofferne reabsorberes, og osteoblaster lægger nyt osteoid ned. Remodellering sker primært på steder med stress og skader, hvilket styrker de berørte områder.
Klinisk relevans – sygdomme i knoglen
Knoglen har en unik histologisk struktur, som er nødvendig for, at den kan udføre sine funktioner. Ændringer i denne struktur, sekundært til sygdom, kan give anledning til flere kliniske tilstande.
Osteogenesis imperfecta er en tilstand, hvor der er unormal syntese af kollagen fra osteoblasterne. De kliniske træk omfatter skrøbelige knogler, knogledeformiteter og blå sclera. Det er en sjælden sygdom, der er genetisk betinget og har et autosomalt dominerende arveligt mønster. Knoglernes skrøbelighed prædisponerer dem for brud – dette har en medicolegal betydning, da det hos børn kan forveksles med forsætlig skade.
Osteoporose henviser til et fald i knogletætheden, hvilket reducerer dens strukturelle integritet. Dette skyldes, at osteoklastaktiviteten (knogleoptagelse) opvejer osteoblastaktiviteten (knogleproduktion). Knoglerne er skrøbelige og har en øget risiko for brud. Der findes tre typer:
- Type 1: Postmenopausal osteoporose – Udvikles hos kvinder efter overgangsalderen på grund af nedsat østrogenproduktion. Østrogen beskytter mod osteoporose ved at øge osteoblasternes aktivitet og mindske osteoklasternes aktivitet.
- Type 2: Senil osteoporose – Opstår som regel over 70 år.
- Type 3: Sekundær osteoporose – Hvor osteoporose opstår på grund af en samtidig eksisterende sygdom (f.eks. kronisk nyresvigt).
Risikofaktorer omfatter alder, køn, kost (D-vitamin og calcium), etnicitet, rygning og immobilitet. Den behandles normalt med bisfosfonater, som optages af osteoklaster, hvilket får dem til at blive inaktive og undergå apoptose. Dette begrænser yderligere nedbrydning af knoglen.
 Fig 1.3 – Røntgenbillede af et barn, der er ramt af rakitis.
Fig 1.3 – Røntgenbillede af et barn, der er ramt af rakitis.Rrakitis er D-vitamin- eller calciummangel hos børn med knogler i vækst. Det betyder, at osteoidet mineraliseres dårligt og forbliver bøjeligt. De epifyseale vækstplader kan derefter blive forvredet under kroppens vægt, hvilket potentielt kan føre til skeletdeformiteter.
Osteomalaci er D-vitamin- eller calciummangel hos voksne med knogler under remodellering. Her er det osteoid, som osteoblasterne lægger ned, dårligt mineraliseret, hvilket fører til stadig svagere knogler og øger deres modtagelighed for brud.
OBS: D-vitaminmangel kan skyldes dårlig kost, mangel på sollys eller en stofskiftesygdom. For eksempel kan nyresvigt forstyrre den anden hydroxylering af D-vitamin, eller en tarmsygdom kan forhindre tilstrækkelig optagelse. En calciummangel kan skyldes kost eller lavt vit. D.