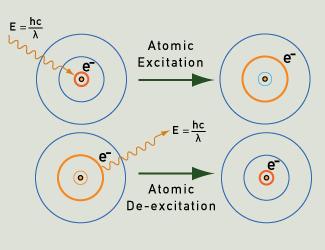
Lysfotonerne udsendes, når en elektron falder tilbage til sin grundtilstand efter at være blevet exciteret.
Flammeprøver
Flammeprøver er nyttige, fordi gas excitationer producerer et signaturlinjens emissionsspektrum for et grundstof. Til sammenligning producerer glødning et kontinuerligt lysbånd med en top, der afhænger af det varme objekts temperatur.
Når atomerne i en gas eller damp bliver exciteret, f.eks. ved opvarmning eller ved påføring af et elektrisk felt, kan deres elektroner bevæge sig fra deres grundtilstand til højere energiniveauer. Når de vender tilbage til deres grundtilstand, idet de følger klart definerede baner i henhold til kvantesandsynligheder, udsender de fotoner med en meget specifik energi. Denne energi svarer til bestemte bølgelængder af lys og frembringer således bestemte farver af lys. Hvert grundstof har et “fingeraftryk” i form af dets linjeemissionsspektrum, som illustreret af nedenstående eksempler.

Linjespektrum for brint.

Linjespektrum for helium.

Linjespektrum for neon.
Da hvert grundstof har et nøjagtigt defineret linjeemissionsspektrum, er forskerne i stand til at identificere dem ved den farve af flammen, de producerer. For eksempel producerer kobber en blå flamme, lithium og strontium en rød flamme, calcium en orange flamme, natrium en gul flamme og barium en grøn flamme.

Dette billede illustrerer de særprægede farver, der produceres ved forbrænding af bestemte grundstoffer.

En flamme fra en oxyacetylenbrænder brænder ved over 3000?C, varm nok til at blive brugt til svejsning under vandet.
Flame
Farven fortæller os om temperaturen i en stearinlysflamme. Den indre kerne af stearinlysflammen er lyseblå med en temperatur på ca. 1670 K (1400 °C). Det er den varmeste del af flammen. Farven inde i flammen bliver gul, orange og til sidst rød. Jo længere man kommer fra flammens centrum, jo lavere bliver temperaturen. Den røde del ligger omkring 1070 K (800 °C).
Den orange, gule og røde farve i en flamme har ikke kun noget med farvetemperaturen at gøre. Gasudladninger spiller også en stor rolle for flammens farve. En af de vigtigste bestanddele i en brændende flamme er sod, som har en kompleks og forskelligartet sammensætning af kulstofforbindelser. Variationen af disse forbindelser skaber et praktisk talt kontinuerligt udvalg af mulige kvantetilstande, som elektroner kan blive exciteret til. Farven på det lys, der udsendes, afhænger af den energi, der udsendes af hver elektron, som vender tilbage til sin oprindelige tilstand.