Interaktioner mellem hjernen og koagulationsprocessen har en lang historie, herunder den observation, at koagulationsmekanismen i centralnervesystemet har en række forskelle fra den, der findes i andre organer – hjernens endothelium udtrykker f.eks. lidt thrombomodulin.
Hvad end mekanismen er, er det svært at undgå den observation, at behandling med antikoagulation (f.eks, med lavmolekylær heparin) ofte dramatisk vender symptomerne, herunder migræne, hukommelsesvanskeligheder og chorea. Sådanne observationer tyder på, at hjernepatologien i mange tilfælde måske ikke så meget er et infarkt, men måske mere relaterer sig til “slamdannelse” af blodforsyningen og nedsat iltning.”
Migræne & Slagtilfælde
“Lider du af hovedpine som teenager?”
“Ja, doktor. De var næsten ugentlige i en periode. De forsvandt i et par år, men de kom tilbage med voldsomhed nu. De findes i min familie.”
Sådan taler den 30-årige kvindelige patient med APS (de mandlige medlemmer af familien optræder sjældnere på APS-klinikkerne).
Det er et så vigtigt diagnostisk spor i vurderingen af en patient med mulig APS. Men på trods af mange års erfaring med APS er der overraskende få data, der vurderer den egentlige rolle af APS i den bredere verden af migræne. Der er så mange grunde til at undersøge forbindelsen – svaret på antikoagulation – som regel godt, ofte slående – undersøgelsen af søskende og andre familiemedlemmer til migræne/APS-patienter. Og frem for alt de forbindelser, der nu rapporteres om mellem migræne og slagtilfælde.
APS/Hughes syndrom er i høj grad en neurologisk tilstand. Hjernefunktionen synes at være særligt ramt – jo flere APS-patienter man ser, jo bredere & bredere spreder de neuro-psykiatriske krusninger sig.
Lige med migræne er slagtilfælde en af de anerkendte komplikationer ved APS/Hughes syndrom. Der er rapporteret tal så højt som 1 ud af 5 unge slagtilfælde (under 45 år), der har positive aPL-tests.14-19
Men ligesom med migræne er anerkendelsen af aPL i forbindelse med ætiologien af slagtilfælde generelt stadig ringe. For eksempel er slagtilfælde i barndommen – som er velkendt klinisk – et oplagt mål for aPL-undersøgelser.
For nogle år siden lancerede den britiske regering et stort slagtilfælde-initiativ, hvor offentligheden blev oplyst om symptomer, tegn og behandling af slagtilfælde. Antifosfolipidsyndromet var ikke på listen.
Krampeanfald
I 1985 observerede vi, at hos lupuspatienter var anfald mere almindelige hos de patienter, der havde positive aPL-tests.20 Siden da er det blevet klart, at epilepsi i alle dens former er en vigtig ledsager af APS. Så meget, at i en undersøgelse af idiopatisk epilepsi hos teenagere viste det sig, at 1 ud af 5 var aPL-positiv.21

Den indledende screening hos jordemoderen eller fødselslægen bør omfatte et simpelt spørgeskema for at udelukke APS.
Image Credit: SPL/Science Source
Forgreningerne af disse observationer er mange. Lad mig give to kliniske eksempler:
For det første kan temporallappeepilepsi i APS være underkendt. En af mine patienter, en kvinde med klassisk APS, blev EEG-tekniker. Under sin uddannelse brugte hun fire af sine søskende som forsøgskaniner. Tre havde unormal aktivitet i temporallappen. Det er interessant at se, hvor ofte en familiehistorie om epilepsi dukker op i anamneseoptagelsen hos patienter med APS.
Den anden kliniske anekdote er blevet offentliggjort andetsteds.22 En 42-årig patient havde en fortid med mild lupus. Hendes største problem – og et problem med en betydelig indvirkning på hendes travle liv – var imidlertid tilbagevendende anfald, både petit mal og grand mal, hvor sidstnævnte krævede specialistbehandling og en kombination af en række antiepileptika. Under sit ophold i London udviklede hun en DVT (det blev konstateret, at hun var aPL-positiv), og der blev indledt rutinemæssig antikoagulation med warfarin. En øjeblikkelig og uventet bonus var en markant reduktion af anfaldsfrekvensen og sværhedsgraden, hvilket krævede langt mindre aggressiv antiepileptisk behandling.
‘THE STILLBIRTH SCANDAL: Hver dag fødes op til tre børn i Det Forenede Kongerige dødfødt, som kunne have levet. En ud af 200 fødsler hos britiske kvinder vil være dødfødt. Det er på tide, at NHS tilpasser nye politikker og en ny holdning. -The Times (London), 28. november 2012
Hukommelsestab
Den mest almindelige manifestation af APS er muligvis hukommelsestab. Ofte ser problemet først dagens lys, når patienten bliver spurgt om symptomet. Så mange patienter tilstår, at de er bekymrede for Alzheimers sygdom. Indtil nu er der kun få detaljerede kliniske undersøgelser. Fra tid til anden og, det skal siges, på en ret desultant måde, har vi udført psykometriske test på udvalgte APS-patienter – og resultaterne har ofte været overraskende. Endnu mere i betragtning af den markante forbedring, der ses i hukommelsestests, når antikoagulationen påbegyndes.23
Multipel sklerose
I betragtning af de fremtrædende neurologiske træk, herunder synsforstyrrelser og fluktuerende myelopati, der ses ved APS, er det ikke overraskende, at et antal tilfælde diagnosticeres som MS.24,25
Området er langt fra ligetil. Nogle inden for neurologien erklærer, at positive aPL-tests faktisk nogle gange ses ved klassisk MS. Jeg vil foretrække at vende billedet om. Sådanne patienter, i hvert fald nogle af dem, kan være APS først og MS dernæst. Selv om en række af disse tilfælde anekdotisk set reagerer på antikoagulation, er svaret i andre tilfælde i bedste fald grænseoverskridende. Uthman har for nylig gennemgået den ret omfattende litteratur om APS vs. MS.26
Andre neurologiske træk
Disse omfatter balanceproblemer (en række tilfælde præsenterer sig som Menières), chorea (undertiden alvorlig),27,28 anosmi, søvnforstyrrelser (herunder katapleksi og narkolepsi) og for nylig autonome forstyrrelser med en række tilfælde af POTS (posturalt ortostatisk takykardiesyndrom).29
Et af de spørgsmål, som der er debat om, er prævalensen af psykiatriske manifestationer.
Det har været min opfattelse, at akut psykose har været mere et træk ved lupus end ved APS, men her kan jeg tage fejl. En af mine patienter, en kvinde med APS og OCD (obsessiv kompulsiv lidelse), fik det bedre med antikoagulationsbehandling. Interessant nok fandt hendes teenagesøn, også en patient med OCD (og aPL-positiv), at de neuropsykiatriske manifestationer var langt mindre fremtrædende, da aspirinbehandlingen blev påbegyndt.
Not the Brain
Bone & joints-Have you suffered any fractures? Et spørgsmål, der måske ikke er en del af den rutinemæssige anamneseoptagelse hos APS-patienter. Og alligevel er spontane knoglefrakturer ved at blive velkendt efter rapporten om 27 spontane metatarsalfrakturer af Dr. Shirish Sangle hos APS-patienter.30
Anekdotiske rapporter tyder på, at (iskæmiske) knoglefrakturer kan være en vigtig manifestation af sygdommen: Min kollega, professor Munther Khamashta, har en patient med Hughes-syndrom med normale DEXA- og parathyreoidea-undersøgelser, som har haft 57 spontane frakturer. Det er klart, at dette er et vigtigt område for klinisk forskning.
Ligevel er avaskulær nekrose (AVN) hoftesmerter ikke ualmindeligt hos vores APS-patienter. MRI har vist tidlig AVN i nogle tilfælde uden andre risikofaktorer, såsom steroider, i nogle tilfælde uden andre risikofaktorer. Mit kliniske indtryk er, at hoftesmerterne ofte forbedres, når der startes med heparin eller warfarin.
Hjerte – en stor bekymring er tilstedeværelsen af angina pectoris og andre hjertesymptomer ved APS. På trods af nogle få tidlige rapporter om myokardieiskæmi og koronar trombose er det først i de senere år, at publikationer, der afslører en høj frekvens af disse komplikationer, er blevet hyppigere.
To eksempler er Greco et al’s forskning, der viser en relativt høj prævalens af positive aPL-tests hos patienter med hjerteiskæmi, og den slående observation, at kvindelige rygere på p-piller, der var aPL-positive, havde en relativ risiko på 22 gange for udvikling af myokardieinfarkt.31,32
De kardiale forbindelser øges af rapporteringen om en sammenhæng med kardialt syndrom X, angina pectoris med normale koronarangiografier.33 Det er et rimeligt bud, at aPL-testning vil blive en standard i den kardiologiske klinik, især hos symptomatiske kvinder under 40 år.
Som migræne er slagtilfælde en af de anerkendte komplikationer ved APS/Hughes syndrom. Der er rapporteret tal så høje som 1 ud af 5 unge slagtilfælde (under 45 år), der har positive aPL-tests.
GI-trakt & lever-Siden vi har gjort vores observationer om fokale stenotiske læsioner i forskellige arterier, herunder arterier celiacus og mesenteriale arterier, har vi fokuseret mere på symptomer på abdominal angina hos patienter med aPL/APS.34 Dette er en vanskelig tilstand at kvantificere, men vi har set en række tilfælde, hvor clopidogrel eller heparin har resulteret i en forbedring (nogle gange markant) af postprandiale smerter.
Men selv om leverinvolvering i lupus er sjælden, ses unormale leverfunktionstest i APS hyppigt. Selv om disse kan varsle alvorlig levertrombose, såsom Budd-Chiari syndrom eller HELLP syndromet under graviditet, der advarer om forestående katastrofal APS, har de oftest en mere godartet prognose.35,36
Et meget positivt tilfælde: Tilbage i begyndelsen af 1980’erne så jeg en teenagepige med en DVT, positiv aPL og Budd-Chiari-syndrom.
Prognosen er dårlig?
Mere end tredive år senere har hun det stadig godt med forsigtig livslang warfarin, som hendes læger i Portugal administrerer.
Goldblatts sygdom, nyren & APS-Renal arterie stenose, set på en klar baggrund af ellers normale arterier, kan efterligne Goldblatts tidlige observationer om udviklingen af hypertension hos dyr med eksperimentelt okkluderede nyrearterier. Sangles opdagelse af nyrerarterie stenose lokaliserede læsioner førte til lignende fund i andre kar, hvilket førte til teorier om lokaliseret trombotisk/endothelial patologi.37
Hud: livedo reticularis, en gåde – Selvom hudsår, dilaterede vener og subunguale splinterblødninger er velkendte følgevirkninger af hudtrombose i APS, har livedo reticularis en aura af mystik.38,39
Diagnostisk set er dens tilstedeværelse et vigtigt spor hos patienter, der mistænkes for at have Hughes-syndromet – herunder seronegativ APS.
Så man ser tilbage på nogle af de tilstande, der er nævnt i denne artikel – MS, migræne, multiple frakturer, hukommelsesproblemer – kan man for eksempel spekulere på, om en omhyggelig notering af tilstedeværelsen eller fraværet af livedo kan vise sig at være betydningsfuld i differentialdiagnosen af disse tilstande.
En ting er sikker: Tilstedeværelsen af livedo tilføjer en ekstra dimension til sværhedsgraden af det kliniske billede.
Graviditet
Den store historie om syndromet er naturligvis i forbindelse med graviditet, hvor succesraten for sunde fødsler i aPL-positive graviditeter er steget fra under 15 % til over 90 %. Der er ingen tvivl om, at diagnosticering og behandling af disse tilfælde har været et betydeligt fremskridt inden for obstetrikken.40
Sørgeligt nok har alle vi, der arbejder med APS, taget os af aPL-positive patienter (hvoraf nogle havde lidt tidlige aborter), som mistede et barn sent i graviditeten. Dødfødsel.
For to år siden offentliggjorde The Times of London en lederartikel med titlen “The Stillbirth Scandal”, som fremhævede de dårlige tal for dødfødsler i Storbritannien.41 Alligevel kunne nogle tilfælde af dødfødsler hos de aPL-positive kvinder have været forhindret. For eksempel viste en nyere undersøgelse fra Utah, at aPL-graviditeter havde en tre- til femdobbelt øget risiko for dødfødsel.42
Kunne mere rutinemæssig aPL-testning under graviditeten hjælpe? Der skal tages hensyn til omkostningerne. Abort er almindeligt, og der er mange årsager. Derfor er den nuværende anbefaling at forbeholde testning til de kvinder, der har tre eller flere aborter. Dette virker hårdt. Måske kunne en simpel screeningsproces hjælpe.
Jeg har foreslået, at en del af den indledende screening hos jordemoderen eller fødselslægen bør omfatte et simpelt spørgeskema i tre dele:
- Har du haft en trombose?
- Lidder du af migræne?
- Har du en familiehistorie med autoimmune sygdomme (f.eks, lupus, RA, multipel sklerose, sygdom i skjoldbruskkirtlen)?
Jeg er sikker på, at et så simpelt spørgeskema kan hjælpe med at identificere en lille risikogruppe.
I de fleste centre er der ingen langsigtet opfølgning, når moderen og barnet er sendt sikkert hjem, når de er blevet sendt sikkert hjem. Alligevel er det ofte sådan, at APS-patienter, der kommer i f.eks. 40-årsalderen med et trombotisk problem, oplyser en tidligere historie om en abort 20 år tidligere. I en ideel verden fortjener kvinder med tilbagevendende aborter regelmæssig langsigtet opfølgning. Men verden er langt fra ideel.
Lupus & APS
De tidlige kliniske undersøgelser af APS blev udført på lupusklinikker og kunne meget vel have omfattet “lupus-karakteristika”. Det er måske overraskende, at tiden har vist lidt forskel mellem primær APS og den APS, der er forbundet med lupus. Der er utvivlsomt nogle klassiske træk ved lupus (f.eks. Libman Sachs endokarditis, slagtilfælde, kramper), som er mere sandsynlige for at være APS-relaterede. Det forekommer også sandsynligt, at aPL-positivitet i lupus giver et højere kronicitetsindeks.
Den tid, der er gået, har også afsløret et positivt fund: Det er meget usædvanligt for patienter med primær APS at udvikle lupus i senere år.
De 3 store
Sammenhængen mellem Hughes syndrom, Sjögrens og hypothyreose er så almindelig, at jeg har valgt at kalde dem de 3 store. Klinisk set er det en vigtig association, fordi de kliniske symptomer på de tre tilstande – træthed, koldt kredsløb, ømhed og smerter samt balance- og hukommelsesproblemer – er fælles for alle tre. Tilsvarende er mange af disse patienter belastet med betegnelsen fibromyalgi.
Hvert af de tre indbyrdes forbundne syndromer kan reagere godt på behandling – f.eks. den kliniske Sjögrens på hydroxychloroquin og så videre. Mange af disse patienter er på min to træer-behandling-willow (aspirin) og cinchona (kinin).
Seronegativ APS
Jeg tror, at en af fordelene ved, at en praktikant-kliniker tilbringer tid i laboratoriet, er erkendelsen af, at mange laboratorieprøver er åbne for variation. Mange, mange undersøgelser har forsøgt at vurdere betydningen af titer, immunglobulinklasse, tredobbelt eller dobbelt positivitet, relevans af “andre” aPL såsom anti-fosfatidyl-serin osv.43,44
Overordnet set har alle disse relevans, men i klinikken passer nogle ikke, f.eks. de patienter med alle de kliniske træk ved APS, hvis aPL-tests forbliver stædigt negative.
For nogle år siden skrev vi en artikel, hvor vi introducerede begrebet seronegativ APS og gjorde opmærksom på patienter med stærke kliniske træk af APS, men med negative test.45 Begrebet går tilbage til de tidlige dage med seronegativ RA og seronegativ lupus – begge betegnelser havde vigtige terapeutiske og prognostiske konsekvenser, selv om de alene var baseret på kliniske observationer.
Der er tre mulige forklaringer på seronegativ APS: 1) Diagnosen er forkert (usandsynligt i alle tilfælde); 2) de tidligere positive tests er blevet negative med tiden (ualmindeligt i min erfaring); eller 3) der er behov for nye tests.46
Måske den mest potente grund til åbenhed om seronegativ APS kommer fra familiestudier. For nogle uger siden så jeg et par enæggede tvillinger – den første med klassisk seropositiv APS, som senere medbragte sin (absolut) enæggede tvillingesøster. Den anden tvilling havde identiske sæt af symptomer, men i modsætning til den første tvilling havde hun negative APL-tests. Begge patienter reagerede på behandlingen.
En gang om året afholder vi et patientmøde på vores hospital. Ved det sidste møde arrangerede vi et simpelt anonymt spørgeskema med to spørgsmål: Er du en patient med APS eller en ven/ægtefælle? Har du en nær kvindelig slægtning (søster, mor, tante) med en autoimmun sygdom (dvs. lupus, RA, skjoldbruskkirtel, multipel sklerose, APS)? Resultatet: Resultatet: 60 % af patienterne havde en positiv historie om autoimmune sygdomme hos nære slægtninge. Mindre end 20 % af venner/ægtefæller svarede positivt.
Det kan være, at min egen erfaring er skævvredet af henvisningsbias fra familier til APS-patienter – men seropositiv eller ej, reagerer de fleste patienter med seronegativ APS lige så godt på behandling.
Hvis nogle af disse personer i familieundersøgelsen faktisk havde seronegativ APS, men alligevel potentielt reagerede på behandling, så er mulighederne spændende. Måske kunne en højere procentdel af vores migræne-, unge slagtilfælde- og unge angina-patienter have gavn af en nærmere undersøgelse for flere af sporene til APS – den tørre Schirmer’s, livedo, familiehistorien med autoimmune sygdomme – for eksempel.
Behandlingsaspekter
På mange måder er det skuffende at indrømme, at der 30 år senere kun er få nye behandlinger. Indførelsen af de nye orale antikoagulantia i behandlingen af APS har været forudsigeligt forsigtig, og det er for tidligt at generalisere.47
Statiner, IVIG og hydroxychlorquin er blevet kastet ind i blandingen, og selvfølgelig har anti-B-cellebehandling fået positive anekdoter. En nylig undersøgelse fra Paris foreslog, at sirolimus, der anvendes ved nyretransplantation, kan have en beskyttende effekt på aPL-induceret vaskulopati.48
Så i 2016 er den nuværende behandling af APS stadig i vid udstrækning begrænset til aspirin, clopidogrel, heparin og warfarin.
Lavdosis aspirin er, trods sine kritikere, naturligvis førstevalg hos mange APS-patienter. Clopidogrel er dog fortsat et nyttigt alternativ hos patienter med gastritis eller hos astmatikere. Men der er en tredje rolle for clopidogrel – vigtig i den praktiske medicins virkelige verden – nemlig hos de patienter, der af en eller anden grund har prøvet aspirin uden klar fordel.
Heparin-Lavmolekylær heparin har i de fleste lande stort set erstattet gammel heparin, og med det er frygten for trombocytopeni og osteoporose stort set forsvundet. Dette er et vigtigt punkt at gøre opmærksom på, fordi mange praktiserende læger er tilbageholdende med at forlænge brugen af heparin.
To observationer: For det første: En række patienter forbedrer sig dramatisk på heparin, for derefter at få det mindre godt med warfarin.
Hvor skal vi gå hen som det næste? Når doseringsproblemer, warfarinresistens og compliance (forhåbentlig) er udelukket, er en umiddelbar mulighed en midlertidig tilbagevenden til heparin. I nogle tilfælde er midlertidig blevet til halvlangvarig. I vores APS-klinik har vi et par dusin af sådanne patienter, som efter eget valg er blevet på subkutan heparin i to år eller mere. Ja, de har oplevet blå mærker, men indtil videre har vi ikke set en forværring af DEXA-scanninger.
Den anden (og meget kliniske) observation vedrører et heparinforsøg. Det er en almindelig observation, at aPL/APS-patienter, der får heparin under graviditeten, ofte er hovedpinefri i hele otte eller ni måneder. Dette fik os til at udvikle et klinisk værktøj – et terapeutisk forsøg, som har stået os godt. Forsøget er et tre- eller fireugers forløb med LMW-heparin.49
Lad mig give et eksempel på brugen heraf: Jeg vil gerne nævne et eksempel: Hos en aPL/APS-patient med tiltagende svær hovedpine på trods af aspirin/clopidogrel (og med en normal hjerne-MRI) kan et forsøg med 10.000 enheder dalteparin (eller enoxaparin) i tre eller fire uger give betydelige resultater. For det første kan det give en overraskende klar indikation af, om antikoagulation er den rigtige vej. For det andet kan det hos den traumatiserede patient, der har været på den velkendte vej med flere specialistkonsultationer med grænseoverskridende klinisk succes, være et vigtigt vendepunkt – det første håndgribelige tegn på forbedring.
Warfarin-Der er ikke meget nyt at sige om warfarin. Det er blevet udskældt af medierne, men det er fortsat et af de mest nyttige lægemidler i vores arsenal. Warfarin beskytter, for at sige det enkelt, mod slagtilfælde og hjerteanfald i APS.
Det er blevet nævnt, at der ofte er behov for en højere INR hos mange APS-patienter – især hos dem med neurologiske træk. Jeg er en stærk tilhænger af brugen af selvtestende INR-maskiner, når det er muligt for vores patienter.
Sværre er nogle antikoagulationsklinikker modstandere af brugen af selvtestende maskiner. Efter min mening er dette forkert. Se på den frihed, som selvtestning for insulinafhængige diabetikere har opnået.
Som læger mener jeg, at vi har en pligt (indtil bedre, nyere antikoagulantia bliver etableret) til at støtte warfarin som et stort set sikkert og effektivt lægemiddel, der har reddet mange tusinde liv.
I 2015 er den nuværende behandling af Hughes syndrom stadig i vid udstrækning begrænset til aspirin, clopidogrel, heparin & warfarin.
Miscellany
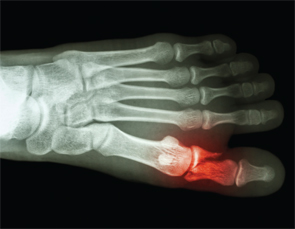
Spontane knoglefrakturer er ved at blive velkendt efter rapporten om 27 spontane metatarsalfrakturer af dr. Shirish Sangle hos APS-patienter.
Image Credit: Puwadol Jaturawutthichai/.com
Familien-Det kommer ikke som nogen overraskelse, at en familiehistorie er en vigtig ledetråd ved Hughes syndrom. Autoimmune sygdomme (især skjoldbruskkirtel) dukker jævnligt op som en diagnose hos slægtninge til vores patienter. Men hvor ofte bliver disse familietilfælde diagnosticeret? Eksempler kunne være den 17-årige datter til en APS-patient, der lider af hovedpine og kirtelfeber, søskende med multipel sklerose eller mor og tante til en nydiagnosticeret APS-patient, der fik et slagtilfælde i begyndelsen af 40’erne.
Det er ikke utænkeligt, at APS har ændret historiens gang, som i det tilfælde, der er rapporteret af min ven, dr. Gerald Weissmann, om dronning Anne af England, der havde 17 mislykkede graviditeter og døde barnløs, hvilket bragte enden på Stuart-regeringen og starten på hannoveranerne – med George III, skatterne i de amerikanske kolonier, revolutionen og fødslen af USA50.
Afkommet – Hidtil har de fleste undersøgelser antydet, at afkommet af aPL-positive mødre ikke har nogen større negative virkninger (bortset fra måske de senere udviklede arvelige APS-egenskaber hos nogle). Nogle foruroligende tilfælde af problemer hos fostre og nyfødte børn viser imidlertid, at der er behov for yderligere undersøgelser. De igangværende undersøgelser af dr. Anne Parke, Angela Tincani, Maria Claire Boffa og andre vil med tiden tilvejebringe nogle af disse manglende data.51,52
Klassifikation vs. diagnose-
Kære læge, jeg vil være taknemmelig, hvis De kan rådgive mig om denne patient. Hun udviklede trombose på den orale p-pille. Hun har haft en positiv test for aPL, men har ikke fået en gentagelsestest 12 uger senere.
Som i tilfælde af lupus bliver klassifikationskriterier nogle gange blandet sammen med diagnose. Mange patienter kommer ikke bevæbnet med test med “12 ugers mellemrum” (dette kriterium blev indført for at dække risikoen for, at en mellemliggende infektion kunne have ført til en forbigående positiv aPL-test – ikke en vigtig faktor i vores vurdering af denne patient).
Der er også økonomiske overvejelser, som i følgende undersøgelse fra Beirut, Libanon.
“Kun 50,5 % fik testet både aCL og LA. … Prisen for hver test var ca. 50 USD for patienten. … Det er endnu uvist, om testomkostningerne til dels kan forklare den meget lille procentdel af patienterne, der gennemgik en opfølgende konfirmatorisk test.”
Den tid, der er gået, har også afsløret et positivt resultat: Det er meget usædvanligt, at patienter med primær APS udvikler lupus i de senere år.
Anerkendelsen af de mange ikke-trombotiske manifestationer af APS har øget vigtigheden af at adskille diagnose fra klassifikation. Måske vil laboratoriefremskridt inden for måling af potentielle risikomarkører med tiden komme os til hjælp.44
Flyskræk – Denne kliniske anekdote optræder regelmæssigt i min klinik. Så meget, at jeg mener, at den bør undersøges nærmere. En række af mine APS-patienter, især før behandlingen er påbegyndt, lider alvorligt af langvarigt jetlag efter en langdistanceflyvning med træthed, hovedpine og forvirring, som nogle gange varer i dagevis.
Interessant nok forsvinder dette fænomen, når først heparin- eller warfarinbehandlingen er påbegyndt med succes. Det vides ikke, om disse symptomer er relateret til en mild cerebral hypoxi, der skyldes et let nedsat kabinetryk, eller ej. Ikke desto mindre supplerer nogle af mine patienter med APS deres aspirinbehandling forud for en langdistanceflyvning med en injektion af LMW-heparin. Selv om placeboeffekten kan være betydelig, er jeg tilstrækkeligt imponeret af disse (observante) patienters kliniske erfaringer til at tro, at fænomenet med forlænget jetlag hos mange af vores patienter er meget reelt.
Fremtiden – På den 14. internationale kongres om antiphospholipidantistoffer, der blev afholdt i Rio de Janeiro i 2013, blev jeg bedt om mine forudsigelser om fremtiden for APS.23 Sammenfattende mener jeg:
- APL-testning vil blive verdensomspændende og rutinemæssig;
- Der vil blive adgang til aPL-testsæt i håndkøb;
- En betydelig delmængde af migrænelidende vil få nyt håb;
- APS vil blive anerkendt som den vigtigste forbindelse mellem migræne og slagtilfælde;
- Hjerteanfald hos unge kvinder (især dem under 45 år) vil blive reduceret;
- Slagtilfælde hos dem under 45 år vil blive reduceret;
- Nogle tilfælde af accelereret arteriel sygdom vil blive anerkendt som værende forbundet med (ubehandlet) aPL;
- Nogle tilfælde af hukommelsestab kan behandles;
- APS vil fortsat have en dybtgående effekt på vores kliniske vurdering og behandling af lupus; og
- Finalt, for at vende tilbage til det indledende tema, vil forekomsten af dødfødsler blive reduceret, bl.a. takket være en mere proaktiv tilgang til aPL-testning i forbindelse med graviditet.
For at gentage en sætning fra 1983-artiklen:1
For dem af os, der er blevet hærdet til nihilisme af mange års studier af forskellige autoantistoffer i SLE, er der en sjælden følelse af begejstring over konsekvenserne af de associationer, der nu rapporteres.
Tredive år senere er den kliniske begejstring stadig ufortrødent.
 Graham R.V. Hughes, MD, FRCP, er en konsulent i reumatologi og leder af London Lupus Centre. Han er uddannet på The London Hospital og tilbragte to år i New York, hvor han arbejdede på indførelsen af den DNA-bindende test under ledelse af Dr. Charles Christian. I 1971 åbnede han en specialklinik i London, som udelukkende beskæftiger sig med lupus og beslægtede sygdomme. Han er grundlægger og redaktør af det internationale tidsskrift Lupus. I 1983 beskrev han antifosfolipidsyndromet, og i 1991 modtog han ILAR-prisen (verdensforskningsprisen) for dette arbejde. Andre hædersbevisninger omfatter Doctor Honoris Causa ved universiteterne i Marseille og Barcelona og Master of the ACR.
Graham R.V. Hughes, MD, FRCP, er en konsulent i reumatologi og leder af London Lupus Centre. Han er uddannet på The London Hospital og tilbragte to år i New York, hvor han arbejdede på indførelsen af den DNA-bindende test under ledelse af Dr. Charles Christian. I 1971 åbnede han en specialklinik i London, som udelukkende beskæftiger sig med lupus og beslægtede sygdomme. Han er grundlægger og redaktør af det internationale tidsskrift Lupus. I 1983 beskrev han antifosfolipidsyndromet, og i 1991 modtog han ILAR-prisen (verdensforskningsprisen) for dette arbejde. Andre hædersbevisninger omfatter Doctor Honoris Causa ved universiteterne i Marseille og Barcelona og Master of the ACR.
- Hughes GR. Trombose, abort, cerebral sygdom og lupus antikoagulans. Br Med J (Clin Res Ed). 1983 Oct 15;287(6399);287(6399):1088-1089.
- Harris EN, Gharavi AE, Boey ML, et al. Anticardiolipin i antistoffer: Påvisning ved radioimmunoassay og sammenhæng med trombose i SLE. Lancet. 1983 Nov 26;2(8361):1211-1214.
- Boey ML, Colaco CB, Gharavi AE, et al. Thrombosis in SLE: Striking association with the presence of circulating lupus anticoagulant. Br Med J (Clin Res Ed). 1983 Oct 8;287:1021-1023.
- Hughes GR. The Prosser White oration 1983: Bindevævssygdomme og huden. Clin Exp Dermatol. 1984 Nov;9(6):535-544.
- Asherson RA, Mackworth-Young CG, Boey ML, Hughes GRV. Pulmonal hypertension ved systemisk lupus erythematosus. Br Med J (Clin Res Ed). 1983 Oct 8;287(6398):1024-1025.
- Derue GJ, Englert HJ, Harris EN, et al. Føtaltab ved systemisk lupus: Forbindelse med anticardiolipin-antistoffer. J Obstet Gynaecol. 1985;5(4):207-209.
- Hughes GR, Harris NN, Gharavi AE. Anticardiolipinsyndromet. J Rheumatol. 1986 Jun;13(3):486-489.
- Hughes GR. Hughes’ syndrom: Det anticardiolipinsyndrom. Et historisk synspunkt. Lupus. 1998;7 Suppl 2:S1-S4.
- Carecchio M, Cantello R, Comi C. Revisiting the molecular mechanism in antiphospholipid syndrome: Beyond vascular damage. J Immunol Res. 2014;2014:239398.
- Bluestein HG, Zvaifler NJ. Hjerne-reaktive lymfocytotoksiske antistoffer i serumet hos patienter med SLE. J Clin Invest. 1976 Feb;57(2):509-516.
- Bresnihan B, Oliver N, Grigor R, Hughes GR. Hjerne-reaktivitet af lymfocytotoksiske anitistoffer i systemisk lupus erythematosus med og uden cerebral involvering. Clin Exp Immunol. 1977 Dec;30(3):333-337.
- Bresnihan B, Hohmeister R, Cutting J, et al. Den neuropsykiatriske lidelse i SLE: Bevis for både vaskulære og immune mekanismer. Ann Rheum Dis. 1979 Aug;38(4):301-306.
- Denburg SD, Behmann SA, Carbotte RM, et al. Lymphocyt antigener i neuropsykiatrisk systemisk lupus erythematosus. Forholdet mellem lymfocyt-antistofspecificiteter og klinisk sygdom. Arthritis Rheum. 1994 Mar;37(3):369-375.
- Harris EN, Gharavi AE, Asherson RA, et al. Cerebral infarkt i SLE. Forbindelse med anticardiolipin-antistoffer. Clin Exp Rheumatol. 1984 Jan-Mar;2(1):47-51.
- Navarrete MG, Brey RL, Levine SR. “Cerebral disease in the antiphospholipid syndrome” i Hughes Syndrome-Antiphospholipid Syndrome. Khamashta MA, ed. Springer, London: 2000.
- Sanna G, Bertolaccini ML, Cuadrado MJ, et al. Inddragelse af centralnervesystemet i antiphospholipid (Hughes) syndromet. Rheumatology (Oxford). 2003 Feb;42(2):200-213.
- Etminan M, Takkouche B, Isorna FC, Samii A. Risk of ischaemic stroke in people with migraine: Systemisk gennemgang og metaanalyse af observationsundersøgelser. BMJ. 2005 Jan 8;330(7482):63.
- Nencini P, Baruffi MC, Abbate R, et al. Lupus antikoagulerende og antikardiolipin-antistoffer hos unge voksne med cerebral iskæmi. Stroke. 1992 Feb;23(2):189-193.
- Hughes GR. Antifosfolipidsyndrom, migræne og slagtilfælde. Lupus. 2010 Apr;19(5):555-556.
- Mackworth-Young CG, Hughes GR. Epilepsi: Et tidligt symptom på systemisk lupus erythematosus. J Neurol Neurosurg Psychiatry. 1985 Feb;48(2):185.
- Cimaz R, Meroni PL, Shoenfeld Y. Epilepsi som en del af systemisk lupus erythematosus og systemisk antiphospholipidsyndrom (Hughes syndrom). Lupus. 2006;15(4):191-194.
- Hughes GR. “Diplomatisk epilepsi” i Forståelse af Hughes-syndromet. Springer-Verlag, London: 2009.
- Hughes GR. Hughes syndrom/APS. 30 år efter, hvad har vi lært? Åbningstale ved den 14. internationale kongres om antiphospholipidantistoffer. Rio de Janeiro, oktober 2013. Lupus. 2014;23;23:400-406.
- Cuadrado MJ, Khamashta MA, Ballesteros A, et al. Kan neurologiske manifestationer af Hughes (antiphospholipid) syndrom adskilles fra multipel sklerose? Analyse af 27 patienter og gennemgang af litteraturen. Medicine (Baltimore). 2000 Jan;79(1):57-68.
- Hughes GR. Migræne, hukommelsestab og “multipel sklerose”. Neurologiske træk ved antiphospholipid (Hughes’) syndrom. Postgrad Med J. 2003 Feb;79(928):81-83.
- Uthman I, Noureldine MH, Berjawi A, et al. Hughes syndrom og multipel sklerose. Lupus. 2015 Feb;24(2):115-121.
- Cervera R, Asherson RA, Font J, et al. Chorea i antiphospholipidsyndromet. Kliniske, radiologiske og immunologiske karakteristika for 50 patienter fra vores klinikker og den nyere litteratur. Medicine (Baltimore). 1997 May;76(3):203-212.
- Baizabal-Carvallo JF, Bonnet C, Jankovic J. Movement disorders in systemic lupus erythematosus and the antiphospholipid syndrome. J Neural Transm (Wien). 2013 Nov;120(11):1579-1589.
- Schofield JR, Blitshteyn S, Shoenfeld Y, et al. Postural tachycardia syndrome (POTS) and other autonomic disorders in antiphospholipid (Hughes) syndrome (APS). Lupus. 2014 Jun;23(7):697-702.
- Sangle S, D’Cruz DP, Khamashta MA, et al. Antiphospholipid antibodies, systemisk lupus erythematosus, and non-traumatic metatarsal fractures. Ann Rheum Dis. 2004 Oct;63(10):1241-1243.
- Greco TP1, Conti-Kelly AM, Greco T Jr., et al. Nyere antiphospholipid antistoffer forudsiger negative resultater hos patienter med akut koronart syndrom. Am J Clin Pathol. 2009 Oct;132(4):613-620.
- Urbanus RT, Siegerink B, Roest M, et al. Antiphospholipid antibodies and risk of myocardial infarction and ischaemic stroke in young women in the RATIO study: En case-kontrol-undersøgelse. Lancet Neurol. 2009 Nov;8(11):998-1005.
- Nair S, Khamashta MA, Hughes GR. Syndrom X og Hughes syndrom. Lupus. 2002;11(5):332.
- Sangle SR, Jan W, Lau IS, et al. Coeliac artery stenosis and antiphospholipid (Hughes) syndrome/antiphospholipid antibodies. Clin Exp Rheumatol. 2006 May-Jun;24(3):349.
- Mackworth-Young CG, Melia WM, Harris EN, et al. Budd-Chiari-syndromet. Mulig patogenetisk rolle af anti-fosfolipidantistoffer. J Hepatol. 1986;3(1):83-86.
- Hanouna G, Morel N, Le Thi Huong D, et al. Catastrophic antiphospholipid syndrome and pregnancy: En erfaring fra 13 tilfælde. Rheumatology (Oxford). 2013 Sep;52(9):1635-1641.
- Sangle SR, D’Cruz DP, Jan W, et al. Renal artery stenosis in antiphospholipid syndrome (Hughes) and hypertension. Ann Rheum Dis. 2003 Oct;62(10):999-1002.
- Englert HJ, Loizou S, Derue GG, et al. Clinical and Immunological features of livedo reticularis in lupus. Am J Med. 1989 Oct;87(4):408-410.
- Sangle SR, D’Cruz DP. Livedo reticularis: En gåde. Isr Med Assoc J. 2015 Feb;17(2):104-107.
- Ateka-Barrutia O, Khamashta MA. Udfordringen ved graviditet for patienter med SLE. Lupus. 2013 Oct;22(12):1295-1308.
- Hughes GR. Skandalen om dødfødsler. Lupus. 2013 Jul;22(8):759-760.
- Silver RM, Parker CB, Reddy UM, et al. Antiphospholipid antibodies in stillbirth. Obstet Gynecol. 2013 Sep;122(3):641-657.
- Rodriguez-Garcia JL, Bertolaccini ML, Cuadrado MJ, et al. Kliniske manifestationer af antiphospholipidsyndrom (APS) med og uden antiphospholipidantistoffer (det såkaldte “seronegative APS”). Ann Rheum Dis. 2012 Feb;71(2):242-244.
- Meroni PL, Chighizab CB, Rovelli F, et al. Antiphospholipidsyndrom i 2014: Flere kliniske manifestationer, nye patogene aktører og nye biomarkører. Arthritis Res Ther. 2014;16(2):209.
- Hughes GR, Khamashta MA. Seronegativt antifosfolipidsyndrom. Ann Rheum Dis. 2003 Dec;62(12):1127.
- Rodguez-Garcia JL, Bertolaccini ML, Cuadrado MJ, et al. Kliniske manifestationer af antiphospholipidsyndrom (APS) med og uden antiphospholipidantistoffer. Ann Rheum Dis. 2012 Feb;71(2):242-244.
- Giles I, Khamashta M, D’Cruz D, et al. A new dawn of anticoagulation for patients with antiphospholipid syndrome. Lupus. 2012 Oct;21(12):1263-1265.
- Canuad G, Bienaimé C, Taborin F, et al. Hæmning af mTORC-vejen i antiphospholipidsyndromet. New Eng J Med. 2014 Jul 24;371(4):303-312.
- Hughes GR. Heparin, antifosfolipidantistoffer og hjernen. Lupus. 2012 Sep;21(10):1039-1040.
- Weissmann G. Queen Anne’s lupus: Fosfolipider og rigets forløb. FASEB J. 2014 Apr;28(4):1527-1530.
- Mekinian A, Lachassinne E, Nicaise-Roland P, et al. European registry of babies born to mothers with antiphospholipid syndrome. Ann Rheum Dis. 2013 Feb;72(2):217-222.
- Nalli C, Iodice A, Andreoti L, et al. Børn født af SLE- og APS-mødre. Lupus. 2014 Oct;23(12):1246-1248.
- Major S, Pashayan N, Atweh S, et al. Praksismønstre for antiphospholipidsyndrom på et tertiært universitetshospital i Libanon. Lupus. 2002;11(11):759–764.