Doseringsform: kapsel
Medicinskt granskad av Drugs.com. Senast uppdaterad den 1 oktober 2020.
- Översikt
- Biverkningar
- Dosering
- Professionell
- Tipsen
- Interaktioner
- Mer
För att minska utvecklingen av läkemedels-resistenta bakterier och bibehålla effektiviteten hos nitrofurantoin (makrokristaller) och andra antibakteriella läkemedel, nitrofurantoin (makrokristaller) ska endast användas för att behandla eller förebygga infektioner som bevisligen eller starkt misstänks vara orsakade av bakterier.
- BESKRIVNING:
- KLINISK FARMACOLOGI:
- MIKROBIOLOGI
- Aktionsmekanism
- Interaktioner med andra antibiotika
- Resistensutveckling
- INDIKATIONER OCH ANVÄNDNING:
- KONTRAINDICATIONER:
- VARNINGAR:
- Pulmonella reaktioner:
- Hepatotoxicitet:
- Neuropati:
- Hemolytisk anemi:
- Clostridium difficile-associerad diarré:
- Föreskrifter:
- Information till patienter:
- Allmänt:
- Läkemedelsinteraktioner:
- Läkemedels-/laboratorietestinteraktioner:
- Carcinogenes, mutagenes, nedsatt fertilitet:
- Graviditet:
- Graviditetskategori B.
- Förlossning och förlossning:
- Sjuksköterskor:
- Pediatrisk användning:
- Geriatrisk användning:
- ADVERSE REAKTIONER:
- Respiratoriska:
- Hepatisk:
- Neurologisk:
- Dermatologiskt:
- Allergiskt:
- Gastrointestinal:
- Hematologiskt:
- Diversifierat:
- Laboratoriska biverkningar:
- Överdosering
- DOSERING OCH ADMINISTRATION:
- Vuxna:
- Pediatriska patienter:
- Hur man får tillgång till:
- PRINCIPAL DISPLAY PANEL – 50 mg
- PRINCIPAL DISPLAY PANEL – 100 mg
- För vanliga frågor
- Mer om nitrofurantoin
- Förbrukarresurser
- Professionella resurser
- Relaterade behandlingsguider
BESKRIVNING:
Nitrofurantoin, USP (makrokristaller) är en syntetisk kemikalie med kontrollerad kristallstorlek. Det är en stabil, gul, kristallin förening. Nitrofurantoin, USP (makrokristaller) är ett antibakteriellt medel för specifika urinvägsinfektioner. Det finns i 25 mg, 50 mg och 100 mg kapslar för oral administrering.
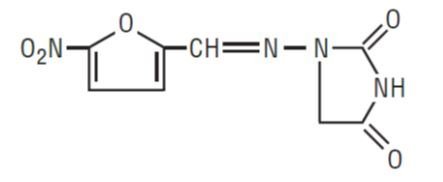
1-AMINO]-2, 4-IMIDAZOLIDINEDIONE
Inaktiva ingredienser: Varje kapsel innehåller D&C Yellow # 10, FD&C Blue # 1, FD&C Blue # 2, FD&C Red # 40, gelatin, järnoxid svart, laktos vattenfri, magnesiumstearat, pregelatiniserad majsstärkelse, natriumlaurylsulfat, talk och titandioxid. Kapslarna på 50 mg och 100 mg innehåller även FD&C Yellow No. 6.
KLINISK FARMACOLOGI:
Nitrofurantoin (makrokristaller) är en större kristallform av nitrofurantoin. Absorptionen av nitrofurantoin (makrokristaller) är långsammare och utsöndringen något mindre jämfört med nitrofurantoin. Blodkoncentrationerna vid terapeutisk dosering är vanligtvis låga. Det är lättlösligt i urin, som det kan ge en brun färg.
Efter en doseringsregim på 100 mg fyra gånger om dagen i 7 dagar var den genomsnittliga läkemedelsåtervinningen i urinen (0 till 24 timmar) på dag 1 och dag 7 37.9% och 35,0%.
Till skillnad från många läkemedel kan närvaron av mat eller medel som fördröjer gastrisk tömning öka biotillgängligheten av nitrofurantoin (makrokristaller), förmodligen genom att möjliggöra bättre upplösning i magsaften.
MIKROBIOLOGI
Nitrofurantoin är ett nitrofuran antimikrobiellt medel med aktivitet mot vissa grampositiva och gramnegativa bakterier.
Aktionsmekanism
Mekanismen för den antimikrobiella verkan av nitrofurantoin är ovanlig bland antibakteriella medel. Nitrofurantoin reduceras av bakteriella flavoproteiner till reaktiva intermediärer som inaktiverar eller förändrar bakteriella ribosomala proteiner och andra akromolekyler. Till följd av sådana inaktiveringar hämmas de vitala biokemiska processerna proteinsyntes, aerob energiomsättning, DNA-syntes, RNA-syntes och cellväggssyntes. Nitrofurantoin är bakteriedödande i urin vid terapeutiska doser. Den breda karaktären hos detta verkningssätt kan förklara avsaknaden av förvärvad bakteriell resistens mot nitrofurantoin, eftersom de nödvändiga multipla och samtidiga mutationerna av målmakromolekylerna sannolikt skulle vara dödliga för bakterierna.
Interaktioner med andra antibiotika
Antagonism har påvisats in vitro mellan nitrofurantoin och kinolonantimikrobiella medel. Den kliniska betydelsen av detta fynd är okänd.
Resistensutveckling
Resistensutveckling mot nitrofurantoin har inte varit ett betydande problem sedan introduktionen 1953. Korsresistens med antibiotika och sulfonamider har inte observerats och överförbar resistens är på sin höjd ett mycket sällsynt fenomen.
Nitrofurantoin har visat sig vara aktivt mot de flesta stammar av följande bakterier både in vitro och vid kliniska infektioner (se Indikationer och användning):
Aeroba och fakultativa grampositiva mikroorganismer:
Staphylococcus aureus
Enterokocker (t.ex. Enterococcus faecalis)
Aeroba och fakultativa gramnegativa mikroorganismer:
Escherichia coli
OBS: Även om nitrofurantoin har utmärkt aktivitet mot Enterococcus faecalis är majoriteten av Enterococcus faecium-isolaten inte mottagliga för nitrofurantoin.
Minst 90 procent av följande mikroorganismer uppvisar en in vitro minsta hämmande koncentration (MIC) som är mindre än eller lika med den mottagliga brytpunkten för nitrofurantoin. Effekten av nitrofurantoin vid behandling av kliniska infektioner orsakade av dessa mikroorganismer har dock inte fastställts i adekvata och välkontrollerade prövningar.
Aeroba och fakultativa grampositiva mikroorganismer:
Koagulasnegativa stafylokocker (inklusive Staphylococcus
epidermidis och Staphylococcus saprophyticus)
Streptococcus agalactiae
Streptokocker av grupp D
Streptokocker av viridangruppen
Aeroba och fakultativa Gram-negativa mikroorganismer:
Citrobacter amalonaticus
Citrobacter diversus
Citrobacter freundii
Klebsiella oxytoca
Klebsiella ozaenae
OBS: Vissa stammar av Enterobacter- och Klebsiella-arter är resistenta mot nitrofurantoin.
Känslighetstestning:
För specifik information om tolkningskriterier för känslighetstest och tillhörande testmetoder och kvalitetskontrollstandarder som erkänns av FDA för detta läkemedel, se: https://www.fda.gov/STIC.
INDIKATIONER OCH ANVÄNDNING:
Nitrofurantoinkapslar (makrokristaller) är specifikt indicerade för behandling av urinvägsinfektioner när de beror på mottagliga stammar av Escherichia coli, enterokocker, Staphylococcus aureus och vissa mottagliga stammar av Klebsiella och Enterobacter arter.
Nitrofurantoin är inte indicerat för behandling av pyelonefrit eller perinefriska abscesser.
För att minska utvecklingen av läkemedelsresistenta bakterier och bibehålla effektiviteten av nitrofurantoinkapslar (makrokristaller) och andra antibakteriella läkemedel ska nitrofurantoinkapslar (makrokristaller) endast användas för att behandla eller förebygga infektioner som bevisligen eller starkt misstänks vara orsakade av mottagliga bakterier. När information om odling och känslighet finns tillgänglig ska den beaktas vid val eller modifiering av antibakteriell behandling. I avsaknad av sådana uppgifter kan lokal epidemiologi och känslighetsmönster bidra till det empiriska valet av terapi.
Nitrofurantoins saknar den bredare vävnadsdistribution som andra terapeutiska medel som är godkända för urinvägsinfektioner har. Följaktligen är många patienter som behandlas med nitrofurantoinkapslar (makrokristaller) predisponerade för persistens eller återkomst av bakteriuri. Urinprover för odling och känslighetstest ska tas före och efter avslutad behandling. Om persistens eller återkomst av bakteriuri förekommer efter behandling med nitrofurantoinkapslar (makrokristaller) bör andra terapeutiska medel med bredare vävnadsdistribution väljas. När man överväger att använda nitrofurantoinkapslar (makrokristaller) ska lägre eradikeringsfrekvens vägas mot den ökade potentialen för systemisk toxicitet och för utveckling av antimikrobiell resistens när medel med bredare vävnadsdistribution används.
KONTRAINDICATIONER:
Anuri, oliguri eller signifikant nedsatt njurfunktion (kreatininclearance under 60 ml per minut eller kliniskt signifikant förhöjt serumkreatinin) är kontraindikationer. Behandling av denna typ av patienter medför en ökad risk för toxicitet på grund av försämrad utsöndring av läkemedlet. På grund av risken för hemolytisk anemi på grund av omogna erytrocytära enzymsystem (glutationinstabilitet) är läkemedlet kontraindicerat hos gravida patienter vid termin (38 till 42 veckors dräktighet), under arbete och förlossning eller när förlossning är nära förestående. Av samma anledning är läkemedlet kontraindicerat hos nyfödda barn under en månad.
Nitrofurantoinkapslar (makrokristaller) är kontraindicerade hos patienter med en tidigare historia av kolestatisk gulsot/hepatisk dysfunktion associerad med nitrofurantoin.
Nitrofurantoinkapslar (makrokristaller) är också kontraindicerade hos de patienter med känd överkänslighet mot nitrofurantoin.
VARNINGAR:
Pulmonella reaktioner:
AKUTA, SUBAKUTA ELLER KRONISKA PULMONARREAKTIONER HAR UPPSTÅTT TILL FRAMTILLT hos PATIENTER SOM BEHANDLATS MED NITROFURANTOIN. OM DESSA REAKTIONER INTRÄFFAR SKA NITROFURANTOIN (MAKROKRISTALLER) AVBRYTAS OCH LÄMPLIGA ÅTGÄRDER VIDTAS. I RAPPORTER HAR LUNGREAKTIONER ANGETTS SOM EN BIDRAGANDE DÖDSORSAK.
KRONISKA LUNGREAKTIONER (DIFFUS INTERSTITIELL PNEUMONIT ELLER LUNGFIBROS, ELLER BÅDA) KAN UTVECKLAS SMYGANDE. DESSA REAKTIONER FÖREKOMMER SÄLLAN OCH I ALLMÄNHET HOS PATIENTER SOM FÅR BEHANDLING I SEX MÅNADER ELLER LÄNGRE. NOGGRANN ÖVERVAKNING AV LUNGTILLSTÅNDET HOS PATIENTER SOM FÅR LÅNGTIDSBEHANDLING ÄR MOTIVERAD OCH KRÄVER ATT FÖRDELARNA MED BEHANDLINGEN VÄGS MOT DE POTENTIELLA RISKERNA (SE ANDNINGSREAKTIONER).
Hepatotoxicitet:
Hepatiska reaktioner, inklusive hepatit, kolestatisk gulsot, kronisk aktiv hepatit och levernekros, förekommer sällan. Dödsfall har rapporterats. Inträdet av kronisk aktiv hepatit kan vara smygande, och patienterna bör övervakas regelbundet för förändringar i biokemiska tester som skulle kunna tyda på leverskada. Om hepatit uppstår ska läkemedlet omedelbart dras in och lämpliga åtgärder vidtas.
Neuropati:
Perifer neuropati, som kan bli allvarlig eller irreversibel, har förekommit. Dödsfall har rapporterats. Tillstånd som nedsatt njurfunktion (kreatininclearance under 60 ml per minut eller kliniskt signifikant förhöjt serumkreatinin), anemi, diabetes mellitus, elektrolytobalans, B-vitaminbrist och försvagande sjukdom kan förstärka förekomsten av perifer neuropati. Patienter som får långtidsbehandling bör övervakas regelbundet för förändringar i njurfunktionen.
Optisk neurit har rapporterats sällan i erfarenhet efter marknadsintroduktion med nitrofurantoinformuleringar.
Hemolytisk anemi:
Fall av hemolytisk anemi av primaquinkänslighetstyp har inducerats av nitrofurantoin. Hemolysen tycks vara kopplad till en glukos-6-fosfatdehydrogenasbrist i de röda blodkropparna hos de drabbade patienterna. Denna brist finns hos 10 procent av svarta och en liten andel av etniska grupper med ursprung i Medelhavsområdet och Mellanöstern. Hemolys är en indikation för avbrytande av nitrofurantoin (makrokristaller); hemolysen upphör när läkemedlet dras tillbaka.
Clostridium difficile-associerad diarré:
Clostridium difficile-associerad diarré (CDAD) har rapporterats vid användning av nästan alla antibakteriella medel, inklusive nitrofurantoin, och kan variera i allvarlighetsgrad från mild diarré till dödlig kolit. Behandling med antibakteriella medel förändrar kolonets normala flora vilket leder till överväxt av C. difficile.
C. difficile producerar toxiner A och B som bidrar till utvecklingen av CDAD. Hypertoxinproducerande stammar av C. difficile orsakar ökad morbiditet och mortalitet, eftersom dessa infektioner kan vara refraktära mot antimikrobiell behandling och kan kräva kolektomi. CDAD måste övervägas hos alla patienter som får diarré efter antibiotikaanvändning. En noggrann anamnes är nödvändig eftersom CDAD har rapporterats förekomma över två månader efter administrering av antibakteriella medel. Om CDAD misstänks eller bekräftas kan pågående antibiotikaanvändning som inte är riktad mot C. difficile behöva avbrytas. Lämplig vätske- och elektrolythantering, proteintillskott, antibiotikabehandling av C. difficile och kirurgisk utvärdering ska sättas in enligt klinisk indikation.
Föreskrifter:
Information till patienter:
Patienterna ska uppmanas att ta nitrofurantoin (makrokristaller) tillsammans med mat för att ytterligare öka toleransen och förbättra läkemedelsabsorptionen. Patienterna ska instrueras att fullfölja hela behandlingen; de ska dock uppmanas att kontakta sin läkare om några ovanliga symtom uppstår under behandlingen.
Många patienter som inte tål mikrokristallint nitrofurantoin kan ta nitrofurantoin (makrokristaller) utan illamående.
Patienter ska rådas att inte använda antacidpreparat som innehåller magnesiumtrisilikat när de tar nitrofurantoin (makrokristaller).
Patienter ska rådas om att antibakteriella läkemedel, inklusive nitrofurantoin (makrokristaller), endast ska användas för att behandla bakteriella infektioner. De behandlar inte virusinfektioner (t.ex. förkylning). När nitrofurantoin (makrokristaller) förskrivs för att behandla en bakteriell infektion ska patienterna informeras om att även om det är vanligt att känna sig bättre tidigt under behandlingen ska läkemedlet tas exakt enligt anvisningarna. Att hoppa över doser eller inte fullfölja hela behandlingen kan (1) minska effektiviteten av den omedelbara behandlingen och (2) öka sannolikheten för att bakterier utvecklar resistens och inte kan behandlas med nitrofurantoin (makrokristaller) eller andra antibakteriella läkemedel i framtiden.
Diarré är ett vanligt problem som orsakas av antibiotika och som vanligtvis upphör när antibiotikan avbryts. Ibland kan patienter efter påbörjad behandling med antibiotika utveckla vattnig och blodig avföring (med eller utan magkramper och feber) även så sent som två eller flera månader efter att de tagit den sista dosen av antibiotikan. Om detta inträffar ska patienterna kontakta sin läkare så snart som möjligt.
Allmänt:
Förskrivning av nitrofurantoin (makrokristaller) i avsaknad av en bevisad eller starkt misstänkt bakterieinfektion eller en profylaktisk indikation är osannolikt att ge nytta för patienten och ökar risken för utveckling av läkemedelsresistenta bakterier.
Läkemedelsinteraktioner:
Antacider som innehåller magnesiumtrisilikat, när de administreras samtidigt med nitrofurantoin, minskar både absorptionshastighet och absorptionsomfattning. Mekanismen för denna interaktion är troligen adsorption av nitrofurantoin på ytan av magnesiumtrisilikat.
Uricosuriska läkemedel, såsom probenecid och sulfinpyrazon, kan hämma den renala tubulära sekretionen av nitrofurantoin. Den resulterande ökningen av nitrofurantoins serumnivåer kan öka toxiciteten, och de minskade urinnivåerna kan minska dess effekt som antibakteriellt medel för urinvägarna.
Läkemedels-/laboratorietestinteraktioner:
Som ett resultat av närvaron av nitrofurantoin kan en falsk-positiv reaktion för glukos i urinen förekomma. Detta har observerats med Benedict- och Fehling-lösningar men inte med glukosenzymtestet.
Carcinogenes, mutagenes, nedsatt fertilitet:
Nitrofurantoin var inte cancerframkallande när det utfodrades till honråttor av typen Holtzman i 44,5 veckor eller till honråttor av typen Sprague-Dawley i 75 veckor. Två kroniska bioassays på gnagare där manliga och kvinnliga Sprague-Dawley-råttor användes och två kroniska bioassays på schweiziska möss och BDF1-möss visade inga tecken på karcinogenicitet.
Nitrofurantoin visade tecken på karcinogen aktivitet hos B6C3F1-möss av honkön, vilket visades genom ökad incidens av tubulära adenom, godartade blandade tumörer och granulosacellstumörer i äggstocken. Hos F344/N-råttor av hankön ökade incidensen av ovanliga tubulära cellneoplasmer i njurarna, osteosarkomer i benen och neoplasmer i den subkutana vävnaden. I en studie med subkutan administrering av 75 mg/kg nitrofurantoin till dräktiga honmöss observerades lungpapillära adenom av okänd betydelse i F1-generationen.
Nitrofurantoin har visat sig inducera punktmutationer i vissa stammar av Salmonella typhimurium och framåtriktade mutationer i L5178Y-lymfomceller från mus. Nitrofurantoin inducerade ett ökat antal systerkromatidbyten och kromosomala aberrationer i kinesiska hamster ovarieceller men inte i mänskliga celler i kultur. Resultaten av det könsbundna recessiva letala testet i Drosophila var negativa efter administrering av nitrofurantoin genom utfodring eller injektion. Nitrofurantoin inducerade inte ärftlig mutation i de undersökta gnagarmodellerna.
Betydelsen av fynden av karcinogenicitet och mutagenicitet i förhållande till den terapeutiska användningen av nitrofurantoin hos människor är okänd.
Administrering av höga doser nitrofurantoin till råttor orsakar tillfälligt spermatogena stillestånd; detta är reversibelt när läkemedlet avbryts. Doser på 10 mg/kg/dag eller mer hos friska manliga män kan i vissa oförutsägbara fall ge ett lätt till måttligt spermatogent stopp med en minskning av antalet spermier.
Graviditet:
Teratogena effekter:
Graviditetskategori B.
Flera reproduktionsstudier har utförts på kaniner och råttor i doser upp till sex gånger den humana dosen och har inte visat några tecken på nedsatt fertilitet eller skada på fostret på grund av nitrofurantoin. I en enda publicerad studie utförd på möss vid 68 gånger den humana dosen (baserat på mg/kg administrerat till moderdjuret) observerades tillväxthämning och en låg förekomst av mindre och vanliga missbildningar. Vid 25 gånger den humana dosen observerades dock inga fostermissbildningar; relevansen av dessa resultat för människor är osäker. Det finns dock inga adekvata och välkontrollerade studier på gravida kvinnor. Eftersom reproduktionsstudier på djur inte alltid är förutsägande för respons hos människor bör detta läkemedel användas under graviditet endast om det är klart nödvändigt.
Icke-teratogena effekter:
Nitrofurantoin har i en publicerad transplacentär karcinogenicitetsstudie visat sig framkalla lungpapillära adenom hos F1-generationen av möss vid doser som är 19 gånger högre än den humana dosen på mg/kg-basis. Förhållandet mellan detta fynd och potentiell karcinogenes hos människa är för närvarande okänt. På grund av osäkerheten om de mänskliga konsekvenserna av dessa djurdata bör detta läkemedel användas under graviditet endast om det är uppenbart nödvändigt.
Förlossning och förlossning:
Se KONTRAINDIKATIONER.
Sjuksköterskor:
Nitrofurantoin har påvisats i spår av spårmängder i mänsklig bröstmjölk. På grund av risken för allvarliga biverkningar av nitrofurantoin hos ammande spädbarn under en månad bör ett beslut fattas om att avbryta amningen eller att avbryta läkemedlet, med hänsyn till läkemedlets betydelse för modern (se KONTRAINDIKATIONER).
Pediatrisk användning:
Nitrofurantoin (makrokristaller) är kontraindicerat hos spädbarn under en månads ålder (se KONTRAINDIKATIONER).
Geriatrisk användning:
Kliniska studier av nitrofurantoin (makrokristaller) omfattade inte ett tillräckligt antal försökspersoner i åldern 65 år och äldre för att avgöra om de reagerar annorlunda än yngre personer. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i respons mellan äldre och yngre patienter. Spontanrapporter tyder på en högre andel lungreaktioner, inklusive dödsfall, hos äldre patienter; dessa skillnader verkar vara relaterade till den högre andelen äldre patienter som får långtidsbehandling med nitrofurantoin. Liksom hos yngre patienter observeras i allmänhet kroniska lungreaktioner hos patienter som får behandling i sex månader eller längre (se VARNINGAR). Spontanrapporter tyder också på en ökad andel allvarliga leverreaktioner, inklusive dödsfall, hos äldre patienter (se VARNINGAR).
I allmänhet bör den högre frekvensen av nedsatt lever-, njur- eller hjärtfunktion och av samtidig sjukdom eller annan läkemedelsbehandling beaktas vid förskrivning av nitrofurantoin (makrokristaller). Det är känt att detta läkemedel i stor utsträckning utsöndras via njurarna och risken för toxiska reaktioner på detta läkemedel kan vara större hos patienter med nedsatt njurfunktion. Anuri, oliguri eller signifikant nedsatt njurfunktion (kreatininclearance under 60 ml per minut eller kliniskt signifikant förhöjt serumkreatinin) är kontraindikationer (se KONTRAINDIKATIONER). Eftersom äldre patienter är mer benägna att ha nedsatt njurfunktion bör försiktighet iakttas vid dosval och det kan vara lämpligt att övervaka njurfunktionen.
ADVERSE REAKTIONER:
Respiratoriska:
KRONISKA, SUBAKUTA ELLER AKUTA PULMONARIEHYPERSENSIBILITETSREAKTIONER KAN UPPTRÄDAS.
KRONISKA PULMONARIEREAKTIONER UPTRÄDERAR ALLMÄNT hos patienter som har fått kontinuerlig behandling i sex månader eller längre. ILLAMÅENDE, DYSPNÉ VID ANSTRÄNGNING, HOSTA OCH FÖRÄNDRAD LUNGFUNKTION ÄR VANLIGA MANIFESTATIONER SOM KAN UPPTRÄDA SMYGANDE. RADIOLOGISKA OCH HISTOLOGISKA FYND AV DIFFUS INTERSTITIELL PNEUMONIT ELLER FIBROS, ELLER BÅDA, ÄR OCKSÅ VANLIGA MANIFESTATIONER AV DEN KRONISKA LUNGREAKTIONEN. FEBER ÄR SÄLLAN FRAMTRÄDANDE.
SVÅRIGHETSGRADEN AV KRONISKA LUNGREAKTIONER OCH DERAS GRAD AV UPPLÖSNING VERKAR VARA RELATERADE TILL BEHANDLINGSTIDEN EFTER DET ATT DE FÖRSTA KLINISKA TECKNEN UPPTRÄTT. LUNGFUNKTIONEN KAN VARA PERMANENT NEDSATT ÄVEN EFTER AVSLUTAD BEHANDLING. Risken är större när kroniska lungreaktioner inte uppmärksammas tidigt.
I subakuta lungreaktioner förekommer feber och eosinofili mindre ofta än i den akuta formen. Efter avslutad behandling kan det ta flera månader att återhämta sig. Om symtomen inte erkänns som läkemedelsrelaterade och nitrofurantoinbehandlingen inte avbryts kan symtomen bli allvarligare.
Akuta lungreaktioner visar sig vanligen genom feber, frossa, hosta, bröstsmärta, dyspné, lunginfiltration med konsolidering eller pleurautgjutning på röntgenbild och eosinofili. Akuta reaktioner uppträder vanligen inom den första behandlingsveckan och är reversibla när behandlingen upphör. Läkningen är ofta dramatisk (se Varningar).
Förändringar i EKG (t.ex, ospecifika ST/T-vågförändringar, grenblock) har rapporterats i samband med lungreaktioner.
Cyanos har sällan rapporterats.
Hepatisk:
Hepatiska reaktioner, inklusive hepatit, kolestatisk gulsot, kronisk aktiv hepatit och levernekros, förekommer sällan (se VARNINGAR).
Neurologisk:
Perifer neuropati, som kan bli svår eller irreversibel, har förekommit. Dödsfall har rapporterats. Tillstånd som nedsatt njurfunktion (kreatininclearance under 60 ml per minut eller kliniskt signifikant förhöjt serumkreatinin), anemi, diabetes mellitus, elektrolytobalans, B-vitaminbrist och försvagande sjukdomar kan öka risken för perifer neuropati (se Varningar).
Astheni, vertigo, nystagmus, yrsel, huvudvärk och dåsighet har också rapporterats vid användning av nitrofurantoin.
Benign intrakraniell hypertension (pseudotumor cerebri), förvirring, depression, optikusneurit och psykotiska reaktioner har rapporterats sällan. Utbuktande fontaneller, som ett tecken på godartad intrakraniell hypertension hos spädbarn, har rapporterats sällan.
Dermatologiskt:
Exfoliativ dermatit och erythema multiforme (inklusive Stevens-Johnsons syndrom) har rapporterats sällan. Övergående alopeci har också rapporterats.
Allergiskt:
Ett lupusliknande syndrom i samband med lungreaktioner på nitrofurantoin har rapporterats. Även angioödem; makulopapulära, erytematösa eller eksematösa eruptioner; pruritus; urtikaria; anafylaxi; arthralgi; myalgi; läkemedelsfeber; frossa och vaskulit (ibland i samband med lungreaktioner) har rapporterats. Överkänslighetsreaktioner utgör de vanligaste spontant rapporterade biverkningarna i den världsomspännande erfarenheten efter marknadsföring av nitrofurantoinformuleringar.
Gastrointestinal:
Nausea, kräkningar och anorexi förekommer oftast. Buksmärta och diarré är mindre vanliga gastrointestinala reaktioner. Dessa dosrelaterade reaktioner kan minimeras genom minskning av dosen. Sialadenit och pankreatit har rapporterats. Det har förekommit sporadiska rapporter om pseudomembranös kolit vid användning av nitrofurantoin. Debuten av symptom på pseudomembranös kolit kan inträffa under eller efter antimikrobiell behandling (se VARNINGAR).
Hematologiskt:
Cyanos sekundärt till methemoglobinemi har rapporterats i sällsynta fall.
Diversifierat:
Som med andra antimikrobiella medel kan superinfektioner orsakade av resistenta organismer, t.ex, Pseudomonas species eller Candida species, kan förekomma.
Laboratoriska biverkningar:
Följande laboratoriebiverkningar har rapporterats vid användning av nitrofurantoin: Ökad AST (SGOT), ökad ALT (SGPT), minskat hemoglobin, ökad serumfosfor, eosinofili, glukos-6-fosfatdehydrogenasbristanemi (se VARNINGAR), agranulocytos, leukopeni, granulocytopeni, hemolytisk anemi, trombocytopeni, megaloblastisk anemi. I de flesta fall försvann dessa hematologiska avvikelser efter avslutad behandling. Aplastisk anemi har rapporterats sällan.
Överdosering
Enstaka incidenter av akut överdosering av nitrofurantoin (makrokristaller) har inte resulterat i några specifika symtom förutom kräkningar. Induktion av kräkningar rekommenderas. Det finns ingen specifik antidot, men ett högt vätskeintag bör upprätthållas för att främja urinutsöndringen av läkemedlet. Det är dialysbart.
DOSERING OCH ADMINISTRATION:
Nitrofurantoinkapslar (makrokristaller) bör ges tillsammans med mat för att förbättra läkemedelsabsorptionen och, hos vissa patienter, toleransen.
Vuxna:
50 mg till 100 mg fyra gånger dagligen — den lägre doseringsnivån rekommenderas vid okomplicerade urinvägsinfektioner.
Pediatriska patienter:
5 till 7 mg/kg kroppsvikt per 24 timmar, givet i fyra delade doser (kontraindicerat under en månads ålder).
Terapin bör fortsätta i en vecka eller i minst 3 dagar efter det att sterilitet i urinen erhållits. Fortsatt infektion indikerar behov av omvärdering.
För långvarig suppressiv behandling hos vuxna kan en minskning av dosen till 50-100 mg vid sänggåendet vara adekvat. För långvarig suppressiv behandling hos pediatriska patienter kan så låga doser som 1 mg/kg per 24 timmar, som ges i en enda dos eller i två delade doser, vara adekvata. Se avsnittet Varningar om risker i samband med långtidsbehandling.
Hur man får tillgång till:
Nitrofurantoinkapslar USP (makrokristaller) finns tillgängliga enligt följande:
50 mg ogenomskinlig, vit kropp och ogenomskinlig, gul hätta med svart bläck med texten ”WATSON” på hättan och ”5780” på kroppen.
NDC 0115-2023-10 flaskor med 100
100 mg opaka, gul kapsel med svart bläck med texten ”WATSON” på locket och ”5781” på kroppen.
NDC 0115-2024-10 flaskor om 100
förvaras vid 20° till 25°C (68° till 77°F) .
Herställd av:
Watson Pharma Private Limited
Verna, Salcette Goa 403722 INDIA
Distribuerad av:
Amneal Pharmaceuticals LLC
Bridgewater, NJ 08807
För att rapportera misstänkta biverkningar, kontakta Amneal Pharmaceuticals på 1-877-835-5472 eller FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch.
Rev. 11-2019-00
PRINCIPAL DISPLAY PANEL – 50 mg

PRINCIPAL DISPLAY PANEL – 100 mg

| NITROFURANTOIN nitrofurantoin kapsel |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||