Vad är enzymer och vad gör de i våra kroppar? Enzymer är i princip proteiner som produceras av levande organismer för att åstadkomma vissa metaboliska och biokemiska reaktioner i kroppen. De är biologiska katalysatorer som påskyndar reaktioner i kroppen. Låt oss ta reda på mer om dem.
Föreslagna videor:
Vad är enzymernas struktur?
Enzymer är som nämnts ovan biologiska katalysatorer. Samtidigt som de påskyndar eller snabbar upp en process tillhandahåller de i själva verket en alternativ väg för processen. Men under processen förblir enzymernas struktur eller sammansättning oförändrad.
Enzymer består faktiskt av 1000-tals aminosyror som är länkade på ett specifikt sätt för att bilda olika enzymer. Enzymkedjorna viker sig för att bilda unika former och det är dessa former som ger enzymet dess karakteristiska kemiska potential. De flesta enzymer innehåller också en icke-proteinkomponent som kallas kofaktor.
Se fler ämnen under Biomolekyler
- Biomakromolekyler
- Bindningslänkande monomerer
- Enzymer
- Metabolisk grund för liv
- Nukleinsyror
- Polysackarider
- Proteiner
Typer av enzymer:
De biokemiska reaktioner som sker i kroppen är i princip av sex typer och de enzymer som åstadkommer dessa reaktioner benämns därefter:
- Oxidoreduktas: Dessa enzymer åstadkommer oxidations- och reduktionsreaktioner och kallas därför oxidoreduktas. I dessa reaktioner överförs elektroner i form av hydridjoner eller väteatomer. När ett substrat oxideras fungerar dessa enzymer som vätedonatorer. Dessa enzymer kallas dehydrogenaser eller reduktas. När syreatomen är acceptör kallas dessa enzymer för oxidaser.
- Transferaser: Dessa enzymer ansvarar för att överföra funktionella grupper från en molekyl till en annan. Exempel: alaninaminotransferas som blandar alfa-aminogruppen mellan alanin och aspartat osv. Vissa transferaser överför också fosfatgrupper mellan ATP och andra föreningar, sockerrester för att bilda disackarider, t.ex. hexokinas i glykolysen.
- Hydrolaser: Dessa enzymer katalyserar reaktioner som innefattar hydrolysprocessen De bryter enkelbindningar genom att tillsätta vatten. Vissa hydrolaser fungerar som matsmältningsenzymer eftersom de bryter peptidbindningarna i proteiner. Hydrolaser kan också vara en typ av transferaser eftersom de överför vattenmolekylen från en förening till en annan. Exempel: Glukos-6-fosfatas som tar bort fosfatgruppen från glukos-6-fosfat och lämnar kvar glukos och H3PO4.
- Lyaser: Dessa enzymer katalyserar reaktioner där funktionella grupper läggs till för att bryta dubbelbindningar i molekyler eller där dubbelbindningar bildas genom avlägsnande av funktionella grupper. Exempel: Pyruvatdekarboxylas är ett lyas som avlägsnar koldioxid från pyruvat. Andra exempel är deaminaser och dehydrataser.
- Isomeraser: Dessa enzymer katalyserar reaktioner där en funktionell grupp flyttas till en annan position inom samma molekyl så att den resulterande molekylen faktiskt är en isomer av den tidigare molekylen. Exempel: triosefosfatisomeras och fosfoglukosisomeras för omvandling av glukos-6-fosfat till fruktos-6-fosfat.
- Ligaser: Dessa enzymer utför en funktion som är motsatt till hydrolasernas. Där hydrolaser bryter bindningar genom att tillföra vatten, bildar ligaser bindningar genom att ta bort vattenkomponenten. Det finns olika underklasser av ligaser som involverar syntesen av ATP.
Hur fungerar enzymer?
För att en reaktion ska kunna ske i universum krävs det energi. I de fall då det inte finns någon aktiveringsenergi spelar en katalysator en viktig roll för att minska aktiveringsenergin och föra reaktionen framåt. Detta fungerar även hos djur och växter. Enzymer hjälper till att minska aktiveringsenergin hos de komplexa molekylerna i reaktionen. Följande steg förenklar hur ett enzym fungerar för att påskynda en reaktion:
Steg 1: Varje enzym har en ”aktiv plats” där en av substratmolekylerna kan binda till. På så sätt bildas ett enzym-substratkomplex.
Steg 2: Denna enzym-substratmolekyl reagerar nu med det andra substratet för att bilda produkten och enzymet frigörs som den andra produkten.
Det finns många teorier som förklarar hur enzymer fungerar. Men det finns två viktiga teorier som vi kommer att diskutera här.
Teori 1: Lås- och nyckelhypotesen
Detta är den mest accepterade av teorierna om enzymers verkan.

Denna teori säger att substratet passar exakt in i enzymets aktiva plats för att bilda ett enzym-substratkomplex. Denna modell beskriver också varför enzymer är så specifika i sin verkan eftersom de är specifika för substratmolekylerna.
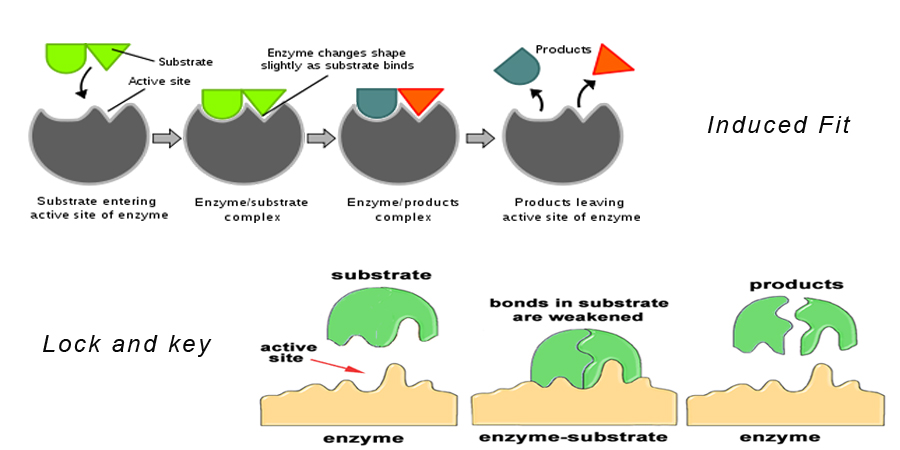
Teori 2: Hypotesen om inducerad passform
Detta liknar hypotesen om lås och nyckel. Den säger att enzymmolekylens form förändras när den närmar sig substratmolekylen på ett sådant sätt att substratmolekylen passar exakt in i enzymets aktiva plats.
Vilka faktorer påverkar enzymaktiviteten i cellen?
- Koncentration av enzymer och substrat: Reaktionshastigheten ökar med ökande substratkoncentration upp till en punkt, bortom vilken varje ytterligare ökning av substratkoncentrationen inte ger någon signifikant förändring av reaktionshastigheten. Detta beror på att efter en viss koncentration av substratet är alla aktiva platser på enzymet fyllda och ingen ytterligare reaktion kan ske.
- Temperatur: Med ökad temperatur ökar enzymaktiviteten på grund av att molekylernas kinetiska energi ökar. Det finns en optimal nivå när enzymerna fungerar bäst och maximalt. Denna temperatur är ofta kroppens normala kroppstemperatur. När temperaturen ökar över en viss gräns börjar enzymerna, som egentligen består av proteiner, att sönderfalla och reaktionshastigheten avtar.
- pH: Enzymer är mycket känsliga för förändringar i pH-värdet och arbetar inom ett mycket litet fönster av tillåtna pH-nivåer. Under eller över den optimala pH-nivån finns det en risk för att enzymerna sönderdelas och att reaktionen därmed blir långsammare.
- Inhibitorer: Förekomst av vissa ämnen som hämmar ett visst enzyms verkan. Detta sker när det hämmande ämnet fäster sig vid enzymets aktiva plats och därigenom förhindrar substratets fästning och bromsar processen.
Löst exempel för dig
Q: Ett enzym verkar genom att?
a. Ökar aktiveringsenergin
b. Minskar aktiveringsenergin
c. Sänka pH
d. Öka pH
Sol: a. Öka aktiveringsenergin
Reaktanterna genomgår inte en kemisk förändring automatiskt. De gör det i övergångstillståndet. Övergångstillståndet har mer fri energi än reaktanterna eller produkterna. Reaktanternas oförmåga att genomgå en förändring på grund av att det krävs extra energi för att omvandla dem till övergångstillståndet kallas ”energibarriär”. Den energi som krävs för att övervinna energibarriären kallas ”aktiveringsenergi”.