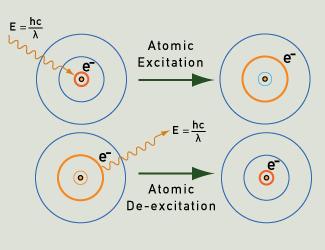
I fotoni di luce sono emessi quando un elettrone torna al suo stato fondamentale dopo essere stato eccitato.
Prove di fiamma
Le prove di fiamma sono utili perché l’eccitazione dei gas produce uno spettro di emissione a linee caratteristiche per un elemento. In confronto, l’incandescenza produce una banda continua di luce con un picco dipendente dalla temperatura dell’oggetto caldo.
Quando gli atomi di un gas o di un vapore sono eccitati, per esempio dal riscaldamento o dall’applicazione di un campo elettrico, i loro elettroni sono in grado di muoversi dal loro stato fondamentale a livelli di energia più elevati. Quando ritornano al loro stato fondamentale, seguendo percorsi ben definiti secondo le probabilità quantistiche, emettono fotoni di energia molto specifica. Questa energia corrisponde a particolari lunghezze d’onda della luce, e quindi produce particolari colori di luce. Ogni elemento ha una “impronta digitale” in termini di spettro di emissione di linee, come illustrato dagli esempi seguenti.

Spettro di linee per l’idrogeno.

Spettro di linee per l’elio.

Spettro delle linee per il neon.
Perché ogni elemento ha uno spettro di emissione delle linee esattamente definito, gli scienziati sono in grado di identificarlo dal colore della fiamma che produce. Per esempio, il rame produce una fiamma blu, il litio e lo stronzio una fiamma rossa, il calcio una fiamma arancione, il sodio una fiamma gialla e il bario una fiamma verde.

Questa immagine illustra i colori distintivi prodotti dalla combustione di particolari elementi.

La fiamma di una torcia ossiacetilenica brucia a più di 3000°C, abbastanza calda da essere usata per la saldatura subacquea.
Fiamma
Il colore ci dice la temperatura della fiamma di una candela. Il nucleo interno della fiamma di una candela è azzurro, con una temperatura di circa 1670 K (1400 °C). Questa è la parte più calda della fiamma. Il colore all’interno della fiamma diventa giallo, arancione e infine rosso. Più ci si allontana dal centro della fiamma, più bassa sarà la temperatura. La parte rossa è intorno ai 1070 K (800 °C).
I colori arancione, giallo e rosso in una fiamma non sono legati solo alla temperatura del colore. Anche le eccitazioni del gas giocano un ruolo importante nel colore della fiamma. Uno dei principali costituenti di una fiamma che brucia è la fuliggine, che ha una composizione complessa e diversa di composti di carbonio. La varietà di questi composti crea una gamma praticamente continua di possibili stati quantici in cui gli elettroni possono essere eccitati. Il colore della luce emessa dipende dall’energia emessa da ogni elettrone che ritorna al suo stato originale.