ARGOMENTI DI CHIMICA GENERALE
Energia: Concetti fondamentali
Forme di energia: Energia cinetica e potenziale.Lavoro ed energia.Calore e temperatura.Energia potenziale elettrostatica.
Energia: cinetica e potenziale
Il concetto di energia è fondamentale per le scienze fisiche. Qui ci proponiamo di esporre alcuni primi principi riguardanti l’energia, e di introdurre alcune delle forme che l’energia assume che sono di particolare importanza per la chimica. Prima di tutto, è spesso molto utile definire un sistema per indicare una particolare parte dell’universo su cui vengono fatte le nostre osservazioni. Il sistema è costituito da un oggetto o da un insieme di oggetti, ed è distinto dal resto dell’universo – che chiamiamo dintorni – da un confine reale o immaginario.
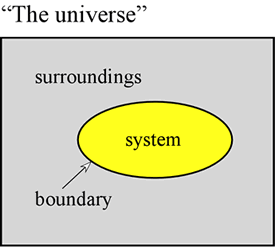
Un campione di gas tenuto all’interno di un volume fisso, come un cilindro di metallo, è un esempio di sistema – uno che sarà importante per noi quando ci occuperemo dello studio delle proprietà generali dei gas. Altri esempi sono un campione di gas dentro un palloncino o una miscela di combustione in un cilindro con un pistone. In entrambi questi casi il sistema è racchiuso da un confine fisico, ma mobile, in modo che il volume del sistema non sia fisso. Un ulteriore esempio che considereremo spesso è quello di una miscela di sostanze in soluzione che subisce una reazione chimica all’interno di una provetta o di un becher. La terminologia qui introdotta è di particolare importanza nello studio di come l’energia si manifesta nei sistemi chimici, che cade in gran parte sotto il titolo della termodinamica.
Nella chimica generale, i sistemi che consideriamo rilevanti sono tipicamente a riposo e gli effetti gravitazionali sono ignorati. Spesso, siamo più interessati a sistemi all’interno dei quali avvengono reazioni chimiche, la composizione chimica del sistema cambia nel tempo. Adottiamo per il momento, tuttavia, una prospettiva più ampia, utilizzando sistemi meccanici come un pendolo oscillante, o palle da biliardo che rotolano e si scontrano, per aiutarci a capire i principi generali relativi all’energia.
Si può dire che un sistema possiede energia in due modi diversi, che chiamiamo energia cinetica e potenziale. L’energia cinetica è l’energia della materia in movimento. La fisica fornisce un’esatta definizione matematica dell’energia cinetica (KE), mostrata nell’equazione (sotto a sinistra).
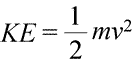
Qui, l’energia cinetica di un oggetto è rappresentata come il prodotto della massa dell’oggetto (m) e il quadrato della sua velocità (v), moltiplicato anche per la costante ½. Se il sistema consiste di più di un oggetto, l’energia cinetica totale è esprimibile come somma delle energie cinetiche dei singoli oggetti.
Possiamo ricavare le unità per l’energia data questa definizione. L’unità SI per l’energia è il joule (J), che è definito come:
1 J = 1 kg-m-s-2
L’energia potenziale è l’energia di un sistema che può tipicamente essere convertita in energia cinetica in qualche forma, e capace di produrre, in qualche misura, una quantità chiamata lavoro (discussa più avanti). Un chiaro esempio di energia potenziale è un mattone sul cornicione di un edificio. Il mattone ha una certa quantità di energia potenziale in virtù della sua altezza – la sua posizione rispetto a un campo gravitazionale. Se diamo al mattone una spinta, in modo che cada dal cornicione, si muove spontaneamente nella direzione della minore energia potenziale gravitazionale, e così facendo guadagna energia cinetica. Un altro esempio è l’energia potenziale elettrica di una batteria (che si esprime in termini di tensione). Quando si fa un circuito con un filo e una lampadina, collegando i due terminali di una batteria, la differenza di potenziale elettrico tra loro fa muovere gli elettroni nel filo (energia cinetica), con conseguente produzione di calore e luce.
Un importante principio generale sull’energia è che essa non può essere né creata né distrutta. Questo è noto come la legge della conservazione dell’energia. Quantitativamente, questo significa che in un sistema come il mattone che cade o il pendolo di un orologio, la somma dell’energia cinetica e potenziale è costante. Questa è in qualche modo un’astrazione, poiché in un pendolo reale, una parte dell’energia viene continuamente persa a causa dell’attrito, e una piccola quantità di energia deve essere aggiunta al pendolo per farlo oscillare (e far funzionare l’orologio). Ma se teniamo conto di questa energia “persa” (che in realtà appare come un aumento dell’energia termica delle molecole dell’aria circostante) con accurate misurazioni sperimentali, si scopre che in effetti l’energia si conserva sempre. Un altro avvertimento è riassunto nella famosa equazione di Einstein E = mc2, che esprime un’equivalenza fondamentale di massa ed energia. Una forma più generale della legge di conservazione dell’energia, che può essere chiamata legge di conservazione della massa-energia, rende conto di questa equivalenza. Tornando alla chimica generale, tali interconversioni materia-energia non sono tipicamente di sua competenza, mentre lo studio delle reazioni nucleari e della radioattività è compreso nella fisica nucleare.
Se consideriamo una reazione chimica in cui i cambiamenti chimici sono accompagnati dalla produzione di calore, sorge una domanda: Che ne è della conservazione dell’energia in questo caso? La risposta è che esiste una forma di energia potenziale, che possiamo chiamare energia potenziale chimica (o semplicemente potenziale chimico), che può essere pensata come residente nella composizione molecolare dei reagenti. Questa energia potenziale viene poi convertita in energia sotto forma di calore, ma si scopre che la quantità netta di energia presente rimane costante, una volta che siamo in grado di definire e misurare la produzione di calore. Un esempio quotidiano di ciò che possiamo ora comprendere come energia potenziale chimica è dato da un motore a benzina, in cui la miscela di benzina e ossigeno possiede una forma latente di energia. Questa energia latente nella miscela benzina/ossigeno viene spesa per produrre l’energia cinetica di un’automobile.
Lavoro ed energia
Il lavoro è un altro concetto che ammette una definizione precisa in fisica. Inoltre, le leggi della meccanica possono essere legate all’energia per mezzo del teorema lavoro-energia. Un calcio a un pallone da calcio, o qualsiasi altro esempio simile, illustra l’idea che l’energia cinetica di un oggetto può essere aumentata dall’applicazione di una forza. Il teorema lavoro-energia, che è una generalizzazione di questa idea, può essere enunciato approssimativamente come segue: La variazione dell’energia che un oggetto possiede è uguale alla grandezza della forza che agisce su di esso, moltiplicata per la distanza attraverso la quale la forza agisce.
Il cambiamento di energia che avviene in un sistema come risultato del lavoro può essere positivo o negativo, dal punto di vista del sistema. Il lavoro può essere fatto da un sistema, o un sistema può avere lavoro fatto su di esso dall’ambiente circostante. Se il lavoro è fatto da un sistema, esso perde energia nell’ambiente circostante. Se il sistema è sottoposto a lavoro, l’energia del sistema aumenta. Per esempio, quando una scintilla che innesca una miscela di combustione in un cilindro con un pistone mobile causa una rapida espansione del sistema, e l’espansione è accoppiata meccanicamente al movimento di un’asta nell’ambiente circostante, il sistema del cilindro compie lavoro sull’ambiente circostante, e così facendo, perde energia. Questo naturalmente è una parte di come un motore a combustione interna converte l’energia potenziale chimica nell’energia cinetica di una macchina in movimento.
Una implicazione del teorema lavoro-energia è per le unità, cioè che il lavoro può essere misurato nelle stesse unità dell’energia. Poiché la seconda legge di Newton è forza = massa × accelerazione, il newton (N), l’unità SI per la forza, è derivato come M × L × T -2, e quindi 1 N = 1 kg m s-2. La forza per la distanza ha quantità M × L2 × T -2, e quindi l’unità SI per l’energia, il joule (J), è definita come 1 J = 1 kg m2 s-2. A questo punto, dovresti verificare da solo che l’equazione per l’energia cinetica coinvolge la stessa combinazione delle quantità fondamentali massa (M), lunghezza (o distanza, L) e tempo (T).
Calore e temperatura
Usiamo le parole calore e temperatura abbastanza frequentemente, e spesso parliamo di calore come una forma di energia. Tutti noi abbiamo un senso intuitivo di cosa siano queste cose, ma qui vogliamo pensare a loro in modo più scientifico, e dare loro definizioni più formali, se possibile. Questo è un preludio necessario alla quantificazione dell’energia corrispondente al calore, e quindi alle misurazioni per verificare la legge di conservazione dell’energia. Ciò che troviamo è che l’energia termica di un sistema può essere paragonata all’energia cinetica totale (come definita sopra) degli atomi e delle molecole che lo compongono. La temperatura di un oggetto o di un sistema è in realtà una misura dell’energia cinetica media degli atomi e/o delle molecole che lo compongono. (N.B. La temperatura non è esattamente uguale all’energia cinetica media delle molecole, ma è direttamente proporzionale ad essa. Per ulteriori dettagli, vedere la pagina web sulla teoria cinetica molecolare).
Un modo per visualizzare ciò che intendiamo per calore e temperatura, e la distinzione tra loro, è quello di considerare un’analogia con la palla da biliardo. In alcuni contesti semplici, il comportamento delle palle da biliardo è un modello adeguato per un insieme di atomi o molecole, come in un campione di un gas. Proprio come le palle da biliardo che sono state appena colpite da una palla da biliardo in rapido movimento, le molecole di un gas si muovono, rimbalzando l’una sull’altra e sulle pareti del contenitore che le contiene. L’energia cinetica totale delle palle da biliardo, che è solo la somma delle energie cinetiche individuali di ogni palla, è analoga al contenuto di energia termica di un campione di molecole di gas. In una “pausa” all’inizio di una partita di biliardo, l’energia cinetica iniziale della palla da biliardo è distribuita tra tutte le palle sul tavolo. Alcune si muovono abbastanza velocemente, altre meno, ma l’analogia con il “calore” o “energia termica” per il sistema delle palle da biliardo è proprio la somma di queste energie cinetiche. D’altra parte, la temperatura del sistema di palle da biliardo sarebbe proporzionale all’energia cinetica media dell’insieme delle palle.
Energia potenziale elettrostatica
La legge di attrazione e repulsione elettrostatica, o legge di Coulomb, descrive la forza esercitata su un oggetto carico per la presenza di un altro oggetto carico. La forza è più facilmente calcolabile quando le cariche possono essere trattate come cariche puntuali molto piccole. La grandezza della forza che un oggetto carico “sente” è proporzionale al prodotto delle cariche (l’unità SI per la carica elettrica è il Coulomb, C), e inversamente proporzionale al quadrato della distanza di separazione tra le cariche (r nella figura a destra). La forza è una forza attrattiva (come la gravità, e indicata da punte di freccia verso l’interno nella figura) se le cariche sono di segno opposto, e repulsiva quando le cariche hanno lo stesso segno.
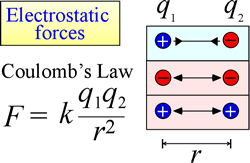
Quando le forze (come quelle elettrostatiche, magnetiche e gravitazionali) possono agire a distanza (attraverso lo spazio, senza contatto meccanico), si dice che gli oggetti soggetti a tali forze sono in un campo di energia potenziale. Abbiamo parlato di energia potenziale gravitazionale sopra, e allo stesso modo nel caso delle forze elettrostatiche, un oggetto carico avrà energia potenziale elettrostatica in virtù della sua posizione in un campo elettrico. Tale campo esiste nelle vicinanze di qualsiasi altra carica o cariche.
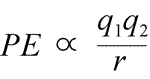
Equazione per l’energia potenziale elettrostatica: PE è proporzionale alle cariche q1 e q2, e inversamente proporzionale alla distanza di separazione, r. La forma della funzione dell’energia potenziale segue matematicamente dall’espressione della forza, la legge di Coulomb.
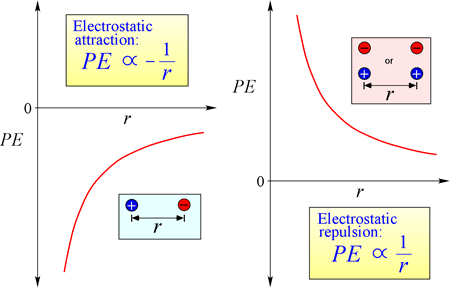
Dato il segno opposto delle cariche in attrazione, l’energia potenziale è sempre negativa, e più le cariche si avvicinano, più negativo – cioè più basso – l’energia potenziale diventa. Come la distanza di separazione, r si avvicina a zero, l’energia potenziale diventa infinitamente negativa. Per cariche dello stesso segno, l’energia di repulsione è sempre positiva, e diventa infinitamente positiva man mano che la distanza di separazione, r si avvicina a zero.
L’energia potenziale elettrostatica è una considerazione importante in chimica. La comprensione della natura dell’atomo, del legame chimico e delle forze intermolecolari sono tutte assolutamente dipendenti dalla considerazione dell’influenza delle interazioni carica-carica che contribuiscono all’energia di un sistema.
Unità importanti
Energia (unità SI) 1 joule = 1 J = 1 kg-m-s-2
Carica elementare, e = 1,60218 × 10-19 C (coulomb, C)
Costante di Faraday: F = NAe = 9,64853 × 104 C-mol-1
Potenziale elettrico: volt, V 1 V = 1 J C-1