annostusmuoto: kapseli
Lääketieteellisesti tarkistettu Drugs.com. Viimeksi päivitetty 1. lokakuuta 2020.
- Yleiskatsaus
- Haittavaikutukset
- Adostus
- Profiili
- Vihjeitä
- Vuorovaikutukset
- Lisätiedot
Vähentääksesi lääkeaineidenresistenttien bakteerien kehittymistä ja ylläpitää nitrofurantoiinin (makrokiteiden) ja muiden antibakteeristen lääkkeiden tehoa, nitrofurantoiinia (makrokiteitä) saa käyttää vain sellaisten infektioiden hoitoon tai ehkäisyyn, joiden on osoitettu tai vahvasti epäillään olevan bakteerien aiheuttamia.
- KUVAUS:
- KLIININEN FARMAKOLOGIA:
- MIKROBIOLOGIA
- VAIKUTUSMEKANISMI
- Vuorovaikutukset muiden antibioottien kanssa
- Resistenssin kehittyminen
- VALMISTEET JA KÄYTTÖAIHEET:
- YHTEENVETO:
- VAROITUKSET:
- Pulmonaaliset reaktiot:
- Hepatotoksisuus:
- Neuropatia:
- Hemolyyttinen anemia:
- Clostridium difficileen liittyvä ripuli:
- EHDOTUKSET:
- Tietoa potilaille:
- Yleistä:
- Lääkeinteraktiot:
- Lääkkeen ja laboratoriotestien yhteisvaikutukset:
- Karsinogeneesi, mutageenisuus, hedelmällisyyden heikentyminen:
- Raskaus:
- Raskausluokka B.
- Synnytys:
- Synnyttävät äidit:
- Pediatrinen käyttö:
- Geriatrinen käyttö:
- Hepatiitti:
- Neurologinen:
- Dermatologiset:
- Allergiset:
- Ruokatorvi:
- Hematologiset:
- Muut:
- Laboratorion haittavaikutukset:
- Yliannostus
- ANNOSTUS JA ANNOSTUS:
- Aikuiset:
- Pediatriset potilaat:
- KÄYTTÖTARVIKKEET:
- VALMISTELUPÄÄLLIKKÖ – 50 mg
- VALMISTELUPÄÄLLIKKÖ – 50 mg
- VALMISTELUPÄÄLLIKKÖ – 50 mg 100 mg
- Tiheästi kysyttyjä kysymyksiä
- Lisätietoa nitrofurantoiinista
- Kuluttajan resurssit
- Ammattilaisen resurssit
- Seuraavat hoito-oppaat
KUVAUS:
Nitrofurantoiini, USP (makrokiteet) on synteettinen kemikaali, jolla on hallittu kiderakenne. Se on stabiili, keltainen, kiteinen yhdiste. Nitrofurantoiini, USP (makrokiteet) on antibakteerinen aine tiettyihin virtsatieinfektioihin. Sitä on saatavana 25 mg:n, 50 mg:n ja 100 mg:n kapseleina suun kautta otettavaksi.
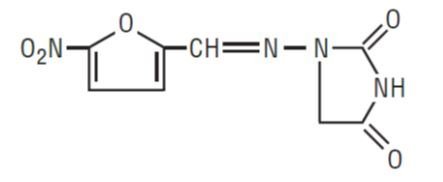
1-AMINO]-2, 4-IMIDAZOLIDINEDIONE
Vaikuttavat aineet: Jokainen kapseli sisältää D&C Yellow # 10, FD&C Blue # 1, FD&C Blue # 2, FD&C Red # 40, gelatiinia, rautaoksidimustaa, vedetöntä laktoosia, magnesiumstearaattia, esigelatinoitua maissitärkkelystä, natriumlauryylisulfaattia, talkkia ja titaanidioksidia. 50 mg:n ja 100 mg:n kapselit sisältävät myös FD&C Yellow No. 6.
KLIININEN FARMAKOLOGIA:
Nitrofurantoiini (makrokiteetit) on nitrofurantoiinin suurempi kidemuoto. Nitrofurantoiinin (makrokiteet) imeytyminen on hitaampaa ja erittyminen jonkin verran vähäisempää verrattuna nitrofurantoiiniin. Veren pitoisuudet terapeuttisella annostuksella ovat yleensä pieniä. Se liukenee hyvin virtsaan, johon se voi antaa ruskean värin.
Käytettäessä annostussuunnitelmaa 100 mg neljä kertaa vuorokaudessa 7 vuorokauden ajan, keskimääräiset virtsan lääkeaineen talteenotot (0-24 tuntia) 1. ja 7. vuorokauden aikana olivat 37.9 % ja 35,0 %.
Monista lääkkeistä poiketen ruoan tai mahalaukun tyhjenemistä hidastavien aineiden läsnäolo voi lisätä nitrofurantoiinin (makrokiteiden) biologista hyötyosuutta, oletettavasti sallimalla paremman liukenemisen mahamehuun.
MIKROBIOLOGIA
Nitrofurantoiini on nitrofuraani-antimikrobinen aine, joka tehoaa tiettyihin grampositiivisiin ja gramnegatiivisiin bakteereihin.
VAIKUTUSMEKANISMI
Nitrofurantoiinin antimikrobisen vaikutuksen mekanismi on epätavallinen antibakteerien joukossa. Bakteerien flavoproteiinit pelkistävät nitrofurantoiinia reaktiivisiksi välituotteiksi, jotka inaktivoivat tai muuttavat bakteerien ribosomaalisia proteiineja ja muita akromolekyylejä. Tällaisen inaktivoitumisen seurauksena elintärkeät biokemialliset prosessit, kuten proteiinisynteesi, aerobinen energia-aineenvaihdunta, DNA-synteesi, RNA-synteesi ja soluseinän synteesi, estyvät. Nitrofurantoiini on terapeuttisina annoksina virtsassa bakterisidinen. Tämän vaikutustavan laaja-alaisuus saattaa selittää sen, ettei bakteereilla ole hankittua resistenssiä nitrofurantoiinia vastaan, sillä tarvittavat useat ja samanaikaiset mutaatiot kohdemakromolekyyleissä olisivat bakteereille todennäköisesti tappavia.
Vuorovaikutukset muiden antibioottien kanssa
Nitrofurantoiinin ja kinoloniantimikrobien välillä on osoitettu in vitro antagonismia. Tämän havainnon kliinistä merkitystä ei tunneta.
Resistenssin kehittyminen
Resistenssin kehittyminen nitrofurantoiinia vastaan ei ole ollut merkittävä ongelma sen käyttöönoton jälkeen vuonna 1953. Ristiresistenssiä antibioottien ja sulfonamidien kanssa ei ole havaittu, ja siirtyvä resistenssi on korkeintaan hyvin harvinainen ilmiö.
Nitrofurantoiinin on osoitettu tehoavan useimpiin seuraavien bakteerikantoihin sekä in vitro että kliinisissä infektioissa (ks. käyttöaiheet ja käyttö):
Aerobiset ja fakultatiiviset grampositiiviset mikro-organismit:
Staphylococcus aureus
Enterokokit (esim. Enterococcus faecalis)
Aerobiset ja fakultatiiviset gramnegatiiviset mikro-organismit:
Escherichia coli
Huomautus: Vaikka nitrofurantoiini tehoaa erinomaisesti Enterococcus faecalis -bakteeriin, suurin osa Enterococcus faecium -isolaateista ei ole herkkiä nitrofurantoiinille.
Vähintään 90 prosentilla seuraavista mikro-organismeista on in vitro pienin inhiboiva pitoisuus (MIC), joka on pienempi tai yhtä suuri kuin nitrofurantoiinin herkkyysraja. Nitrofurantoiinin tehoa näiden mikro-organismien aiheuttamien kliinisten infektioiden hoidossa ei kuitenkaan ole osoitettu riittävissä ja hyvin kontrolloiduissa tutkimuksissa.
Aerobiset ja fakultatiiviset grampositiiviset mikro-organismit:
Koagulaasinegatiiviset stafylokokit (mukaan lukien Staphylococcus
epidermidis ja Staphylococcus saprophyticus)
Streptococcus agalactiae
Ryhmän D streptokokit
Viridans-ryhmään kuuluvia streptokokkeja
Aerobiset ja fakultatiiviset gram-…negatiiviset mikro-organismit:
Citrobacter amalonaticus
Citrobacter diversus
Citrobacter freundii
Klebsiella oxytoca
Klebsiella ozaenae
HUOMAUTUS: Jotkin Enterobacter- ja Klebsiella-lajien kannat ovat resistenttejä nitrofurantoinille.
Herkkyystestaus:
Kohtaisia tietoja herkkyystestien tulkintakriteereistä ja niihin liittyvistä testimenetelmistä sekä FDA:n tälle lääkkeelle tunnustamista laadunvalvontastandardeista, ks: https://www.fda.gov/STIC.
VALMISTEET JA KÄYTTÖAIHEET:
Nitrofurantoiinikapselit (makrokiteet) on erityisesti tarkoitettu virtsatieinfektioiden hoitoon silloin, kun ne johtuvat herkistä Escherichia coli-, enterokokki- ja Staphylococcus aureus -bakteerikannoista sekä tietyistä herkistä Klebsiella- ja Enterobacter-heimon lajikannoista.
Nitrofurantoiini ei ole tarkoitettu pyelonefriitin tai perinefriittisten paiseiden hoitoon.
Lääkkeille resistenttien bakteerien kehittymisen vähentämiseksi ja nitrofurantoiinikapselien (makrokiteiden) ja muiden antibakteeristen lääkkeiden tehon säilyttämiseksi nitrofurantoiinikapseleita (makrokiteitä) saa käyttää vain sellaisten infektioiden hoitoon tai ehkäisyyn, joiden on osoitettu tai vahvasti epäillään olevan herkkien bakteerien aiheuttamia. Kun viljely- ja herkkyystietoja on saatavilla, ne on otettava huomioon antibakteerista hoitoa valittaessa tai muutettaessa. Jos tällaisia tietoja ei ole, paikallinen epidemiologia ja herkkyysmallit voivat vaikuttaa osaltaan hoidon empiiriseen valintaan.
Nitrofurantoineilla ei ole muiden virtsatieinfektioihin hyväksyttyjen terapeuttisten aineiden laajempaa kudosjakelua. Näin ollen monet potilaat, joita hoidetaan nitrofurantoiinikapseleilla (makrokiteillä), ovat alttiita bakteriurian pysyvyydelle tai uudelleen ilmaantumiselle. Virtsanäytteet viljelyä ja herkkyysmääritystä varten on otettava ennen hoidon lopettamista ja sen jälkeen. Jos bakteriuria jatkuu tai ilmaantuu uudelleen nitrofurantoiinikapseleiden (makrokiteiden) hoidon jälkeen, on valittava muita terapeuttisia aineita, joilla on laajempi kudosjakauma. Harkittaessa nitrofurantoiinikapselien (makrokiteiden) käyttöä, alhaisemmat eradikaatioluvut on suhteutettava lisääntyneeseen systeemisen toksisuuden ja mikrobilääkeresistenssin kehittymisen mahdollisuuteen, kun käytetään aineita, joilla on laajempi kudosjakauma.
YHTEENVETO:
Anuria, oliguria tai merkittävä munuaistoiminnan heikentyminen (kreatiniinipuhdistuma alle 60 ml minuutissa tai kliinisesti merkitsevästi kohonnut seerumin kreatiniinipitoisuus) ovat vasta-aiheita. Tämäntyyppisten potilaiden hoitoon liittyy lisääntynyt toksisuuden riski lääkkeen heikentyneen erittymisen vuoksi. Erytrosyyttien epäkypsistä entsyymijärjestelmistä (glutationin epävakaus) johtuvan hemolyyttisen anemian mahdollisuuden vuoksi lääke on vasta-aiheinen raskaana oleville potilaille tiineyden aikana (38-42 raskausviikolla), synnytyksen ja synnytyksen aikana tai kun synnytyksen käynnistyminen on lähellä. Samasta syystä lääke on vasta-aiheinen alle kuukauden ikäisille vastasyntyneille.
Nitrofurantoiinikapselit (makrokiteet) ovat vasta-aiheisia potilaille, joilla on aiemmin esiintynyt kolestaattista keltatautia/maksan toimintahäiriötä nitrofurantoiinin yhteydessä.
Nitrofurantoiinikapselit (makrokiteet) ovat vasta-aiheisia myös niille potilaille, joilla on tunnettu yliherkkyys nitrofurantoiinille.
VAROITUKSET:
Pulmonaaliset reaktiot:
AKUUTTEJA, SUBAKUUTTEJA TAI KROONISIA PULMONAARISIA REAKTIOITA ON HAVAINNOITTU POTILAILLA, JOILLA ON HALVAUTUNUT NITROFURANTOINIA. JOS NÄITÄ REAKTIOITA ILMENEE, NITROFURANTOIINI (MAKROKITEET) ON LOPETETTAVA JA RYHDYTTÄVÄ ASIANMUKAISIIN TOIMENPITEISIIN. RAPORTTIEN MUKAAN KEUHKOREAKTIOT OVAT OLLEET OSASYYNÄ KUOLEMAAN.
KROONISET KEUHKOREAKTIOT (DIFFUUSI INTERSTITIAALINEN PNEUMONIITTI TAI KEUHKOFIBROOSI TAI MOLEMMAT) VOIVAT KEHITTYÄ SALAKAVALASTI. NÄITÄ REAKTIOITA ESIINTYY HARVOIN JA YLEENSÄ POTILAILLA, JOTKA SAAVAT HOITOA KUUSI KUUKAUTTA TAI PIDEMPÄÄN. PITKÄAIKAISHOITOA SAAVIEN POTILAIDEN KEUHKOTILAN TARKKA SEURANTA ON PERUSTELTUA JA EDELLYTTÄÄ, ETTÄ HOIDON HYÖTYJÄ PUNNITAAN MAHDOLLISIA RISKEJÄ VASTAAN (KS. HENGITYSREAKTIOT).
Hepatotoksisuus:
Maksareaktioita, mukaan lukien hepatiitti, kolestaattinen keltaisuus, krooninen aktiivinen hepatiitti ja maksanekroosi, esiintyy harvoin. Kuolemantapauksia on raportoitu. Kroonisen aktiivisen hepatiitin puhkeaminen voi olla salakavalaa, ja potilaita on seurattava säännöllisesti sellaisten biokemiallisten testien muutosten varalta, jotka viittaisivat maksavaurioon. Jos hepatiittia esiintyy, lääke on poistettava välittömästi ja ryhdyttävä asianmukaisiin toimenpiteisiin.
Neuropatia:
Perifeeristä neuropatiaa, joka voi muuttua vaikeaksi tai peruuttamattomaksi, on esiintynyt. Kuolemantapauksia on raportoitu. Tilat, kuten munuaisten vajaatoiminta (kreatiniinipuhdistuma alle 60 ml minuutissa tai kliinisesti merkitsevästi kohonnut seerumin kreatiniini), anemia, diabetes mellitus, elektrolyyttitasapainon häiriö, B-vitamiinin puute ja invalidisoiva sairaus voivat lisätä perifeerisen neuropatian esiintymistä. Pitkäaikaista hoitoa saavia potilaita on seurattava säännöllisesti munuaistoiminnan muutosten varalta.
Optista neuriittia on raportoitu harvoin markkinoille tulon jälkeisessä kokemuksessa nitrofurantoiinivalmisteista.
Hemolyyttinen anemia:
Nitrofurantoiini on aiheuttanut primaakiiniherkkyystyyppistä hemolyyttistä anemiaa. Hemolyysi näyttää liittyvän glukoosi-6-fosfaattidehydrogenaasin puutteeseen sairastuneiden potilaiden punasoluissa. Tätä puutosta esiintyy 10 prosentilla mustista ja pienellä prosentilla Välimeren ja Lähi-idän alkuperää olevista etnisistä ryhmistä. Hemolyysi on indikaatio nitrofurantoiinin (makrokiteiden) lopettamiselle; hemolyysi lakkaa, kun lääke lopetetaan.
Clostridium difficileen liittyvä ripuli:
Clostridium difficileen liittyvää ripulia (CDAD, Clostridium difficile associated diarrhea) on raportoitu lähes kaikkien antibakteeristen lääkeaineiden, mukaan lukien nitrofurantoiinin, käytön yhteydessä, ja sen vaikeusaste voi vaihdella lievästä ripulista kuolemaan johtavaan paksusuolen tulehdukseen. Hoito antibakteerisilla aineilla muuttaa paksusuolen normaalia kasvistoa, mikä johtaa C. difficilen liikakasvuun.
C. difficile tuottaa toksiineja A ja B, jotka edistävät CDAD:n kehittymistä. Hypertoksiineja tuottavat C. difficile -kannat aiheuttavat lisääntynyttä sairastuvuutta ja kuolleisuutta, sillä nämä infektiot voivat olla vastustuskykyisiä mikrobilääkehoidolle ja vaatia kolektomian. CDAD on otettava huomioon kaikilla potilailla, joilla esiintyy ripulia antibioottien käytön jälkeen. Huolellinen anamneesi on tarpeen, koska CDAD:n on raportoitu esiintyvän yli kaksi kuukautta antibakteeristen aineiden antamisen jälkeen. Jos CDAD:tä epäillään tai se on vahvistettu, jatkuva antibioottien käyttö, jota ei ole suunnattu C. difficile -bakteeria vastaan, on ehkä lopetettava. Asianmukainen neste- ja elektrolyyttihoito, proteiinilisäys, C. difficilen antibioottihoito ja kirurginen arviointi on aloitettava kliinisten indikaatioiden mukaan.
EHDOTUKSET:
Tietoa potilaille:
Potilaita on neuvottava ottamaan nitrofurantoiini (makrokiteet) ruuan kanssa, jotta siedettävyys paranee entisestään ja lääkkeen imeytyminen tehostuu. Potilaita on ohjeistettava suorittamaan koko hoitojakso loppuun; heitä on kuitenkin kehotettava ottamaan yhteyttä lääkäriin, jos hoidon aikana ilmenee epätavallisia oireita.
Monet potilaat, jotka eivät siedä mikrokiteistä nitrofurantoiinia, pystyvät ottamaan nitrofurantoiinia (makrokiteitä) ilman pahoinvointia.
Potilaita on neuvottava olemaan käyttämättä magnesiumtrisilikaattia sisältäviä happamuudensäätövalmisteita nitrofurantoiinia (makrokiteitä) otettaessa.
Potilaita on neuvottava, että antibakteerisia lääkkeitä, mukaan lukien nitrofurantoiinia (makrokiteitä), saa käyttää vain bakteeri-infektioiden hoitoon. Niillä ei hoideta virusinfektioita (esim. flunssaa). Kun nitrofurantoiinia (makrokiteitä) määrätään bakteeri-infektion hoitoon, potilaille on kerrottava, että vaikka on tavallista, että olo paranee hoidon alkuvaiheessa, lääkitys on otettava täsmälleen ohjeiden mukaan. Annosten väliin jättäminen tai koko hoitojakson suorittamatta jättäminen voi (1) heikentää välittömän hoidon tehoa ja (2) lisätä todennäköisyyttä, että bakteerit kehittävät resistenssiä eivätkä ole tulevaisuudessa hoidettavissa nitrofurantoiinilla (makrokiteillä) tai muilla antibakteerilääkkeillä.
Ripuli on yleinen antibioottien aiheuttama ongelma, joka yleensä loppuu, kun antibiootti lopetetaan. Joskus antibioottihoidon aloittamisen jälkeen potilaille voi ilmaantua vetisiä ja verisiä ulosteita (vatsakouristusten ja kuumeen kanssa tai ilman niitä) jopa vielä kahden tai useamman kuukauden kuluttua viimeisen antibioottiannoksen ottamisesta. Jos näin tapahtuu, potilaiden on otettava yhteyttä lääkäriin mahdollisimman pian.
Yleistä:
Nitrofurantoiinin (makrokiteiden) määrääminen ilman todistettua tai vahvasti epäiltyä bakteeri-infektiota tai ennaltaehkäisevää käyttöaihetta ei todennäköisesti hyödytä potilasta ja lisää lääkkeelle vastustuskykyisten bakteerien kehittymisen riskiä.
Lääkeinteraktiot:
Magnesiumtrisilikaattia sisältävät antasidit, kun niitä annetaan samanaikaisesti nitrofurantoiinin kanssa, vähentävät sekä imeytymisnopeutta että -laajuutta. Tämän yhteisvaikutuksen mekanismina on todennäköisesti nitrofurantoiinin adsorptio magnesiumtrisilikaatin pinnalle.
Urikosuria aiheuttavat lääkkeet, kuten probenesidi ja sulfinpyratsoni, voivat estää nitrofurantoiinin munuaistubulaarista eritystä. Tästä johtuva nitrofurantoiinin seerumipitoisuuksien nousu voi lisätä toksisuutta, ja virtsan alentuneet pitoisuudet voivat heikentää sen tehoa virtsateiden antibakteerisena lääkkeenä.
Lääkkeen ja laboratoriotestien yhteisvaikutukset:
Nitrofurantoiinin läsnäolon seurauksena voi esiintyä väärän positiivinen reaktio glukoosin suhteen virtsassa. Tätä on havaittu Benedictin ja Fehlingin liuoksilla, mutta ei glukoosi-entsyymitestillä.
Karsinogeneesi, mutageenisuus, hedelmällisyyden heikentyminen:
Nitrofurantoiini ei ollut karsinogeeninen, kun sitä syötettiin naaraspuolisille Holtzman-rotille 44,5 viikon ajan tai naaraspuolisille Sprague-Dawley-rotille 75 viikon ajan. Kahdessa kroonisessa jyrsijöiden biotestissä, joissa käytettiin urospuolisia ja naaraspuolisia Sprague-Dawley-rotteja, ja kahdessa kroonisessa biotestissä sveitsiläisillä hiirillä ja BDF1-hiirillä ei havaittu viitteitä karsinogeenisuudesta.
Nitrofurantoiini esitti viitteitä karsinogeenisesta aktiivisuudesta naaraspuolisilla B6C3F1-hiirillä, mikä näkyi lisääntyneinä tubulaaristen adenoomien, hyvänlaatuisten sekakasvainten ja munasarjojen granuloosasolukudoskasvainten esiintyvyytenä. Urospuolisilla F344/N-rotilla esiintyi enemmän harvinaisia munuaisten tubulaarisia solukasvaimia, luun osteosarkoomia ja ihonalaisen kudoksen kasvaimia. Eräässä tutkimuksessa, jossa tiineille naarashiirille annettiin ihon alle 75 mg/kg nitrofurantoiinia, havaittiin F1-sukupolvessa keuhkojen papillaarisia adenoomia, joilla ei ollut merkitystä.
Nitrofurantoiinin on osoitettu aiheuttavan pistemutaatioita tietyissä Salmonella typhimurium -kannoissa ja eteenpäin suuntautuvia mutaatioita hiiren lymfoomasoluissa L5178Y. Nitrofurantoiini aiheutti lisääntyneitä sisarkromatidivaihtoja ja kromosomipoikkeavuuksia kiinalaisen hamsterin munasarjasoluissa mutta ei ihmisen soluissa viljelyssä. Sukupuoleen sidoksissa olevan resessiivisen letaalisuuskokeen tulokset Drosofiassa olivat negatiivisia, kun nitrofurantoiinia annettiin ruokintana tai injektiona. Nitrofurantoiini ei aiheuttanut periytyvää mutaatiota tutkituissa jyrsijämalleissa.
Karsinogeenisuus- ja mutageenisuuslöydösten merkitystä suhteessa nitrofurantoiinin terapeuttiseen käyttöön ihmisillä ei tunneta.
Suurten nitrofurantoiiniannosten antaminen rotille aiheuttaa tilapäisen spermatogeenisen pysähdyksen; tämä on palautuvaa, kun lääkkeen käyttö lopetetaan. Annokset 10 mg/kg/vrk tai suuremmat terveille ihmisuroksille voivat tietyissä ennalta arvaamattomissa tapauksissa aiheuttaa lievän tai keskivaikean spermatogeenisen pysähtymisen, johon liittyy siittiöiden määrän väheneminen.
Raskaus:
Teratogeeniset vaikutukset:
Raskausluokka B.
Kaneilla ja rotilla on tehty useita lisääntymistutkimuksia annoksilla, jotka ovat jopa kuusinkertaisia ihmisannokseen nähden, eikä niissä ole ilmennyt viitteitä hedelmällisyyden heikkenemisestä tai nitrofurantoiinin sikiölle aiheuttamista haitoista. Yhdessä julkaistussa tutkimuksessa, joka tehtiin hiirillä 68-kertaisella annoksella ihmisannokseen verrattuna (perustuen emolle annettuun mg/kg), havaittiin kasvun hidastumista ja pienten ja yleisten epämuodostumien vähäistä esiintyvyyttä. Sikiön epämuodostumia ei kuitenkaan havaittu 25-kertaisella annoksella ihmisannokseen nähden; näiden havaintojen merkityksestä ihmisiin ei ole varmuutta. Riittäviä ja hyvin kontrolloituja tutkimuksia raskaana olevilla naisilla ei kuitenkaan ole. Koska eläimillä tehdyt lisääntymistutkimukset eivät aina ennusta ihmisen vastetta, tätä lääkettä tulisi käyttää raskauden aikana vain, jos se on selvästi tarpeen.
Ei-teratogeeniset vaikutukset:
Yhdessä julkaistussa transplacentaalista karsinogeenisuutta koskeneessa tutkimuksessa osoitettiin nitrofurantoiinin aiheuttavan F1-sukupolven hiirillä keuhkojen papillaarisia adenoomia annoksilla, jotka olivat 19-kertaisia mg/kg:n annokseen verrattuna. Tämän havainnon suhdetta ihmisen mahdolliseen karsinogeneesiin ei tällä hetkellä tiedetä. Koska näiden eläintietojen vaikutuksista ihmisiin ei ole varmuutta, tätä lääkettä tulee käyttää raskauden aikana vain, jos se on selvästi tarpeen.
Synnytys:
Katso vasta-aiheet.
Synnyttävät äidit:
Nitrofurantoiinia on havaittu ihmisen äidinmaidossa pieniä määriä. Koska nitrofurantoiini voi aiheuttaa vakavia haittavaikutuksia alle kuukauden ikäisille imettäville imeväisille, on päätettävä imetyksen keskeyttämisestä tai lääkkeen lopettamisesta ottaen huomioon lääkkeen merkitys äidille (ks. vasta-aiheet).
Pediatrinen käyttö:
Nitrofurantoiini (makrokide) on vasta-aiheinen alle kuukauden ikäisille imeväisille (ks. vasta-aiheet).
Geriatrinen käyttö:
Nitrofurantoiini (makrokide) -valmisteen kliinisiin tutkimuksiin ei sisältynyt riittävää määrää yli 65-vuotiaita koehenkilöitä, jotta olisi voitu määritellä, reagoivatko he eri tavalla kuin nuoremmat. Muissa raportoiduissa kliinisissä kokemuksissa ei ole havaittu eroja vasteissa iäkkäiden ja nuorempien potilaiden välillä. Spontaanien raporttien mukaan keuhkoreaktioiden, mukaan lukien kuolemaan johtaneet reaktiot, osuus on suurempi iäkkäillä potilailla; nämä erot näyttävät liittyvän siihen, että pitkäaikaista nitrofurantoiinihoitoa saavien iäkkäiden potilaiden osuus on suurempi. Kuten nuoremmilla potilailla, kroonisia keuhkoreaktioita havaitaan yleensä potilailla, jotka saavat hoitoa kuusi kuukautta tai pidempään (ks. VAROITUKSET). Spontaanit raportit viittaavat myös vakavien maksareaktioiden, mukaan lukien kuolemaan johtaneet reaktiot, lisääntyneeseen osuuteen iäkkäillä potilailla (ks. VAROITUKSET).
Yleisesti heikentyneen maksan, munuaisten tai sydämen toiminnan sekä samanaikaisen sairauden tai muun lääkehoidon suurempi esiintymistiheys on otettava huomioon nitrofurantoiinia (makrokiteetit) määrättäessä. Tämän lääkkeen tiedetään erittyvän merkittävästi munuaisten kautta, ja tämän lääkkeen aiheuttamien toksisten reaktioiden riski voi olla suurempi potilailla, joiden munuaisten toiminta on heikentynyt. Anuria, oliguria tai merkittävä munuaistoiminnan heikkeneminen (kreatiniinipuhdistuma alle 60 ml minuutissa tai kliinisesti merkitsevästi kohonnut seerumin kreatiniini) ovat vasta-aiheita (ks. vasta-aiheet). Koska iäkkäillä potilailla munuaistoiminta on todennäköisemmin heikentynyt, annoksen valinnassa on noudatettava varovaisuutta, ja munuaistoiminnan seuranta voi olla hyödyllistä. HUONOVOINTISUUS, RASITUKSEEN LIITTYVÄ HENGENAHDISTUS, YSKÄ JA MUUTTUNUT KEUHKOJEN TOIMINTA OVAT YLEISIÄ OIREITA, JOTKA VOIVAT ILMAANTUA SALAKAVALASTI. DIFFUUSIN INTERSTITIAALISEN PNEUMONIITIN TAI FIBROOSIN TAI MOLEMPIEN RADIOLOGISET JA HISTOLOGISET LÖYDÖKSET OVAT MYÖS YLEISIÄ KROONISEN KEUHKOREAKTION ILMENEMISMUOTOJA. KUUMETTA ESIINTYY HARVOIN.
KROONISTEN KEUHKOREAKTIOIDEN VAKAVUUS JA NIIDEN HÄVIÄMISASTE NÄYTTÄVÄT OLEVAN YHTEYDESSÄ HOIDON KESTOON ENSIMMÄISTEN KLIINISTEN OIREIDEN ILMAANTUMISEN JÄLKEEN. KEUHKOJEN TOIMINTA VOI OLLA PYSYVÄSTI HEIKENTYNYT MYÖS HOIDON LOPETTAMISEN JÄLKEEN. RISKI ON SUUREMPI, JOS KROONISIA KEUHKOREAKTIIVISIA REAKTIOITA EI TUNNISTETA AIKAISESTI.
Subakuuteissa keuhkoreaktioissa kuumetta ja eosinofiliaa esiintyy harvemmin kuin akuutissa muodossa. Hoidon lopettamisen jälkeen toipuminen voi vaatia useita kuukausia. Jos oireita ei tunnisteta lääkkeeseen liittyviksi eikä nitrofurantoiinihoitoa lopeteta, oireet voivat pahentua.
Akuutit keuhkoreaktiot ilmenevät tavallisesti kuumeena, vilunväristyksinä, yskänä, rintakipuna, hengenahdistuksena, keuhkoinfiltraationa, johon liittyy konsolidaatiota tai keuhkopussin effuusiota röntgenkuvassa, ja eosinofiliana. Akuutit reaktiot ilmaantuvat yleensä ensimmäisen hoitoviikon aikana, ja ne ovat palautuvia, kun hoito lopetetaan. Ratkaisu on usein dramaattinen (ks. VAROITUKSET).
Muutokset EKG:ssä (esim, epäspesifiset ST/T-aaltomuutokset, kimpunhaaralohko) on raportoitu keuhkoreaktioiden yhteydessä.
Syanoosia on raportoitu harvoin.
Hepatiitti:
Hepatiittisia reaktioita, mukaan lukien hepatiitti, kolestaattinen keltaisuus, krooninen aktiivinen hepatiitti ja maksanekroosi, on esiintynyt harvoin (ks. VAROITUKSET).
Neurologinen:
Perifeeristä neuropatiaa, joka voi muuttua vaikeaksi tai palautumattomaksi, on esiintynyt. Kuolemantapauksia on raportoitu. Tilat, kuten munuaisten vajaatoiminta (kreatiniinipuhdistuma alle 60 ml minuutissa tai kliinisesti merkitsevästi kohonnut seerumin kreatiniini), anemia, diabetes mellitus, elektrolyyttitasapainon häiriö, B-vitamiinin puutos ja invalidisoivat sairaudet voivat lisätä perifeerisen neuropatian mahdollisuutta (ks. Varoitukset).
Nitrofurantoiinin käytön yhteydessä on raportoitu myös asteniaa, huimausta, nystagmusta, huimausta, päänsärkyä ja uneliaisuutta.
Harvoin on raportoitu hyvänlaatuista kallonsisäistä hypertensiota (pseudotumor cerebri), sekavuutta, masennusta, näköhermotulehdusta ja psykoottisia reaktioita. Hyvänlaatuisen kallonsisäisen hypertension merkkinä vauvoilla esiintyviä pullistuneita fontanelleja on raportoitu harvoin.
Dermatologiset:
Exfoliatiivista dermatiittia ja erythema multiformea (mukaan lukien Stevens-Johnsonin oireyhtymä) on raportoitu harvoin. Myös ohimenevää hiustenlähtöä on raportoitu.
Allergiset:
Lupuksen kaltaista oireyhtymää, johon liittyy keuhkoreaktioita nitrofurantoiinille, on raportoitu. Myös angioedeemaa; makulopapulaarisia, erytemaattisia tai ekseemaattisia ihottumia; kutinaa; urtikariaa; anafylaksiaa; niveltulehdusta; nivelkipua; myalgiaa; lääkekuumetta; vilunväristyksiä; ja vaskuliittia (joskus keuhkoreaktioihin liittyen) on raportoitu. Yliherkkyysreaktiot ovat yleisimpiä spontaanisti raportoituja haittavaikutuksia maailmanlaajuisessa markkinoille tulon jälkeisessä kokemuksessa nitrofurantoiinivalmisteista.
Ruokatorvi:
Yökkäys, oksentelu ja anoreksia esiintyvät useimmiten. Vatsakipu ja ripuli ovat harvinaisempia ruoansulatuskanavan reaktioita. Nämä annokseen liittyvät reaktiot voidaan minimoida pienentämällä annosta. Sialadeniittia ja haimatulehdusta on raportoitu. Nitrofurantoiinin käytön yhteydessä on raportoitu satunnaisesti pseudomembranoottista koliittia. Pseudomembranoottisen koliitin oireiden puhkeaminen voi tapahtua mikrobilääkehoidon aikana tai sen jälkeen (ks. VAROITUKSET).
Hematologiset:
Methemoglobinemiasta johtuvaa sekundaarista syanoosia on raportoitu harvoin.
Muut:
Muut:
Kuten muittenkin mikrobilääkkeiden kohdalla, vastustuskykyisten mikrobilääkkeille alttiiden organismeja aiheuttamat superinfektiot, esim, Pseudomonas- tai Candida-lajit, voi esiintyä.
Laboratorion haittavaikutukset:
Nitrofurantoiinin käytön yhteydessä on raportoitu seuraavia laboratorion haittavaikutuksia: kohonnut AST (SGOT), kohonnut ALT (SGPT), alentunut hemoglobiini, kohonnut seerumin fosfori, eosinofilia, glukoosi-6-fosfaattidehydrogenaasin puutosanemia (ks. VAROITUKSET), agranulosytoosi, leukopenia, granulosytopenia, hemolyyttinen anemia, trombosytopenia, megaloblastinen anemia. Useimmissa tapauksissa nämä hematologiset poikkeavuudet hävisivät hoidon lopettamisen jälkeen. Aplastista anemiaa on raportoitu harvoin.
Yliannostus
Nitrofurantoiinin (makrokiteiden) akuutin yliannostuksen satunnaiset tapaukset eivät ole johtaneet mihinkään muihin erityisiin oireisiin kuin oksenteluun. Emeesin indusoiminen on suositeltavaa. Spesifistä vastalääkettä ei ole, mutta runsasta nesteen saantia on ylläpidettävä lääkkeen erittymisen edistämiseksi virtsaan. Se on dialysoitavissa.
ANNOSTUS JA ANNOSTUS:
Nitrofurantoiinikapselit (makrokiteet) tulee antaa ruuan kanssa lääkkeen imeytymisen ja joillakin potilailla siedon parantamiseksi.
Aikuiset:
50 mg-100 mg neljä kertaa vuorokaudessa — alempaa annostustasoa suositellaan komplisoitumattomiin virtsatieinfektioihin.
Pediatriset potilaat:
5-7 mg painokiloa kohti vuorokaudessa, annettuna neljänä jaettuna annoksena (vasta-aiheinen alle kuukauden iässä).
Hoitoa on jatkettava viikon ajan tai vähintään 3 vuorokautta virtsan steriiliyden saavuttamisen jälkeen. Infektion jatkuminen viittaa uudelleenarvioinnin tarpeeseen.
Aikuisten pitkäaikaisessa suppressiivisessa hoidossa annoksen pienentäminen 50-100 mg:aan nukkumaanmenoaikana voi olla riittävä. Pediatristen potilaiden pitkäaikaiseen suppressiiviseen hoitoon voivat olla riittäviä annokset, jotka ovat niinkin pieniä kuin 1 mg/kg vuorokaudessa annettuna kerta-annoksena tai kahtena jaettuna annoksena. Ks. kohta VAROITUKSET PITKÄAIKAISEEN HOITOON LIITTYVIÄ RISKEJÄ KOSKEVAT VAROTOIMET.
KÄYTTÖTARVIKKEET:
Nitrofurantoiinikapseleita USP (makrokiteet) on saatavana seuraavasti:
50 mg:n läpinäkymätön, valkoinen runko ja läpinäkymätön, keltainen korkki, jossa on mustalla musteella tehty painatus, jossa on merkinnät ”WATSON” korkissa ja ”5780” rungossa.
NDC 0115-2023-10 pulloa 100
100 mg läpinäkymätön, keltainen kapseli, johon on painettu mustalla musteella ”WATSON” korkissa ja ”5781” rungossa.
NDC 0115-2024-10 pulloa, 100 kpl
Säilytä 20°-25°C (68°-77°F) .
Valmistaja:
Watson Pharma Private Limited
Verna, Salcette Goa 403722 INDIA
Jälleenmyyjä:
Amneal Pharmaceuticals LLC
Bridgewater, NJ 08807
Jos haluat ilmoittaa Epäillyistä haittavaikutuksista, ota yhteyttä Amneal Pharmaceuticalsiin numeroon 1-877-835-5472 tai FDA:han numeroon 1-800-FDA-1088 tai www.fda.gov/medwatch.
Rev. 11-2019-00
VALMISTELUPÄÄLLIKKÖ – 50 mg

VALMISTELUPÄÄLLIKKÖ – 50 mg

VALMISTELUPÄÄLLIKKÖ – 50 mg 100 mg

| NITROFURANTOIN nitrofurantoiinikapseli |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Labeler – Amneal Pharmaceuticals of New York LLC (123797875)
Amneal Pharmaceuticals of New York LLC
Tiheästi kysyttyjä kysymyksiä
Lisätietoa nitrofurantoiinista
Kuluttajan resurssit
Ammattilaisen resurssit
Muut tuotemerkit Macrobid, Makrodantin, Furadantin Seuraavat hoito-oppaat
Lääketieteellinen vastuuvapauslauseke |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||