Kammiovärinä (AF) on yleisin jatkuva takyarytmihäiriö, jota esiintyy 1-2 prosentilla väestöstä. Keuhkovaltimoiden eristys (PVI) on AF-ablaation tärkein tukipilari.1 Vaikka tämä toimenpide on tehokas estämään rytmihäiriön uusiutumista potilailla, joilla on paroksismaalinen AF, jos se tehdään yksin, sillä on vain rajallinen menestys pysyvän AF:n hoidossa.1,2 Alkuperäiset tiedot viittasivat siihen, että rytmihäiriön uusiutumista voitaisiin vähentää ylimääräisellä linja-ablaatiolla tai monimutkaisella fraktioidulla eteiselektrogrammaablaatiolla. Metaanalyysien3 ja satunnaistettujen kontrolloitujen tutkimusten4 viimeaikaiset tulokset eivät kuitenkaan ole vahvistaneet PVI:n jälkeisen lisäablaation hyötyä, mikä korostaa pysyvän PVI:n merkitystä myös pysyvän AF:n hoidossa.
Viime vuosina kryoballooni-ablaatiosta on tullut varteenotettava vaihtoehtoinen lähestymistapa radiotaajuusablaatiolle, ja se on osoittautunut vähintään yhtä tehokkaaksi kuin PVI potilailla, joilla on paroksismaalinen AF. FIRE & ICE-tutkimuksen viimeaikaiset tulokset ovat lopullisesti ratkaisseet tämän alan keskustelun.5 Lisäksi tämän toimenpiteen suhteellisen yksinkertaisuuden, nopeamman oppimiskäyrän -ja mikä ehkä vielä tärkeämpää- huomattavan toistettavuuden6 vuoksi se on otettu laajalti käyttöön kliinisessä käytännössä.6
Toisaalta pysyvän AF:n toimenpidehoito on edelleen haastavaa: tätä lähestymistapaa ei ole standardoitu tai täydellistetty, ja innovaatiolle on tilaa. Tässä tilanteessa kysymys kryoablaation mahdollisesta roolista on mielenkiintoinen.
KLIINISET TODISTUKSET
Vaikka kiinnostus AF-ablaation tehokkuuteen pysyvää AF:ää sairastavilla potilailla on lisääntymässä, seurantatietoja uuden 28 mm:n toisen sukupolven kryoablaatiokatetrin (Arctic Front Advance, Medtronic Inc., Minneapolis, MN) käyttämisen jälkeisestä seurannasta on vielä vähän. Tähän mennessä kryoballoniablaation jälkeisiä tuloksia persistoivan AF:n hoidossa on arvioitu epäsuorasti meta-analyyseissä, satunnaistamattomissa vertailuissa7 ja havainnointitutkimuksissa.8-10
Ciconte ym.9 raportoivat, että 60 %:lla persistoivaa AF:ää sairastavista potilaista ei esiintynyt eteisperäistä rytmihäiriötä hoidon jälkeen uudella kryoballoni-katetrilla. Pysyvän AF:n kesto, joka oli riippumaton rytmihäiriöiden uusiutumisen ennustaja seurannan aikana, antaa selkeää tukea ablaatiolle taudin varhaisemmissa vaiheissa.
Retrospektiivisessä tutkimuksessa, johon osallistui 48 potilasta, joilla oli pysyvä AF, yhden vuoden kliininen onnistumisprosentti oli 69 %.10
Toisessa yksihaaraisessa tutkimuksessa arvioitiin toisen sukupolven kryoablaation tehokkuutta indeksitoimenpiteenä 100 pysyvän AF-potilaan ryhmässä (keskimääräinen kesto 5,5 ± 3,7 kuukautta).8 Keskimääräisen 10,6 ± 6,3 kuukauden seurannan jälkeen eteisperäistä rytmihäiriötä ei ollut uusiutunut 67 %:lla potilaista kolmen kuukauden tyhjentämisjakson jälkeen. Ainoa merkittävä riippumaton ennustaja uusiutumiselle oli eteisperäisen takyarytmian esiintyminen tyhjentämisjakson aikana.
Yksittäisessä keskitetyssä, ei-prospektiivisessa, ei-satunnaistetussa tutkimuksessa arvioitiin myös RF:n käyttöä verrattuna kryoablaatioon vain pysyvän AF:n potilailla.7 Kyseisessä tutkimuksessa arvioitiin RF-ablaation (käyttäen kontaktivoimaablaatiokatetria) ja kryoablaation (käyttäen 28 mm:n toisen sukupolven kryopalloa) toimenpidetulosta 100 potilaan kohortissa, joilla oli lääkkeille refraktorinen persistentti AF (AF:n keskimääräinen kesto oli RF-ablaatio- ja kryoablaatioryhmissä 7,2 ja 7,6 kuukautta). Sekä toimenpide- että läpivalaisuaika olivat merkittävästi lyhyempiä kryoablaatioryhmässä, mutta eteisrytmihäiriöistä vapaiden potilaiden osuus oli samankaltainen molemmissa ryhmissä 12 kuukauden seurannan jälkeen (60 % kryoablaatioryhmässä vs. 56 % RF-ablaatioryhmässä, P = .71). Monimuuttuja-analyysissä ainoiksi riippumattomiksi epäonnistumisen ennustetekijöiksi osoittautuivat jälleen pysyvän AF:n kesto ja uusiutumiset tyhjentämisjakson aikana.
Viimeisessä prospektiivisessa, monikeskuksisessa, satunnaistamattomassa tutkimuksessa verrattiin yhden ablaatiomenetelmän jälkeisiä tuloksia, joissa käytettiin ensimmäisen sukupolven kryopallokuuablaatiota pelkkää PVI:n poistoa varten vs. avoimmunoidulla RF-ablaatiolla vaiheittaisen lähestymistavan avulla kohortissa, johon kuului potilaita, joilla oli pysyvän AF:n aiheuttama persistentti AF. 11 Tulokset, jotka osoittivat noin 55 prosentin vapautta eteisperäisistä rytmihäiriöistä keskimäärin 15,6 ± 11,5 kuukauden seurannassa yksittäisen ablaation jälkeen sekä kryoballoonilla että RF-ablaatiolla, olivat samankaltaisia kuin käytettävissä olevat tiedot. Useat havainnot olivat huomionarvoisia:
- –
Ensiksi, kliiniset tulokset olivat samankaltaisia molemmissa hoitohaaroissa, vaikka RF-ryhmässä tehtiin PVI:n lisäksi muita ja laajempia ablaatioita kuin PVI.
- –
Toiseksi, komplikaatioiden määrä oli samankaltainen kahdella tekniikalla.
- –
Kolmanneksi toimenpiteen kesto oli lyhyempi kryoablaatiolla.
Pysyvän AF:n ablaation patofysiologiasta ja optimaalisesta strategiasta ei ole vielä varmuutta, minkä vuoksi tämän hoidon peruspilarina on edelleen pysyvän PVI:n saavuttaminen.4 Tämän saavuttamiseksi kryoablaatio näyttäisi olevan pätevä vaihtoehtoinen terapeuttinen lähestymistapa RF:lle. PVI:n lisäksi tehtävään lisäablaatioon liittyy pidempi toimenpideaika.4 Koska RF-ablaatiomenetelmää ei ole standardoitu (suurimmalle osalle RF-haarassa olleista potilaista kehittyi lisäleesioita), on epäselvää, johtuvatko tulokset energialähteestä vai ablaatiostrategiasta. Lisäksi keskipitkän aikavälin tuloksia ei näytä merkittävästi parantavan PVI:n lisäksi tehdyt ylimääräiset biatriumleesiot pysyvää AF:ää sairastavilla potilailla.4
SHOOTING AT THE RIGHT TARGET?
Syyt siihen, että lisäablaatio ei ole lisännyt hyötyjä, ovat vielä selvittämättä. Yksi mahdollisuus on laajempaan ablaatioon perustuvan substraattilähestymistavan iatrogeeninen potentiaali, joka saattaa suosia uusien rytmihäiriöalueiden kehittymistä epätäydellisesti abloidun kudoksen tai epätäydellisten johtumissalpausten vuoksi. Toinen mahdollisuus on, että syyllinen alue ei ole rutiininomaisesti tunnistettu, eivätkä monimutkaiset fraktioidut eteiselektrogrammit tai lineaariset leesiot ole optimaalisia täydentäviä kohteita ablaatiota varten.12 Tässä hypoteesissa on edelleen tarve paikantaa myrskyn silmä (kohdistamalla toimenpiteet roottoreihin tai ganglioihin)13 , mahdollisesti käyttämällä uudempia kartoitusalgoritmeja. Käytettävissä olevat tiedot tukevat myös AF:n keston ja siten AF:n sähköisen uudelleenmuodostuksen (AF synnyttää AF:n) merkitystä, koska vain AF:n kesto oli riippumaton rytmihäiriöiden uusiutumisen ennustaja propensity-score-vertailussa,11 kuten Tilz ym. ovat aiemmin raportoineet.2
Monet meneillään olevat tutkimukset auttavat selvittämään kryoablaatiokäsittelyn turvallisuutta ja tehokkuutta pysyvää AF:ää sairastavilla potilailla. Cryoballoon Ablation for Early Persistent Atrial Fibrillation -tutkimus (Cryo4 Persistent AF – NCT02213731) on eurooppalainen monikeskuksinen, prospektiivinen, yksihaarainen pilottitutkimus, jonka tavoitteena on arvioida pelkällä kryoablaatiolla toteutetun PVI:n onnistumisprosenttia yhden vuoden kuluttua potilailla, joilla on alle 12 kuukautta jatkunut jatkuva AF. Tutkimus on edelleen rekrytointivaiheessa, ja ensimmäisiä tuloksia odotetaan vuoden 2017 loppuun mennessä. Seuraavana tavoitteena on verrata tuloksia satunnaistetussa tutkimuksessa RF:n vaiheittaisen lähestymistavan ja PVI:n kryoablaation välillä homogeenisessa potilasryhmässä, jolla on jatkuva AF. Tämän laajamittaisen satunnaistetun tutkimuksen tuloksia odotetaan innolla.
PERUSTEET JA RAJOITUKSET
Pysyvää AF:ää sairastavilla potilailla suurimmatkin PV:n maksimihalkaisijat (20 mm:n ja 23 mm:n välillä) ovat huomattavasti alhaisemmat kuin kriittinen 28 mm:n arvo (kliinisessä rutiinikäytännössäkin käytettävän kryopallon maksimihalkaisija).14 Tämän pallon ja PV:n halkaisijoiden välisen epäsuhdan vuoksi, kun tämä laite asetetaan PV-antrumia vasten, sen jäähdytysosa on kosketuksissa sekä PV-antrumin että viereisen eteiskudoksen kanssa, mikä näyttää olevan tämän toimenpiteen tärkeä etu. Kenigsberg ym.15 laskivat PV:n kryoablaation jälkeen abloitavan sydänkudoksen pinta-alan vasemman eteisen kryoablaation jälkeisellä kolmiulotteisella elektroanatomisella jännitekartoituksella. Tätä menetelmää käyttäen nämä kirjoittajat osoittivat hienosti, että 28 mm:n kryopallolaitteella tehdyn kryoablaation jälkeen sähköisesti ehjäksi jääneen vasemman eteisen takaseinämän pinnan prosenttiosuus oli vain 27 %.
Huomattakoon, että vaikka kryopallolaite käsitteellisesti kohdistuu vain PV:iin, se tekee myös merkittävää sähköistä poistoa vasemman eteisen takaseinämässä (kuva). Laajentamalla jäähdytysalueen ympärysmittaa tämä laite voi antaa lisähyötyä ablatoimalla paikallisia tekijöitä rakenteissa, jotka vaikuttavat AF:n laukaisemiseen ja ylläpitämiseen, kuten ganglioniset pleksit ja roottorit, millä on mahdollisesti merkittäviä terapeuttisia vaikutuksia potilailla, joilla on pysyvää AF:ää13. Tämä ominaisuus voisi myös selittää ainakin osittain edellä mainittujen tutkimusten tulokset.
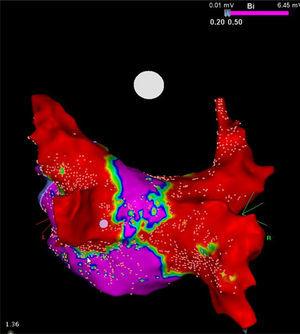
High-density-jännitekartta takaseinämästä kryoablaatiotoimenpiteen jälkeen potilaalla, jolla on jatkuva eteisvärinä. Huomaa molempien suurten arpien (punainen) väliin jäävä kapea käytävä (violetti), joka on saatu 28 mm:n Artic Front Advance -kryopallolla (Medtronic, Minneapolis, MN, Yhdysvallat). Prof. Mario Oliveira, Santa Martan sairaala, Lissabon, Portugali.
Vaikka kryoballoonien onnistumisprosentit ovat vertailukelpoisia RF:n onnistumisprosenttien kanssa ei-satunnaistetuissa tutkimuksissa potilailla, joilla on pysyvää AF:ää, rytmihäiriöiden uusiutumisprosentin suhteellisen korkea osuus molemmissa ryhmissä on edelleen selittämättä, ja se ei ehkä johdu ainoastaan PV:n johtumisen palautumisesta. Tämä mahdollisuus on mainittu tutkimuksissa, jotka herättävät huolta muiden kuin PVI-lähteiden roolista uusiutumisen mekanismina.9
Pysyvän AF:n invasiivinen hoito on edelleen haastavaa sen monimuotoisen patofysiologian vuoksi. Tarvitaan uusia mekanistisia oivalluksia, jotta pysyvän AF:n hoitoon voidaan soveltaa yksilöllisesti räätälöityä lähestymistapaa, mutta siihen asti, kunnes tällaista tietoa on saatavilla, ensivaiheen itsenäinen PVI saattaa olla riittävä ainakin potilaille, joilla on vähemmän vaikea pysyvä AF. Tämän ”vähemmän on enemmän” -lähestymistavan perusteella kryoballoonip PVI voi osoittautua riittäväksi ablaatiostrategiaksi pysyvän AF:n hoidossa, sillä se mahdollistaa luotettavan PVI:n ja siihen liittyvän viereisen eteislihaksen sydänlihaksen poiston. Lisäsubstraatin muokkaamisesta ei näytä olevan lisähyötyä. Tämä ”minimalistinen” menettely on hyväksyttävä ensimmäinen vaihtoehto potilaille, joilla on suhteellisen äskettäin ilmennyt oireinen jatkuva AF, eli joilla on ”enemmän laukaisijaa kuin substraattia” (tai joiden substraatti on keskittynyt PV:n ostian ympärille…). Suurella (28 mm) toisen sukupolven kryopallolla saadaan todellakin samanlaisia tuloksia kuin monimutkaisemmilla toimenpiteillä, joissa käytetään RF-energiaa ja kehittyneitä menetelmiä. Huomattakoon, että oppimiskäyrä, toistettavuus ja turvallisuus näyttävät puoltavan kryopallolaitteen käyttöä vähemmän kokeneissa käsissä. Tässä tilanteessa ja edellä mainitussa potilaiden alaryhmässä PVI suurella toisen sukupolven kryoballoonilla näyttää olevan järkevä alkuvaiheen lähestymistapa, joka parantaa merkittävästi yli puolet potilaista. Potilaille, joilla AF on uusiutunut, tämä ensimmäinen toimenpide ei ole hyödytön. Huomattavassa määrässä substraattia (oikean ja vasemman PV-antran ympärillä), joka on jo hoidettu, toisessa toimenpiteessä, tällä kertaa RF:llä, keskitytään nimittäin pääasiassa PV:n ulkopuolisiin polttopisteisiin, fragmentoituneisiin potentiaaleihin, mikro- tai makroreentranttipiireihin jne.
Käsityksemme mukaan tämä kaksivaiheinen strategia on yhteensopiva pienen ja keskisuuren volyymin keskusten kanssa, jotka keskittyvät pääasiassa PVI:hen ja työskentelevät yhdessä monimutkaisempien menettelyjen suorittamisesta vastaavien korkea-asteen lähetteiden keskusten kanssa. Jälkimmäiset joutuvat käsittelemään niitä noin 40 % potilaista, joilla on uusiutumia ensimmäisen ”kryo-tyhjennyksen” jälkeen.
”Vähemmän on enemmän”, mutta se ei silti riitä…
CONFLICTS OF INTEREST
S. Boveda saa konsulttipalkkioita Medtronicilta, Boston Scientificiltä ja Livanovalta.