Miten elämä alkoi maapallolla? Miten nuorella, kivisellä planeetalla kemikaalit saattoivat yhdistyä juuri oikealla tavalla muodostaakseen ensimmäiset solut? Miten nämä alkukantaiset solut alkoivat käyttäytyä elämän tavoin: kasvaa, jakautua ja siirtää edullisia ominaisuuksia seuraavalle sukupolvelle?
Leämän synty on erityisen hämärän peitossa, koska geologiset tallenteet – kivikerrokset ja niihin upotetut fossiilit, jotka sisältävät vihjeitä maapallon ja elämän historiasta – katoavat noin 3,9 miljardia vuotta sitten, kun planeetan kuoren liikkeet pyyhkivät ne pois. Tämän seurauksena tutkijoilla ei ole suoria todisteita maapallon alkuaikojen olosuhteista, mukaan lukien todisteet molekyyleistä, jotka ovat saattaneet pyöriä alkulammikoissa ja muodostaa elämän rakennusaineita.
Tämä herättää paljon kysymyksiä, juuri sellaisia suuria kysymyksiä, joihin Jack Szostak on kiinnostunut. Hän ja muut uskovat voivansa rekonstruoida laboratoriossa pitkän polun, joka johti avaruuden kemikaaleista Maan muodostumiseen, planeetan elämää edeltävään kemiaan, varhaisiin protosoluihin ja lopulta kehittyneisiin soluihin, joissa on aineenvaihdunta ja proteiinisynteesi. Tällaiset laajat tutkimukset vaativat asiantuntemusta monilta aloilta, kuten kemiasta ja biokemiasta, geologiasta ja geofysiikasta sekä tähtitieteestä.
Szostak (lausutaan shah-stak) saattaa olla ihanteellinen henkilö etsimään vastauksia. Nobel-palkittu, Harvardin lääketieteellisen tiedekunnan genetiikan professori, kemian ja kemiallisen biologian professori humanistisessa ja luonnontieteellisessä tiedekunnassa, Massachusetts General Hospitalin (MGH) Rich Distinguished Investigator ja Howard Hughes Medical Institute -tutkija, jota muut kuvaavat nerokkaaksi ja motivoituneeksi tiedemieheksi. Mutta hänet tunnetaan myös lempeästä nöyryydestään, johon kuuluu halukkuus sukeltaa syvälle hänelle uusiin aiheisiin, sekä kollegiaalisuudestaan ja siitä, että hän auttaa edistämään ideoiden vaihtoa, joka vie tiedettä eteenpäin.
Hänen oma tutkimuksensa keskittyy elämän syntyprosessin yhteen osaan: protosoluun, ”todella, todella yksinkertaiseen alkusoluun, joka saattoi muodostua kemikaaleista, joita oli olemassa jo varhaisessa vaiheessa maapallon pinnalla”, Szostak kertoo. Hän toivoo voivansa ymmärtää, miten se kasvaisi ja jakautuisi, alkaisi monistua ja lopulta kehittyisi. ”Emme ehkä tiedä, mitä oikeasti tapahtui, mutta ehkä voimme selvittää erilaisia mahdollisia reittejä”, hän sanoo. ”Voimme vain yrittää koota laboratoriossa asioita, jotka vaikuttavat uskottavilta.”
”Suunnattu evoluutio”
Tänään elokuussa Szostak täytti neljäkymmentä vuotta Harvardissa ja kolmekymmentäviisi vuotta MGH:ssa (jossa hänen laboratorionsa sijaitsee). Hänen laboratorionsa teki 1980-luvulla hiivakokeita ymmärtääkseen DNA:n rekombinaation genetiikkaa ja biokemiaa – työ, joka johti kaksoissäikeen katkeamisen korjausmalliin, joka kuvaa sitä, miten pitkät DNA-säikeet katkeavat, vaihtavat segmenttejä ja yhdistyvät sitten uudelleen. Tämä johti myöhempiin tutkimuksiin, jotka koskivat rekombinaatiomekanismia meioosin eli siittiöiden ja munasolujen syntyyn johtavan solunjakautumisen aikana.
Samana aikana hänen tutkimusryhmänsä teki myös tärkeitä löytöjä telomeereistä – kromosomien päissä olevista suojapäällysteistä, jotka varmistavat DNA:n oikean monistumisen solujen jakautuessa. Tästä tutkimuksesta Szostak sai myöhemmin vuoden 2009 fysiologian tai lääketieteen Nobel-palkinnon, jonka hän jakoi tutkijoiden Elizabeth Blackburnin, Sc.D. ’06, joka on nykyään UC:n emerita San Franciscossa, ja Carol Greiderin, Johns Hopkinsin yliopistosta, kanssa.
Kun Szostak sai puhelinsoiton Ruotsista varhain aamulla lokakuussa 2009, hän oli jo käyttänyt yli 20 vuotta perustavanlaatuisen panoksen tekemiseen muillakin tieteenaloilla. Telomeerilöytöjen jälkeen 1980-luvun puolivälissä (tutkimus yhdisti lyhentyneet telomeerit moniin ikääntymiseen liittyviin sairauksiin) monet tutkijat tulivat alalle, ja Szostak päätti vaihtaa suuntaa. ”Oli melko selvää, mitä seuraavien kokeiden piti olla, ja tuntui siltä, että kaikki, mitä teimme, tehtäisiin joka tapauksessa”, hän muisteli. ”En ole koskaan ollut sitä mieltä, että on paljon järkeä tehdä asioita, jotka tehtäisiin joka tapauksessa. Se sai minut todella katselemaan ympärilleni ja miettimään, millaisia muita tieteellisiä kysymyksiä voisin ryhtyä käsittelemään”, hän sanoi. Vuonna 1984 hän otti vastaan tarjouksen siirtää laboratorionsa silloisesta Sidney Farber Cancer Institute -laitoksesta MGH:hen ja liittyä sikäläisiin tutkijoihin, jotka työskentelivät perustutkimuksen parissa. ”Se oli uskomaton tarjous: kaikki tutkimukseni saisi täyden rahoituksen 10 vuodeksi”, Szostak muistelee. ”Se sopi minulle täydellisesti, sillä se antoi minulle mahdollisuuden vaihtaa suuntaa murehtimatta apurahojen kirjoittamisesta uudella alalla.”
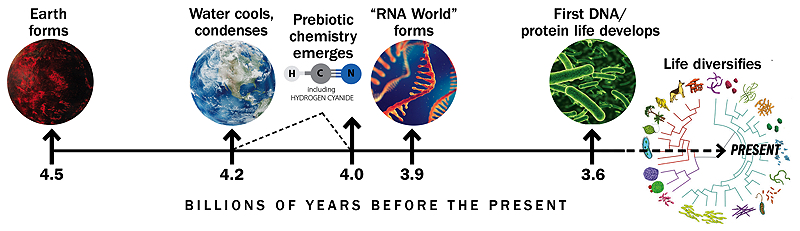
Timeline perustuu Gerald Joycen vastaavaan grafiikkaan
Harkittuaan vaihtoehtojaan hän päätyi ribosyymeiksi kutsuttuihin RNA-entsyymeihin, alaan, jonka hän näki ”mielenkiintoisena, helposti käsiteltävänä eikä kovinkaan kilpailluna”. Hän ja hänen jatko-opiskelijansa alkoivat kehittää välineitä RNA:n, solujen yksisäikeisten molekyylien, jotka kopioivat DNA:n sisältämää geneettistä tietoa, kehittämiseen. Koeputkissa hänen ryhmänsä sai RNA:n omaksumaan uusia tehtäviä, kuten tunnistamaan kohdemolekyylejä ja katalysoimaan reaktioita. Tämä ”suunnatuksi evoluutioksi” kutsuttu prosessi sisälsi mutaatioiden tuomista RNA-juosteisiin, sellaisten muunnosten etsimistä, jotka pystyisivät suorittamaan hyödyllisiä toimintoja, ja näiden uusien molekyylien lisääntymisen sallimista. He tekivät samanlaista työtä myös DNA:n, peptidien ja proteiinien kanssa.
Sostak sai vuonna 1994 National Academy of Sciences Award in Molecular Biology -palkinnon yhdessä tutkija Gerald Joycen, nykyisin Salk Institute for Biological Studies -instituutissa työskentelevän tutkija Gerald Joycen kanssa siitä, että he kehittivät RNA:n in vitro -evoluution samanaikaisesti, mutta itsenäisesti. ”Se on teknologia, jonka avulla voidaan valmistaa molekyylejä, jotka tekevät käskyjäsi”, Joyce selitti haastattelussa ja kuvaili sitä samankaltaiseksi kuin sitä, miten maataloustutkijat jalostavat lehmiä tuottamaan enemmän maitoa tai kehittävät kuivuutta kestäviä viljelykasveja. ”Tämä on molekulaarinen versio siitä. Ja sitä harjoitetaan nyt hyvin laajalti”, hän lisää (ks. ”Harnessing Evolution”, tammi-helmikuu 2017, sivu 15), keino kehittää uusia molekyylejä erilaisiin käyttötarkoituksiin, kuten lääkkeisiin.
Sostakille suunnattua evoluutiota koskeva työ herätti uusia kysymyksiä. ”Kiinnostuin yhä enemmän siitä, miten evoluutio sai alkunsa ihan itsestään varhaisella maapallolla”, hän muistelee. ”On eri asia asettaa valikoivia paineita ja tehdä darwinistista evoluutiota laboratoriossa, jossa on entsyymejä, opiskelijoita ja välineitä. Mutta jotenkin darwinistinen evoluutio sai alkunsa aivan itsestään.” Koska kyky kehittyä on elämän keskeinen ominaisuus, Szostak esitti yhden tieteen peruskysymyksistä: Miten elämä sai alkunsa?
Origins: ”Three Big, Fundamental Questions”
Kanadalais-amerikkalainen Szostak syntyi Lontoossa, jossa hänen isänsä opiskeli ilmailutekniikan diplomi-insinööriksi. Perhe palasi lopulta Kanadaan, jossa he asuivat ensin Ottawassa ja sitten Montrealissa, ja hänen isänsä työskenteli Kanadan ilmavoimissa. (Szostakin aksentissa on edelleen viitteitä hänen kanadalaisesta perinnöstään.) Hänen äitinsä työskenteli monta vuotta hallinnollisissa tehtävissä teollisuuskemikaaliyrityksessä, ja Szostak teki siellä ensimmäisen kesätyönsä teini-ikäisenä testaten värien kestävyyttä yrityksen väriainelaboratoriossa. ”Työ oli toistuvaa ja tylsää, mutta se antoi minulle ensimmäisen näkemykseni siitä, miten tärkeää on testata ja testata tuotteita todellista käyttöä varten”, hän muistelee. Tuolloin hän oli jo ”vakavasti kiinnostunut” luonnontieteistä, matematiikasta ja tekniikasta. Hän väitteli biokemian tohtoriksi 25-vuotiaana Cornellissa ja kutsuu ohjaajaansa Ray Wua tärkeäksi mentorikseen: ”Hän loi loistavan laboratorioympäristön, mutta näytti minulle myös, miten hankkia apua projektiin ongelmien kohdatessa.”
Vaikka Szostak on urallaan tehnyt jonkin verran käytännöllistä, soveltavaa tutkimusta – yksi hänen perustamastaan yrityksestä, Ra Pharma, on keksinyt lääkkeen myasthenia gravis -sairauteen, jonka kliiniset tutkimukset alkavat pian vaiheen III tutkimuksissa – hän suhtautuu intohimoisimmin perustutkimukseen.
”Tämä on jännittävää aikaa ryhtyä neurotieteiden pariin, koska nyt voidaan ratkaista ongelmia, joita ei osattu edes ajatella 30 vuotta sitten.”
”Mielestäni on kolme suurta tieteellistä peruskysymystä, jotka ovat erittäin kiinnostavia: elämän alkuperä, maailmankaikkeuden alkuperä ja mielen tai tietoisuuden alkuperä”, hän tarjoaa istuessaan rauhallisessa, lähes tyhjässä toimistossaan Mallinckrodt-laboratoriossa Oxford Streetillä Cambridgessa. (Toimisto on tarkoitettu satunnaisia kokouksia varten; Szostak työskentelee pääasiassa laboratoriossaan MGH:ssa.) Elämän alkuperän jälkeen mielen alkuperä kiinnostaa häntä eniten. Kun hän 1980-luvulla suunnitteli, mitä tekisi telomeeritutkimuksensa jälkeen, hän harkitsi siirtymistä neurotieteen tutkimukseen ja jopa osallistui Harvardin seminaareihin aiheesta. ”Se oli kiehtovaa, mutta myös masentavaa, koska teknologia oli niin alkeellista”, hän muistelee. Hän on seurannut kiinnostuneena, miten alan välineet ovat sittemmin kehittyneet. ”Tämä on jännittävää aikaa nuorille neurotieteiden pariin hakeutumiselle, koska kaiken uuden teknologian ansiosta nyt voidaan ratkaista ongelmia, joita ei voinut edes ajatella 30 vuotta sitten”, hän sanoo. ”Silti kokonaisongelma on edelleen niin valtava ja jossain määrin pelottava. Näen asian niin, että työskentelen näistä suurista ongelmista helpoimman parissa.” Koska elämän alkuperää koskevat kysymykset sopivat hyvin nykyiseen tutkimusteknologiaan, hän lisää, että se on hänen mielestään ”ratkaistavissa oleva ongelma.”
Malliprotosolut ja ”sotkuinen” RNA
Szostakin työryhmä on valmistanut malliprotosoluja 2000-luvun alkupuolelta lähtien ja pyrkinyt selvittämään, miten protosolut ovat saattaneet alunperin rakentua ja kehittyä. Nämä alkukantaiset rakenteet olivat ”äärimmäisen yksinkertaisia” verrattuna nykyisin maapallolla olevaan yksinkertaisimpaan yksisoluiseen bakteeriin, hän selittää. Protosoluissa oli todennäköisesti minimaalinen rasvakalvo ja alun perin vain yksi geeni, joka antoi solulle jonkin edun. Nykyaikaisilla bakteereilla sen sijaan ”on vähintään satoja ja tyypillisesti tuhansia geenejä.”
Vaikka joissakin teorioissa on esitetty, että varhainen elämä syntyi syvänmeren hydrotermisten purkausaukkojen läheisyydessä, Szostak on vakuuttuneempi tutkimuksista, jotka osoittavat, että varhaisimmat solut kehittyivät maalla lammikoissa tai lammikoissa, mahdollisesti vulkaanisesti aktiivisilla alueilla. Ultraviolettivalo ja salamaniskut ovat voineet auttaa muuntamaan ilmakehän molekyylejä syanidiksi ja muiksi käyttökelpoisiksi aineiksi elämän rakennusaineiksi. Matalassa vedessä nämä aineet saattoivat kerääntyä suurina pitoisuuksina, ja tulivuoritoiminta saattoi synnyttää kuumia ja kylmiä lämpötilavaihteluita, jotka olivat hyödyllisiä tietyille kemiallisille reaktioille.
Historiaa maapallosta ja elämän synnystä
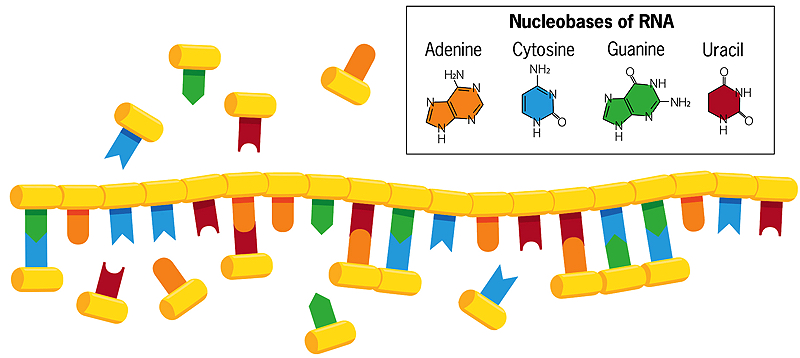
Toisin kuin kaksisäikeisessä DNA:ssa, jossa emäkset sytosiini ja tymiini muodostavat parin vastakkaisen säikeen guaniinin ja adeniinin kanssa, RNA:n yksisäikeisen säikeen emäkset voivat vedessä muodostaa assosiaatioita vapaana leijuvien nukleobaasien kanssa (yllä olevassa kuvassa). Jos nämä vapaasti liikkuvat emäkset sitten sulautuvat toisiinsa, syntyy RNA-juosteesta uusi peilikopio, joka hajoaa alkuperäisestä, kun vettä lämmitetään. Kun tämä uusi säie vuorostaan monistuu, se luo itsestään peilikopion, joka vastaa alkuperäistä RNA-säiettä. Joskus tässä kopiointiprosessissa tapahtuu virheitä, ja hyödylliset virheet jatkuvat. Jokainen ketju, joka toimii mallina omalle replikaatiolleen, kehittyy näin ja on vuorovaikutuksessa ympäristönsä kanssa.
Jotkut tiedemiehet, kuten Gerald Joyce, esittävät, että elämä on saattanut alkaa solujen ulkopuolelta, jolloin vapaana leijuvat molekyylit ovat kohdanneet toisensa ja muodostaneet sidoksia, jotka mahdollistavat sen, että ne voivat toimia elämän tavoin. Szostak kuitenkin väittää, että solukalvo oli välttämätön, osittain siksi, että se pitäisi hyödylliset geneettiset molekyylit yhdessä ja estäisi geneettisesti koodattujen ribosyymien tuottamia hyödyllisiä aineenvaihduntatuotteita ajelehtimasta pois ympäröivässä vedessä tai joutumasta muiden ohi kulkevien protosolujen saaliiksi.
Sostakin laboratoriossa tehdyissä kokeissa osoitettiin, miten tällainen kalvo voisi kasvaa ja jakautua. Tutkijat yhdistivät rasvahappoja, kuten öljyhappoa, veteen ja puskuriin (pitääkseen liuoksen pH:n vakaana) ja ravistelivat sitten liuosta. Mikroskoopilla tarkasteltuna ainesosat olivat kasautuneet vesikkeleiksi: pyöreiksi, nestetäytteisiksi rakenteiksi, joissa oli kaksikerroksiset kalvot. Kun ympäristöön lisättiin ylimääräisiä rasvahappoja, jotka toimivat ravinteina, vesikkelit kasvoivat pitkiä, karvamaisia säikeitä, jotka olivat niin hauraita, että kevytkin ilman puhallus mikroskoopin objektilasissa sai ne hajoamaan palasiksi. Szostakin työryhmä saavutti samanlaisia tuloksia erilaisilla kalvoja muodostavilla molekyyleillä ja erilaisissa ympäristöissä, mikä viittaa siihen, että tämä on uskottava tapa, jolla protosolukalvo voi kasvaa ja jakautua. Mutta miten tämä rakenne voisi siirtää hyödyllistä geneettistä materiaalia seuraavalle tytärsolusukupolvelle? ”Perintöaines näyttää itse asiassa paljon vaikeammalta ongelmalta”, hän sanoo.
Jakaakseen perittyjä ominaisuuksia peräkkäisten sukupolvien kanssa nykyiset solut luottavat DNA:han – kaksoiskierteiseen molekyyliin, joka koostuu adeniini-, sytosiini-, guaniini- ja tymiini-nukleoaasista – geneettisen informaation tallentamiseen ja siirtämiseen. DNA:n monistaminen soluissa edellyttää kuitenkin sekä yksijuosteista RNA-molekyyliä että proteiinien entsyymejä, ja geneettisesti koodatut proteiinit ovat aivan liian monimutkaisia muodostuakseen spontaanisti maapallon alkuaikoina. Koska RNA voi sekä varastoida ja välittää geneettistä tietoa (kuten DNA) että katalysoida kemiallisia reaktioita (kuten proteiinien entsyymit), monet tutkijat uskovat, että alkukantaiset solut käyttivät RNA-molekyylejä sekä geneettisten että entsymaattisten roolien täyttämiseen.
1960-luvun lopulla brittiläinen tiedemies Leslie Orgel ehdotti, että RNA tai jotain sen kaltaista olisi voinut olla maapallon ensimmäinen molekyyli, joka on voinut reprodusoitua ja kehittyä; tämä tunnettiin nimellä ”RNA-maailma”- hypoteesi. Orgel ja muut työskentelivät vuosikymmeniä ymmärtääkseen, miten RNA-ketjut olisivat voineet yhdistyä ja monistua, mutta heidän ponnistelunsa eivät olleet täysin onnistuneita. ”Alkuvaiheessa edistyttiin paljon, mutta sitten homma vain pysähtyi, koska ongelmia oli tusinoittain, eikä silloin ollut selvää vastausta mihinkään niistä”, Szostak selittää. ”Lähes kaikki turhautuivat ja ajattelivat: ’Ehkä elämä ei alkanutkaan RNA:sta. Ehkä on olemassa jotain yksinkertaisempaa, helpommin valmistettavaa ja helpommin monistettavaa.”
”Tiedämme nyt niin paljon enemmän, ja vain pilkkomalla asiat yksittäisiin, pienempiin ongelmiin olemme pystyneet ratkaisemaan joitakin niistä.”
Tutkijat etsivät vaihtoehtoja RNA:lle, ”ja se johti 10-20 vuoden todella mielenkiintoiseen kemian työhön, jonka aikana kehitettiin paljon mielenkiintoisia molekyylejä”, Szostak toteaa. ”Mutta toistaiseksi ei ole löytynyt mitään RNA:ta yksinkertaisempaa tai parempaa, joka todella toimisi.” Jotkut tutkijat kannattavat ”aineenvaihdunta ensin” -hypoteesia, jonka mukaan elämä olisi voinut alkaa ilman geneettistä materiaalia itseään ylläpitävien reaktioiden avulla, mutta Szostak ja muut eivät ole siitä vakuuttuneita. Noin seitsemän vuotta sitten hän alkoi tarkastella uudelleen niitä esteitä, joita Orgel ja hänen aikalaisensa kohtasivat RNA-synteesin ymmärtämisessä. ”Tiedämme nyt niin paljon enemmän”, hän selittää, ”ja vain pilkkomalla asiat yksittäisiin, pienempiin ongelmiin olemme pystyneet ratkaisemaan joitakin niistä.”
Szostakin laboratorio keskittyy nyt lähes kokonaan siihen, miten alkukantainen RNA on voinut kopioida itseään. Nykyaikainen RNA muodostuu hyvin säännönmukaisella, ennustettavalla tavalla, jossa nukleotidien rakennuspalikat napsahtavat yhteen kuin ketju. Jokaisessa lohkossa on sokeri (riboosi), fosfaatti ja yksi neljästä nukleoaasista (joita kutsutaan myös typpiemäksiksi) -adeniini, sytosiini, guaniini ja urasiili (yleensä A, C, G ja U). Riboosifosfaattiyksiköt liittyvät toisiinsa ja muodostavat RNA:n ”selkärangan”. Nykysoluissa proteiinientsyymit katalysoivat reaktion, jossa nukleotidiyksiköt yhdistyvät RNA-ketjuiksi.
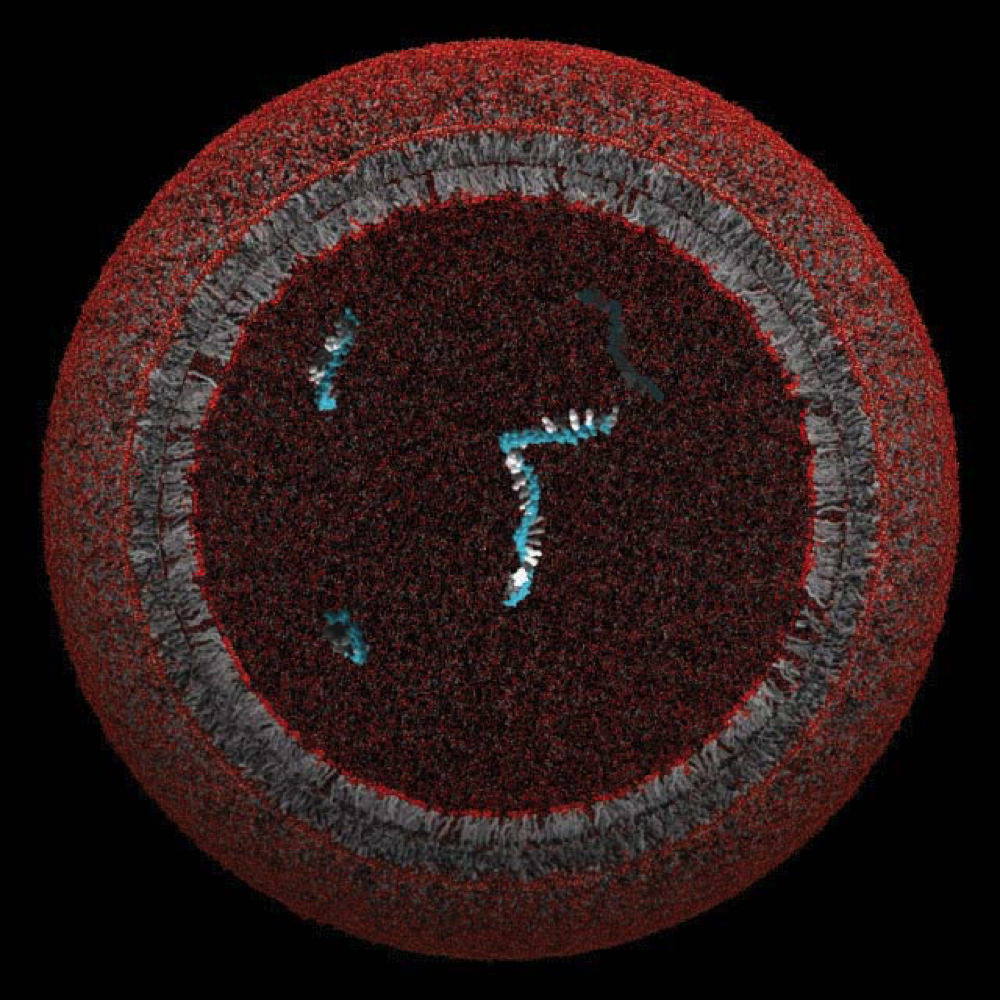
Malliprotosolu, jonka lipidikalvo on saattanut sulkea sisäänsä ja suojata yhtä ainoaa geeniä
Kuva on toimitettu Szostakin laboratorion luvalla
Maailman alkuaikojen protosoluissa RNA-ketju olisi toiminut templaattina, jonka varaan uusi, komplementaarinen nukleotidiketju kasaantui, ennen kuin se irrottautui ylimääräiseksi templaattina, jonka varaan muut vapaana liikkujat olisivat voineet napsahtaa yhteen. Mutta toisin kuin ennustettavissa oleva nykyaikainen RNA, varhaisella RNA:lla ei ollut proteiineja, jotka olisivat katalysoineet rakentamisprosessia. (Koska proteiineja ei voi muodostua ilman niiden synteesiin tarvittavaa monimutkaista ja pitkälle kehittynyttä solukoneistoa, useimmat tutkijat uskovat, että niitä ei todennäköisesti ollut olemassa alkuaikojen maapallolla). Alkuaikojen RNA oli siis todennäköisesti sotkuisempaa, ja sen sokerirunko ja emäkset vaihtelivat paljon enemmän, Szostak sanoo. Hänen ryhmänsä tekee parhaillaan kokeita ”saadakseen jonkinlaisen käsityksen siitä, mitä vaihtelua siedettäisiin ja mitä karsittaisiin pois”. Tämänhetkinen mallimme on, että aluksi on jotain, joka on sotkuista ja jossa on paljon erilaisia variaatioita, ja replikaatiosyklien aikana päädytään johonkin, joka on lähempänä nykyaikaista homogeenista RNA:ta.”
Sostakin ja jatko-opiskelija Seohyun Kimin vuonna 2018 tekemässä artikkelissa havainnollistetaan varhaista RNA:ta ja sen A-, C-, G- ja U-rakenneosioita koskevaa mahdollista vaihtelua. Tutkijat ovat edistyneet sen ymmärtämisessä, miten C ja U ovat voineet syntyä prebioottisissa kemiallisissa reaktioissa, mutta he ovat kamppailleet A:n ja G:n kanssa. Szostak ja Kim ehdottavat, että RNA on saattanut alkaa erilaisista nukleobaaseista, ja heidän kokeensa ovat osoittaneet, että nukleosidi inosiini, joka voidaan valmistaa A:sta (adeniinista), toimii tehokkaasti G:n (guanosiinin) sijasta. ”Tämä yksinkertaistaa koko ongelmaa”, Szostak selittää. ”Nyt meidän on vain tiedettävä, miten A:ta valmistetaan.”
Muut laboratorion viimeaikaiset kokeet ovat keskittyneet metalli-ioneihin, joita tarvitaan RNA:n kopiointiprosessin käynnistämiseen. Tutkijat käyttävät tavallisesti magnesiumia, ”mutta meidän on käytettävä sitä hyvin suurina pitoisuuksina”, millä on kielteisiä sivuvaikutuksia, jotka laukaisevat RNA:n hajoamisen tai solukalvon tuhoutumisen. ”Toivottavasti löydämme jonkin yksinkertaisen, uskottavan tavan saada kaikki toimimaan vähemmällä magnesiumilla, tai ehkä meidän on ajateltava koko ongelma uudelleen ja lähestyttävä sitä eri suunnasta”, Szostak selittää. ”Tunnustelemme vain pimeässä ja yritämme nähdä, mistä voisi löytyä polku ratkaisuun.”

Vulkanismista johtuva lämpeneminen ja jäähtyminen, kuten Yellowstonen Grand Prismatic Spring -lähteellä, olisi helpottanut RNA:n varhaista evoluutiota.
Photograph by Istock Images
Joillakin poluilla ei onnistu, ja ne tuottavat jopa virheitä. Vuonna 2016 Szostakin laboratorio julkaisi Nature Chemistry -lehdessä artikkelin, joka osoitti, että peptidi olisi voinut auttaa RNA:n monistumista ilman entsyymejä. Pian sen jälkeen laboratorioon liittyi tutkijatoveri Tivoli Olsen, joka ei pystynyt toistamaan näitä tuloksia. Hänen tekemänsä tarkastelu paljasti, että tutkimusryhmä oli tulkinnut tietoja väärin, ja Szostak perui artikkelin. ”Työskentelemme vaikeiden ongelmien parissa, ja kuten Feynman taisi sanoa, vaikeinta tieteessä on olla huijaamatta itseään”, Szostak sanoo. Mahdollinen ratkaisu oli jännittävä, ”ja luulen, että se vain sokaisee meidät siitä, mitä oli tekeillä.” ”Pelastava asia”, hän lisää, on se, että he löysivät virheet itse, vaikka hän toivookin, että se olisi tapahtunut ”ennen artikkelin julkaisemista eikä sen jälkeen”. Sanoisin, että monet ajatuksistamme ovat lopulta vääriä, mutta yleensä huomaamme sen melko nopeasti.”
Hän suhtautuu toiveikkaasti muiden laboratorioiden viimeaikaisten keksintöjen mahdollisuuksiin; esimerkiksi John Sutherland Medical Research Councilin (MRC) molekyylibiologian laboratoriosta Cambridgessa Englannissa löysi hiljattain uuden tekniikan nukleotidien aktivoimiseksi, eli näiden rakennuspalikoiden kemialliseksi muokkaamiseksi, jotta ne antaisivat virtaa replikaatioprosessille. Sutherland jakoi nämä havainnot Szostakin laboratorion kanssa ennen niiden julkaisemista, ja Szostak sanoo, että he tutkivat parhaillaan tapoja sisällyttää tämä tekniikka omiin kokeisiinsa.
Kunhan hänen ryhmänsä kokoaa toimivia protosoluja, jotka sisältävät RNA:n palasia, he odottavat, että joidenkin erityisten RNA-sekvenssien sisältämä informaatio antaisi jonkinlaista hyötyä sitä ympäröivälle protosolulle. Aiemmat työt viittaavat esimerkiksi siihen, että jotkin RNA-sekvenssit voisivat taittua ribotsyymiksi, joka voisi valmistaa hieman kehittyneempiä lipidejä solukalvoa varten. ”Mikä tahansa RNA-sekvenssi, joka tekee jotakin, mikä auttaa omia solujaan selviytymään tai monistumaan nopeammin, alkaa vallata populaatiota”, Szostak selittää. ”Se on darwinistisen evoluution alku. Ja sitten olemme taas biologeja.”
Nobel-palkinnon saatuaan Szostak olisi voinut jättää laboratorionsa ja omistautua matkustelulle ja puhujakutsuille, mutta ”hän keskittyy tieteeseen”, Gerald Joyce sanoo. ”Sitä ihailen hänessä eniten.” Jotkut saattavat pitää perustutkimusta älyllisenä ylellisyytenä, mutta sen harjoittajat väittävät, että kaikki soveltava tiede alkaa perustutkimuksen tuloksista. ”Kun Crick ja Watson istuivat alas ja alkoivat tehdä pahvisia malleja DNA:n rakenteesta, heillä ei ollut aavistustakaan siitä, että se synnyttäisi 70 vuotta myöhemmin miljardien dollarien arvoisen teollisuuden”, John Sutherland toteaa.
Szostak on edelleen sitoutunut työstämään näitä suuria ja haastavia kysymyksiä ja jatkamaan vuosikymmenten työtä. ”Toivon, että pystyn rakentamaan kehittyvän solujärjestelmän ennen kuin jään eläkkeelle”, hän sanoo. Hän on optimistinen mahdollisuuksiensa suhteen. ”Uskon, että olemme pääsemässä sinne. Vielä on muutama vaikea ongelma, ja sitten uskon, että kaikki on toivottavasti ratkaistu parissa vuodessa.” Hän jatkaa.