Mitä ovat entsyymit ja mitä ne tekevät elimistössämme? Entsyymit ovat periaatteessa proteiineja, joita elävät organismit tuottavat tiettyjen aineenvaihdunnallisten ja biokemiallisten reaktioiden aikaansaamiseksi elimistössä. Ne ovat biologisia katalyyttejä, jotka nopeuttavat reaktioita elimistössä. Tutustutaanpa niihin tarkemmin.
Suggested Videos:
Mikä on entsyymien rakenne?
Ensiymit ovat, kuten edellä mainittiin, biologisia katalyyttejä. Vaikka ne nopeuttavat tai nopeuttavat jotakin prosessia, ne itse asiassa tarjoavat prosessille vaihtoehtoisen reitin. Mutta prosessin aikana entsyymien rakenne tai koostumus pysyy muuttumattomana.
Ensyymit koostuvat itse asiassa tuhansista aminohapoista, jotka liittyvät tietyllä tavalla toisiinsa muodostaen erilaisia entsyymejä. Entsyymiketjut taittuvat muodostaen ainutlaatuisia muotoja, ja juuri nämä muodot antavat entsyymille sen tyypillisen kemiallisen potentiaalin. Useimmat entsyymit sisältävät myös muun kuin proteiinikomponentin, joka tunnetaan nimellä kofaktori.
Selaa lisää aiheita kohdasta Biomolekyylit
- Biomakromolekyylit
- Sidoksia yhdistävät monomeerit
- Ensiymit
- Metabolinen perusta elämälle
- Nukleiinihapot
- Polysakkaridit
- Proteiinit
Ensiymien tyypit:
Kehossa tapahtuvia biokemiallisia reaktioita on periaatteessa 6 tyyppiä ja näitä reaktioita aikaansaavat entsyymit on nimetty vastaavasti:
- Oksidoreduktaasit: Nämä entsyymit saavat aikaan hapettumis- ja pelkistymisreaktioita, ja siksi niitä kutsutaan oksidoreduktaaseiksi. Näissä reaktioissa siirretään elektroneja hydridi-ionien tai vetyatomien muodossa. Kun substraattia hapetetaan, nämä entsyymit toimivat vedyn luovuttajina. Näitä entsyymejä kutsutaan dehydrogenaaseiksi tai reduktaaseiksi. Kun happiatomi on akseptorina, näitä entsyymejä kutsutaan oksidaaseiksi.
- Transferaasit: Nämä entsyymit vastaavat funktionaalisten ryhmien siirtämisestä molekyylistä toiseen. Esimerkki: Alaniiniaminotransferaasi, joka sekoittaa alfa-aminoryhmän alaniinin ja aspartaatin välillä jne. Jotkut transferaasit siirtävät myös fosfaattiryhmiä ATP:n ja muiden yhdisteiden välillä, sokerijäämiä disakkaridien muodostamiseksi, kuten heksokinaasi glykolyysissä.
- Hydrolaasit: Nämä entsyymit katalysoivat reaktioita, joihin liittyy hydrolyysiprosessi. ne rikkovat yksittäisiä sidoksia lisäämällä vettä. Jotkut hydrolaasit toimivat ruoansulatusentsyymeinä, koska ne rikkovat proteiinien peptidisidoksia. Hydrolaasit voivat olla myös eräänlaisia transferaaseja, koska ne siirtävät vesimolekyylin yhdisteestä toiseen. Esimerkki: Glukoosi-6-fosfataasi, joka poistaa fosfaattiryhmän glukoosi-6-fosfaatista, jolloin jäljelle jää glukoosia ja H3PO4.
- Lyaasit: Nämä entsyymit katalysoivat reaktioita, joissa funktionaalisia ryhmiä lisätään molekyylien kaksoissidosten katkaisemiseksi tai joissa kaksoissidoksia muodostuu poistamalla funktionaalisia ryhmiä. Esimerkki: Pyruvaattidekarboksylaasi on lyaasi, joka poistaa CO2:n pyruvaatista. Muita esimerkkejä ovat deaminaasit ja dehydraasit.
- Isomeraasit: Nämä entsyymit katalysoivat reaktioita, joissa funktionaalinen ryhmä siirretään toiseen paikkaan samassa molekyylissä siten, että syntyvä molekyyli on itse asiassa aiemman molekyylin isomeeri. Esimerkki: triosfosfaatti-isomeraasi ja fosfoglukoosi-isomeraasi glukoosi-6-fosfaatin muuttamiseksi fruktoosi-6-fosfaatiksi.
- Ligaseja: Nämä entsyymit suorittavat hydrolaaseille päinvastaista tehtävää. Siinä missä hydrolaasit rikkovat sidoksia lisäämällä vettä, ligaasit muodostavat sidoksia poistamalla vesikomponentin. Ligaaseilla on erilaisia alaluokkia, joihin liittyy ATP:n synteesi.
Miten entsyymit toimivat?
Mitä tahansa maailmankaikkeudessa tapahtuvaa reaktiota varten tarvitaan energiaa. Tapauksissa, joissa aktivaatioenergiaa ei ole tarjolla, katalysaattorilla on tärkeä rooli aktivaatioenergian vähentämisessä ja reaktion eteenpäin viemisessä. Tämä toimii myös eläimissä ja kasveissa. Entsyymit auttavat vähentämään reaktiossa olevien monimutkaisten molekyylien aktivoitumisenergiaa. Seuraavat vaiheet yksinkertaistavat, miten entsyymi toimii nopeuttaakseen reaktiota:
Vaihe 1: Jokaisella entsyymillä on ”aktiivinen alue”, johon yksi substraattimolekyyleistä voi sitoutua. Näin muodostuu entsyymi-substraatti-kompleksi.
Vaihe 2: Tämä entsyymi-substraattimolekyyli reagoi nyt toisen substraatin kanssa muodostaen tuotteen ja entsyymi vapautuu toisena tuotteena.
On olemassa monia teorioita, jotka selittävät entsyymien toimintaa. On kuitenkin kaksi tärkeää teoriaa, joita käsittelemme tässä.
Teoria 1: Lukko-avain-hypoteesi
Tämä on entsyymien toimintaa koskevista teorioista hyväksytyin.

Tässä teoriassa sanotaan, että substraatti mahtuu tarkalleen entsyymin aktiiviseen kohtaan muodostaen entsyymi-substraatti-kompleksin. Tämä malli kuvaa myös sitä, miksi entsyymit ovat niin spesifisiä toiminnassaan, koska ne ovat spesifisiä substraattimolekyyleille.
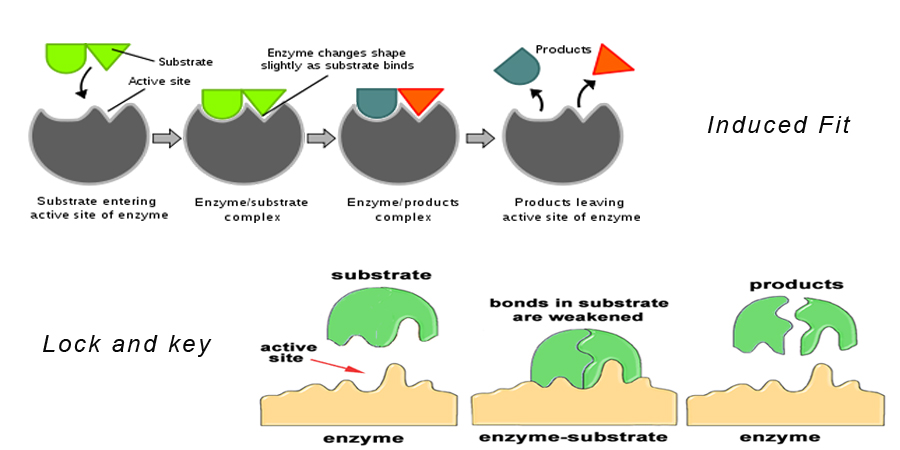
Teoria 2: Indusoidun istuvuuden hypoteesi
Tämä on samankaltainen kuin lukko-avain-hypoteesi. Sen mukaan entsyymimolekyylin muoto muuttuu sen lähestyessä substraattimolekyyliä siten, että substraattimolekyyli sopii täsmälleen entsyymin aktiiviseen kohtaan.
Mitkä tekijät vaikuttavat entsyymien aktiivisuuteen solussa?
- Entsyymien ja substraattien konsentraatio: Reaktionopeus kasvaa substraattikonsentraation kasvaessa tiettyyn pisteeseen asti, jonka jälkeen substraattikonsentraation lisäys ei aiheuta merkittävää muutosta reaktionopeudessa. Tämä johtuu siitä, että tietyn substraattikonsentraation jälkeen kaikki entsyymin aktiiviset paikat ovat täynnä, eikä reaktiota voi enää tapahtua.
- Lämpötila: Lämpötilan noustessa entsyymiaktiivisuus kasvaa, koska molekyylien kineettinen energia kasvaa. On olemassa optimitaso, jolloin entsyymit toimivat parhaimmillaan ja maksimissaan. Tämä lämpötila on usein kehon normaali ruumiinlämpötila. Kun lämpötila nousee yli tietyn rajan, entsyymit, jotka itse asiassa koostuvat proteiineista, alkavat hajota ja reaktionopeus hidastuu.
- pH: Entsyymit ovat hyvin herkkiä pH:n muutoksille, ja ne toimivat hyvin pienessä sallitun pH:n ikkunassa. Optimaalisen pH-tason alapuolella tai yläpuolella on vaarana, että entsyymit hajoavat ja siten reaktio hidastuu.
- Inhibiittorit: Tiettyjen aineiden läsnäolo, jotka estävät tietyn entsyymin toimintaa. Tämä tapahtuu, kun inhiboiva aine kiinnittyy entsyymin aktiiviseen kohtaan estäen siten substraatin kiinnittymisen ja hidastaen prosessia.
Ratkottu esimerkki sinulle
Q: Entsyymi toimii?
a. Lisäämällä aktivaatioenergiaa
b. Vähentää aktivaatioenergiaa
c. Alentamalla pH:ta
d. pH:n nostaminen
Sol: a. Aktivoitumisenergian nostaminen
Reaktantit eivät muutu kemiallisesti automaattisesti. Ne tekevät sen siirtymätilassa. Siirtymätilassa on enemmän vapaata energiaa kuin reagoijilla tai tuotteilla. Reaktanttien kyvyttömyyttä käydä läpi muutosta, koska niiden siirtyminen siirtymätilaan vaatii ylimääräistä energiaa, kutsutaan ”energiaesteeksi”. Energiaesteen ylittämiseen tarvittavaa energiaa kutsutaan ’aktivoitumisenergiaksi’.