Allgemeine Behandlung nicht heilender Wunden
Betrachten Sie den gesamten Patienten
Eine erfolgreiche Behandlung schwieriger Wunden erfordert die Beurteilung des gesamten Patienten und nicht nur der Wunde. Systemische Probleme beeinträchtigen oft die Wundheilung; umgekehrt können nicht heilende Wunden auf eine systemische Pathologie hinweisen.
Berücksichtigen Sie die negativen Auswirkungen von endokrinen Erkrankungen (z. B. Diabetes, Hypothyreose), hämatologischen Erkrankungen (z. B. Anämie, Polyzythämie, myeloproliferative Störungen), kardiopulmonalen Problemen (z. B, chronisch obstruktive Lungenerkrankung, Herzinsuffizienz), Magen-Darm-Probleme, die zu Unterernährung und Vitaminmangel führen, Fettleibigkeit und periphere Gefäßerkrankungen (z. B. atherosklerotische Erkrankungen, chronische Veneninsuffizienz, Lymphödeme).
Charakterisieren Sie die Wunde
Beurteilen Sie Folgendes: (1) Größe und Tiefe der Beteiligung und das Ausmaß der Unterminierung, (2) das Erscheinungsbild der Wundoberfläche – ist sie nekrotisch oder lebensfähig, (3) Menge und Charakteristik(en) des Wundexsudats und (4) Status des Wundrandgewebes (z. B. pigmentiert, vernarbt, atrophisch, cellulitisch).
Ausreichende Oxygenierung sicherstellen
Der übliche Grund für eine unzureichende Oxygenierung des Gewebes ist eine lokale Vasokonstriktion als Folge einer sympathischen Überaktivität. Dies kann aufgrund eines Blutvolumendefizits, nicht gelinderter Schmerzen oder Hypothermie auftreten, insbesondere im distalen Bereich der Extremitäten.
Ausreichende Ernährung sicherstellen
Ausreichende Ernährung ist eine oft übersehene Voraussetzung für eine normale Wundheilung. Kümmern Sie sich um eine Eiweiß-Kalorien-Mangelernährung und einen Mangel an Vitaminen und Mineralien.
Eine unzureichende Eiweiß-Kalorien-Ernährung, selbst nach nur wenigen Tagen des Hungerns, kann die normalen Wundheilungsmechanismen beeinträchtigen. Bei gesunden Erwachsenen liegt der tägliche Nährstoffbedarf bei etwa 1,25-1,5 g Protein pro Kilogramm Körpergewicht und 25-30 Kalorien/kg. Dieser Bedarf kann jedoch bei Patienten mit großen Wunden steigen.
Verdacht auf Mangelernährung bei Patienten mit chronischen Krankheiten, unzureichender sozialer Unterstützung, multisystemischen Traumata oder gastrointestinalen oder neurologischen Problemen, die die orale Aufnahme beeinträchtigen können. Proteinmangel tritt bei etwa 25 % aller hospitalisierten Patienten auf. Häufig lassen sich bei einer gründlichen körperlichen Untersuchung Anzeichen für eine Mangelernährung feststellen, z. B. zeitliche Auszehrung, Verlust von subkutanem Fett, Knöchel-/Sakralödeme, ausgeprägte Schlüsselbeine.
Chronische Mangelernährung kann anhand anthropometrischer Daten zum Vergleich von tatsächlichem und idealem Körpergewicht und durch Beobachtung niedriger Serumalbuminwerte diagnostiziert werden. Präalbumin im Serum ist ein empfindlicher Indikator für eine relativ akute Unterernährung, da seine Halbwertszeit 2 bis 3 Tage beträgt (gegenüber 21 Tagen bei Albumin). Ein Serumpräalbuminspiegel von weniger als 16-17 g/dL deutet auf ein gewisses Maß an Mangelernährung hin, während ein Spiegel von weniger als 10 g/dL auf eine schwere Protein-Kalorien-Mangelernährung hindeutet.
Vitamin- und Mineralstoffmangel müssen ebenfalls korrigiert werden. Ein Vitamin-A-Mangel reduziert das Fibronektin auf der Wundoberfläche, was die Chemotaxis der Zellen, die Adhäsion und die Gewebereparatur verringert. Vitamin C ist für die Hydroxylierung von Prolin und die anschließende Kollagensynthese erforderlich.
Vitamin E, ein fettlösliches Antioxidans, reichert sich in Zellmembranen an, wo es mehrfach ungesättigte Fettsäuren vor der Oxidation durch freie Radikale schützt, Lysosomen stabilisiert und die Kollagensynthese hemmt. Vitamin E hemmt die Prostaglandinsynthese, indem es die Phospholipase-A2-Aktivität beeinträchtigt, und wirkt daher entzündungshemmend. Eine Vitamin-E-Supplementierung kann die Narbenbildung vermindern.
Zink ist Bestandteil von etwa 200 Enzymen im menschlichen Körper, einschließlich der DNA-Polymerase, die für die Zellproliferation erforderlich ist, und der Superoxid-Dismutase, die von Leukozyten während des Débridements produzierte Superoxid-Radikale abfängt.
Behandeln Sie die zugrundeliegende Infektion
Die zu berücksichtigenden Aspekte sind Wundinfektion versus Kolonisation und Osteomyelitis.
Eine positive Wundkultur ist kein Beweis für eine Wundinfektion. Opportunistische Mikroorganismen können jede Wunde kolonisieren. Wundexsudat, das von Natur aus bakterizid ist, verhindert, dass sich eine Oberflächenkontamination zu einer tiefen Wundinfektion entwickelt. Wenn jedoch eine Ischämie der Wunde oder eine systemische Immunschwäche vorliegt, vermehren sich pathogene Mikroorganismen, bis eine übermäßige Konzentration von Bakterien in der Wunde die Heilung verhindert. Dies ist der Vorbote einer echten Wundinfektion. Multiresistente Organismen treten immer häufiger auf.
Faul riechende Drainage, ein spontan blutendes Wundbett, fadenscheiniges, brüchiges Gewebe, vermehrtes Wundexsudat, zunehmende Schmerzen, umgebende Zellulitis, Krepitus, Nekrose, Fasziitis und regionale Lymphadenopathie charakterisieren die infizierte Wunde. Fieber, Schüttelfrost, Unwohlsein, Leukozytose und eine erhöhte Erythrozytensedimentationsrate sind häufige systemische Manifestationen einer Wundinfektion.
Die Wundinfektion erfordert ein chirurgisches Debridement und eine angemessene systemische Antibiotikatherapie. Topische Antiseptika werden in der Regel vermieden, da sie aufgrund ihrer Zytotoxizität für heilende Zellen die Wundheilung beeinträchtigen.
Der Nachweis, dass keine Osteomyelitis vorliegt, ist oft ebenso schwierig wie der Nachweis ihrer Anwesenheit. Obwohl eine Osteomyelitis mit Fieber, Unwohlsein, chronischer Müdigkeit und eingeschränkter Beweglichkeit der betroffenen Extremität einhergehen kann, stellen sich die Patienten oft nur mit einer nicht heilenden Wunde oder einem chronisch drainierenden Sinustrakt vor, der über einem Knochen oder Gelenk liegt.
Einfache Röntgenaufnahmen, CT-Scans, Radionuklid-Knochenscans und MRTs spielen eine Rolle bei der Abklärung einer Osteomyelitis. Allzu oft ist selbst eine umfassende bildgebende Untersuchung nicht diagnostisch. Daher sollte ein negativer Befund bei der radiologischen Untersuchung den Arzt nicht davon abhalten, eine Kürettage des verdächtigen Knochens durchzuführen, der unter einer chronisch drainierenden Wunde liegt.
Osteomyelitis wird mit einer chirurgischen Kürettage und geeigneten systemischen Antibiotika behandelt. Sorgen Sie für ein Wundbett, das der Wundheilung förderlich ist.
Nicht vitales Gewebe chirurgisch und mit geeigneter Spülung debridieren. Erhebliche Mengen an nicht lebensfähigem und fibrös eitrigem Gewebe müssen chirurgisch entfernt werden.
Ein erstes aggressives Debridement im Operationssaal unter örtlicher Betäubung mit Sedierung oder unter Regional- oder Vollnarkose ist oft sinnvoll. Das anschließende Débridement kann ambulant unter örtlicher Betäubung mit Lidocain-Gel oder Spray und durch sanfte Exzision mit einer Irisschere und einer Pinzette oder durch Schaben mit einer Kürette durchgeführt werden.
Der Verbandwechsel erfordert eine saubere, aber nicht unbedingt sterile Technik.
Fremdkörper entfernen
Auf die Möglichkeit von Fremdkörpern achten, die die Heilung traumatischer Wunden verhindern können, einschließlich Straßentrümmern und zurückgebliebenen Fragmenten von Verbands- oder Nahtmaterial.
Spülen
Die Wunde vorsichtig mit einer physiologischen Kochsalzlösung spülen. Wenn die Kosten eine wichtige Rolle spielen, kann der Patient zu Hause eine Kochsalzlösung aus 1 Gallone destilliertem Wasser und 8 Teelöffeln Kochsalz zubereiten. Die Lösung wird abgekocht und dann vor der Verwendung auf Raumtemperatur abgekühlt.
Wenn Oberflächenexsudat vorhanden ist, sollte eine Spülung unter Druck in Betracht gezogen werden. Mit Kochsalzlösung, die mit einer 35-mL-Spritze durch einen 19-Gauge-Angiokatheter gepresst wird, kann ein Spüldruck von etwa 8 psi erreicht werden. Die Wundoberfläche mit weicher, feuchter Gaze abtupfen; lebensfähiges Granulationsgewebe nicht zerstören.
Die Whirlpool-Behandlung ist großen und infizierten Wunden vorbehalten.
Für ein feuchtes (nicht nasses) Wundbett sorgen
Nach dem Débridement einen feuchten Kochsalzverband, ein isotonisches Natriumchloridgel (z. B. Normlgel , IntraSite-Gel) oder eine hydroaktive Paste (z. B. DuoDerm ) anlegen. Eine optimale Wundabdeckung erfordert feuchte bis nasse Verbände, die das autolytische Debridement unterstützen, Exsudat absorbieren und die umgebende normale Haut schützen.
Ein Polyvinylfolienverband (z. B. OpSite , Tegaderm ), der semipermeabel für Sauerstoff und Feuchtigkeit und undurchlässig für Bakterien ist, ist eine gute Wahl für Wunden, die weder trocken noch stark exsudativ sind.
Für trockene Wunden sind Hydrokolloid-Verbände wie DuoDerm oder IntraSite hydrocolloid, die für Sauerstoff, Feuchtigkeit und Bakterien undurchlässig sind. Sie halten ein feuchtes Milieu aufrecht und unterstützen das autolytische Debridement. Sie sind eine gute Wahl für relativ ausgetrocknete Wunden.
Für exsudative Wunden sind absorbierende Verbände wie Kalziumalginate (z. B. Kaltostat, Curasorb) und Hydrofaserverbände (z. B. Aquacel und Aquacel-AG) hochgradig absorbierend und für exsudative Wunden geeignet. Alginate sind in Strangform erhältlich, die sich zum Abdecken tiefer Wunden eignet.
Für stark exsudierende Wunden sind imprägnierte Mullverbände wie Mesalt (Scott) geeignet. Zweimal täglicher Verbandwechsel kann erforderlich sein.
Für infizierte Wunden ist Silbersulfadiazin (Silvadene) zu verwenden, wenn der Patient nicht allergisch gegen Sulfonamide ist. Ist der Patient allergisch gegen Sulfa, ist Bacitracin-Zink-Salbe eine gute Alternative. Ein Hydrofaser-Verband mit ionischem Silber (Aquacel-AG) ist ebenfalls eine gute Wahl.
Bei chronischen und hartnäckigen Wunden kann die Verwendung von Leptospermum- oder Manuka-Honig-imprägnierten Produkten hilfreich sein, um den Wundverschluss voranzutreiben.
Das Verbinden eines schwierigen anatomischen Bereichs (z. B. um ein Fersengeschwür) erfordert einen hochgradig anpassungsfähigen Verband, wie z. B. ein extradünnes Hydrokolloid. Die Sicherung eines Verbandes an einer sehr feuchten, schwierigen Stelle (z. B. um ein Sakrokoccygealulkus) erfordert einen anpassungsfähigen und stark haftenden Verband, wie z. B. ein Wafer-Hydrokolloid.
Hydrogel-Folien und nicht haftende Formen sind nützlich für die Sicherung eines Wundverbands, wenn die umgebende Haut empfindlich ist.
Tabelle 1. Merkmale und Verwendung von Wund- undVerbandsmaterialien (Tabelle in einem neuen Fenster öffnen)
|
Kategorie |
Beispiele |
Beschreibung |
Anwendungsbeispiele |
|
Alginat |
AlgiSite, Comfeel, Curasorb, Kaltogel, Kaltostat, Sorbsan, Tegagel |
Alginatverbände werden aus Algenextrakt hergestellt und enthalten Guluron- und Mannuronsäure, die für Zugfestigkeit sorgen, sowie Kalzium- und Natriumalginate, die eine Absorptionsfähigkeit verleihen. Einige können Fasern in der Wunde hinterlassen, wenn sie nicht gründlich gespült werden. Diese Verbände werden mit einer sekundären Abdeckung gesichert. |
Diese Verbände sind stark absorbierend und nützlich für Wunden mit reichlich Exsudat. Die Alginatschnur ist besonders nützlich, um exsudative Wundhöhlen oder Sinustrakte zu verpacken. |
|
Hydrofaser |
Aquacel, Aquacel-Ag, Versiva |
Ein saugfähiges Textilfaserkissen, Hydrofaser ist auch als Band zum Verpacken von tiefen Wunden erhältlich. Dieses Material ist mit einer Sekundärkompresse abgedeckt. Die Hydrofaser verbindet sich mit dem Wundexsudat und bildet ein hydrophiles Gel. Aquacel-Ag enthält 1,2 % ionisches Silber, das starke antimikrobielle Eigenschaften gegen viele Organismen aufweist, darunter Methicillin-resistenter Staphylococcus aureus und Vancomycin-resistente Enterokokken. |
Hydrofaser-Saugverbände für exsudative Wunden. |
|
Debridementmittel |
Hypergel (hypertonisches Kochsalzgel), Santyl (Kollagenase), Accuzyme (Papain-Harnstoff) |
Verschiedene Produkte bieten ein chemisches oder enzymatisches Debridement. |
Debridementmittel sind bei nekrotischen Wunden als Ergänzung zum chirurgischen Debridement nützlich. |
|
Schaum |
LYOfoam, Spyrosorb, Allevyn |
Polyurethanschaum hat ein Absorptionsvermögen. |
Diese Verbände sind nützlich für die Reinigung von granulierenden Wunden mit minimalem Exsudat. |
|
Hydrokolloid |
CombiDERM, Comfeel, DuoDerm CGF Extra Thin, Granuflex, Tegasorb |
Hydrokolloid-Verbände bestehen aus einer mikrogranularen Suspension natürlicher oder synthetischer Polymere, wie Gelatine oder Pektin, in einer Haftmatrix. Das Granulat geht bei der Absorption des Wundexsudats von einem halbhydratisierten Zustand in ein Gel über. |
Hydrokolloidverbände sind für trockene nekrotische Wunden, Wunden mit minimalem Exsudat und für saubere granulierende Wunden geeignet. |
|
Hydrogel |
Aquasorb, DuoDerm, Intrasite Gel, Granugel, Normlgel, Nu-Gel, Purilon Gel, KY Jelly |
Hydrogel-Verbände sind semipermeable hydrophile Polymere auf Wasser- oder Glycerinbasis; kühlende Eigenschaften können Wundschmerzen verringern. Diese Gele können je nach dem Hydratationszustand der Wunde Wasser verlieren oder aufnehmen. Sie werden mit einer sekundären Abdeckung gesichert. |
Diese Verbände sind für trockene, schorfige, nekrotische Wunden (Schorf) geeignet. |
|
Niedrig haftende Verbände |
Mepore, Skintact, Release |
Niedrig haftende Verbände bestehen aus verschiedenen Materialien, die sich leicht entfernen lassen, ohne die darunterliegende Haut zu beschädigen. |
Diese Verbände eignen sich für akute kleinere Wunden, wie z. B. Hautrisse, oder als Abschlussverband für chronische Wunden, die fast verheilt sind. |
|
Transparente Folien |
OpSite, Skintact, Release, Tegaderm, Bioclusive |
Transparente Folien sind hochgradig anpassungsfähige Acrylat-Klebefolien ohne Absorptionsvermögen und mit geringer Hydratationsfähigkeit. Sie können dampfdurchlässig oder perforiert sein. |
Diese Verbände sind für saubere, trockene Wunden mit minimalem Exsudat geeignet. Sie werden auch verwendet, um ein darunter liegendes absorbierendes Material zu befestigen, um Bereiche mit hoher Reibung und Bereiche, die schwer zu verbinden sind (z. B. Fersen), zu schützen und um intravenöse Katheter zu befestigen. |
Ziehen Sie andere topische Wirkstoffe in Betracht
Topisch applizierte Wachstumsfaktoren aus Blutplättchen haben eine bescheidene positive Wirkung auf die Wundheilung. Becaplermin-Gel 0,01 % (Regranex), ein rekombinanter menschlicher Wachstumsfaktor aus Blutplättchen (PDGF), der gentechnisch hergestellt wird, ist von der US-amerikanischen Food and Drug Administration (FDA) zur Förderung der Heilung von diabetischen Fußgeschwüren zugelassen. Regranex ist kontraindiziert bei Personen mit bekanntem Hautkrebs an der Applikationsstelle. Gefriergetrocknetes, plättchenreiches Plasma hat sich in einer Tierstudie als vielversprechend erwiesen.
Kollagen macht einen erheblichen Anteil des nekrotischen Weichgewebes in chronischen Wunden aus. Das Enzym Kollagenase, das aus der Fermentation von Clostridium histolyticum gewonnen wird, trägt dazu bei, nicht lebensfähiges Gewebe von der Oberfläche von Wunden zu entfernen. Kollagenase ist jedoch kein Ersatz für eine erste chirurgische Exzision einer stark nekrotischen Wunde.
Andere topische Mittel, die zur Wundbehandlung verwendet wurden, sind Zucker, Antazida und Vitamin A&D-Salbe.
Vermeiden Sie zytotoxische Mittel wie Wasserstoffperoxid, Povidon-Jod, Essigsäure und Dakin-Lösung (Natriumhypochlorit).
Kompressionstherapie in Betracht ziehen
Prüfen Sie die Zweckmäßigkeit einer Kompressionstherapie. Kompression ist bei Geschwüren, die durch ein Extremitätenödem verursacht oder verschlimmert werden, angebracht. Bei signifikanter arterieller Zuflussbeeinträchtigung muss die Kompression möglicherweise ganz vermieden werden.
Stützstrümpfe oder elastische Wickel mit einem Druck von ca. 40-60 mm Hg bei Fehlen einer arteriellen Erkrankung und 20-30 mm Hg bei Vorliegen oder Verdacht auf eine leichte arterielle Insuffizienz verwenden.
Schmerzbehandlung
Wundschmerzen durch Anfeuchten der Verbände vor dem Entfernen lindern. Erwägen Sie die Verwendung von 2%igem topischem Lidocain-Gel während der Wundversorgung. (Anekdotische Berichte beschreiben die Verwendung von topischem Morphin- und Diamorphin-Gel zur Linderung von Dekubitus-Schmerzen bei Patienten, die unheilbar krank sind, aber diese Verwendung ist nicht von der FDA zugelassen.)
Behandlung bestimmter Arten von Wunden
Druckgeschwüre
Die Behandlung von Dekubitus erfordert eine längere chirurgische und pflegerische Versorgung. Während des langen Behandlungszeitraums, der erforderlich ist, bleibt der Patient dem Risiko ausgesetzt, dass sich an anderen Stellen neue Druckgeschwüre entwickeln. Die Behandlung, insbesondere die Indikation für Lagerungsflächen, basiert auf einer angemessenen Einstufung des Dekubitus.
Milne et al. berichteten über die Ergebnisse des Programms eines Langzeit-Akutkrankenhauses zur Reduzierung des Auftretens von Druckgeschwüren. Die Einrichtung nutzte eine Fehler- und Wirkungsanalyse, um festzustellen, wo Verbesserungen in der Pflege am nötigsten waren. Das Krankenhaus stellte fest, dass seine als überdurchschnittlich hoch eingeschätzten Dekubitusraten mit Problemen wie dem Mangel an 1) Wundpflegefachkräften, 2) Methoden zur konsistenten Dokumentation von Präventions- und Wunddaten und 3) einem interdisziplinären Ansatz des Wundpflegeteams zusammenhingen. Nachdem das Krankenhaus diese Probleme in Angriff genommen hatte, sank die Inzidenz von Dekubitus in der Einrichtung innerhalb von 12 Monaten von 41 % (Ausgangswert) auf durchschnittlich 4,2 %.
Tabelle 2. Einstufung von Dekubitus (Tabelle in einem neuen Fenster öffnen)
|
Stadium |
Definition |
Erscheinungsbild |
Geeignete topische Behandlung |
Durchschnittliche Heilungszeit (d) |
|
I |
Nicht bleichbares Erythem der intakten Haut |
Rötliche Haut, die bei Druckentlastung nicht verschwindet; Verfärbung; Erwärmung; Verhärtung |
DuoDerm q2-3d |
|
|
II |
Teilweiser Hautverlust mit Beteiligung der Epidermis und/oder Dermis |
Rissbildung, Blasenbildung, flache Krater, Abschürfungen |
Reinigung mit Kochsalzlösung; DuoDerm/Tegaderm-Verband |
|
|
III |
Vollständiger Hautverlust bis in das subkutane Fettgewebe oder die Faszie |
Ausgeprägter Ulkusrand; tiefer Krater (im Allgemeinen 2.075 mm oder tiefer) |
Abtragen; mit Kochsalzlösung spülen; DuoDerm/Tegaderm auftragen |
|
|
IV |
Vollständiger Hautverlust mit ausgedehnter Beteiligung des darunter liegenden Gewebes |
Ausgedehnte Nekrosen; Schädigung der darunter liegenden Strukturen wie Muskeln, Knochen, Sehnen oder Gelenkkapseln |
Chirurgisches Débridement; Spülen mit Kochsalzlösung (möglicherweise unter Druck); Anlegen moderner aktueller Verbände; Erwägung von Antibiotika |
|
|
*Wenn die darüber liegende Haut nekrotisch ist, kann die Stadieneinteilung erst nach dem Débridement genau erfolgen. |
||||
Druckgeschwüre erfordern häufig die folgenden Schritte:
-
Débridement: Das Geschwür muss oft chirurgisch entfernt werden, meist bis auf den darunter liegenden Knochen. Wenn kein Erythem, Ödem, Fluktuation oder Drainage vorhanden ist, muss sauberer, trockener Schorf nicht chirurgisch entfernt werden, sondern kann mit Hilfe von Verbänden (z. B. Kolloiden, Hydrogelen), die ein feuchtes Milieu zur Förderung der Autolyse bieten, aufgeweicht und abgelöst werden.
-
Topische Wundversorgung: Wochen- oder monatelange tägliche Verbandwechsel sind erforderlich, bevor die Wunde zu granulieren beginnt und sauber genug für einen myokutanen Lappenverschluss erscheint.
-
Behandlung von Infektionen: Das Debridement ist ein sauberes, nicht steriles Verfahren. Häufige Débridements halten die oberflächliche Kolonisation auf einem akzeptablen Niveau. Abstrichkulturen sind oft bedeutungslos, da sie nur die Oberflächenbesiedlung einer lokalen Infektion widerspiegeln, die keine antibiotische Behandlung erfordert. Im Allgemeinen sind systemische Antibiotika nicht sinnvoll, es sei denn, es liegen Anzeichen einer fortschreitenden Infektion vor, wie Bakteriämie, Septikämie, fortschreitende Zellulitis oder hartnäckige Osteomyelitis.
-
Kontrolle der chronischen Wundkontamination: Chronische Wundkontamination aufgrund von Stuhlinkontinenz kann bei typischerweise bettlägerigen Patienten, die zur Entwicklung von sakralen und ischialen Druckgeschwüren neigen, ein ärgerliches Problem darstellen. Diese Arten von Geschwüren sind in den nachstehenden Abbildungen dargestellt. Die erste Behandlung besteht in einer diätetischen Behandlung. Zu den Nahrungsmitteln, die den Stuhl eindicken, gehören Apfelmus, Bananen, gekochte Milch, Brot, Käse, cremige Erdnussbutter, Grütze, Haferkleie, Haferflocken, Nudeln, Brezeln, Reis, Tapioka und Joghurt. In seltenen Fällen ist eine Stuhlableitung mittels Kolostomie erforderlich.
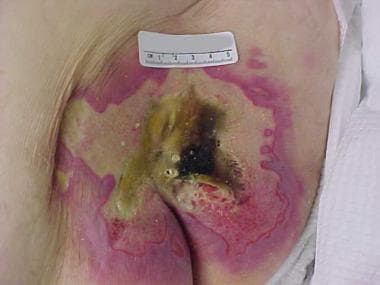 Das Bild eines fortgeschrittenen sakralen Druckgeschwürs zeigt die Auswirkungen von Druck, Scherung und Feuchtigkeit.
Das Bild eines fortgeschrittenen sakralen Druckgeschwürs zeigt die Auswirkungen von Druck, Scherung und Feuchtigkeit. 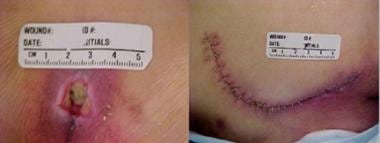 Sakrales Druckgeschwür vor und nach Lappenverschluss.
Sakrales Druckgeschwür vor und nach Lappenverschluss. 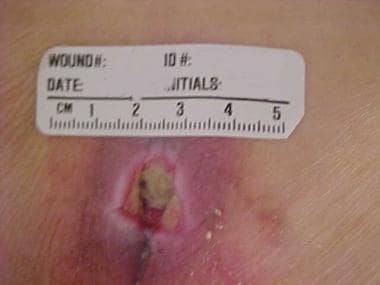 Sakralulkus.
Sakralulkus. -
Positionierung: Patienten mit Dekubitus oder solche, bei denen das Risiko eines Dekubitus besteht, sollten alle 2 Stunden im Bett gewendet werden. Patienten, die immobil sind, sollten nicht direkt auf den Trochantern gelagert werden; Schaumstoffkeile und -kissen sind nützlich, um Druckpunkte zu polstern, den direkten Kontakt zwischen Knochenvorsprüngen zu verhindern und die Fersen von der Bettfläche abzuheben. Druckgeschwüre können auch durch Scherkräfte verursacht werden, wenn die Patienten im Bett nach unten rutschen; daher sollte man versuchen, das Kopfende des Bettes so niedrig wie möglich anzuheben, wenn es der Gesundheitszustand des Patienten zulässt.
-
Verwendung von Lagerungsflächen
Auf Lagerungsflächen wird wie folgt eingegangen:
-
Bundesrechtliche Vorschriften (Medicare Bulletin 405) schreiben vor, dass Patienten mit Dekubitus oder solche, bei denen die Gefahr eines Dekubitus besteht, auf eine geeignete Lagerungsfläche gelegt werden müssen.
-
Bundesweit geltende Pflegestandards schreiben vor, welche Auflageflächen zulässig sind, und sehen sowohl zivil- als auch strafrechtliche Sanktionen für Einrichtungen des Gesundheitswesens vor, die die Vorschriften nicht einhalten.
-
Die ordnungsgemäße Vorbeugung und Behandlung von Druckgeschwüren in Gesundheitseinrichtungen wird durch Bundesvorschriften vorgeschrieben (Ch IV § 483.25 (c)(1)&(2), 10/1/95), in denen es heißt: „Auf der Grundlage der umfassenden Beurteilung eines Bewohners muss die Einrichtung sicherstellen, dass (1) ein Bewohner, der ohne Dekubitus in die Einrichtung kommt, keinen Dekubitus entwickelt, es sei denn, der klinische Zustand des Bewohners zeigt, dass er unvermeidbar war, und (2) ein Bewohner mit Dekubitus die notwendige Behandlung und Dienstleistungen erhält, um die Heilung zu fördern, Infektionen zu verhindern und die Entstehung neuer Dekubitus zu vermeiden.“
-
Eine Auflagefläche der Klasse I ist ein einfaches Druckpolstergerät, das wie folgt erforderlich ist:
-
Für Patienten, die ihre Körperposition nicht selbständig ändern können, um den Druck wirksam zu lindern
-
Für Patienten, die ein Druckgeschwür am Rumpf oder Becken in irgendeinem Stadium haben, sowie einen beeinträchtigten Ernährungszustand, Stuhl- oder Harninkontinenz, veränderte Sinneswahrnehmung oder beeinträchtigter Kreislauf
-
-
Eine Auflagefläche der Klasse II ist eine druckentlastende Vorrichtung, die den Druck über Knochenvorsprüngen auf weniger als 32 mm Hg reduziert und dies über einen längeren Zeitraum. Eine Lagerungsfläche der Klasse II ist wie folgt erforderlich:
-
Für Patienten, die mehrere Druckgeschwüre am Rumpf oder Becken haben, die sich trotz einer umfassenden Behandlung nicht gebessert haben, einschließlich einer Auflagefläche der Klasse I für einen Dekubitus im Stadium II, III, oder IV Dekubitus seit mindestens einem Monat
-
Für Patienten mit großen oder mehrfachen Dekubitus des Stadiums III oder IV am Rumpf oder Becken
-
Für Patienten, die innerhalb der letzten 60 Jahre einen Myokutanlappen oder ein Hauttransplantationsverfahren für einen Dekubitus am Rumpf oder Becken innerhalb der letzten 60 Tage hatten und unmittelbar vor der Entlassung aus einem Krankenhaus oder einer Pflegeeinrichtung innerhalb der letzten 30 Tage auf einer Lagerungsfläche der Klasse II oder III lagen
-
-
Eine Lagerungsfläche der Klasse III ist ein fortschrittliches druckentlastendesDruckentlastungsvorrichtung. Eine Lagerungsfläche der Klasse III, d. h. ein luftbefeuchtetes Bett, darf nur verwendet werden, wenn ein umfassender konservativer Behandlungsplan nach 30 Tagen versagt. (Beachten Sie, dass ein luftdurchströmtes Bett für jeden Patienten mit einer schweren pulmonalen Beeinträchtigung kontraindiziert ist, da das Fehlen einer festen Rückenstütze das Husten unwirksam macht und die trockene Luft die pulmonalen Sekrete verdickt). Ein solches konservatives Behandlungsprogramm umfasst Folgendes:
-
Aufklärung des Patienten und des Pflegepersonals. Eine Seite zur Patienteninformation über Dekubitus ist verfügbar.
-
Begutachtung durch einen zugelassenen Mediziner, mindestens wöchentlich
-
angemessenes Drehen und Lagern
-
Verwendung einer Liegefläche der Klasse II
-
angemessene Wundversorgung Wundversorgung
-
Angemessener Umgang mit Inkontinenz
-
Angemessener Umgang mit der Ernährung
-
Tabelle 3. Stützflächen (Tabelle in einem neuen Fenster öffnen)
|
Klasse |
Typ |
Grundsatz |
Beispiele |
|
I |
Einfache |
Druck-Druckentlastende Auflage oder Matte |
3- bis 5-Zoll-Schaumstoffmatratze, Gel-Auflage, Eierkarton-Matratze |
|
II |
Advanced |
Luftunterstützte* Auflage für Matratze mit geringem Luftverlust; Nicht angetriebener, fortschrittlicher, druckreduzierender Matratzenersatz oder angetriebenes Luft*-Schwebebett mit oder ohne niedrigem Luftverlust |
Roho Trockenschwebematratzen-System, Pegasus Renaissance Matratze |
|
III |
Luftfluidisierung |
Flotation durch gefilterte Luft*, die durch Porzellankügelchen gepumpt wird |
Clinitron Bett |
|
*LangfristigeDie langfristige Verwendung von Beatmungsgeräten ist bei Patienten mit chronisch obstruktiven Lungenerkrankungen relativ kontraindiziert, wie chronische Bronchitis, Emphysem und Asthma. |
|||
Zusätzlicher Schutz wird wie folgt beschrieben:
-
Angemessene Entlastung für ischiale Ulzera: Sakrale Ulzera entstehen in der Regel durch längere Rückenlage oder durch Scherkräfte, insbesondere durch das Abrutschen des Patienten im Bett bei erhöhtem Kopf. Andererseits entstehen Ischialulzera häufig durch langes Sitzen in Kopfhochlage im Bett oder im Rollstuhl. Daher erfordert die Entlastung zur Vorbeugung und Behandlung von Sitzbeinhöhlengeschwüren Stützflächen zum Sitzen sowie Matratzenstützflächen. Auch die Sitzdauer muss begrenzt werden.
-
Fersenschutz: Druckgeschwüre im Fersenbereich treten häufig bei bettlägerigen Patienten auf, auch wenn sie nur für wenige Tage immobilisiert sind, wie zum Beispiel nach einer Hüftoperation. Ein Dekubitus an der Ferse ist in der Abbildung unten dargestellt. Die Vorbeugung und Behandlung von Druckgeschwüren an der Ferse erfordert eine Entlastung. Entlastungsvorrichtungen werden in der Regel je nach Verfügbarkeit ausgewählt und umfassen die folgenden:
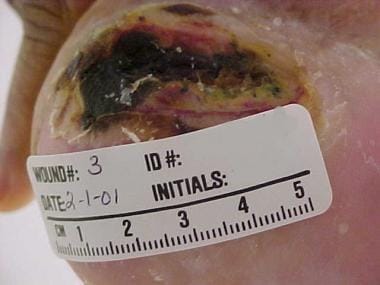 Fersendekubitus.
Fersendekubitus. Siehe nachstehende Liste:
-
Stiefel sind einfache Druckpolster, die die Ferse mit Polyesterfasern, ikonisierten Fasern oder Schaumstoff umgeben.
-
Stiefel bestehen aus einer festen Außenschale, die mit einer druckentlastenden Polsterung versehen ist. Sie können auch Positionierungsmöglichkeiten bieten, um Kontrakturen und Fußsenkungen zu behandeln.
-
Kissen aus Polyester und Schaffellvlies oder speziellem Gummi oder Kunststoff legen eine anpassungsfähige, weiche Auflage zwischen Ferse und Matratze.
-
Federungsvorrichtungen isolieren die Ferse und übertragen das Gewicht auf den Unterschenkel. Diese Vorrichtungen haben auch Positionierungsmöglichkeiten, die bei der Behandlung von Kontrakturen und Fußsenkungen nützlich sind.
-
Aufblasbare Vorrichtungen aus Kunststoffplatten umgeben die Ferse und das angrenzende Gewebe.
-
Venöse Geschwüre
Die Behandlung venöser Geschwüre umfasst eine Kompressionstherapie, die Bereitstellung eines feuchten Wundmilieus und das Debridement nekrotischen Gewebes. Die meisten venösen Ulzera heilen allein durch diese Maßnahmen ab. Einige erfordern eine Spalthauttransplantation oder die Anwendung von biotechnologisch hergestellter Haut (z. B. Apligraf, Dermagraft). Pentoxifyllin (Trental) und Rosskastaniensamen (erhältlich in Supermärkten und Reformhäusern) beschleunigen nachweislich die Heilung von venösen Stauungsulzera. In einigen Fällen reicht die Kompressionstherapie nicht aus, um die Heilung von venösen Ulzera aufrechtzuerhalten, und ein chirurgisches Venenstripping oder die Ligatur von Venenperforatoren kann hilfreich sein.
Eine Studie an 98 Gliedmaßen mit aktiven chronischen venösen Ulzera ergab, dass alle bis auf eine einen venösen Reflux hatten; die Studie legte auch nahe, dass die meisten dieser Patienten von einem chirurgischen oder endovaskulären Eingriff profitieren würden. Andere Studien wiesen auf einen eher bescheidenen Nutzen einer korrigierenden Venenoperation hin.
Tabelle 4. Kompressionsverbände für venöse Ulzera* (Tabelle in einem neuen Fenster öffnen)
|
Typ |
Beschreibung |
Beispiele |
|
Einlagig |
Einlagig-Lagen einfacher schlauchförmiger gewebter Nylon/Elastik-Binden können mit Rechtecken bedruckt werden, die sich zu Quadraten dehnen, wenn eine angemessene Wickelspannung (30-40 mm Hg) angelegt wird. |
ACE-Bandage, Comperm (Conco Medical), Setopress (Seton Healthcare Group) |
|
Dreilagig |
Die Lagen umfassen eine polsternde Absorptionsschicht, eine Kompressionsverbandschicht und einen kohäsiven Kompressionsverband. Die Verbände können je nach Wundexsudat bis zu 1 Woche an Ort und Stelle verbleiben. |
Dyna-Flex (Johnson & Johnson) |
|
Vier Lagen |
Die Lagen umfassen eine Wundkontaktschicht aus Vliesstoff, die für Wundexsudat durchlässig ist, und 4 darüberliegende Verbände. Die Verbände können je nach Exsudatmenge bis zu 1 Woche an Ort und Stelle verbleiben. |
Profore (Smith & Nephew) |
|
Imprägnierter Wickel |
Der poröse, flexible Okklusivverband besteht aus dehnbarer Gaze und einer nicht aushärtenden Zinkoxidpaste. |
Unna-Stiefel (ConvaTec) |
|
*Kompressionswickel sind bei schwerer arterieller Verschlusskrankheit kontraindiziert. Einige dieser Produkte sind bei Patienten mit Latexallergie kontraindiziert. |
||
Diabetische Fußgeschwüre
Die Behandlung von diabetischen Fußgeschwüren erfordert Folgendes: (1) geeignetes therapeutisches Schuhwerk, (2) tägliche Kochsalzlösung oder ähnliche Verbände, um ein feuchtes Wundmilieu zu schaffen, (3) Débridement, wenn nötig, (4) Antibiotikatherapie, wenn eine Osteomyelitis vorliegt, (5) optimale Blutzuckereinstellung und (6) Beurteilung und Korrektur der peripheren arteriellen Insuffizienz. Siehe auch Diabetische Geschwüre.
Wundabdeckung mit kultivierten menschlichen Zellen oder heterogenen Verbänden und/oder Transplantaten, Anwendung rekombinanter Wachstumsfaktoren, Unterdruck-Wundtherapie und hyperbare Sauerstoffbehandlungen können ebenfalls von Nutzen sein.
Lymphödem
Obwohl Lymphödeme in der Regel keine Ursache für Ulzerationen sind, können Geschwüre an den Extremitäten aufgrund eines unbehandelten Lymphödems nicht abheilen. Nächtliches Hochlagern der Beine und elastische Wickel oder Stützstrümpfe sind geeignete Hilfsmittel bei der Behandlung einer rezidivierenden Wunde an einer ödematösen Extremität. Bei fortgeschrittenen und nicht ansprechenden Lymphödemen ist eine komplexe entstauende Physiotherapie eine nützliche Behandlungsoption.
 Das Bild eines fortgeschrittenen sakralen Druckgeschwürs zeigt die Auswirkungen von Druck, Scherung und Feuchtigkeit.
Das Bild eines fortgeschrittenen sakralen Druckgeschwürs zeigt die Auswirkungen von Druck, Scherung und Feuchtigkeit.  Sakrales Druckgeschwür vor und nach Lappenverschluss.
Sakrales Druckgeschwür vor und nach Lappenverschluss.  Sakralulkus.
Sakralulkus.  Fersendekubitus.
Fersendekubitus.