Forma de dozare: capsulă
Revizuit medical de Drugs.com. Ultima actualizare la 1 octombrie 2020.
- Vizualizare
- Efecte secundare
- Dosare
- Profesional
- Sfaturi
- Consilii
- Interacțiuni
- Mai multe
Pentru a reduce dezvoltarea de medicamente-bacteriilor rezistente și menținerea eficacității nitrofurantoinei (macrocristale) și a altor medicamente antibacteriene, nitrofurantoina (macrocristale) trebuie utilizat numai pentru a trata sau preveni infecțiile a căror cauză bacteriană este dovedită sau puternic suspectată.
- DESCRIERE:
- FARMACOLOGIE CLINICĂ:
- MICROBIOLOGIE
- Mecanism de acțiune
- Interacțiuni cu alte antibiotice
- Dezvoltarea rezistenței
- INDICAȚII ȘI UTILIZARE:
- CONTRAINDICAȚII:
- Atenționări:
- Reacții pulmonare:
- Hepatotoxicitate:
- Neuropatie:
- Anemie hemolitică:
- Diarree asociată cu Clostridium difficile:
- PRECAUȚII:
- Informații pentru pacienți:
- Generalități:
- Interacțiuni medicamentoase:
- Interacțiuni medicament/teste de laborator:
- Carcinogeneză, mutageneză, afectarea fertilității:
- Femeie:
- Categoria B de fertilitate.
- Lucru și naștere:
- Mame care alăptează:
- Utilizare pediatrică:
- Utilizare geriatrică:
- REACȚII EXTREME:
- Respiratorii:
- Reacții hepatice:
- Neurologice:
- Dermatologice:
- Alergice:
- Gastro-intestinale:
- Hematologic:
- Diverse:
- Evenimente adverse de laborator:
- Supradozaj
- DOSAGE ȘI ADMINISTRARE:
- Adulți:
- Pacienți pediatrici:
- CUM SE FURNIZEAZĂ:
- PRINCIPAL DISPLAY PANEL – 50 mg
- PRINCIPAL DISPLAY PANEL – 100 mg
- Întrebări frecvente
- Mai multe despre nitrofurantoină
- Resurse pentru consumatori
- Resurse pentru profesioniști
- Ghiduri terapeutice conexe
DESCRIERE:
Nitrofurantoina, USP (macrocristale) este o substanță chimică de sinteză cu dimensiunea cristalină controlată. Este un compus stabil, galben, cristalin. Nitrofurantoina, USP (macrocristale) este un agent antibacterian pentru infecții specifice ale tractului urinar. Este disponibil sub formă de capsule de 25 mg, 50 mg și 100 mg pentru administrare orală.
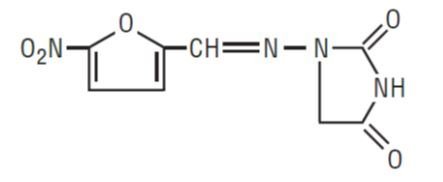
1-AMINO]-2, 4-IMIDAZOLIDINEDIONE
Ingrediente inactive: Fiecare capsulă conține D&C Galben # 10, FD&C Albastru # 1, FD&C Albastru # 2, FD&C Roșu # 40, gelatină, oxid de fier negru, lactoză anhidră, stearat de magneziu, amidon de porumb pregelatinizat, lauril sulfat de sodiu, talc și dioxid de titan. Capsulele de 50 mg și 100 mg conțin, de asemenea, FD&C Galben nr. 6.
FARMACOLOGIE CLINICĂ:
Nitrofurantoina (macrocristale) este o formă cristalină mai mare de nitrofurantoină. Absorbția nitrofurantoinei (macrocristale) este mai lentă și excreția sa este ceva mai mică în comparație cu nitrofurantoina. Concentrațiile sanguine la doze terapeutice sunt de obicei scăzute. Este foarte solubil în urină, căreia îi poate conferi o culoare brună.
În urma administrării unei doze de 100 mg de patru ori pe zi, timp de 7 zile, media recuperărilor urinare de medicament (de la 0 la 24 de ore) în ziua 1 și în ziua 7 a fost de 37 de doze.9% și 35,0%.
În comparație cu multe medicamente, prezența alimentelor sau a agenților care întârzie golirea gastrică poate crește biodisponibilitatea nitrofurantoinei (macrocristale), probabil prin faptul că permite o mai bună dizolvare în sucurile gastrice.
MICROBIOLOGIE
Nitrofurantoina este un agent antimicrobian nitrofuranic cu activitate împotriva anumitor bacterii Gram-pozitive și Gram-negative.
Mecanism de acțiune
Mecanismul acțiunii antimicrobiene a nitrofurantoinei este neobișnuit în rândul antibacterienilor. Nitrofurantoina este redusă de către flavoproteinele bacteriene la intermediari reactivi care inactivează sau alterează proteinele ribozomiale bacteriene și alte acromolecule. Ca urmare a acestor inactivări, sunt inhibate procesele biochimice vitale de sinteză a proteinelor, metabolismul energetic aerob, sinteza ADN-ului, sinteza ARN-ului și sinteza peretelui celular. Nitrofurantoina este bactericidă în urină la doze terapeutice. Natura amplă a acestui mod de acțiune poate explica lipsa rezistenței bacteriene dobândite la nitrofurantoină, deoarece mutațiile multiple și simultane necesare ale macromoleculelor țintă ar fi probabil letale pentru bacterii.
Interacțiuni cu alte antibiotice
Antagonismul a fost demonstrat in vitro între nitrofurantoină și antimicrobienele quinolone. Semnificația clinică a acestei constatări este necunoscută.
Dezvoltarea rezistenței
Dezvoltarea rezistenței la nitrofurantoină nu a reprezentat o problemă semnificativă de la introducerea sa în 1953. Rezistența încrucișată cu antibioticele și sulfonamidele nu a fost observată, iar rezistența transferabilă este, cel mult, un fenomen foarte rar.
Nitrofurantoina s-a dovedit a fi activă împotriva majorității tulpinilor următoarelor bacterii, atât in vitro, cât și în infecțiile clinice (vezi pct. Indicații și mod de utilizare):
Microorganisme Gram-pozitive aerobe și facultative:
Staphylococcus aureus
Enterococi (de ex. Enterococcus faecalis)
Microorganisme Gram-negative erogene și facultative:
Escherichia coli
NOTA: Deși nitrofurantoina are o activitate excelentă împotriva Enterococcus faecalis, majoritatea izolatelor de Enterococcus faecium nu sunt sensibile la nitrofurantoină.
Acel puțin 90 la sută din următoarele microorganisme prezintă o concentrație minimă inhibitorie (CMI) in vitro mai mică sau egală cu punctul de rupere sensibil pentru nitrofurantoină. Cu toate acestea, eficacitatea nitrofurantoinei în tratarea infecțiilor clinice datorate acestor microorganisme nu a fost stabilită în cadrul unor studii adecvate și bine controlate.
Microorganisme Gram-pozitive aerobe și facultative:
Stafilococi coagulazo-negativi (inclusiv Staphylococcus
epidermidis și Staphylococcus saprophyticus)
Streptococcus agalactiae
Streptococci din grupul D
Streptococi din grupul Viridans
Streptococi Gram-erobi și facultativi
.negative:
Citrobacter amalonaticus
Citrobacter diversus
Citrobacter freundii
Klebsiella oxytoca
Klebsiella ozaenae
NOTA: Unele tulpini ale speciilor Enterobacter și Klebsiella sunt rezistente la nitrofurantoină.
Testarea sensibilității:
Pentru informații specifice privind criteriile de interpretare a testelor de sensibilitate și metodele de testare asociate și standardele de control al calității recunoscute de FDA pentru acest medicament, vă rugăm să consultați: https://www.fda.gov/STIC.
INDICAȚII ȘI UTILIZARE:
Nitrofurantoina capsule (macrocristale) este indicată în mod specific pentru tratamentul infecțiilor tractului urinar atunci când sunt datorate tulpinilor sensibile de Escherichia coli, enterococi, Staphylococcus aureus și anumitor tulpini sensibile ale speciilor Klebsiella și Enterobacter.
Nitrofurantoina nu este indicată pentru tratamentul pielonefritei sau al abceselor perinefrice.
Pentru a reduce dezvoltarea bacteriilor rezistente la medicamente și pentru a menține eficacitatea nitrofurantoinei capsule (macrocristale) și a altor medicamente antibacteriene, nitrofurantoina capsule (macrocristale) trebuie utilizată numai pentru a trata sau preveni infecțiile care sunt dovedite sau puternic suspectate a fi cauzate de bacterii sensibile. Atunci când sunt disponibile informații privind cultura și sensibilitatea, acestea trebuie luate în considerare la selectarea sau modificarea tratamentului antibacterian. În absența unor astfel de date, epidemiologia locală și modelele de susceptibilitate pot contribui la selectarea empirică a terapiei.
Nitrofurantoinelor le lipsește distribuția tisulară mai largă a altor agenți terapeutici aprobați pentru infecțiile tractului urinar. În consecință, mulți pacienți care sunt tratați cu capsule de nitrofurantoină (macrocristale) sunt predispuși la persistența sau reapariția bacteriuriei. Probele de urină pentru culturi și teste de sensibilitate trebuie obținute înainte și după terminarea tratamentului. Dacă apare persistența sau reapariția bacteriuriei după tratamentul cu nitrofurantoină capsule (macrocristale), trebuie selectați alți agenți terapeutici cu distribuție tisulară mai largă. Atunci când se ia în considerare utilizarea capsulelor de nitrofurantoină (macrocristale), ratele mai mici de eradicare trebuie puse în balanță cu potențialul crescut de toxicitate sistemică și de dezvoltare a rezistenței antimicrobiene atunci când sunt utilizați agenți cu distribuție tisulară mai largă.
CONTRAINDICAȚII:
Anuria, oliguria sau insuficiența semnificativă a funcției renale (clearance-ul creatininei sub 60 ml pe minut sau creatinina serică crescută semnificativ din punct de vedere clinic) reprezintă contraindicații. Tratamentul acestui tip de pacienți comportă un risc crescut de toxicitate din cauza excreției deficitare a medicamentului. Din cauza posibilității de anemie hemolitică datorată sistemelor enzimatice eritrocitare imature (instabilitatea glutationului), medicamentul este contraindicat la pacientele gravide la termen (38 până la 42 săptămâni de gestație), în timpul travaliului și al nașterii sau atunci când debutul travaliului este iminent. Din același motiv, medicamentul este contraindicat la nou-născuții cu vârsta mai mică de o lună.
Nitrofurantoina capsule (macrocristale) este contraindicată la pacienții cu antecedente de icter colestatic/disfuncție hepatică asociată cu nitrofurantoina.
Capsulele de nitrofurantoină (macrocristale) sunt, de asemenea, contraindicate la acei pacienți cu hipersensibilitate cunoscută la nitrofurantoină.
Atenționări:
Reacții pulmonare:
REACȚII PULMONARE ACUTE, SUBACUTE SAU CRONICE AU FOST OBSERVATE LA PACIENȚII TRATAȚI CU NITROFURANTOINĂ. ÎN CAZUL APARIȚIEI ACESTOR REACȚII, NITROFURANTOINA (MACROCRISTALE) TREBUIE ÎNTRERUPTĂ ȘI TREBUIE LUATE MĂSURI ADECVATE. RAPOARTELE AU CITAT REACȚIILE PULMONARE CA FIIND O CAUZĂ CARE A CONTRIBUIT LA DECES.
REACȚIILE PULMONARE CRONICE (PNEUMONITĂ INTERSTIȚIALĂ DIFUZĂ SAU FIBROZĂ PULMONARĂ, SAU AMBELE) SE POT DEZVOLTA INSIDIOS. ACESTE REACȚII APAR RAR ȘI, ÎN GENERAL, LA PACIENȚII CARE PRIMESC TRATAMENT TIMP DE ȘASE LUNI SAU MAI MULT. MONITORIZAREA ATENTĂ A STĂRII PULMONARE A PACIENȚILOR CARE PRIMESC TRATAMENT PE TERMEN LUNG ESTE JUSTIFICATĂ ȘI NECESITĂ CA BENEFICIILE TRATAMENTULUI SĂ FIE PUSE ÎN BALANȚĂ CU RISCURILE POTENȚIALE (VEZI REACȚII RESPIRATORII).
Hepatotoxicitate:
Reacțiile hepatice, incluzând hepatită, icter colestatic, hepatită cronică activă și necroză hepatică, apar rar. Au fost raportate cazuri mortale. Debutul hepatitei cronice active poate fi insidios, iar pacienții trebuie monitorizați periodic pentru modificări ale testelor biochimice care ar putea indica leziuni hepatice. Dacă apare hepatita, medicamentul trebuie retras imediat și trebuie luate măsuri adecvate.
Neuropatie:
Au apărut cazuri de neuropatie periferică, care poate deveni severă sau ireversibilă. Au fost raportate decese. Afecțiuni precum insuficiența renală (clearance-ul creatininei sub 60 ml pe minut sau creatinină serică crescută semnificativ din punct de vedere clinic), anemia, diabetul zaharat, dezechilibrul electrolitic, deficitul de vitamina B și bolile debilitante pot favoriza apariția neuropatiei periferice. Pacienții care primesc tratament pe termen lung trebuie monitorizați periodic pentru modificări ale funcției renale.
Nerita optică a fost raportată rar în experiența postcomercializare cu formulări de nitrofurantoină.
Anemie hemolitică:
Cazuri de anemie hemolitică de tip sensibilitate la primachina au fost induse de nitrofurantoină. Hemoliza pare să fie legată de un deficit de glucoză-6-fosfat dehidrogenază în globulele roșii ale pacienților afectați. Această deficiență se întâlnește la 10 la sută dintre negri și la un mic procent din grupurile etnice de origine mediteraneană și din Orientul Apropiat. Hemoliza este o indicație pentru întreruperea tratamentului cu nitrofurantoină (macrocristale); hemoliza încetează la retragerea medicamentului.
Diarree asociată cu Clostridium difficile:
Diarreea asociată cu Clostridium difficile (CDAD) a fost raportată la utilizarea aproape tuturor agenților antibacterieni, inclusiv a nitrofurantoinei, și poate varia ca severitate de la diaree ușoară până la colită fatală. Tratamentul cu agenți antibacterieni modifică flora normală a colonului, ceea ce duce la o creștere excesivă a C. difficile.
C. difficile produce toxinele A și B care contribuie la apariția CDAD. Tulpinile de C. difficile care produc hipertoxine determină o morbiditate și o mortalitate crescute, deoarece aceste infecții pot fi refractare la terapia antimicrobiană și pot necesita colectomie. CDAD trebuie să fie luată în considerare la toți pacienții care prezintă diaree în urma utilizării de antibiotice. Este necesară o anamneză medicală atentă, deoarece s-a raportat că CDAD apare la peste două luni după administrarea de agenți antibacterieni. Dacă CDAD este suspectată sau confirmată, este posibil să fie necesară întreruperea utilizării continue a antibioticelor care nu sunt direcționate împotriva C. difficile. Administrarea adecvată a fluidelor și electroliților, suplimentarea cu proteine, tratamentul antibiotic al C. difficile și evaluarea chirurgicală trebuie instituite conform indicațiilor clinice.
PRECAUȚII:
Informații pentru pacienți:
Pacienții trebuie sfătuiți să ia nitrofurantoină (macrocristale) cu alimente pentru a spori și mai mult toleranța și a îmbunătăți absorbția medicamentului. Pacienții trebuie instruiți să completeze întreaga cură de tratament; cu toate acestea, trebuie sfătuiți să își contacteze medicul dacă apar simptome neobișnuite în timpul tratamentului.
Mulți pacienți care nu pot tolera nitrofurantoina microcristalină sunt capabili să ia nitrofurantoină (macrocristale) fără grețuri.
Pacienții trebuie sfătuiți să nu utilizeze preparate antiacide care conțin trisilicat de magneziu în timpul tratamentului cu nitrofurantoină (macrocristale).
Pacienții trebuie sfătuiți că medicamentele antibacteriene, inclusiv nitrofurantoina (macrocristale), trebuie utilizate numai pentru tratarea infecțiilor bacteriene. Acestea nu tratează infecțiile virale (de exemplu, răceala comună). Atunci când nitrofurantoina (macrocristale) este prescrisă pentru a trata o infecție bacteriană, pacienților trebuie să li se spună că, deși este obișnuit să se simtă mai bine la începutul tratamentului, medicamentul trebuie luat exact așa cum este indicat. Sărirea dozelor sau nefinalizarea cursului complet al terapiei poate (1) să diminueze eficacitatea tratamentului imediat și (2) să crească probabilitatea ca bacteriile să dezvolte rezistență și să nu mai poată fi tratate cu nitrofurantoină (macrocristale) sau cu alte medicamente antibacteriene în viitor.
Diarreea este o problemă frecventă cauzată de antibiotice care, de obicei, se termină atunci când antibioticul este întrerupt. Uneori, după începerea tratamentului cu antibiotice, pacienții pot dezvolta scaune apoase și sângeroase (cu sau fără crampe stomacale și febră) chiar și la două sau mai multe luni după ce au luat ultima doză de antibiotic. Dacă acest lucru se întâmplă, pacienții trebuie să își contacteze medicul cât mai curând posibil.
Generalități:
Prezentarea nitrofurantoinei (macrocristale) în absența unei infecții bacteriene dovedite sau puternic suspectate sau a unei indicații profilactice este puțin probabil să ofere beneficii pacientului și crește riscul de apariție a bacteriilor rezistente la medicamente.
Interacțiuni medicamentoase:
Antacidele care conțin trisilicat de magneziu, atunci când sunt administrate concomitent cu nitrofurantoina, reduc atât rata cât și gradul de absorbție. Mecanismul acestei interacțiuni este probabil adsorbția nitrofurantoinei pe suprafața trisilicatului de magneziu.
Medicamente uricosurice, cum ar fi probenecidul și sulfinpirazona, pot inhiba secreția tubulară renală a nitrofurantoinei. Creșterea rezultată a nivelurilor serice de nitrofurantoină poate crește toxicitatea, iar scăderea nivelurilor urinare ar putea diminua eficacitatea sa ca antibacterian al tractului urinar.
Interacțiuni medicament/teste de laborator:
Ca urmare a prezenței nitrofurantoinei, poate apărea o reacție fals-pozitivă pentru glucoză în urină. Acest lucru a fost observat cu soluțiile Benedict și Fehling, dar nu și cu testul enzimatic pentru glucoză.
Carcinogeneză, mutageneză, afectarea fertilității:
Nitrofurantoina nu a fost cancerigenă atunci când a fost administrată șobolanilor Holtzman femele timp de 44,5 săptămâni sau șobolanilor Sprague-Dawley femele timp de 75 de săptămâni. Două teste biologice cronice la rozătoare utilizând șobolani Sprague-Dawley masculi și femele și două teste biologice cronice la șoareci elvețieni și la șoareci BDF1 nu au evidențiat nicio dovadă de carcinogenitate.
Nitrofurantoina a prezentat dovezi de activitate carcinogenă la femelele de șoareci B6C3F1, așa cum reiese din creșterea incidenței adenoamelor tubulare, a tumorilor mixte benigne și a tumorilor cu celule granuloase ale ovarelor. La șobolanii masculi F344/N, s-a înregistrat o incidență crescută a neoplasmelor cu celule tubulare renale neobișnuite, a osteosarcoamelor osoase și a neoplasmelor țesutului subcutanat. Într-un studiu care a implicat administrarea subcutanată a 75 mg/kg de nitrofurantoină la șoareci femele gestante, au fost observate adenoame papilare pulmonare de semnificație necunoscută la generația F1.
S-a demonstrat că nitrofurantoina induce mutații punctiforme în anumite tulpini de Salmonella typhimurium și mutații directe în celulele de limfom de șoarece L5178Y. Nitrofurantoina a indus un număr crescut de schimburi de cromatide surori și aberații cromozomiale în celulele ovarelor de hamster chinezesc, dar nu și în celulele umane în cultură. Rezultatele testului letal recesiv recesiv legat de sex la Drosophila au fost negative după administrarea de nitrofurantoină prin hrănire sau prin injectare. Nitrofurantoina nu a indus mutații ereditare în modelele de rozătoare examinate.
Nu se cunoaște semnificația constatărilor privind carcinogenitatea și mutagenitatea în raport cu utilizarea terapeutică a nitrofurantoinei la om.
Administrarea de doze mari de nitrofurantoină la șobolani determină un stop spermatogenic temporar; acesta este reversibil la întreruperea administrării medicamentului. Dozele de 10 mg/kg/zi sau mai mari la bărbații sănătoși de sex uman pot produce, în anumite cazuri imprevizibile, un stop spermatogen ușor până la moderat, cu o scădere a numărului de spermatozoizi.
Femeie:
Efecte teratogene:
Categoria B de fertilitate.
S-au efectuat mai multe studii de reproducere la iepuri și șobolani la doze de până la șase ori mai mari decât doza umană și nu au evidențiat nicio dovadă de afectare a fertilității sau de vătămare a fătului din cauza nitrofurantoinei. Într-un singur studiu publicat, efectuat la șoareci la doze de 68 de ori mai mari decât doza umană (pe baza mg/kg administrate mamei), s-a observat un retard de creștere și o incidență scăzută a malformațiilor minore și comune. Cu toate acestea, la o doză de 25 de ori mai mare decât doza umană, nu au fost observate malformații fetale; relevanța acestor rezultate la om este incertă. Cu toate acestea, nu există studii adecvate și bine controlate la femeile însărcinate. Deoarece studiile de reproducere la animale nu sunt întotdeauna predictive pentru răspunsul la om, acest medicament trebuie utilizat în timpul sarcinii numai dacă este în mod clar necesar.
Efecte neteratogene:
Nitrofurantoina a demonstrat într-un studiu publicat de carcinogenitate transplacentară că induce adenoame papilare pulmonare la șoarecii din generația F1 la doze de 19 ori mai mari decât doza umană pe bază de mg/kg. Relația dintre această constatare și potențiala carcinogeneză la om este în prezent necunoscută. Din cauza incertitudinii privind implicațiile la om ale acestor date obținute la animale, acest medicament trebuie utilizat în timpul sarcinii numai dacă este în mod clar necesar.
Lucru și naștere:
Vezi CONTRAINDICAȚII.
Mame care alăptează:
Nitrofurantoina a fost detectată în laptele matern uman în cantități infime. Din cauza potențialului de reacții adverse grave cauzate de nitrofurantoină la sugarii care alăptează cu vârsta sub o lună, trebuie luată o decizie privind întreruperea alăptării sau întreruperea administrării medicamentului, ținând cont de importanța medicamentului pentru mamă (vezi pct. CONTRAINDICAȚII).
Utilizare pediatrică:
Nitrofurantoina (macrocristale) este contraindicată la sugarii cu vârsta sub o lună (vezi pct. CONTRAINDICAȚII).
Utilizare geriatrică:
Studiile clinice cu nitrofurantoina (macrocristale) nu au inclus un număr suficient de subiecți cu vârsta de 65 ani și peste pentru a determina dacă aceștia răspund diferit față de subiecții mai tineri. Alte experiențe clinice raportate nu au identificat diferențe de răspuns între pacienții vârstnici și cei mai tineri. Rapoartele spontane sugerează o proporție mai mare de reacții pulmonare, inclusiv decese, la pacienții vârstnici; aceste diferențe par a fi legate de proporția mai mare de pacienți vârstnici care primesc tratament cu nitrofurantoină pe termen lung. Ca și la pacienții mai tineri, reacțiile pulmonare cronice sunt în general observate la pacienții care primesc tratament timp de șase luni sau mai mult (vezi pct. ATENȚIONARE). Rapoartele spontane sugerează, de asemenea, o proporție crescută de reacții hepatice severe, inclusiv decese, la pacienții vârstnici (vezi punctul ATENȚIONARE).
În general, frecvența mai mare a scăderii funcției hepatice, renale sau cardiace, precum și a bolilor concomitente sau a altor terapii medicamentoase trebuie luată în considerare la prescrierea nitrofurantoinei (macrocristale). Se știe că acest medicament este excretat substanțial de către rinichi, iar riscul de reacții toxice la acest medicament poate fi mai mare la pacienții cu funcție renală deficitară. Anuria, oliguria sau insuficiența semnificativă a funcției renale (clearance-ul creatininei sub 60 ml pe minut sau creatinină serică crescută semnificativ din punct de vedere clinic) sunt contraindicații (vezi pct. CONTRAINDICAȚII). Deoarece pacienții vârstnici au o probabilitate mai mare de a avea funcția renală diminuată, trebuie să se acorde atenție la selectarea dozei și poate fi utilă monitorizarea funcției renale.
REACȚII EXTREME:
Respiratorii:
POT APĂREA REACȚII DE HIPERSENSIBILITATE PULMONARĂ CRONICĂ, SUBACUTĂ SAU ACUTĂ.
REACȚII PULMONARE CRONICĂ APAR ÎN GENERAL LA PACIENȚII CARE AU PRIMIT TRATAMENT CONTINUU timp de ȘASE LUNI SAU MAI MULT. STARE DE RĂU, DISPNEE LA EFORT, TUSE ȘI ALTERAREA FUNCȚIEI PULMONARE SUNT MANIFESTĂRI FRECVENTE CARE POT APĂREA INSIDIOS. CONSTATĂRILE RADIOLOGICE ȘI HISTOLOGICE DE PNEUMONITĂ INTERSTIȚIALĂ DIFUZĂ SAU FIBROZĂ, SAU AMBELE, SUNT, DE ASEMENEA, MANIFESTĂRI FRECVENTE ALE REACȚIEI PULMONARE CRONICE. FEBRA ESTE RAREORI PROEMINENTĂ.
GRAVITATEA REACȚIILOR PULMONARE CRONICE ȘI GRADUL LOR DE REZOLUȚIE PAR SĂ FIE LEGATE DE DURATA TRATAMENTULUI DUPĂ APARIȚIA PRIMELOR SEMNE CLINICE. FUNCȚIA PULMONARĂ POATE FI AFECTATĂ PERMANENT, CHIAR ȘI DUPĂ ÎNCETAREA TRATAMENTULUI. RISCUL ESTE MAI MARE CÂND REACȚIILE PULMONARE CRONICE NU SUNT RECUNOAȘTETE TEMPORAT.
În reacțiile pulmonare subacute, febra și eozinofilia apar mai rar decât în forma acută. La încetarea tratamentului, recuperarea poate necesita câteva luni. Dacă simptomele nu sunt recunoscute ca fiind legate de medicament și tratamentul cu nitrofurantoină nu este întrerupt, simptomele pot deveni mai severe.
Reacțiile pulmonare acute se manifestă frecvent prin febră, frisoane, tuse, durere toracică, dispnee, infiltrație pulmonară cu consolidare sau revărsare pleurală la radiografie și eozinofilie. Reacțiile acute apar de obicei în prima săptămână de tratament și sunt reversibile odată cu încetarea tratamentului. Rezoluția este adesea dramatică (vezi pct. ATENȚIE).
Schimbări ale EKG (de ex, modificări nespecifice ale undei ST/T, bloc de ramură) au fost raportate în asociere cu reacții pulmonare.
Cianoza a fost raportată rar.
Reacții hepatice:
Reacțiile hepatice, inclusiv hepatită, icter colestatic, hepatită cronică activă și necroză hepatică, apar rareori (vezi pct. AVERTIZĂRI).
Neurologice:
Nevropatie periferică, care poate deveni severă sau ireversibilă, a apărut. Au fost raportate decese. Afecțiuni precum insuficiența renală (clearance-ul creatininei sub 60 ml pe minut sau creatinină serică crescută semnificativ din punct de vedere clinic), anemia, diabetul zaharat, dezechilibrul electrolitic, deficitul de vitamina B și bolile debilitante pot crește posibilitatea apariției neuropatiei periferice (vezi punctul ATENȚIONARE).
Astenia, vertijul, nistagmusul, amețeala, cefaleea și somnolența au fost, de asemenea, raportate la utilizarea nitrofurantoinei.
Au fost raportate rar hipertensiune intracraniană benignă (pseudotumor cerebri), confuzie, depresie, nevrită optică și reacții psihotice. Fontanelele bombate, ca semn de hipertensiune intracraniană benignă la sugari, au fost raportate rar.
Dermatologice:
Dermatită exfoliativă și eritem multiform (inclusiv sindromul Stevens-Johnson) au fost raportate rar. A fost raportată, de asemenea, alopecie tranzitorie.
Alergice:
A fost raportat un sindrom asemănător lupusului asociat cu reacții pulmonare la nitrofurantoină. De asemenea, au fost raportate angioedem; erupții maculopapuloase, eritematoase sau eczematoase; prurit; urticarie; anafilaxie; artralgie; mialgie; febră medicamentoasă; frisoane; și vasculită (uneori asociată cu reacții pulmonare). Reacțiile de hipersensibilitate reprezintă cele mai frecvente reacții adverse raportate spontan în experiența postcomercializare la nivel mondial cu formulările de nitrofurantoină.
Gastro-intestinale:
Nausea, emeza și anorexia apar cel mai des. Durerea abdominală și diareea sunt reacții gastrointestinale mai puțin frecvente. Aceste reacții legate de doză pot fi minimizate prin reducerea dozei. Au fost raportate sialadenită și pancreatită. Au fost raportate sporadic cazuri de colită pseudomembranoasă la utilizarea nitrofurantoinei. Apariția simptomelor de colită pseudomembranoasă poate apărea în timpul sau după tratamentul antimicrobian (vezi pct. ATENȚIONARE).
Hematologic:
Au fost raportate rareori cianoză secundară la methemoglobinemie.
Diverse:
Ca și în cazul altor agenți antimicrobieni, suprainfecțiile cauzate de organisme rezistente, de ex, specii de Pseudomonas sau specii de Candida, pot apărea.
Evenimente adverse de laborator:
Au fost raportate următoarele evenimente adverse de laborator la utilizarea nitrofurantoinei: creșterea AST (SGOT), creșterea ALT (SGPT), scăderea hemoglobinei, creșterea fosforului seric, eozinofilie, anemie prin deficit de glucoză-6-fosfat-dehidrogenază (vezi pct. ATENȚIONARE), agranulocitoză, leucopenie, granulocitopenie, anemie hemolitică, trombocitopenie, anemie megaloblastică. În majoritatea cazurilor, aceste anomalii hematologice s-au rezolvat după întreruperea tratamentului. Rareori a fost raportată anemie aplastică.
Supradozaj
Incidentele ocazionale de supradozaj acut de nitrofurantoină (macrocristale) nu au determinat alte simptome specifice în afară de vărsături. Se recomandă inducerea emezei. Nu există un antidot specific, dar trebuie menținut un aport ridicat de lichide pentru a favoriza excreția urinară a medicamentului. Este dializabil.
DOSAGE ȘI ADMINISTRARE:
Nitrofurantoina capsule (macrocristale) trebuie administrată cu alimente pentru a îmbunătăți absorbția medicamentului și, la unii pacienți, toleranța.
Adulți:
50 mg până la 100 mg de patru ori pe zi – nivelul de dozare mai mic este recomandat pentru infecțiile necomplicate ale tractului urinar.
Pacienți pediatrici:
5 până la 7 mg/kg de greutate corporală pe 24 de ore, administrate în patru doze divizate (contraindicat la vârsta sub o lună).
Terapia trebuie continuată timp de o săptămână sau timp de cel puțin 3 zile după obținerea sterilității urinei. Continuarea infecției indică necesitatea reevaluării.
Pentru tratamentul supresiv pe termen lung la adulți, o reducere a dozei la 50-100 mg la culcare poate fi adecvată. Pentru tratamentul supresiv pe termen lung la pacienții pediatrici, doze de până la 1 mg/kg la 24 de ore, administrate într-o singură doză sau în două doze divizate, pot fi adecvate. A SE VEDEAȚI SECȚIUNEA AVERTIZĂRI PRIVIND RISCURILE ASOCIATE TERAPIEI PE TERMEN LUNGIT.
CUM SE FURNIZEAZĂ:
Capsulele de nitrofurantoină USP (macrocristale) sunt disponibile după cum urmează:
Capsule de 50 mg corp alb opac și capac galben opac, imprimat cu cerneală neagră cu „WATSON” pe capac și „5780” pe corp.
NDC 0115-2023-10 flacoane a câte 100
100 mg capsulă opacă, galbenă, imprimată cu cerneală neagră cu „WATSON” pe capac și „5781” pe corp.
NDC 0115-2024-10 flacoane a 100
Să se păstreze la temperaturi cuprinse între 20° și 25°C (68° și 77°F) .
Fabricat de:
Watson Pharma Private Limited
Verna, Salcette Goa 403722 INDIA
Distribuit de:
Watson Pharma Private Limited
Verna, Salcette Goa 403722 INDIA
Distribuit de:
Amneal Pharmaceuticals LLC
Bridgewater, NJ 08807
Pentru a raporta reacții adverse SUSPECTE, contactați Amneal Pharmaceuticals la 1-877-835-5472 sau FDA la 1-800-FDA-1088 sau www.fda.gov/medwatch.
Rev. 11-2019-00
PRINCIPAL DISPLAY PANEL – 50 mg

PRINCIPAL DISPLAY PANEL – 100 mg

| NITROFURANTOINA nitrofurantoină capsulă |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||