Liga Internațională Împotriva Epilepsiei (ILAE) și-a revizuit definiția epilepsiei în 2014 pentru a maximiza identificarea și tratamentul precoce al pacienților cu epilepsie.1 Definiția conceptuală a ILAE a epilepsiei, formulată pentru prima dată în 2005, este „o tulburare a creierului caracterizată printr-o predispoziție durabilă de a genera crize epileptice”. În practică, această definiție a corespuns pacienților cu două sau mai multe crize neprovocate la mai mult de 24 de ore distanță. Știm, însă, că nu toți pacienții cu o singură criză neprovocată au aceeași probabilitate de a avea o a doua criză. Conform noii definiții ILAE, pacienții cu o singură criză neprovocată și o probabilitate de recurență a crizelor de peste 60% îndeplinesc acum criteriile pentru un diagnostic de epilepsie.
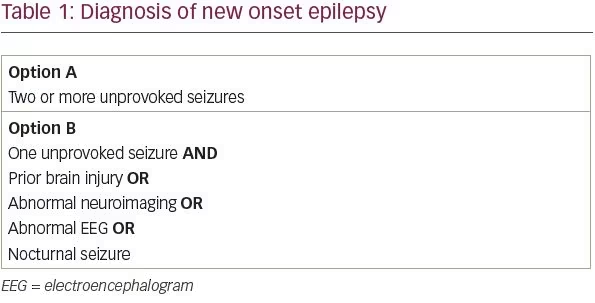
Într-o analiză sistematică a studiilor care evaluează riscul de recurență a crizelor după o singură criză neprovocată, între 21 și 45% dintre pacienți au avut o altă criză neprovocată în primii 2 ani.2 Din punct de vedere practic, au fost identificați patru factori de risc care dublează aproximativ riscul de recurență a crizelor la un pacient: o leziune cerebrală anterioară, o constatare neuroimagistică anormală care corespunde focarului suspectat de criză, descărcări epileptiforme focale sau generalizate pe electroencefalogramă (EEG) sau o criză nocturnă.3-6 Astfel, pacienții cu o singură criză neprovocată și cel puțin unul dintre acești patru factori de risc au probabil o șansă mai mare de 60% de a avea crize recurente și pot fi diagnosticați cu epilepsie (tabelul 1).
Deși un studiu timpuriu important a sugerat că o examinare neurologică anormală a fost asociată cu un risc crescut de recurență a crizelor, un studiu de urmărire al aceluiași grup nu a constatat nicio creștere a riscului.3,7 Același studiu de urmărire a constatat că faptul de a avea un frate sau o soră cu epilepsie crește riscul de recurență în rândul pacienților cu epilepsie idiopatică, dar chiar și în rândul acestor pacienți, riscul de recurență este de numai 46% la 5 ani. Astfel, constatările examenului neurologic și istoricul familial de epilepsie trebuie luate în considerare atunci când se evaluează un pacient cu o primă criză, dar aceste caracteristici singure nu sunt suficiente pentru a pune un diagnostic de epilepsie.
Considerarea tratamentului cu medicamente antiepileptice în epilepsia cu debut nou
Majoritatea studiilor timpurii privind recurența crizelor după o criză inițială neprovocată au inclus atât pacienți tratați cu medicamente antiepileptice (AED), cât și netratați, ceea ce face dificilă estimarea riscului real de recurență a crizelor. Studiul FIRST a constatat că 51% dintre pacienții care nu au început un AED după o primă criză au avut o altă criză în termen de 2 ani, în timp ce doar 25% dintre cei care au început un AED au avut o altă criză în aceeași perioadă.8 Cu toate acestea, studiile ulterioare au arătat că, deși tratamentul cu AED reduce riscul de recurență a crizelor în primii 2 ani după o criză inițială, acesta nu afectează probabilitatea de remisiune a crizelor pe termen lung sau calitatea vieții.9,10 Deoarece tratamentul precoce cu AED nu este garantat că va schimba rezultatul general al pacientului, iar AED nu sunt medicamente complet benigne, nu toți pacienții care sunt diagnosticați cu epilepsie aleg să înceapă tratamentul imediat.
Toate deciziile privind tratamentul cu AED trebuie luate în colaborare cu pacientul, după o discuție atentă a riscurilor și beneficiilor, punând în balanță riscul de vătămare datorat convulsiilor și potențialele efecte adverse ale AED. Prezența unui tip de criză care este asociat cu un risc mai mare de vătămare sau de deces, cum ar fi crizele tonico-clonice sau status epilepticus, poate fi un factor care să influențeze decizia pacientului și a medicului de a începe sau nu AED.11-13
Caracterizarea tipului de epilepsie
Determinarea tipului de epilepsie al pacientului – focală sau generalizată – în momentul diagnosticului inițial este importantă deoarece ajută la predicția prognosticului și ghidează selecția unei AED adecvate. Această determinare se face de obicei pe baza semiologiei crizelor împreună cu rezultatele imagisticii prin rezonanță magnetică (IRM) și EEG. Simptomele motorii sau senzoriale lateralizate, devierea forțată a ochilor sau întoarcerea capului, automatismele, tulburările de limbaj și fenomenele experiențiale sugerează un debut focal, în timp ce sacadarea mioclonică bilaterală sau activitatea tonică bilaterală inițială sugerează un debut generalizat.
Cu toate acestea, semiologia singură poate fi înșelătoare: crizele focale pot fi lipsite de trăsături de lateralizare la debut și mai mult de jumătate dintre pacienții cu epilepsie generalizată au simptome de crize focale.14 Mai mult, trei sferturi dintre pacienții cu epilepsie focală sunt amnezici pentru cel puțin unele dintre crizele lor, iar 30% sunt amnezici pentru toate crizele.15 În plus, până la 60% dintre pacienți nu au o aură care să le precedă crizele.16 Acești factori fac ca diagnosticul și caracterizarea epilepsiei să fie o provocare la mulți pacienți.
Majoritatea pacienților cu o primă criză ar trebui să facă un RMN, cu excepția cazului în care există o contraindicație. IRM are un randament mai mare decât tomografia computerizată (CT) pentru detectarea leziunilor epileptogene focale.17-19 Prezența unei leziuni focale poate confirma un debut focal dacă localizarea leziunii corespunde semiologiei pacientului. Pentru pacienții cu un sindrom electroclinic clar de epilepsie primară generalizată electroclinică, cum ar fi epilepsia mioclonică juvenilă, neuroimagistica poate să nu fie necesară.
În cazul în care se obține un RMN, secvențele recomandate includ o secvență 3D T1 cu felii izotrope de 1 mm (de ex, ecou de gradient rapid pregătit pentru magnetizare ), secvențe T2 și FLAIR axiale și coronale cu felii ≤3 mm și o secvență T2* axială pentru hemosiderină și calcificare (de exemplu, imagistică ponderată în funcție de susceptibilitate sau ecou de gradient ).20 Contrastul nu este necesar pentru toți pacienții, dar ar trebui luat în considerare pentru pacienții cu vârsta de peste 50 de ani, din cauza probabilității mai mari de tumoră cerebrală metastatică sau primară în această grupă de vârstă. Atunci când este posibil, se preferă RMN de 3 Tesla în locul celui de 1,5 Tesla, deoarece este mai sensibil pentru leziunile epileptogene.21,22 Recent, scanerele RMN de 7 Tesla au crescut și mai mult sensibilitatea, dar acestea sunt de obicei disponibile doar prin intermediul protocoalelor de cercetare.23
EEG este cealaltă modalitate esențială pentru diagnosticarea și caracterizarea epilepsiei nou apărute. Un singur EEG de rutină poate fi insuficient pentru detectarea anomaliilor epileptiforme; o meta-analiză recentă a 15 studii a constatat că sensibilitatea unui EEG de rutină a fost de 17%.24 Pentru a crește acest randament, medicii ar trebui să ia în considerare efectuarea unui EEG prelungit de 60 de minute, a unui EEG cu privare de somn sau a până la trei EEG-uri de rutină în serie.25-27 Înregistrările EEG ambulatorii cresc, de asemenea, probabilitatea de a detecta anomalii epileptiforme; beneficiile înregistrării prelungite se diminuează după 48 de ore, deoarece 95% dintre anomalii sunt detectate în acest interval de timp.28 Un studiu video EEG în staționar poate fi luat în considerare în scenarii specifice, cum ar fi diferențierea crizelor epileptice de atacurile psihogene non-epileptice.29
Selectarea unui medicament antiepileptic-epilepsie focală
Studiul SANAD-Tratamentul de primă linie al epilepsiei focale cu debut nou
Obiectivul tratamentului cu MEA în epilepsia cu debut nou este de a controla crizele cu un singur MEA, minimizând în același timp efectele adverse. Deși există multe medicamente disponibile pentru tratamentul epilepsiei focale, există puține studii controlate care să compare eficacitatea și tolerabilitatea acestora. Studiul SANAD, publicat în 2007, a fost un studiu de referință cu 1.721 de pacienți cu epilepsie focală randomizați la tratament cu carbamazepină, gabapentin, lamotrigină, oxcarbazepină sau topiramat.30 Rezultatul principal a fost timpul până la eșecul tratamentului, definit ca întreruperea tratamentului din cauza crizelor necontrolate sau a efectelor adverse. Lamotrigina a fost semnificativ mai bună decât carbamazepina, gabapentina și topiramatul, și nesemnificativ mai bună decât oxcarbazepina. Cu toate acestea, pentru timpul până la remisiunea de 12 luni, carbamazepina a fost semnificativ mai bună decât gabapentina și nesemnificativ mai bună decât lamotrigina, topiramatul și oxcarbazepina.30
Rezultatele studiului SANAD sugerează că lamotrigina este cel mai bun tratament de primă linie pentru epilepsia focală datorită combinației sale de eficacitate și tolerabilitate, carbamazepina fiind o alternativă rezonabilă la pacienții care o pot tolera.
Medicamente antiepileptice noi pentru tratamentul de primă linie al epilepsiei focale
De la publicarea studiului SANAD, au intrat pe piață mai multe medicamente noi pentru epilepsia focală. Deși toate aceste medicamente au fost inițial studiate ca tratamente adjuvante, multe dintre ele sunt acum utilizate ca monoterapie, iar unele, în special levetiracetamul, sunt acum utilizate în mod obișnuit ca tratament de primă linie. Un avantaj major al acestor medicamente noi este că dozele pot fi crescute rapid la pacienții cu crize frecvente, fără riscul apariției sindromului Stevens-Johnson, un efect advers cunoscut al lamotriginei și, într-o mai mică măsură, al carbamazepinei.
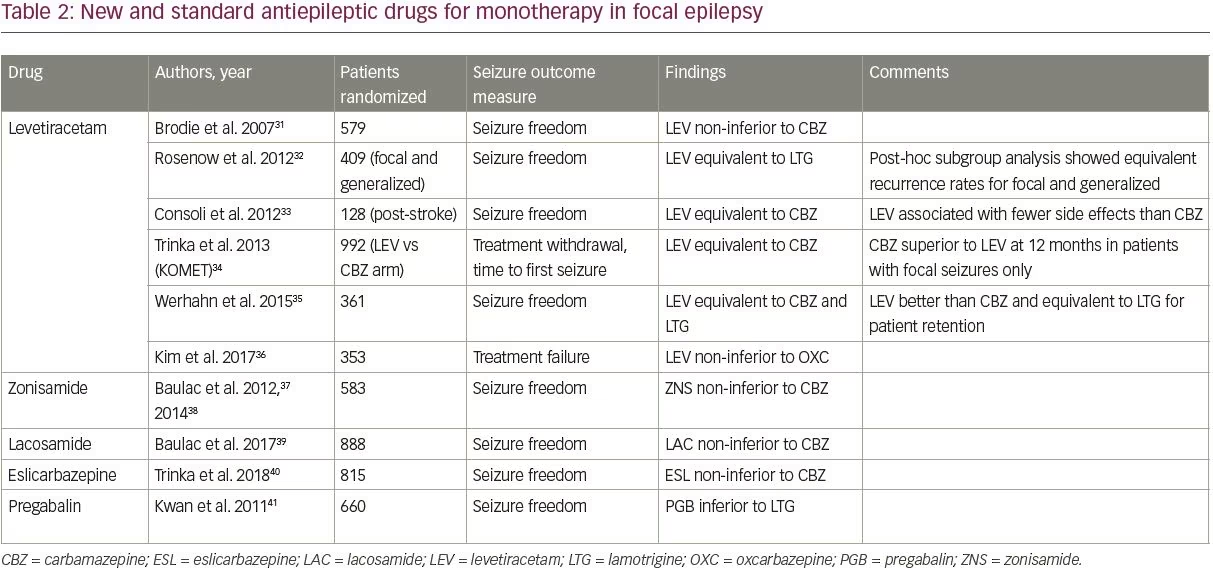
Printre noile DEA, patru – levetiracetam, zonisamidă, lacosamidă și eslicarbazepină – au fost comparate cu DEA mai vechi în studii randomizate controlate, așa cum se arată în tabelul 2.31-41 Studiile au fost identificate utilizând filtrul de studii clinice din PubMed și termenii de căutare „monotherapy,” și „”, și au fost incluse dacă au studiat pacienți adulți cu epilepsie focală comparând o MEA mai nouă cu una dintre MEA standard (cele incluse în studiul SANAD).
Dintre cele patru AED noi, levetiracetamul este cel mai bine studiat și cel mai larg prescris; acesta a devenit în mare măsură AED de primă linie implicită pentru epilepsia cu debut nou datorită ușurinței de titrare și profilului său favorabil de efecte secundare. Levetiracetamul este acum cel mai frecvent prescris AED de primă linie la adulții mai în vârstă, reprezentând 45,5% din prescripții.42 Studiile au arătat că levetiracetamul are o eficacitate similară în comparație cu MAE mai vechi, deși a fost inferior carbamazepinei într-o analiză de subgrup a unui studiu (tabelul 2).
Important este faptul că doar două studii au comparat levetiracetamul cu lamotrigina; ambele studii au constatat o eficacitate similară pentru cele două medicamente.32,35 Ramura de epilepsie focală a studiului SANAD II, care va fi cel mai amplu studiu de comparare a eficacității și tolerabilității pe termen lung a levetiracetamului și a lamotriginei, este în prezent în curs de desfășurare (ISRCTN30294119).
În afara levetiracetamului, datele de înaltă calitate care evaluează noile DEA ca monoterapie sunt limitate. Zonisamida, lacosamida și eslicarbazepina s-au dovedit a fi toate non-inferioare carbamazepinei într-un singur studiu fiecare (tabelul 2); zonisamida este, de asemenea, studiată în brațul focal al studiului SANAD II. Acești trei agenți pot fi luați în considerare ca opțiuni pentru tratamentul de primă linie, în funcție de comorbiditățile și contraindicațiile pacientului. Pregabalina a fost, de asemenea, studiată în comparație cu lamotrigina și a fost inferioară,41 și, prin urmare, nu este recomandată ca
tratament de primă linie.
Brivaracetamul a fost bine tolerat în două studii randomizate de conversie de la politerapie la monoterapie, dar numărul de pacienți care au rămas pe brivaracetam la sfârșitul acestor studii a fost prea mic pentru a determina eficacitatea sa ca monoterapie;43 de asemenea, nu a fost studiat în comparație directă cu AED-uri mai vechi. Astfel, în acest moment nu există dovezi suficiente pentru a recomanda brivaracetam în monoterapie ca tratament de primă linie.
Clobazam, perampanel și cenobamat sunt MEA noi cu potențial de utilizare ca monoterapie. Atât clobazamul, cât și perampanelul au fost eficace și bine tolerate în cadrul unor mici studii retrospective care au inclus pacienți cu epilepsie atât focală, cât și generalizată.44,45 Clobazamul a fost, de asemenea, superior carbamazepinei și fenitoinei într-un studiu randomizat la pacienți pediatrici, dar nu a fost comparat direct cu MAE mai vechi la o populație adultă.46 Cenobamatul, un intensificator al inactivării rapide și lente a canalelor de sodiu cu dozare o dată pe zi, a demonstrat recent eficacitatea ca agent adjuvant pentru pacienții cu epilepsie focală, dar nu a fost încă studiat ca monoterapie.47
Rezumat al tratamentului de primă linie pentru epilepsia focală
Levetiracetam a avut performanțe la fel de bune sau ușor mai slabe decât cele ale medicamentelor antiepileptice mai vechi în studiile head-to-head,31-36 și este un tratament rezonabil de primă linie la pacienții fără antecedente de probleme psihiatrice, în special dacă crizele sunt frecvente sau dacă pacienții au dificultăți cu programul de titrare a lamotriginei. La pacienții cu comorbidități psihiatrice, recomandăm lamotrigina ca tratament de primă linie. Studiul SANAD II, în curs de desfășurare, va răspunde mai definitiv la întrebarea care dintre aceste două AED este superior atât în ceea ce privește eficacitatea, cât și tolerabilitatea. În funcție de comorbiditățile pacientului și de toleranța la efectele secundare, mai multe dintre AED-urile mai vechi (carbamazepină, oxcarbazepină, topiramat) și AED-urile mai noi (zonisamidă, lacosamidă, eslicarbazepină) pot fi alternative rezonabile. Brivaracetamul, clobazamul, perampanelul și cenobamatul pot fi opțiuni viabile în viitor, dar nu există dovezi suficiente în acest moment. Gabapentina și pregabalina nu trebuie utilizate ca tratamente de primă linie.
Selectarea unui medicament antiepileptic-epilepsie generalizată sau neclasificată
Etalonul SANAD-Tratamentul de primă linie al epilepsiei generalizate nou apărute
Etalonul SANAD din 2007 a inclus un al doilea braț, care a studiat pacienții cu epilepsie generalizată sau epilepsie care nu a putut fi clasificată definitiv la momentul inițierii tratamentului.48 Valproatul a fost semnificativ mai bun decât topiramatul în ceea ce privește timpul până la eșecul tratamentului în analiza globală și semnificativ mai bun atât decât topiramatul, cât și decât lamotrigina la pacienții cu un diagnostic confirmat de epilepsie generalizată. Pentru timpul până la remisiunea la 12 luni, valproatul a fost semnificativ mai bun decât lamotrigina în ambele grupuri, dar nu a fost semnificativ diferit de topiramat în niciunul dintre grupuri. Astfel, valproatul a părut să aibă cea mai bună combinație de eficacitate și tolerabilitate dintre cele trei medicamente studiate.
În ciuda succesului valproatului în SANAD, utilizarea sa în afara cadrului de studiu este problematică din cauza efectelor sale adverse. În rândul femeilor de vârstă fertilă, valproatul este contraindicat din cauza teratogenității, deoarece crește semnificativ riscul de malformații congenitale și deficite neurocognitive pe termen lung.49-52 Începând cu 2018, Uniunea Europeană a interzis utilizarea valproatului la femeile de vârstă fertilă, cu excepția cazului în care acestea sunt înscrise într-un program de prevenire a sarcinii.53 Valproatul are, de asemenea, alte câteva efecte secundare nedorite, inclusiv creșterea în greutate, căderea părului, sindromul ovarelor polichistice și encefalopatia hepatică.54-57 Sunt necesare tratamente alternative de primă linie, în special pentru femeile aflate la vârsta fertilă.
Alternative mai noi la valproat pentru tratamentul epilepsiei generalizate
Levetiracetamul este noua MEA pentru epilepsia generalizată, cel mai studiat pe scară largă. Două dintre studiile de monoterapie descrise mai sus au inclus, de asemenea, pacienți cu epilepsie generalizată.32,34 În studiul KOMET, levetiracetamul a fost echivalent cu valproatul atât în ceea ce privește rata de retragere a tratamentului, cât și timpul până la prima criză.34 Levetiracetamul s-a dovedit, de asemenea, echivalent cu lamotrigina în ceea ce privește rata de eliberare a crizelor într-un eșantion eterogen; analiza post-hoc a subgrupurilor a arătat că acest lucru era valabil atât pentru epilepsia focală, cât și pentru cea generalizată.32
Recent, Marson și colegii au prezentat rezultatele ramurii de epilepsie generalizată a studiului SANAD II.58 Valproatul a fost superior levetiracetamului în ceea ce privește timpul până la eșecul tratamentului, timpul până la prima criză și timpul până la remisiunea de 24 de luni. În mod interesant, diferența în ceea ce privește timpul până la eșecul tratamentului a fost atribuită controlului inadecvat al crizelor, mai degrabă decât efectelor adverse, ceea ce sugerează că valproatul nu a fost mai slab tolerat decât levetiracetamul în acest eșantion.
După cum s-a menționat mai sus, atât clobazamul, cât și perampanelul s-au dovedit a avea o bună eficacitate și tolerabilitate în studii observaționale retrospective care au inclus pacienți cu epilepsie generalizată, dar niciunul dintre aceste medicamente nu a fost comparat cu oricare dintre medicamentele mai vechi într-un studiu randomizat.44,45 Din cunoștințele noastre, niciunul dintre celelalte MEA noi nu a fost studiat ca monoterapie la pacienții cu epilepsie generalizată.
Rezumat al tratamentului de primă linie pentru epilepsia generalizată și neclasificată
Deși rezultatele SANAD II sugerează că valproatul rămâne cel mai eficient MEA pentru epilepsia generalizată sau neclasificată, nu îl recomandăm ca tratament de primă linie din cauza efectelor sale adverse. Lamotrigina este o alegere bună dacă frecvența crizelor este suficient de scăzută pentru a permite creșterea lentă a dozei. Dacă este nevoie de un debut rapid, poate fi utilizat levetiracetamul. Dacă convulsiile sunt refractare la acești doi agenți, se poate utiliza valproatul după o discuție atentă a riscurilor și beneficiilor.
Consilierea pacienților cu epilepsie nou-înființată
Pacienții cu un nou diagnostic de epilepsie au, de obicei, multe întrebări despre boală și impactul acesteia asupra vieții lor. Cele mai frecvente întrebări se referă la prognosticul pe termen lung al epilepsiei, dacă trebuie să înceapă tratamentul cu AED și dacă tratamentul cu AED va fi pe tot parcursul vieții. După cum s-a discutat mai sus, pacienții ar trebui să fie informați că tratamentul imediat cu AED reduce riscul de recurență timpurie a crizelor, dar nu schimbă prognosticul general al epilepsiei, iar decizia de a începe sau nu un AED ar trebui să fie luată în mod individualizat. Pacienții ar trebui să fie informați că aproximativ jumătate dintre pacienți vor obține controlul convulsiilor cu primul AED, în timp ce încă 20% vor răspunde la un al doilea sau al treilea medicament.59 În plus, aceștia ar trebui să fie conștienți de faptul că orice încercare de întrerupere a tratamentului cu AED nu ar trebui inițiată decât după cel puțin 2 ani de absență a convulsiilor și că aproape jumătate dintre pacienți vor avea o recurență a convulsiilor după retragerea AED.60
În afara controlului convulsiilor, cele mai frecvente întrebări practice se referă la conducerea auto. Orice criză cu afectare a conștiinței – absentă, tonico-clonică sau focală inconștientă – poate provoca daune semnificative dacă apare în timp ce pacientul conduce. Cele mai multe state cer un interval de libertate a crizelor înainte ca un pacient să poată relua șofatul. Medicii trebuie să se asigure că pacienții sunt familiarizați cu legile din statul lor. Unele state le cer medicilor să raporteze pacienții lor cu epilepsie sau convulsii la Departamentul pentru Vehicule cu Motor, în timp ce altele nu o fac.61 Este important de reținut că, în statele în care nu există obligativitatea raportării, este posibil ca medicii să nu beneficieze de protecție juridică atunci când divulgă un diagnostic de epilepsie fără consimțământul pacientului. În aceste cazuri, medicii vor trebui să pună în balanță riscurile ca pacientul să continue să conducă (în special în cazul șoferilor profesioniști) cu riscurile de ramificații juridice ale încălcării confidențialității pacientului. Toate conversațiile despre condusul auto trebuie să fie documentate în dosarul medical al pacientului.
Femeile aflate la vârsta fertilă trebuie, în plus, să fie consiliate cu privire la implicațiile epilepsiei și ale DAE asupra sarcinii. Pacientele trebuie să fie conștiente de faptul că convulsiile, în special convulsiile tonico-clonice generalizate, și unele DAE, pot avea efecte adverse asupra fătului în curs de dezvoltare. La femeile care nu planifică o sarcină, este preferabilă contracepția cu acțiune îndelungată cu un dispozitiv intrauterin sau o injecție de depozit, deoarece acestea minimizează oportunitatea de eroare de utilizare. Pacientele trebuie să știe, de asemenea, că tratamentul cu AED inductoare de enzime poate scădea eficacitatea contracepției hormonale.62 Toate femeile cu epilepsie care planifică o sarcină trebuie să își informeze neurologul din timp; dacă o sarcină este neplanificată, neurologul trebuie informat cât mai curând posibil. În plus, toate femeile cu epilepsie aflate la vârsta fertilă ar trebui să ia acid folic, indiferent dacă este sau nu planificată o sarcină, deoarece acest lucru reduce riscul de defecte ale tubului neural care se dezvoltă la începutul primului trimestru, adesea înainte de a se cunoaște o sarcină.63
Cel mai dificil subiect de discutat cu pacienții nou diagnosticați este moartea subită și neașteptată în epilepsie (SUDEP). Factorii de risc pentru SUDEP includ frecvența mare a crizelor, vârsta timpurie de debut, durata îndelungată a bolii, crizele tonico-clonice generalizate, crizele nocturne, faptul de a locui singur, sexul masculin, dependența de alcool și abuzul de substanțe.64-66 Cei mai mulți neurologi consideră că toți pacienții cu epilepsie ar trebui să fie informați despre SUDEP, în timp ce unii susțin că consilierea SUDEP este necesară doar pentru pacienții care prezintă un risc ridicat.67 Recomandăm discutarea SUDEP cu toți pacienții cu epilepsie cu debut nou, ca parte a unei discuții inițiale despre importanța respectării tratamentului medicamentos, cu consiliere mai frecventă și mai extinsă pentru pacienții cu risc ridicat.
.