INTRODUCERE
Contracțiile ventriculare premature (PVC) care își au originea în tractul de ieșire al ventriculului drept (RVOT) apar de obicei la pacienții fără afecțiuni cardiace structurale. Ele se pot prezenta sub forma unor PVC izolate sau incesante, sau sub formă de tahicardie (până la 80% din tahicardiile ventriculare idiopatice). Principalul mecanism cauzal este activitatea declanșată, dar au fost, de asemenea, postulate mecanisme de reintrare sau de automatism anormal.
Pacienții se prezintă, de obicei, cu simptome asociate cu exercițiul fizic, stresul sau utilizarea de stimulente. Simptomele pot afecta calitatea vieții, iar tipul incesant de VE poate duce la tahicardiomiopatie.
Betablocantele sau verapamilul prezintă de obicei doar o eficacitate limitată în controlul acestui tip de PVC. Ablația prin radiofrecvență poate fi eficientă, dar este îngreunată de faptul că această PVC are o inducibilitate limitată și imprevizibilă. Metodele convenționale ghidate prin fluoroscopie pot fi de un folos limitat dacă PVC sunt puține, deoarece cartografierea activării este complexă, iar cartografierea stimulării are o rezoluție spațială scăzută.
Sistemele de cartografiere fără contact (NCMS) s-au dovedit utile în localizarea bătăilor ectopice și ca ghid în ablația acestora.1, 2 În această lucrare, descriem ablația PVC RVOT utilizând Ensite Array NCMS (St. Jude Medical, St. Paul, Minnesota, Statele Unite). Acest sistem utilizează un cateter multielectrode array (MAC) cu un balon de 7,5 ml și 64 de microelectrozi pentru a localiza tahicardia. MAC furnizează simultan peste 3000 de electrograme virtuale unipolare de la o singură bătaie și le afișează într-o imagine tridimensională din camera de interes.
METODE Caracteristicile pacienților
Cele patru pacienți fără boală cardiacă structurală, dar cu PVC RVOT simptomatică incesantă au fost supuși ablației cu ajutorul NCMS între ianuarie 2006 și decembrie 2009. Vârsta medie a pacienților a fost de 43±6 ani și 50% au fost de sex masculin.
Toți au avut o calitate slabă a vieții din cauza PVC foarte simptomatice și frecvente (medie, 30 763±4710 PVC / zi). Toți eșuaseră la cel puțin 2 medicamente antiaritmice, dintre care unul a fost întotdeauna un betablocant. Ablația fusese încercată anterior la 2 dintre pacienți cu ajutorul unui sistem convențional, dar fără succes.
La toți pacienții, activitatea extrasistolică era rară în ziua procedurii. Medicamentele antiaritmice au fost întrerupte cu cel puțin 5 jumătăți de viață înainte de procedură și s-a evitat sedarea.
Studiu electrofiziologic
Un cateter de ablație de 4 mm (Livewire TC, St. Jude Medical) a fost plasat în ventriculul drept (VD). Dacă, după infuzie de izoproterenol și stimulare ventriculară, nu a fost posibilă obținerea unei PVC suficiente pentru a realiza cartografierea activării, atunci a fost introdus MAC.
MAC a fost avansat pe un fir de ghidare de 0,035″ folosind fluoroscopie și balonul a fost plasat în RVOT la 2 până la 3 cm de valva pulmonară. Anticoagularea cu heparină a fost inițiată în acest moment. Anatomia VD a fost apoi reconstruită, acordându-se o atenție deosebită la RVOT și la situația valvei pulmonare (figura 1). O distanță de
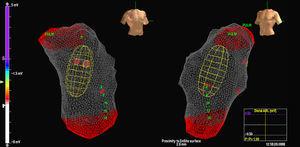
Figura 1. Imagine a cateterului cu matrice de multielectrozi în tractul de ieșire al ventriculului drept.
Subiectiv, au fost analizate 3 bătăi extrasistolice pentru fiecare morfologie de PVC prezentată de pacient și au fost obținute offline hărți izopotențiale și izocrone. Filtre de 30 până la 500Hz au fost folosite pentru electrogramele bipolare și un filtru trece înalt de 2-Hz a fost folosit cu electrogramele virtuale unipolare.
Harta izopotențială reprezintă dinamic activarea folosind zonele de amplitudine maximă a tensiunii și arată cum se deplasează frontul de undă. Cel mai timpuriu punct de activare este definit ca fiind punctul care prezintă cea mai timpurie activare în raport cu debutul QRS și prezintă o morfologie QS cu o deviere negativă rapidă pe electrograma unipolară. Harta izopotențială identifică, de asemenea, punctul de plecare al frontului de undă înainte ca acesta să se răspândească în restul miocardului. Harta izocronei este o hartă convențională a timpului de activare a suprafeței endocardice și utilizează un semnal unipolar virtual.
Tinta pentru ablație a fost atât zona de activare cea mai timpurie, cât și punctul de plecare al frontului de activare. Radiofrecvența a fost aplicată ocazional în aceste locuri, cu un control al temperaturii limitat la 50W, temperaturi sub 55°C și o durată de 60 de secunde. Ablația a fost considerată reușită dacă PVC a dispărut în timpul aplicării și nu a fost reintrodusă.
Toate procedurile au fost efectuate de același electrofiziolog, care a dirijat inginerul care a operat NCMS.
REZULTATE
Trei pacienți au avut o singură morfologie de PVC, în timp ce un pacient a avut 2 morfologii. În 3 cazuri, localizarea a fost septală, în timp ce în celelalte 2 cazuri a fost în peretele liber al RVOT. În toate cazurile, harta izopotențială (figura 2) a fost cea care a localizat cu cea mai mare acuratețe focarul de origine; harta izocronei a avut o valoare relativ mică (figura 3).
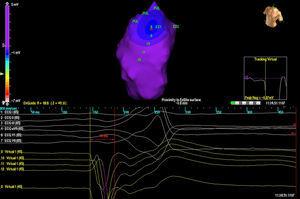
Figura 2. Harta izopotențială la un pacient cu 2 extrasistole ventriculare diferite cu originea în tractul de ieșire al ventriculului drept. Fiecare ieșire este reprezentată prin literele EX (1 și 2). Punctul de activare cel mai timpuriu este prezentat în EX1, cu imaginea QS în unipolaritatea virtuală (mai jos).
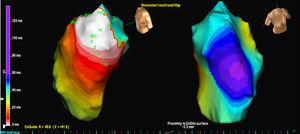
Figura 3. Harta izocronică a ieșirii EX1 pentru aceleași extrasistole ventriculare analizate în figura 1 . Albul indică cea mai timpurie activare, iar movul indică cea mai târzie activare.
Am confirmat, de asemenea, în toate cazurile, că PVC nu a fost cauzată mecanic și că a coincis cu morfologia PVC-ului clinic. La un pacient, balonul a fost foarte aproape de suprafața endocardică unde a luat naștere PVC-ul și a trebuit să fie repoziționat pentru a permite o mobilizare adecvată a electrocateterului de ablație.
După identificarea locului de origine, a fost utilizată o medie de 3 aplicații de radiofrecvență pe focar pentru a ablaționa atât punctul de activare cel mai timpuriu, cât și punctul de plecare al frontului de activare. Timpul mediu de aplicare a fost de 113±15s pentru fiecare focar. S-a observat o creștere a activității ectopice care a precedat terminarea aplicației.
Timp mediu de fluoroscopie a fost de 31±11 (21-46) min și timpul total al procedurii a fost de 136±38min, deși acesta a scăzut de-a lungul curbei de învățare, de la 190min pentru prima procedură la 100min pentru cea de-a patra.
Am obținut o rată de succes acut de 100%, fără complicații și fără reapariția PVC cu infuzie de izoproterenol sau repetarea protocolului de stimulare. După o medie de 30±16 luni, pacienții au rămas asimptomatici fără terapie medicamentoasă, iar în cadrul monitorizării Holter la vizita de urmărire la 1 an numărul mediu de PVC a fost de 159±113/zi.
DISCUȚII
Deși alți autori au demonstrat utilitatea NCMS pentru ablația PVC RVOT,2, 3 utilizarea sa nu este larg răspândită.4 În experiența noastră, s-au obținut rezultate excelente încă de la primele cazuri. Ratele de succes de peste 80% sunt de obicei raportate pentru ablația tahicardiei ventriculare RVOT5; cu toate acestea, noi am obținut o rată de succes mai mare, chiar dacă am reușit să cartografiem doar PVC izolată. Obiectivul nostru final acut a fost dispariția PVC și a fost limitat de frecvența scăzută a PVC în timpul procedurii. Acest lucru a făcut necesară confirmarea eficacității ablației în timpul urmăririi prin scăderea frecvenței PVC în monitorizarea Holter.
Aritmia la pacienții noștri a avut o origine focală, ceea ce este în concordanță cu observațiile altor autori.2, 6 Ablația a fost limitată la punctul de activare cel mai timpuriu, ceea ce ar fi putut contribui la rata mare de succes.
NCMN a necesitat doar o singură bătaie pentru a localiza cu precizie originea PVC-ului. Deși am preferat să confirmăm localizarea prin cartografierea altor PVC identice, locul de origine nu a fost modificat. În experiența noastră, ablația cu succes a fost realizată numai pe baza hărții izopotențiale.
Una dintre limitările sistemului este că localizează cel mai timpuriu punct de activare în endocardul camerei explorate, chiar și atunci când punctul nu este localizat în endocard, ci în epicard sau într-o altă cameră atașată. În aceste cazuri, analiza unipolară virtuală ajută la indicarea faptului că originea nu se află în endocardul VD, deoarece în acest caz cel mai timpuriu punct endocardic ar prezenta un rS.
În plus, MAC poate produce PVC mecanică și, fiind localizată în RVOT, poate fi confundată cu PVC clinică. Pentru diferențiere, am analizat corespondența electrocardiografică cu PVC clinică și am confirmat că punctul de origine al PVC nu a fost în contact cu balonul.
PVC poate, de asemenea, să se origineze foarte aproape de locul unde este localizat MAC, împiedicând astfel accesul la cateterul de ablație. În astfel de cazuri, poate fi necesară repoziționarea balonului.
În seria noastră, NCMS s-a dovedit a fi un mijloc eficient și sigur de îndepărtare a PVC izolate, greu de indus în RVOT și a contribuit la reducerea complexității procedurilor implicate.
CONFLICTE DE INTERESE
Nici unul declarat.
Recunoștințe
Am dori să-i mulțumim lui Joaquín Panduro pentru revizuirea critică a manuscrisului.
Recepționat la 21 ianuarie 2011
Acceptat la 1 mai 2011
.