Os átomos podem ganhar ou perder elétrons a fim de formar íons em um processo chamado ionização (compostos formados desta forma são chamados de compostos iônicos). Quando os compostos iônicos se dissolvem na água, seus íons se separam uns dos outros em um processo chamado de dissociação. Uma característica interessante da água e muitos outros compostos covalentes é que eles também podem se dissociar em íons. Ao contrário dos compostos iônicos, como o cloreto de sódio, eles não são ionizados antes de se dissociarem; eles realizam ionização e dissociação ao mesmo tempo.
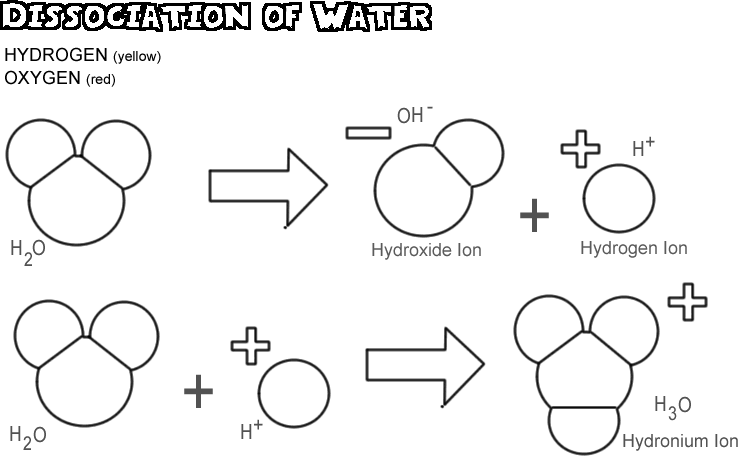
Dissociação da Água
Quando a água se dissocia, um dos núcleos de hidrogênio deixa seu elétron para trás com o átomo de oxigênio para se tornar um íon de hidrogênio, enquanto o oxigênio e outros átomos de hidrogênio se tornam um íon de hidróxido. Como o íon hidrogênio não tem elétron para neutralizar a carga positiva em seu próton, ele tem uma unidade completa de carga positiva e é simbolizado como H+. O íon hidróxido retém o elétron deixado para trás e assim tem uma unidade completa de carga negativa, simbolizada por OH-. O íon hidrogênio (próton) não vagueia muito tempo por si só antes de se fixar ao átomo de oxigênio de uma segunda molécula de água não ionizada para formar um íon hidrônio (H3O +)
Em qualquer amostra de água, muito poucas moléculas são dissociadas de cada vez: de fato, apenas cerca de uma em 550 milhões. Há, no entanto, uma mudança constante; como um íon de hidrogênio se liga novamente a um íon de hidróxido para formar uma molécula de água, outra molécula de água se dissocia para substituir o íon de hidrogênio e o íon de hidróxido em solução.
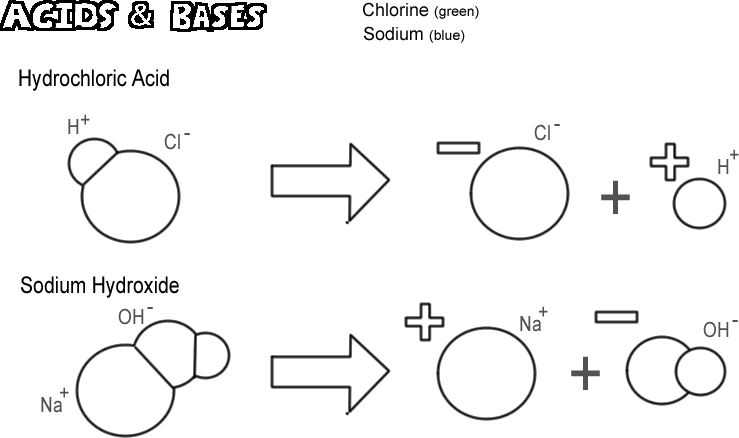
Ácido clorídrico
Determinadas moléculas, iônicas e covalentes, se dissociam de tal forma que liberam um íon de hidrogênio sem liberar um íon de hidróxido. Estas substâncias são chamadas ácidos. Uma vez que um íon de hidrogênio é realmente apenas um próton na maioria dos casos, a definição do químico de um ácido é um “doador de prótons”. Se muitos prótons (íons de hidrogênio) são “doados”, o efeito pode ser muito profundo, como queimar a pele ou dissolver o metal. O ácido ilustrado é o ácido clorídrico. O ácido clorídrico puro é um gás, mas dissolve-se facilmente na água para produzir uma solução de íon hidrogênio e íon cloreto. Como quase tudo está dissociado em água, é chamado de ácido forte. Os ácidos que não se dissociam completamente são chamados de ácidos fracos.
Hidróxido de sódio
O oposto de um ácido é uma base, também conhecida como um álcali. Uma base forte típica é o hidróxido de sódio, o principal componente da lixívia. O hidróxido de sódio dissocia-se para formar um íon de sódio e um íon de hidróxido. Uma base é definida como um “aceitador de prótons”. As bases mais comuns produzem o íon hidróxido quando se dissociam, e é o íon hidróxido que aceita o protão. Uma base forte pode dar à sua pele uma queimadura muito pior do que um ácido.
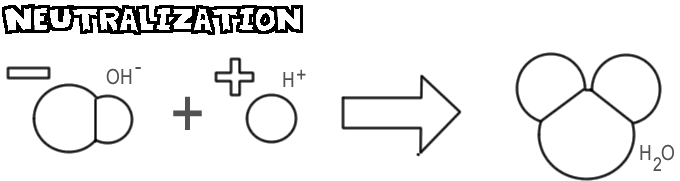
Neutralização
Quando uma base e um ácido são misturados, o íon hidróxido e a base combinam com o íon hidrogênio do ácido para formar água. Este processo é chamado de neutralização.
Questões:
1. O que acontece quando um átomo ganha ou perde um electrão?