A fibrilação atrial (FA) é a taquiarritmia sustentada mais frequente, ocorrendo em 1% a 2% da população em geral. O isolamento da veia pulmonar (IVP) é o pilar da ablação da FA.1 Embora este procedimento seja eficaz na prevenção da recorrência da arritmia em pacientes com FA paroxística, se realizado isoladamente, tem apenas sucesso limitado na FA persistente.1,2 Dados iniciais sugeriram que a recorrência da arritmia poderia ser diminuída pela ablação adicional da linha ou ablação complexa do eletrograma atrial fracionado. Entretanto, o benefício da ablação adicional além da IVP não foi confirmado pelos resultados recentes de meta-análises3 e estudos controlados randomizados,4 enfatizando a importância da IVP durável, mesmo na FA persistente.
A ablação por criobalão tornou-se uma abordagem alternativa viável à ablação por radiofrequência (RF) nos últimos anos e provou ser pelo menos tão eficaz quanto a IVP em pacientes com FA paroxística. Os resultados recentes do ensaio FIRE & ICE estabeleceram definitivamente o debate neste campo.5 Além disso, devido à relativa simplicidade, à curva de aprendizado mais rápida – e talvez até mais importante – à notável reprodutibilidade6 deste procedimento, ele tem sido amplamente adotado na prática clínica.6
Por outro lado, o tratamento intervencionista da FA persistente permanece desafiador: esta abordagem não tem sido padronizada ou aperfeiçoada e há espaço para inovação. Nesse cenário, a questão de um possível papel da crioablação é interessante.
EVIDÊNCIA CLÍNICA
Embora haja um interesse crescente na eficácia da ablação da FA em pacientes com FA persistente, os dados de acompanhamento após o uso do novo cateter criobalão de segunda geração de 28 mm (Arctic Front Advance, Medtronic Inc., Minneapolis, MN) ainda são limitados. Até o momento, os resultados da ablação pós-cryoballoon na FA persistente foram avaliados indiretamente por meta-análises, comparações não-randomizadas,7 e estudos observacionais.8-10
Ciconte et al.9 relataram que 60% dos pacientes com FA persistente estavam livres de taquiarritmia atrial após o tratamento com o novo cateter de criobalão. A duração da FA persistente, que foi um preditor independente de recorrência de arritmia durante o seguimento, fornece um claro suporte para a ablação em estágios iniciais da doença.
Num estudo retrospectivo de 48 pacientes com FA persistente, a taxa de sucesso clínico de 1 ano foi de 69%.10
Um outro estudo de um único braço avaliou a eficácia da crioablação de segunda geração em um grupo de 100 pacientes com FA persistente como um procedimento índice (duração média de 5,5 ± 3,7 meses).8 Após um seguimento médio de 10,6 ± 6,3 meses, não houve recorrência de taquiarritmia atrial em 67% dos pacientes, após um período de 3 meses de bloqueio. O único preditor independente significativo de recorrência foi a ocorrência de taquiarritmia atrial durante o período de blanking.
Um estudo monocêntrico, não prospectivo e não randomizado também avaliou a RF em comparação com a crioablação apenas em pacientes com FA persistente.7 Nesse estudo, o resultado procedimental da ablação por RF (usando um cateter de ablação por força de contato) em comparação com a crioablação (usando o crioobalão de segunda geração de 28 mm) foi avaliado em uma coorte de 100 pacientes com FA persistente refratária (as durações médias da FA foram de 7,2 e 7,6 meses, respectivamente, nos grupos de ablação por RF e crioablação). Os tempos de procedimento e fluoroscopia foram significativamente menores no grupo de crioablação, mas a taxa de pacientes livres de arritmias atriais foi semelhante entre os 2 grupos após 12 meses de seguimento (60% nos grupos de crioablação vs 56% nos grupos de ablação por RF, P = .71). Na análise multivariada, os únicos preditores independentes de falência foram novamente encontrados para a duração da FA persistente e recidivas durante o período de obturação.
Finalmente, um estudo prospectivo, multicêntrico e não randomizado comparou os resultados após um único procedimento de ablação, utilizando a ablação por criobalão de primeira geração apenas para a IVP versus ablação por RF aberta através de uma abordagem gradual em uma coorte de pacientes com FA persistente.11 Os resultados, mostrando cerca de 55% de liberdade das arritmias atriais durante um seguimento médio de 15,6 ± 11,5 meses após uma única ablação, tanto com o criobalão quanto com a RF, foram semelhantes aos dados disponíveis. Vários achados foram dignos de nota:
- –
Primeiro, os resultados clínicos foram semelhantes nos 2 braços de tratamento, embora o grupo RF tenha sido submetido a ablação adicional e mais extensa além da IVP.
- –
Segundo, a taxa de complicações foi semelhante com as 2 técnicas.
- –
Terceira, a duração do procedimento foi menor com a crioablação.
Ainda há incerteza sobre a fisiopatologia e estratégia ideal para a ablação persistente da FA e, portanto, a base desta terapia continua sendo a obtenção de uma IVP durável.4 Para conseguir isto, a crioablação parece ser uma abordagem terapêutica alternativa válida para a RF. O desempenho da ablação adicional em cima da IVP está associado a um tempo de procedimento mais longo.4 Como a abordagem de ablação por RF não foi padronizada (a maioria dos pacientes no braço de RF desenvolveu lesões adicionais), não está claro se os resultados se devem à fonte de energia ou à estratégia de ablação. Além disso, os resultados a médio prazo não parecem ser significativamente melhorados por lesões biatriais adicionais além da IVP em pacientes com FA persistente.4
SHOOTING AT THE RIGHT TARGET?
As razões para a falta de um benefício maior com a ablação adicional ainda não foram elucidadas. Uma possibilidade é o potencial iatrogênico de uma abordagem de substrato com ablação mais extensa, o que pode favorecer o desenvolvimento de novas áreas de arritmogênese devido ao tecido incompletamente ablactado ou linhas incompletas de bloqueio de condução. Outra possibilidade é que a área culpada não seja rotineiramente identificada e nem eletrogramas atriais fracionados complexos nem lesões lineares são os alvos complementares ideais para a ablação.12 Nessa hipótese, ainda há a necessidade de apontar o olho da tempestade (através de rotores ou gânglios),13 possivelmente através do uso de novos algoritmos de mapeamento. Os dados disponíveis também fornecem suporte para o papel da duração da FA, e consequentemente a remodelação elétrica da FA (FA gera FA), pois apenas a duração da FA foi um preditor independente da recorrência da arritmia na comparação propensity-score,11 como relatado anteriormente por Tilz et al.2
Estudos em andamento ajudarão a elucidar a segurança e eficácia da crioablação em pacientes com FA persistente. O estudo Cryoballoon Ablation for Early Persistent Atrial Fibrillation (Cryo4 Persistent AF – NCT02213731) é um estudo piloto europeu multicêntrico, prospectivo e de braço único, com o objetivo de avaliar a taxa de sucesso da IVP apenas pela crioablação a 1 ano em pacientes com menos de 12 meses de história de FA persistente. Este estudo ainda está em fase de recrutamento e os primeiros resultados são esperados no final de 2017. O próximo objetivo será comparar os resultados em um estudo randomizado entre a abordagem por etapas da RF e a crioablação da IVP em um grupo homogêneo de pacientes com FA persistente. Os resultados deste estudo randomizado em larga escala são aguardados com expectativa.
STRENGTHS AND LIMITATIONS
Em pacientes com FA persistente, mesmo os maiores diâmetros máximos de PV (entre 20mm e 23mm) são substancialmente inferiores ao valor crítico de 28mm (o diâmetro máximo do criobalão utilizado na prática clínica de rotina).14 Devido a este desajuste entre os diâmetros do balão e FV, quando este dispositivo é posicionado contra o antro FV, sua parte de resfriamento está em contato tanto com a antra FV quanto com o tecido atrial adjacente, o que parece ser um benefício importante deste procedimento. Kenigsberg et al.,15 calcularam a área do tecido cardíaco aletado após a crioablação PV por meio do mapeamento tridimensional da tensão eletroanatômica do átrio esquerdo após a crioablação. Utilizando este método, estes autores demonstraram, de forma agradável, que após a crioablação com o dispositivo criobalão de 28 mm, a porcentagem da superfície da parede posterior do átrio esquerdo que permaneceu eletricamente intacta foi de apenas 27%.
Observar, embora o criobalão conceitualmente vise apenas as PVs, também realiza substancial descascamento elétrico da parede posterior do átrio esquerdo (Figura). Ao estender a circunferência da área de resfriamento, este dispositivo pode conferir um benefício colateral ao ablatar os contribuintes locais em estruturas que contribuem para desencadear e manter a FA, como a plexi ganglionar e os rotores, o que possivelmente tem grandes implicações terapêuticas para os pacientes com FA persistente.13 Esta característica também poderia explicar, pelo menos parcialmente, os resultados dos ensaios acima mencionados.
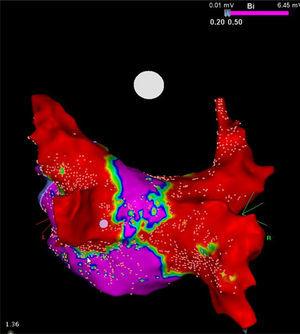
Mapa de alta densidade de tensão da parede posterior após procedimento de crioablação em paciente com fibrilação atrial persistente. Note o corredor estreito (roxo) restante entre as duas grandes cicatrizes (vermelho) obtidas com o criobalão Artic Front Advance 28mm (Medtronic, Minneapolis, MN, Estados Unidos). Cortesia do Prof. Mário Oliveira, Hospital Santa Marta, Lisboa, Portugal.
Embora as taxas de sucesso do criobalão sejam comparáveis às da RF em estudos não randomizados de pacientes com FA persistente, a taxa relativamente alta de recorrência de arritmia em ambos os grupos permanece inexplicável e pode não ser atribuída apenas à recuperação da condução dos VPs. Esta possibilidade tem sido mencionada em estudos que levantaram preocupações sobre o papel de fontes não relacionadas à IVP como mecanismo de recidiva.9
Na FA persistente, o tratamento invasivo permanece desafiador devido à sua patofisiologia diversificada. Novos insights mecanicistas são necessários para permitir uma abordagem individualizada da FA persistente, mas, até que tal conhecimento se torne disponível, a IVP autônoma de primeira intenção pode ser suficiente, pelo menos para pacientes com FA persistente menos grave. Com base nesta abordagem “menos é mais”, a IVP criobalão pode ser uma estratégia de ablação adequada na FA persistente, permitindo uma IVP confiável com o descascamento adjunto do miocárdio atrial vizinho. A modificação adicional do substrato não parece oferecer benefício adicional. Este procedimento “minimalista” é uma primeira opção aceitável em pacientes com história relativamente recente de FA persistente sintomática, ou seja, com “mais gatilho do que substrato” (ou com um substrato concentrado ao redor dos óstios PVs…). De fato, o grande (28mm) criobalão de segunda geração fornece resultados similares aos de procedimentos mais complexos usando energia de RF e métodos sofisticados. De notar que a curva de aprendizagem, reprodutibilidade e segurança parecem ser a favor do dispositivo criobalão em mãos menos experientes. Neste cenário, e no subgrupo de pacientes acima mencionado, a IVP com o grande criobalão de segunda geração parece ser uma abordagem inicial razoável, proporcionando uma melhora significativa para mais da metade dos candidatos. Para pacientes com recidivas de FA, este primeiro procedimento não será inútil. De fato, em uma quantidade considerável de substrato (ao redor da antra PV direita e esquerda) que já foi tratada, o segundo procedimento, por RF desta vez, irá focar principalmente em focos extra-VP, potenciais fragmentados, circuitos micro ou macroreentrantes, etc.
Em nossa opinião, esta estratégia de 2 passos é compatível com a implantação de centros de baixo a médio volume, focando principalmente IVP, e trabalhando em conjunto com centros de referência terciária realizando os procedimentos mais complexos. Estes últimos terão que lidar com os cerca de 40% dos pacientes com recidivas após o primeiro “crio-debulking”.
“Less is more”, mas ainda assim, não é suficiente…
CONFLICTS OF INTEREST
S. Boveda recebe taxas de consultoria da Medtronic, Boston Scientific e Livanova.