INTRODUÇÃO
Contrações Ventriculares Precoce (PVC) originárias da via de saída do ventrículo direito (VSVD) geralmente aparecem em pacientes sem doença cardíaca estrutural. Podem apresentar-se na forma de PVC isolado ou incessante, ou como taquicardia (até 80% da taquicardia ventricular idiopática). O principal mecanismo causal é a atividade desencadeada, mas também têm sido postulados mecanismos de reentrada ou de automaticidade anormal.
Patientes geralmente apresentam sintomas associados a exercício, estresse ou uso de estimulantes. Os sintomas podem afetar a qualidade de vida e o tipo incessante de EM pode levar a taquicardiomiopatia.
Beta bloqueadores ou verapamil geralmente mostram apenas eficácia limitada no controle deste tipo de PVC. A ablação por radiofrequência pode ser eficaz, mas é prejudicada pelo facto deste PVC ter uma inducibilidade limitada e imprevisível. Métodos convencionais guiados fluoroscopicamente podem ser de uso limitado se o PVC for escasso, porque o mapeamento de ativação é complexo e o mapeamento de estimulação tem uma baixa resolução espacial.
Sistemas de mapeamento sem contato (NCMS) têm se mostrado úteis na localização de batimentos ectópicos e como guia em sua ablação.1, 2 Neste artigo descrevemos a ablação do PVC RVOT usando o Ensite Array NCMS (St. Jude Medical, St. Paul, Minnesota, Estados Unidos). Este sistema utiliza um cateter multieletrodo (MAC) com um balão de 7,5ml e 64 microeletrodos para localizar a taquicardia. O MAC fornece mais de 3000 eletrogramas unipolares virtuais simultaneamente a partir de um único batimento e os exibe em uma imagem tridimensional da câmara de interesse.
MÉTODOS Características do paciente
Quatro pacientes sem doença cardíaca estrutural, mas com incessante PVC RVOT sintomático foram submetidos à ablação usando NCMS entre janeiro de 2006 e dezembro de 2009. A média de idade dos pacientes foi de 43±6 anos e 50% eram do sexo masculino.
Todos tinham má qualidade de vida devido ao PVC altamente sintomático e frequente (média, 30 763±4710 PVC / dia). Todos tinham falhado em pelo menos 2 drogas anti-arrítmicas, sendo que uma delas era sempre um beta bloqueador. A ablação havia sido tentada anteriormente em 2 dos pacientes usando um sistema convencional, mas sem sucesso.
Em todos os pacientes, a atividade extra-sistólica era escassa no dia do procedimento. Drogas antiarrítmicas foram descontinuadas pelo menos 5 meias-vidas antes do procedimento e a sedação foi evitada.
Estudo eletrofisiológico
Um cateter de ablação de 4 mm (Livewire TC, St. Jude Medical) foi colocado no ventrículo direito (VD). Se, após infusão de isoproterenol e estimulação ventricular, não foi possível obter PVC suficiente para realizar o mapeamento de ativação, então a MAC foi introduzida.
A MAC foi avançada em um fio-guia 0.035″ usando fluoroscopia e o balão foi colocado na VSVD a 2 a 3cm da valva pulmonar. A anticoagulação com heparina foi iniciada neste ponto. A anatomia do VD foi então reconstruída, com especial atenção para a VSVD e a situação da valva pulmonar (Figura 1). Uma distância de
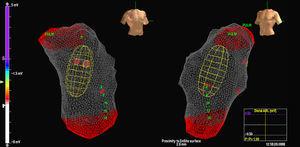
Figure 1. Imagem do cateter multieletrodo na via de saída do ventrículo direito.
Subseqüentemente, 3 batimentos extra-sistólicos foram analisados para cada morfologia de PVC apresentada pelo paciente e mapas isopotenciais e isocrônicos foram obtidos off-line. Filtros de 30 a 500Hz foram utilizados para eletrogramas bipolares e um filtro passa-alto 2-Hz foi utilizado com os eletrogramas unipolares virtuais.
O mapa isopotencial representa dinamicamente a ativação utilizando áreas de máxima amplitude de tensão e mostra como a frente de onda viaja. O primeiro ponto de ativação é definido como o ponto que mostra a primeira ativação em relação ao QRS e mostra uma morfologia QS com deflexão negativa rápida sobre o eletrograma unipolar. O mapa isopotencial também identifica o ponto de partida da frente de onda antes de se espalhar para o resto do miocárdio. O mapa isocrônico é um mapa convencional do tempo de ativação da superfície endocárdica, e utiliza um sinal unipolar virtual.
O alvo para a ablação foi tanto a área de ativação mais inicial quanto o ponto de partida da frente de ativação. A radiofrequência foi ocasionalmente aplicada nestes locais, com controle de temperatura limitado a 50W, temperaturas abaixo de 55°C e uma duração de 60s. A ablação foi considerada bem sucedida se o PVC desaparecesse durante a aplicação e não fosse re-induzido.
Todos os procedimentos foram realizados pelo mesmo eletrofisiologista, que dirigiu o engenheiro operando o NCMS.
RESULTADOS
Três pacientes tinham uma única morfologia de PVC, enquanto um paciente tinha duas morfologias. Em 3 casos, a localização foi septal, enquanto nos outros 2 casos foi na parede livre da VSVD. Em todos os casos, foi o mapa isopotencial (Figura 2) que mais precisamente localizou o foco de origem; o mapa isocrônico foi de relativamente pouco valor (Figura 3).
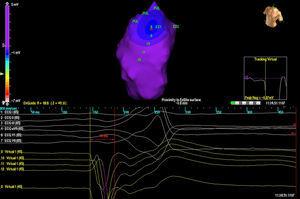
Figure 2. Mapa isopotencial em um paciente com 2 extra-sístoles ventriculares diferentes provenientes da via de saída do ventrículo direito. Cada saída é representada pelas letras EX (1 e 2). O primeiro ponto de ativação é mostrado em EX1, com a imagem de QS nos unipolares virtuais (abaixo).
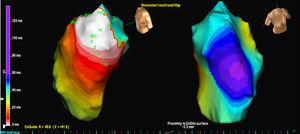
Figure 3. Mapa isocrônico da saída EX1 para as mesmas extra-sístoles ventriculares analisadas na Figura 1 . O branco indica ativação mais precoce e o roxo indica ativação mais recente.
Confirmamos também em todos os casos que o PVC não foi causado mecanicamente e que coincidiu com a morfologia do PVC clínico. Em um paciente, o balão estava muito próximo da superfície endocárdica de origem do PVC e teve que ser reposicionado para permitir a mobilização adequada do eletrocatéter de ablação.
Abaixo identificou o local de origem, uma média de 3 aplicações de radiofreqüência por foco foi usada para ablação tanto do ponto de ativação mais precoce quanto do ponto de partida da frente de ativação. O tempo médio de aplicação foi de 113±15s para cada foco. Um aumento na atividade ectópica foi observado antes do término da aplicação.
O tempo de fluoroscopia do meio foi de 31±11 (21-46) min e o tempo total do procedimento foi de 136±38min, embora isso tenha diminuído ao longo da curva de aprendizado, de 190min para o primeiro procedimento para 100min para o quarto.
Atingimos uma taxa de 100% de sucesso agudo sem complicações e sem reaparição do PVC com infusão de isoproterenol ou repetição do protocolo de estimulação. Após uma média de 30±16 meses, os pacientes permaneceram assintomáticos sem terapia medicamentosa, e na monitorização de Holter na visita de seguimento de 1 ano o número médio de PVC foi de 159±113/dia.
DISCUSSÃO
Embora outros autores tenham demonstrado a utilidade do SGCN para ablação do PVC VSVD,2, 3 seu uso não é generalizado.4 Em nossa experiência, excelentes resultados foram alcançados desde os primeiros casos. Taxas de sucesso superiores a 80% são usualmente relatadas para ablação da taquicardia ventricular da VSVD5; entretanto, obtivemos uma taxa de sucesso maior, embora só tenhamos sido capazes de mapear PVC isolado. Nosso desfecho agudo foi o desaparecimento da PVC, e foi limitado pela baixa freqüência da PVC durante o procedimento. Isto fez com que fosse necessário confirmar a eficácia da ablação durante o seguimento através da diminuição da freqüência de PVC na monitorização de Holter.
Arritmia em nossos pacientes teve origem focal, o que é consistente com as observações de outros autores.2, 6 A ablação foi limitada ao ponto de ativação mais precoce, o que pode ter contribuído para a alta taxa de sucesso.
O NCMS necessitou apenas de uma batida para localizar com precisão a origem do PVC. Embora tenhamos preferido confirmar a localização mapeando outro PVC idêntico, o local de origem não foi modificado. Em nossa experiência, a ablação bem sucedida foi obtida com base apenas no mapa isopotencial.
Uma das limitações do sistema é que ele localiza o ponto de ativação mais precoce no endocárdio da câmara explorada, mesmo quando o ponto não está localizado no endocárdio, mas no epicárdio ou em outra câmara anexa. Nestes casos, a análise unipolar virtual ajuda a indicar que a origem não está no endocárdio do VD, pois neste caso o ponto endocárdio mais precoce apresentaria um rS.
Mais ainda, o MAC pode produzir PVC mecânico e, estando localizado no VDOT, pode ser confundido com PVC clínico. Para diferenciar, analisamos a correspondência eletrocardiográfica com o PVC clínico e confirmamos que o ponto de origem do PVC não estava em contato com o balão.
O PVC também pode ter origem muito próxima à localização do MAC, impedindo assim o acesso ao cateter de ablação. Nesses casos, pode ser necessário reposicionar o balão.
Em nossa série, o NCMS provou ser um meio eficaz e seguro de remover o PVC RVOT isolado, de difícil introdução e ajudou a reduzir a complexidade dos procedimentos envolvidos.
CONFLITOS DE INTERESSE
Nenhum declarado.
Aceites
Gostaríamos de agradecer a Joaquín Panduro por sua revisão crítica do manuscrito.
Recebido 21 de janeiro de 2011
Aceito em 1 de maio de 2011