Doseringsvorm: capsule
Medisch beoordeeld door Drugs.com. Laatst bijgewerkt op 1 okt 2020.
- Overzicht
- Bijwerkingen
- Dosering
- Professional
- Tips
- Interacties
- Meer
Om de ontwikkeling van geneesmiddel-resistente bacteriën te verminderen en de werkzaamheid van nitrofurantoïne (macrocrystals) en andere antibacteriële geneesmiddelen te behouden, nitrofurantoïne (macrocrystals) mag alleen worden gebruikt voor de behandeling of preventie van infecties waarvan bewezen is of sterk vermoed wordt dat ze door bacteriën worden veroorzaakt.
- Beschrijving:
- CLINISCHE FARMACOLOGIE:
- MICROBIOLOGIE
- Werkingsmechanisme
- Interacties met andere antibiotica
- Ontwikkeling van resistentie
- INDICATIES EN GEBRUIK:
- CONTRAINDICATIES:
- WAARSCHUWINGEN:
- Pulmonale reacties:
- Hepatotoxiciteit:
- Neuropathie:
- Hemolytische anemie:
- Clostridium difficile-geassocieerde diarree:
- VOORZORGSMAATREGELEN:
- Informatie voor patiënten:
- Algemeen:
- Geneesmiddeleninteracties:
- Interacties tussen geneesmiddelen en laboratoriumtests:
- Carcinogenese, mutagenese, verminderde vruchtbaarheid:
- Zwangerschap:
- Zwangerschapscategorie B.
- Labor and Delivery:
- Nonterende moeders:
- Pediatrisch gebruik:
- Geriatrisch gebruik:
- ADVERSE REACTIES:
- Respiratoire:
- Hepatisch:
- Neurologisch:
- Dermatologisch:
- Allergisch:
- Gastro-intestinaal:
- Hematologisch:
- Diversen:
- Laboratoriumbijwerkingen:
- Overdosering
- DOSERING EN TOEDIENING:
- Volwassenen:
- Pediatrische patiënten:
- HOW SUPPLIED:
- PRINCIPAL DISPLAY PANEL – 50 mg
- PRINCIPAL DISPLAY PANEL – 100 mg
- PRINCIPAL DISPLAY PANEL – 100 mg
- Veel gestelde vragen
- Meer over nitrofurantoïne
- Consumenteninformatie
- Professionele informatie
- Gerelateerde behandelingsgidsen
Beschrijving:
Nitrofurantoïne, USP (macrokristallen) is een synthetische chemische stof van gecontroleerde kristalgrootte. Het is een stabiele, gele, kristallijne verbinding. Nitrofurantoïne, USP (macrokristallen) is een antibacterieel middel voor specifieke urineweginfecties. Het is verkrijgbaar in capsules van 25 mg, 50 mg en 100 mg voor orale toediening.
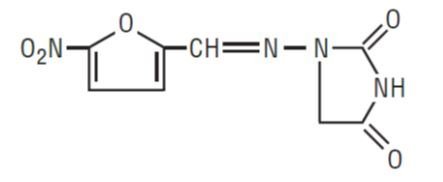
1-AMINO]-2, 4-IMIDAZOLIDINEDIONE
Inactieve bestanddelen: Elke capsule bevat D&C geel # 10, FD&C blauw # 1, FD&C blauw # 2, FD&C rood # 40, gelatine, ijzeroxide zwart, lactose watervrij, magnesiumstearaat, voorgegelatineerd maïszetmeel, natriumlaurylsulfaat, talk en titaniumdioxide. De capsules van 50 mg en 100 mg bevatten ook FD&C geel nr. 6.
CLINISCHE FARMACOLOGIE:
Nitrofurantoïne (macrokristallen) is een grotere kristalvorm van nitrofurantoïne. De absorptie van nitrofurantoïne (macrokristallen) is langzamer en de uitscheiding iets minder in vergelijking met nitrofurantoïne. De bloedconcentraties bij therapeutische dosering zijn meestal laag. Het is goed oplosbaar in de urine, waaraan het een bruine kleur kan geven.
Na een doseringsschema van viermaal daags 100 mg gedurende 7 dagen, was de gemiddelde terugvinding van het geneesmiddel in de urine (0 tot 24 uur) op dag 1 en dag 7 37.9% en 35,0%.
In tegenstelling tot veel andere geneesmiddelen kan de aanwezigheid van voedsel of middelen die de maaglediging vertragen de biologische beschikbaarheid van nitrofurantoïne (macrocrystals) verhogen, vermoedelijk door een betere oplossing in maagsappen mogelijk te maken.
MICROBIOLOGIE
Nitrofurantoïne is een nitrofuran antimicrobieel middel met activiteit tegen bepaalde Gram-positieve en Gram-negatieve bacteriën.
Werkingsmechanisme
Het mechanisme van de antimicrobiële werking van nitrofurantoïne is ongebruikelijk onder antibacteriële middelen. Nitrofurantoïne wordt door bacteriële flavoproteïnen gereduceerd tot reactieve tussenproducten die bacteriële ribosomale proteïnen en andere acromoleculen inactiveren of veranderen. Als gevolg van dergelijke inactiveringen worden de vitale biochemische processen van eiwitsynthese, aëroob energiemetabolisme, DNA-synthese, RNA-synthese en celwandsynthese geremd. Nitrofurantoïne is bij therapeutische doses bactericide in de urine. De breedwerkende aard van dit werkingsmechanisme kan het gebrek aan verworven bacteriële resistentie tegen nitrofurantoïne verklaren, aangezien de noodzakelijke meervoudige en gelijktijdige mutaties van de doelmacromoleculen waarschijnlijk dodelijk zouden zijn voor de bacteriën.
Interacties met andere antibiotica
Antagonisme is in vitro aangetoond tussen nitrofurantoïne en chinolon-antimicrobiële stoffen. De klinische betekenis van deze bevinding is onbekend.
Ontwikkeling van resistentie
Ontwikkeling van resistentie tegen nitrofurantoïne is sinds de introductie in 1953 geen significant probleem geweest. Kruisresistentie met antibiotica en sulfonamiden is niet waargenomen, en overdraagbare resistentie is hooguit een zeer zeldzaam verschijnsel.
Nitrofurantoïne is werkzaam gebleken tegen de meeste stammen van de volgende bacteriën, zowel in vitro als bij klinische infecties (zie Indicaties en gebruik):
Aërobe en facultatieve Gram-positieve micro-organismen:
Staphylococcus aureus
Enterococcen (bijv. Enterococcus faecalis)
Aërobe en facultatieve Gram-negatieve micro-organismen:
Escherichia coli
NOTA: Hoewel nitrofurantoïne uitstekend werkt tegen Enterococcus faecalis, is het merendeel van de Enterococcus faecium-isolaten niet vatbaar voor nitrofurantoïne.
Met ten minste 90 procent van de volgende micro-organismen is de in vitro minimaal remmende concentratie (MIC) kleiner dan of gelijk aan het breekpunt voor gevoeligheid van nitrofurantoïne. De werkzaamheid van nitrofurantoïne bij de behandeling van klinische infecties veroorzaakt door deze micro-organismen is echter niet vastgesteld in adequate en goed gecontroleerde onderzoeken.
Aërobe en facultatieve Gram-positieve micro-organismen:
Coagulase-negatieve stafylokokken (inclusief Staphylococcus
epidermidis en Staphylococcus saprophyticus)
Streptococcus agalactiae
Streptokokken van groep D
Streptokokken van groep Viridans
Aërobe en facultatieve Gram-negatieve micro-organismen:
Citrobacter amalonaticus
Citrobacter diversus
Citrobacter freundii
Klebsiella oxytoca
Klebsiella ozaenae
NOOT: Sommige stammen van Enterobacter-soorten en Klebsiella-soorten zijn resistent tegen nitrofurantoïne.
Vertrouwbaarheidstests:
Voor specifieke informatie over de interpretatiecriteria van gevoeligheidstests en bijbehorende testmethoden en door de FDA erkende kwaliteitscontrolenormen voor dit geneesmiddel, zie: https://www.fda.gov/STIC.
INDICATIES EN GEBRUIK:
Nitrofurantoïnecapsules (macrokristallen) zijn specifiek geïndiceerd voor de behandeling van urineweginfecties wanneer deze worden veroorzaakt door vatbare stammen van Escherichia coli, enterokokken, Staphylococcus aureus, en bepaalde vatbare stammen van Klebsiella en Enterobacter-soorten.
Nitrofurantoïne is niet geïndiceerd voor de behandeling van pyelonefritis of perinefrische abcessen.
Om de ontwikkeling van geneesmiddelenresistente bacteriën te verminderen en de effectiviteit van nitrofurantoïne capsules (macrocrystals) en andere antibacteriële geneesmiddelen te behouden, dienen nitrofurantoïne capsules (macrocrystals) alleen te worden gebruikt voor de behandeling of preventie van infecties waarvan bewezen is of sterk vermoed wordt dat ze worden veroorzaakt door vatbare bacteriën. Wanneer gegevens over kweek en gevoeligheid beschikbaar zijn, dient hiermee rekening te worden gehouden bij de keuze of wijziging van een antibacteriële therapie. Bij gebrek aan dergelijke gegevens kunnen lokale epidemiologie en gevoeligheidspatronen bijdragen tot de empirische therapiekeuze.
Nitrofurantoïnen missen de bredere weefseldistributie van andere therapeutische middelen die zijn goedgekeurd voor infecties van de urinewegen. Bijgevolg zijn veel patiënten die met nitrofurantoïnecapsules (macrokristallen) worden behandeld, gepredisponeerd voor persistentie of het opnieuw optreden van bacteriurie. Urinemonsters voor kweek- en gevoeligheidstests moeten voor en na beëindiging van de therapie worden verkregen. Indien persistentie of het opnieuw optreden van bacteriurie optreedt na behandeling met nitrofurantoïne capsules (macrocrystals), dienen andere therapeutische middelen met een bredere weefseldistributie te worden geselecteerd. Bij het overwegen van het gebruik van nitrofurantoïne capsules (macrocrystals) moeten lagere eradicatiepercentages worden afgewogen tegen het verhoogde potentieel voor systemische toxiciteit en voor de ontwikkeling van antimicrobiële resistentie wanneer middelen met een bredere weefseldistributie worden gebruikt.
CONTRAINDICATIES:
Anurie, oligurie, of significante stoornis van de nierfunctie (creatinineklaring minder dan 60 ml per minuut of klinisch significant verhoogd serumcreatinine) zijn contra-indicaties. Behandeling van dit type patiënten brengt een verhoogd risico op toxiciteit met zich mee vanwege een verminderde excretie van het geneesmiddel. Vanwege de mogelijkheid van hemolytische anemie als gevolg van onvolgroeide erytrocytenenzymsystemen (glutathioninstabiliteit) is het geneesmiddel gecontra-indiceerd bij zwangere patiënten die voldragen zijn (38 tot 42 weken zwangerschap), tijdens de bevalling, of wanneer het begin van de bevalling ophanden is. Om dezelfde reden is het geneesmiddel gecontra-indiceerd bij pasgeborenen jonger dan één maand.
Nitrofurantoïnecapsules (macrokristallen) zijn gecontra-indiceerd bij patiënten met een voorgeschiedenis van cholestatische geelzucht/ leverfunctiestoornissen geassocieerd met nitrofurantoïne.
Nitrofurantoïne capsules (macrocrystals) zijn ook gecontra-indiceerd bij patiënten met bekende overgevoeligheid voor nitrofurantoïne.
WAARSCHUWINGEN:
Pulmonale reacties:
ACUTE, SUBACUTE, OF CHRONISCHE PULMONAIRE REACTIES ZIJN VOORgekomen bij patiënten die met NITROFURANTOIN werden BEHANDELD. INDIEN DEZE REACTIES OPTREDEN, MOET NITROFURANTOÏNE (MACROCRYSTALS) WORDEN GESTAAKT EN MOETEN PASSENDE MAATREGELEN WORDEN GENOMEN. IN RAPPORTEN ZIJN PULMONALE REACTIES GENOEMD ALS EEN BIJDRAGENDE DOODSOORZAAK.
CHRONISCHE PULMONALE REACTIES (DIFFUSE INTERSTITIËLE PNEUMONITIS OF PULMONALE FIBROSE, OF BEIDE) KUNNEN ZICH SLUIPEND ONTWIKKELEN. DEZE REACTIES KOMEN ZELDEN VOOR EN MEESTAL BIJ PATIËNTEN DIE GEDURENDE ZES MAANDEN OF LANGER WORDEN BEHANDELD. NAUWLETTEND TOEZICHT OP DE PULMONALE CONDITIE VAN PATIËNTEN DIE LANGDURIG WORDEN BEHANDELD IS GERECHTVAARDIGD EN VEREIST DAT DE VOORDELEN VAN DE BEHANDELING WORDEN AFGEWOGEN TEGEN DE POTENTIËLE RISICO’S (ZIE RESPIRATOIRE REACTIES).
Hepatotoxiciteit:
Hepatologische reacties, waaronder hepatitis, cholestatische geelzucht, chronische actieve hepatitis, en levernecrose, komen zelden voor. Er zijn sterfgevallen gemeld. Het begin van chronische actieve hepatitis kan sluipend zijn, en patiënten moeten periodiek worden gecontroleerd op veranderingen in biochemische tests die zouden wijzen op leverschade. Indien hepatitis optreedt, dient het geneesmiddel onmiddellijk te worden teruggetrokken en dienen passende maatregelen te worden genomen.
Neuropathie:
Perifere neuropathie, die ernstig of onomkeerbaar kan worden, is voorgekomen. Er zijn sterfgevallen gemeld. Condities zoals nierinsufficiëntie (creatinineklaring lager dan 60 ml per minuut of klinisch significant verhoogd serumcreatinine), anemie, diabetes mellitus, elektrolytenonbalans, vitamine B-deficiëntie en invaliderende ziekte kunnen het optreden van perifere neuropathie bevorderen. Patiënten die langdurig worden behandeld, moeten periodiek worden gecontroleerd op veranderingen in de nierfunctie.
Optische neuritis is zelden gemeld in postmarketingervaring met nitrofurantoïneformuleringen.
Hemolytische anemie:
Gevallen van hemolytische anemie van het primaquine-gevoeligheidstype zijn geïnduceerd door nitrofurantoïne. Hemolyse lijkt verband te houden met een glucose-6-fosfaat dehydrogenase-deficiëntie in de rode bloedcellen van de getroffen patiënten. Deze deficiëntie komt voor bij 10% van de zwarten en bij een klein percentage van de etnische groepen van Mediterrane en Nabije-Oosterse oorsprong. Hemolyse is een indicatie voor het staken van nitrofurantoïne (macrocrystals); hemolyse stopt wanneer het geneesmiddel wordt ingetrokken.
Clostridium difficile-geassocieerde diarree:
Clostridium difficile-geassocieerde diarree (CDAD) is gemeld bij gebruik van bijna alle antibacteriële middelen, waaronder nitrofurantoïne, en kan in ernst variëren van milde diarree tot fatale colitis. Behandeling met antibacteriële middelen verandert de normale flora van het colon, wat leidt tot overgroei van C. difficile.
C. difficile produceert toxinen A en B die bijdragen tot de ontwikkeling van CDAD. Hypertoxineproducerende stammen van C. difficile veroorzaken een verhoogde morbiditeit en mortaliteit, aangezien deze infecties refractair kunnen zijn voor antimicrobiële therapie en colectomie kunnen vereisen. CDAD moet worden overwogen bij alle patiënten die zich met diarree na antibioticagebruik presenteren. Een zorgvuldige anamnese is noodzakelijk omdat CDAD meer dan twee maanden na de toediening van antibacteriële middelen kan optreden. Als CDAD wordt vermoed of bevestigd, kan het nodig zijn het gebruik van antibiotica die niet tegen C. difficile zijn gericht, te staken. Passend vocht- en elektrolytenbeheer, eiwitsuppletie, antibiotische behandeling van C. difficile, en chirurgische evaluatie moeten worden ingesteld zoals klinisch geïndiceerd.
VOORZORGSMAATREGELEN:
Informatie voor patiënten:
Patiënten moet worden geadviseerd nitrofurantoïne (macrocrystals) met voedsel in te nemen om de tolerantie verder te verhogen en de absorptie van het geneesmiddel te verbeteren. Patiënten moeten worden geïnstrueerd om de volledige kuur te voltooien; zij moeten echter worden geadviseerd om contact op te nemen met hun arts als zich tijdens de therapie ongewone symptomen voordoen.
Veel patiënten die microkristallijne nitrofurantoïne niet kunnen verdragen, zijn in staat om nitrofurantoïne (macrokristallen) zonder misselijkheid in te nemen.
Patiënten moet worden geadviseerd geen antacidepreparaten te gebruiken die magnesiumtrisilicaat bevatten terwijl ze nitrofurantoïne (macrocrystals) innemen.
Patiënten moet worden geadviseerd dat antibacteriële geneesmiddelen, waaronder nitrofurantoïne (macrocrystals), alleen mogen worden gebruikt voor de behandeling van bacteriële infecties. Ze behandelen geen virale infecties (bijv. verkoudheid). Wanneer nitrofurantoïne (macrocrystals) wordt voorgeschreven om een bacteriële infectie te behandelen, moet aan de patiënten worden verteld dat, hoewel het gebruikelijk is dat zij zich in het begin van de behandeling beter voelen, de medicatie precies volgens voorschrift moet worden ingenomen. Het overslaan van doses of het niet voltooien van de volledige kuur kan (1) de effectiviteit van de onmiddellijke behandeling verminderen en (2) de kans vergroten dat bacteriën resistentie ontwikkelen en in de toekomst niet meer te behandelen zijn met nitrofurantoïne (macrocrystals) of andere antibacteriële geneesmiddelen.
Diarree is een veel voorkomend probleem dat wordt veroorzaakt door antibiotica en dat gewoonlijk ophoudt wanneer het antibioticum wordt gestaakt. Soms kunnen patiënten na het begin van de behandeling met antibiotica waterige en bloederige ontlasting krijgen (met of zonder buikkrampen en koorts), zelfs nog twee of meer maanden nadat ze de laatste dosis van het antibioticum hebben ingenomen. Als dit zich voordoet, moeten patiënten zo snel mogelijk contact opnemen met hun arts.
Algemeen:
Het voorschrijven van nitrofurantoïne (macrocrystals) bij afwezigheid van een bewezen of sterk vermoede bacteriële infectie of een profylactische indicatie levert waarschijnlijk geen voordeel op voor de patiënt en verhoogt het risico op de ontwikkeling van geneesmiddelenresistente bacteriën.
Geneesmiddeleninteracties:
Antaciden die magnesiumtrisilicaat bevatten, verminderen bij gelijktijdige toediening met nitrofurantoïne zowel de snelheid als de mate van absorptie. Het mechanisme voor deze interactie is waarschijnlijk adsorptie van nitrofurantoïne aan het oppervlak van magnesiumtrisilicaat.
Uricosurische geneesmiddelen, zoals probenecid en sulfinpyrazone, kunnen de renale tubulaire secretie van nitrofurantoïne remmen. De resulterende stijging van de nitrofurantoïneserumspiegel kan de toxiciteit verhogen, en de verlaagde urinespiegels kunnen de werkzaamheid van nitrofurantoïne als antibacterieel middel voor de urinewegen verminderen.
Interacties tussen geneesmiddelen en laboratoriumtests:
Als gevolg van de aanwezigheid van nitrofurantoïne kan een vals-positieve reactie voor glucose in de urine optreden. Dit is waargenomen bij Benedict’s en Fehling’s oplossingen, maar niet bij de glucose-enzymatische test.
Carcinogenese, mutagenese, verminderde vruchtbaarheid:
Nitrofurantoïne was niet carcinogeen bij toediening aan vrouwelijke Holtzman-ratten gedurende 44,5 weken of aan vrouwelijke Sprague-Dawley-ratten gedurende 75 weken. Twee chronische bioassays bij knaagdieren met mannelijke en vrouwelijke Sprague-Dawley-ratten en twee chronische bioassays bij Zwitserse muizen en BDF1-muizen toonden geen aanwijzingen voor carcinogeniteit.
Nitrofurantoïne vertoonde aanwijzingen voor carcinogene activiteit bij vrouwelijke B6C3F1-muizen, zoals blijkt uit de verhoogde incidentie van tubulaire adenomen, goedaardige gemengde tumoren en granulosaceltumoren van de eierstok. Bij mannelijke F344/N-ratten waren er verhoogde incidenties van niet-alledaagse neoplasma’s van nierbuiscellen, osteosarcoom van het bot en neoplasma’s van het onderhuidse weefsel. In één onderzoek met onderhuidse toediening van 75 mg/kg nitrofurantoïne aan drachtige vrouwelijke muizen werden bij de F1-generatie longpapillaire adenomen van onbekende betekenis waargenomen.
Nitrofurantoïne bleek puntmutaties te induceren in bepaalde stammen Salmonella typhimurium en voorwaartse mutaties in L5178Y-muizenlymfoomcellen. Nitrofurantoïne induceerde verhoogde aantallen verwisselingen van geslachtschromatiden en chromosoomafwijkingen in Chinese hamster-ovariumcellen, maar niet in menselijke cellen in cultuur. De resultaten van de geslachtsgebonden recessieve letaliteitstest bij Drosophila waren negatief na toediening van nitrofurantoïne via voedsel of injectie. Nitrofurantoïne induceerde geen erfelijke mutatie in de onderzochte knaagdiermodellen.
De betekenis van de bevindingen inzake carcinogeniteit en mutageniteit met betrekking tot het therapeutisch gebruik van nitrofurantoïne bij de mens is onbekend.
De toediening van hoge doses nitrofurantoïne aan ratten veroorzaakt een tijdelijke spermatogene stagnatie; deze is omkeerbaar bij het staken van het geneesmiddel. Doseringen van 10 mg/kg/dag of meer bij gezonde menselijke mannen kunnen in bepaalde onvoorspelbare gevallen een lichte tot matige spermatogene stagnatie veroorzaken met een afname van het aantal zaadcellen.
Zwangerschap:
Teratogene effecten:
Zwangerschapscategorie B.
Er zijn verschillende voortplantingsstudies uitgevoerd bij konijnen en ratten met doses tot zes maal de menselijke dosis en deze hebben geen aanwijzingen opgeleverd voor verminderde vruchtbaarheid of schade aan de foetus als gevolg van nitrofurantoïne. In één gepubliceerd onderzoek bij muizen met 68 maal de menselijke dosis (gebaseerd op mg/kg toegediend aan het moederdier) werden groeivertraging en een lage incidentie van kleine en gewone misvormingen waargenomen. Bij 25 maal de menselijke dosis werden echter geen foetale misvormingen waargenomen; de relevantie van deze bevindingen voor de mens is onzeker. Er zijn echter geen adequate en goed gecontroleerde studies bij zwangere vrouwen. Omdat voortplantingsstudies bij dieren niet altijd voorspellend zijn voor de reactie bij de mens, mag dit geneesmiddel tijdens de zwangerschap alleen worden gebruikt als het duidelijk nodig is.
Niet-teratogene effecten:
Nitrofurantoïne heeft in één gepubliceerde transplacentale carcinogeniteitsstudie aangetoond dat het longpapillaire adenomen in de F1-generatie muizen induceert bij doses die 19 keer de menselijke dosis bedragen op een basis van mg/kg. De relatie van deze bevinding tot mogelijke carcinogenese bij de mens is momenteel onbekend. Vanwege de onzekerheid over de implicaties van deze dierlijke gegevens voor de mens, mag dit geneesmiddel tijdens de zwangerschap alleen worden gebruikt indien dit duidelijk nodig is.
Labor and Delivery:
Zie CONTRA-INDICATIES.
Nonterende moeders:
Nitrofurantoïne is in sporenhoeveelheden gedetecteerd in de moedermelk van de mens. Vanwege de mogelijkheid van ernstige bijwerkingen van nitrofurantoïne bij zogende zuigelingen jonger dan één maand, moet worden besloten of de borstvoeding moet worden gestaakt of dat het geneesmiddel moet worden gestaakt, rekening houdend met het belang van het geneesmiddel voor de moeder (zie CONTRA-INDICATIES).
Pediatrisch gebruik:
Nitrofurantoïne (macrocrystals) is gecontra-indiceerd bij zuigelingen jonger dan één maand (zie CONTRA-INDICATIES).
Geriatrisch gebruik:
Clinische studies van nitrofurantoïne (macrocrystals) omvatten niet voldoende proefpersonen van 65 jaar en ouder om te bepalen of zij anders reageren dan jongere proefpersonen. Andere gerapporteerde klinische ervaring heeft geen verschillen in reacties tussen ouderen en jongere patiënten vastgesteld. Spontane meldingen suggereren een hoger percentage pulmonale reacties, inclusief fatale afloop, bij oudere patiënten; deze verschillen lijken verband te houden met het hogere percentage oudere patiënten dat langdurig met nitrofurantoïne wordt behandeld. Net als bij jongere patiënten worden chronische longreacties in het algemeen waargenomen bij patiënten die gedurende zes maanden of langer worden behandeld (zie WAARSCHUWINGEN). Spontane meldingen wijzen ook op een verhoogd aandeel van ernstige leverreacties, met inbegrip van fatale afloop, bij oudere patiënten (zie WAARSCHUWINGEN).
In het algemeen moet bij het voorschrijven van nitrofurantoïne (macrocrystals) rekening worden gehouden met de grotere frequentie van verminderde lever-, nier- of hartfunctie, en van gelijktijdige ziekte of andere geneesmiddelentherapie. Van dit geneesmiddel is bekend dat het in belangrijke mate door de nieren wordt uitgescheiden, en het risico van toxische reacties op dit geneesmiddel kan groter zijn bij patiënten met een verminderde nierfunctie. Anurie, oligurie of een significante stoornis van de nierfunctie (creatinineklaring minder dan 60 ml per minuut of klinisch significant verhoogd serumcreatinine) zijn contra-indicaties (zie CONTRA-INDICATIES). Omdat oudere patiënten een grotere kans hebben op een verminderde nierfunctie, is voorzichtigheid geboden bij de keuze van de dosis en kan het nuttig zijn de nierfunctie te controleren.
ADVERSE REACTIES:
Respiratoire:
CHRONISCHE, SUBACUTE, OF ACUTE PULMONAIRE HYPERSENSITIVITEITSREACTIES KUNNEN OPTREDEN.
CHRONISCHE PULMONAIRE REACTIES KUNNEN OPTREDEN ALGEMEEN BIJ PATIËNTEN DIE ZES MAANDEN OF LANGER EEN VOORTDURENDE BEHANDELING HEBBEN GECURSULEERD. MALAISE, DYSPNEU BIJ INSPANNING, HOEST EN VERANDERDE LONGFUNCTIE ZIJN VEEL VOORKOMENDE VERSCHIJNSELEN DIE SLUIPEND KUNNEN OPTREDEN. RADIOLOGISCHE EN HISTOLOGISCHE BEVINDINGEN VAN DIFFUSE INTERSTITIËLE PNEUMONITIS OF FIBROSE, OF BEIDE, ZIJN OOK VEEL VOORKOMENDE MANIFESTATIES VAN DE CHRONISCHE LONGREACTIE. KOORTS IS ZELDEN PROMINENT AANWEZIG.
DE ERNST VAN DE CHRONISCHE LONGREACTIES EN DE MATE WAARIN ZIJ VERDWIJNEN, LIJKEN VERBAND TE HOUDEN MET DE DUUR VAN DE THERAPIE NA HET VERSCHIJNEN VAN DE EERSTE KLINISCHE VERSCHIJNSELEN. DE LONGFUNCTIE KAN BLIJVEND VERMINDERD ZIJN, ZELFS NA HET STAKEN VAN DE THERAPIE. HET RISICO IS GROTER WANNEER CHRONISCHE PULMONAIRE REACTIES NIET EERLIJK WORDEN HERKEND.
Bij subacute pulmonale reacties komen koorts en eosinofilie minder vaak voor dan bij de acute vorm. Na het staken van de therapie kan het herstel enkele maanden duren. Als de symptomen niet worden herkend als geneesmiddelgerelateerd en nitrofurantoïne-therapie niet wordt gestaakt, kunnen de symptomen ernstiger worden.
Acute pulmonale reacties uiten zich gewoonlijk door koorts, koude rillingen, hoest, pijn op de borst, dyspneu, pulmonale infiltratie met consolidatie of pleurale effusie op röntgenfoto’s, en eosinofilie. Acute reacties treden gewoonlijk op in de eerste week van de behandeling en zijn omkeerbaar na het staken van de behandeling. De resolutie is vaak dramatisch (zie WAARSCHUWINGEN).
Veranderingen in EKG (bijv, niet-specifieke ST/T-golfveranderingen, bundeltakblok) zijn gemeld in associatie met pulmonale reacties.
Cyanose is zelden gemeld.
Hepatisch:
Hepatische reacties, waaronder hepatitis, cholestatische geelzucht, chronische actieve hepatitis en levernecrose, komen zelden voor (zie WAARSCHUWINGEN).
Neurologisch:
Perifere neuropathie, die ernstig of irreversibel kan worden, is voorgekomen. Er zijn sterfgevallen gemeld. Aandoeningen zoals nierinsufficiëntie (creatinineklaring lager dan 60 ml per minuut of klinisch significant verhoogd serumcreatinine), bloedarmoede, diabetes mellitus, onbalans in elektrolyten, vitamine B-deficiëntie en invaliderende ziekten kunnen de kans op perifere neuropathie vergroten (zie WAARSCHUWINGEN).
Asthenie, vertigo, nystagmus, duizeligheid, hoofdpijn en slaperigheid zijn ook gemeld bij het gebruik van nitrofurantoïne.
Benigne intracraniële hypertensie (pseudotumor cerebri), verwardheid, depressie, neuritis optica, en psychotische reacties zijn zelden gemeld. Uitpuilende fontanellen, als teken van goedaardige intracraniële hypertensie bij zuigelingen, zijn zelden gemeld.
Dermatologisch:
Exfoliatieve dermatitis en erythema multiforme (inclusief Stevens-Johnson syndroom) zijn zelden gemeld. Voorbijgaande alopecia is ook gemeld.
Allergisch:
Een lupusachtig syndroom geassocieerd met pulmonale reacties op nitrofurantoïne is gemeld. Ook zijn angio-oedeem; maculopapuleuze, erythemateuze of eczemateuze erupties; pruritus; urticaria; anafylaxie; artralgie; myalgie; medicijnkoorts; koude rillingen; en vasculitis (soms geassocieerd met pulmonale reacties) gerapporteerd. Overgevoeligheidsreacties vormen de meest frequente spontaan gemelde bijwerkingen in wereldwijde postmarketingervaring met nitrofurantoïneformuleringen.
Gastro-intestinaal:
Nausea, emesis, en anorexie komen het vaakst voor. Buikpijn en diarree zijn minder vaak voorkomende gastro-intestinale reacties. Deze dosis-gerelateerde reacties kunnen worden geminimaliseerd door verlaging van de dosering. Sialadenitis en pancreatitis zijn gemeld. Er zijn sporadische meldingen geweest van pseudomembraneuze colitis bij het gebruik van nitrofurantoïne. Het begin van pseudomembraneuze colitis-symptomen kan optreden tijdens of na antimicrobiële behandeling (zie WAARSCHUWINGEN).
Hematologisch:
Cyanose secundair aan methemoglobinemie is zelden gemeld.
Diversen:
Zoals bij andere antimicrobiële middelen kunnen superinfecties veroorzaakt door resistente organismen, bijv, Pseudomonas species of Candida species, kunnen voorkomen.
Laboratoriumbijwerkingen:
De volgende laboratoriumbijwerkingen zijn gemeld bij het gebruik van nitrofurantoïne: verhoogde AST (SGOT), verhoogde ALT (SGPT), verlaagd hemoglobine, verhoogd serumfosfor, eosinofilie, glucose-6-fosfaat dehydrogenase deficiëntie anemie (zie WAARSCHUWINGEN), agranulocytose, leukopenie, granulocytopenie, hemolytische anemie, trombocytopenie, megaloblastaire anemie. In de meeste gevallen verdwenen deze hematologische afwijkingen na het staken van de therapie. Aplastische anemie is zelden gemeld.
Overdosering
Eenmalige incidenten van acute overdosering van nitrofurantoïne (macrocrystals) hebben niet geleid tot specifieke symptomen anders dan braken. Inductie van emesis wordt aanbevolen. Er is geen specifiek antidotum, maar een hoge vochtinname moet worden gehandhaafd om de uitscheiding van het geneesmiddel via de urine te bevorderen. Het is dialyseerbaar.
DOSERING EN TOEDIENING:
Nitrofurantoïne capsules (macrocrystals) dienen met voedsel te worden gegeven om de absorptie van het geneesmiddel en, bij sommige patiënten, de tolerantie te verbeteren.
Volwassenen:
50 mg tot 100 mg viermaal daags — de lagere dosering wordt aanbevolen voor ongecompliceerde urineweginfecties.
Pediatrische patiënten:
5 tot 7 mg/kg lichaamsgewicht per 24 uur, gegeven in vier verdeelde doses (gecontra-indiceerd onder de leeftijd van één maand).
De therapie moet worden voortgezet gedurende één week of gedurende ten minste 3 dagen nadat steriliteit van de urine is verkregen. Aanhoudende infectie wijst op de noodzaak van herbeoordeling.
Voor langdurige suppressieve therapie bij volwassenen kan een verlaging van de dosering tot 50-100 mg bij het slapen gaan voldoende zijn. Voor suppressieve therapie op lange termijn bij pediatrische patiënten kunnen doses zo laag als 1 mg/kg per 24 uur, gegeven in een enkele dosis of in twee verdeelde doses, toereikend zijn. ZIE DE WAARSCHUWINGEN MET BETREKKING TOT DE RISICO’S BIJ LANGDURIGE THERAPIE.
HOW SUPPLIED:
Nitrofurantoïne Capsules USP (macrokristallen) zijn als volgt verkrijgbaar:
50 mg ondoorzichtig, wit lichaam en ondoorzichtig, geel dopje met zwarte opdruk “WATSON” op het dopje en “5780” op het lichaam.
NDC 0115-2023-10 flesjes van 100
100 mg ondoorzichtige, gele capsule met zwarte opdruk “WATSON” op de dop en “5781” op de romp.
NDC 0115-2024-10 flesjes à 100
Bewaren bij 20° tot 25°C (68° tot 77°F) .
Gemaakt door:
Watson Pharma Private Limited
Verna, Salcette Goa 403722 INDIA
Distributie door:
Amneal Pharmaceuticals LLC
Bridgewater, NJ 08807
Om VERWACHTE BIJWERKINGEN TE MELDEN, neem contact op met Amneal Pharmaceuticals op 1-877-835-5472 of FDA op 1-800-FDA-1088 of www.fda.gov/medwatch.
Rev. 11-2019-00
PRINCIPAL DISPLAY PANEL – 50 mg

PRINCIPAL DISPLAY PANEL – 100 mg

PRINCIPAL DISPLAY PANEL – 100 mg

. 100 mg

| NITROFURANTOIN nitrofurantoïne-capsule |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
| NITROFURANTOIN nitrofurantoïne-capsule |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
Etiketteerder -. Amneal Pharmaceuticals of New York LLC (123797875)
Veel gestelde vragen
- Welke antibiotica worden gebruikt om UTI te behandelen?
- Wat is “dual release” nitrofurantoine?
Meer over nitrofurantoïne
- Bijwerkingen
- Tijdens zwangerschap of borstvoeding
- Doseringsinformatie
- Patiëntentips
- Gebruiksaanwijzing
- Gebruiksaanwijzing
- Gebruiksaanwijzing
- Gebruiksaanwijzing
- Gebruiksaanwijzing
- Images
- Drug Interactions
- Compare Alternatives
- Support Group
- Pricing & Coupons
- En Español
- 1538 Reviews
- Drug class: urineweg-infectiva
Consumenteninformatie
- Patiënteninformatie
- Nitrofurantoïne (geavanceerd lezen)
Professionele informatie
- Voorschrijf Informatie
- Nitrofurantoïne (Professioneel patiëntenadvies)
- Nitrofurantoïne Capsules (FDA)
- Nitrofurantoïne Orale Suspensie (FDA)
Andere merken Macrobid, Macrodantin, Furadantin
Gerelateerde behandelingsgidsen
- Infectie van de urinewegen
- Voorkomen van blaasontsteking
- Blaasontsteking
Medische disclaimer