Atriumfibrilleren (AF) is de meest frequente aanhoudende tachyaritmie en komt voor bij 1% tot 2% van de bevolking. Longveneuze isolatie (PVI) is de belangrijkste methode voor AF-ablatie.1 Hoewel deze procedure effectief is in het voorkomen van nieuwe ritmestoornissen bij patiënten met paroxysmale AF, heeft ze, als ze alleen wordt uitgevoerd, slechts beperkt succes bij persisterende AF.1,2 De eerste gegevens suggereerden dat nieuwe ritmestoornissen zouden kunnen worden verminderd door aanvullende lijnablatie of complexe gefractioneerde atriale elektrogramablatie. Het voordeel van aanvullende ablatie naast PVI is echter niet bevestigd door de recente resultaten van meta-analyses3 en gerandomiseerde gecontroleerde onderzoeken,4 die het belang van duurzame PVI benadrukken, zelfs bij persisterend AF.
In de afgelopen jaren is cryoballonablatie een levensvatbaar alternatief geworden voor radiofrequente (RF) ablatie en heeft bewezen minstens even effectief te zijn als PVI bij patiënten met paroxysmale AF. De recente resultaten van de FIRE & ICE trial hebben het debat op dit gebied definitief beslecht.5 Bovendien is deze procedure, vanwege de relatieve eenvoud, de snellere leercurve -en misschien nog wel belangrijker- de opmerkelijke reproduceerbaarheid6 ervan, op grote schaal in de klinische praktijk ingevoerd.6
Aan de andere kant blijft de interventionele behandeling van persisterend AF een uitdaging: deze benadering is niet gestandaardiseerd of geperfectioneerd en er is ruimte voor innovatie. In deze setting is de vraag naar een mogelijke rol van cryoablatie interessant.
KLINISCHE EVIDENTIE
Hoewel er toenemende belangstelling is voor de werkzaamheid van AF-ablatie bij patiënten met persisterend AF, zijn de follow-upgegevens na gebruik van de nieuwe 28-mm tweede-generatie cryoballonkatheter (Arctic Front Advance, Medtronic Inc., Minneapolis, MN) nog steeds beperkt. Tot op heden zijn de resultaten van postcryoballoonablatie bij persisterend AF indirect beoordeeld door meta-analyses, niet-gerandomiseerde vergelijkingen,7 en observationele studies.8-10
Ciconte et al.9 meldden dat 60% van de patiënten met persisterend AF vrij was van atriale tachyaritmie na behandeling met de nieuwe cryoballoonkatheter. De duur van persisterend AF, die een onafhankelijke voorspeller was van het terugkeren van aritmie tijdens de follow-up, biedt duidelijke steun voor ablatie in vroegere stadia van de ziekte.
In een retrospectieve studie van 48 patiënten met persisterend AF, was het 1-jarig klinisch succespercentage 69%.10
Een andere eenarmige studie beoordeelde de werkzaamheid van de tweede-generatie cryoablatie in een groep van 100 persisterende AF-patiënten als indexprocedure (gemiddelde duur 5,5 ± 3,7 maanden).8 Na een gemiddelde follow-up van 10,6 ± 6,3 maanden, waren er geen recidieven van atriale tachyaritmie bij 67% van de patiënten na een blanking-periode van 3 maanden. De enige significante onafhankelijke voorspeller van herval was het optreden van atriale tachyaritmie tijdens de blanco periode.
Een single-center, niet-prospectieve, niet-gerandomiseerde studie evalueerde ook RF in vergelijking met cryoablatie bij uitsluitend persisterende AF-patiënten.7 In die studie werd het procedurele resultaat van RF-ablatie (met behulp van een contact-krachtablatiekatheter) vergeleken met cryoablatie (met behulp van de 28-mm tweede-generatie cryoballon) geëvalueerd in een cohort van 100 patiënten met medicijnrefractair persisterend AF (de gemiddelde duur van AF was respectievelijk 7,2 en 7,6 maanden in de RF-ablatie- en cryoablatiegroepen). Zowel de procedure- als de fluoroscopietijd waren significant korter in de cryoablatiegroep, maar het percentage patiënten zonder atriale aritmieën was vergelijkbaar tussen de 2 groepen na 12 maanden follow-up (60% in de cryoablatie- vs 56% in de RF-ablatiegroep, P = .71). Bij multivariate analyse bleken de enige onafhankelijke voorspellers van falen opnieuw de duur van persisterend AF en recidieven tijdens de blanking periode te zijn.
Ten slotte vergeleek een prospectieve, multicenter, niet-gerandomiseerde studie de resultaten na een enkele ablatieprocedure, waarbij uitsluitend gebruik werd gemaakt van cryoballonablatie van de eerste generatie voor PVI vs. open RF-ablatie via een stapsgewijze benadering in een cohort van propensity-matched patiënten met persisterend AF.11 De resultaten, die ongeveer 55% vrijheid van atriale aritmieën lieten zien tijdens een gemiddelde follow-up van 15,6 ± 11,5 maanden na een enkele ablatie, zowel met de cryoballon als met RF, waren vergelijkbaar met de beschikbare gegevens. Verschillende bevindingen waren opmerkelijk:
- –
Ten eerste, klinische resultaten waren vergelijkbaar in de 2 behandelingsarmen, ook al onderging de RF-groep aanvullende en uitgebreidere ablatie dan PVI.
- –
Ten tweede, het complicatiepercentage was vergelijkbaar met de 2 technieken.
- –
Ten derde, de duur van de procedure was korter met cryoablatie.
Er is nog steeds onzekerheid over de pathofysiologie en de optimale strategie voor persisterende AF ablatie, en daarom blijft de steunpilaar van deze therapie het bereiken van een duurzame PVI.4 Om dit te bereiken lijkt cryoablatie een valide alternatieve therapeutische benadering van RF te zijn. Het uitvoeren van bijkomende ablatie bovenop PVI gaat gepaard met een langere proceduretijd.4 Omdat de RF-ablatiebenadering niet gestandaardiseerd is (de meeste patiënten in de RF-arm ontwikkelden bijkomende laesies), is het onduidelijk of de resultaten te wijten zijn aan de energiebron of aan de ablatiestrategie. Bovendien lijken de resultaten op middellange termijn niet significant te verbeteren door extra biatriale laesies naast PVI bij persisterende AF-patiënten.4
HOOT HET RECHTE DOEL AAN?
De redenen voor het ontbreken van een verbeterd voordeel van extra ablatie moeten nog worden opgehelderd. Eén mogelijkheid is het iatrogene potentieel van een substraatbenadering met uitgebreidere ablatie, die de ontwikkeling van nieuwe gebieden van aritmogenese door onvolledig geablseerd weefsel of onvolledige lijnen van geleidingsblokkade kan bevorderen. Een andere mogelijkheid is dat het schuldige gebied niet routinematig wordt geïdentificeerd en dat noch complexe gefractioneerde atriale elektrogrammen noch lineaire laesies de optimale aanvullende doelen voor ablatie zijn.12 In deze hypothese blijft het nodig om het oog van de storm te lokaliseren (door rotors of ganglia te targeten)13 , mogelijk door gebruik te maken van nieuwere mapping algoritmen. De beschikbare gegevens ondersteunen ook de rol van de duur van AF, en bijgevolg de elektrische AF-remodellering (AF begets AF), omdat alleen de duur van AF een onafhankelijke voorspeller was van het terugkeren van aritmie in de propensity-score vergelijking,11 zoals eerder gerapporteerd door Tilz et al.2
Verschillende lopende trials zullen helpen om de veiligheid en doeltreffendheid van cryoablatie bij persisterende AF-patiënten te verduidelijken. De Cryoballoon Ablation for Early Persistent Atrial Fibrillation trial (Cryo4 Persistent AF – NCT02213731) is een Europese multicenter, prospectieve, single-arm pilotstudie, gericht op het evalueren van het succespercentage van PVI uitsluitend door middel van cryoablatie na 1 jaar bij patiënten die zich presenteren met een persisterende AF-geschiedenis van minder dan 12 maanden. Deze studie bevindt zich nog in de rekruteringsfase en de eerste resultaten worden eind 2017 verwacht. Het volgende doel zal zijn om de resultaten in een gerandomiseerde studie te vergelijken tussen de stapsgewijze RF-benadering en PVI-cryoablatie in een homogene groep patiënten met persisterend AF. Naar de resultaten van deze grootschalige gerandomiseerde studie wordt reikhalzend uitgekeken.
STRENGDHEDEN EN BEPERKINGEN
Bij persisterende AF-patiënten zijn zelfs de hoogste maximale PV-diameters (tussen 20 en 23 mm) aanzienlijk lager dan de kritische waarde van 28 mm (de maximale diameter van de cryoballon die in de routine klinische praktijk wordt gebruikt).14 Vanwege deze discrepantie tussen de diameters van de ballon en PVs, wanneer dit apparaat is geplaatst tegen de PV antrum, het koelende deel is in contact met zowel de PV antra en de aangrenzende atriale weefsel, dat lijkt te zijn een belangrijk voordeel van deze procedure. Kenigsberg et al.,15 berekende het gebied van het geableerde hartweefsel na PV cryoablatie door 3-dimensionale elektro-anatomische spanning mapping van het linker atrium na cryoablatie. Met behulp van deze methode, deze auteurs mooi aangetoond dat, na cryoablatie met de 28-mm cryoballon apparaat, het percentage van de linker atrium achterwand oppervlak dat bleef elektrisch intact was slechts 27%.
Opgemerkt, hoewel de cryoballon conceptueel richt zich alleen op de PV’s, het voert ook aanzienlijke elektrische debulking van de achterwand van de linker atrium (figuur). Door het uitbreiden van de omtrek van het koelgebied, kan dit apparaat een bijkomend voordeel bieden door het ableren van lokale bijdragen aan structuren die bijdragen aan het triggeren en in stand houden van AF, zoals ganglionische plexi en rotors, wat mogelijk belangrijke therapeutische implicaties heeft voor patiënten met persisterende AF.13 Dit kenmerk zou ook, althans gedeeltelijk, de resultaten van de bovengenoemde trials kunnen verklaren.
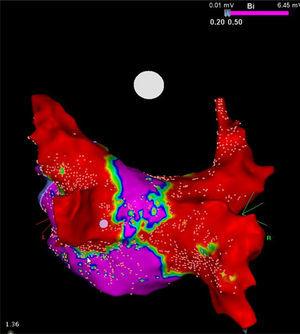
Hoge-densiteit spanningskaart van de achterwand na een cryoablatieprocedure bij een patiënt met persisterend atriumfibrilleren. Let op de smalle corridor (paars) die overblijft tussen beide grote littekens (rood), verkregen met de 28 mm Artic Front Advance cryoballon (Medtronic, Minneapolis, MN, Verenigde Staten). Met dank aan Prof. Mario Oliveira, Santa Marta Ziekenhuis, Lissabon, Portugal.
Hoewel de succespercentages van cryoballon vergelijkbaar zijn met die van RF in niet-gerandomiseerde studies van patiënten met persisterend AF, blijft het relatief hoge aantal terugkerende aritmieën in beide groepen onverklaard en zou het niet alleen te wijten kunnen zijn aan geleidingsherstel van de PVs. Deze mogelijkheid is genoemd in studies die bezorgdheid uitten over de rol van niet-PVI bronnen die het mechanisme voor herval leveren.9
In persistent AF blijft invasieve behandeling een uitdaging vanwege de diverse pathofysiologie. Nieuwe mechanistische inzichten zijn nodig om een individueel aangepaste benadering van persisterend AF mogelijk te maken, maar totdat dergelijke kennis beschikbaar komt, kan een eerste-intentie standalone PVI voldoende zijn, ten minste voor patiënten met minder ernstig persisterend AF. Op basis van deze “minder is meer”-benadering kan cryoballon PVI een adequate ablatiestrategie blijken te zijn bij persisterend AF, die betrouwbare PVI mogelijk maakt met bijkomende debulking van het naburige atriale myocardium. Bijkomende substraatmodificatie lijkt geen bijkomend voordeel op te leveren. Deze “minimalistische” procedure is een aanvaardbare eerste optie bij patiënten met een relatief recente geschiedenis van symptomatisch persisterend AF, d.w.z. met “meer trigger dan substraat” (of met een substraat geconcentreerd rond de PVs ostia…). De grote (28 mm) cryoballon van de tweede generatie levert inderdaad resultaten op die vergelijkbaar zijn met die van meer complexe procedures waarbij RF-energie en verfijnde methoden worden gebruikt. De leercurve, reproduceerbaarheid en veiligheid lijken in het voordeel te zijn van het cryoballonapparaat in minder ervaren handen. In deze setting, en in de bovengenoemde subgroep van patiënten, lijkt PVI met de grote cryoballon van de tweede generatie een redelijke initiële benadering te zijn, die een significante verbetering oplevert voor meer dan de helft van de kandidaten. Voor patiënten met AF-recidieven zal deze eerste procedure niet nutteloos zijn. In een aanzienlijk deel van het substraat (rond de rechter en linker PV antra) dat reeds behandeld is, zal de tweede procedure, met RF deze keer, zich vooral richten op extra-PVs foci, gefragmenteerde potentialen, micro- of macroreentrant circuits enz.
Naar onze mening is deze 2-stappen strategie verenigbaar met de inzet van lage- tot midden-volume centra die zich vooral richten op PVI’s, en hand in hand werken met tertiaire verwijzingscentra die de meer complexe procedures uitvoeren. Deze laatste zullen moeten omgaan met de ongeveer 40% van de patiënten die recidieven hebben na de eerste “cryo-debulking”.
“Less is more”, maar toch, het is niet genoeg…
CONFLICTS OF INTEREST
S. Boveda ontvangt adviesvergoedingen van Medtronic, Boston Scientific en Livanova.