Interacties tussen hersenen en stollingsproces hebben een lange geschiedenis, inclusief de observatie dat het stollingsmechanisme in het centrale zenuwstelsel een aantal verschillen vertoont met dat in andere organen – het endotheel van de hersenen brengt bijvoorbeeld weinig trombomoduline tot expressie.
Wat het mechanisme ook is, het is moeilijk de observatie te vermijden dat behandeling met antistolling (b.v, met laag moleculair gewicht heparine) vaak de symptomen drastisch terugdraait, inclusief de migraine, de geheugen moeilijkheden en de chorea. Dergelijke waarnemingen suggereren dat de hersenpathologie in veel gevallen misschien niet zozeer een infarct is, maar meer te maken heeft met “dichtslibben” van de bloedtoevoer en verminderde oxygenatie.
Migraine & Beroerte
“Had u als tiener last van hoofdpijn?”
“Ja, dokter. Een tijd lang waren ze bijna wekelijks. Ze gingen weg voor een paar jaar, maar ze kwamen terug met een wraak nu. Het zit in mijn familie.”
Zo spreekt de 30-jarige vrouwelijke patiënt met APS (de mannelijke familieleden komen minder vaak voor in APS-klinieken).
Dit is zo’n belangrijke diagnostische aanwijzing bij de beoordeling van een patiënt met mogelijke APS. Toch zijn er, ondanks de vele jaren ervaring met APS, verrassend weinig gegevens die de ware rol van APS in de bredere wereld van migraine beoordelen. Er zijn zoveel redenen om het verband te bestuderen – de reactie op antistolling – meestal goed, vaak opvallend – de studie van broers en zussen en andere familieleden van migraine/APS-patiënten. En bovenal de verbanden die nu worden gemeld tussen migraine en beroerte.
APS/Hughes-syndroom is in hoge mate een neurologische aandoening. De hersenfunctie lijkt een speciaal doelwit te zijn – hoe meer APS-patiënten men ziet, hoe breder & de neuro-psychiatrische rimpelingen zich verspreiden.
Naast migraine is beroerte een van de erkende complicaties van het APS/Hughes-syndroom. Er zijn cijfers gerapporteerd van 1 op de 5 jonge beroerten (jonger dan 45 jaar) met een positieve aPL test.14-19
Echter, net als bij migraine, is de herkenning van aPL in de etiologie van beroerten in het algemeen nog steeds slecht. Bijvoorbeeld, beroerte bij kinderen – klinisch goed herkend – is een uitstekend doelwit voor aPL studies.
Enkele jaren geleden lanceerde de Britse regering een groot beroerte-initiatief, waarbij het publiek werd voorgelicht over de symptomen, tekenen en behandeling van beroerte. Het antifosfolipiden syndroom stond niet op de lijst.
Stuipen
In 1985 stelden we vast dat bij lupus patiënten, aanvallen vaker voorkwamen bij die patiënten met positieve aPL testen.20 Sindsdien is het duidelijk geworden dat epilepsie, in al zijn vormen, een belangrijk begeleidend verschijnsel is van APS. Zozeer zelfs, dat in een onderzoek naar idiopathische epilepsie bij tieners, 1 op de 5 aPL-positief bleek te zijn.21

Bij de eerste screening door de verloskundige of gynaecoloog zou een eenvoudige vragenlijst moeten worden afgenomen om APS uit te sluiten.
Image Credit: SPL/Science Source
De vertakkingen van deze observaties zijn velerlei. Laat me twee klinische voorbeelden geven:
Ten eerste, temporale kwab epilepsie in APS kan onder-herkend zijn. Een van mijn patiënten, een vrouw met klassieke APS, werd EEG-technicus. Tijdens haar opleiding gebruikte ze vier van haar broers en zussen als proefkonijn. Drie hadden abnormale temporale kwab activiteit. Het is interessant om te zien hoe vaak een familiegeschiedenis van epilepsie opduikt in de anamnese van patiënten met APS.
De tweede klinische anekdote is elders gepubliceerd.22 Een 42-jarige patiënte had een voorgeschiedenis van milde lupus. Haar grootste probleem, dat een grote impact had op haar drukke leven, waren echter de recidiverende aanvallen, zowel petit mal als grand mal, waarbij de laatste specialistische zorg en de combinatie van een aantal anti-epileptica vereiste. Tijdens haar verblijf in Londen ontwikkelde zij een DVT (zij bleek aPL-positief te zijn), en er werd begonnen met een routine-anticoagulatie met warfarine. Een onmiddellijk en onverwacht voordeel was een duidelijke vermindering van de frequentie en de ernst van de aanvallen, waardoor veel minder agressieve anti-epileptische behandeling nodig was.
‘HET STILLE GEBOREN SCHANDAL: Elke dag worden in het Verenigd Koninkrijk wel drie baby’s doodgeboren die nog hadden kunnen leven. Eén op de 200 geboorten van Britse vrouwen wordt doodgeboren. Het is tijd voor de NHS om een nieuw beleid en een nieuwe houding aan te nemen. -The Times (Londen), 28 nov. 2012
Geheugenverlies
Mogelijk de meest voorkomende manifestatie van APS is geheugenverlies. Vaak komt het probleem pas aan het licht als de patiënt naar het symptoom wordt gevraagd. Veel patiënten bekennen dus dat ze zich zorgen maken over Alzheimer. Tot op heden zijn er weinig gedetailleerde klinische studies. Van tijd tot tijd, en het moet gezegd worden, op een tamelijk desultatieve manier, hebben we psychometrische testen uitgevoerd op geselecteerde APS patiënten – en de resultaten waren vaak verrassend. De resultaten zijn vaak verrassend, temeer daar er een opvallende verbetering wordt waargenomen bij geheugentests wanneer met antistolling wordt begonnen.23
Multiple Sclerosis
Gezien de prominente aanwezigheid van neurologische kenmerken, waaronder visusstoornissen en fluctuerende myelopathie, die bij APS wordt gezien, is het niet verwonderlijk dat in een aantal gevallen de diagnose MS wordt gesteld.24,25
Het onderwerp is verre van eenduidig. Sommigen in de neurologie verklaren dat positieve aPL-testen in feite soms bij klassieke MS worden gezien. Ik zou het beeld liever omkeren. Dergelijke patiënten, althans een aantal, kunnen in de eerste plaats APS hebben en in de tweede plaats MS. Hoewel anekdotisch gezien een aantal van dergelijke gevallen reageert op antistolling, is de respons bij anderen op zijn best grensverleggend. Uthman heeft onlangs een overzicht gegeven van de vrij omvangrijke literatuur over APS versus MS.26
Andere neurologische kenmerken
Daaronder vallen evenwichtsproblemen (een aantal gevallen presenteert zich als de ziekte van Menière), chorea (soms ernstig),27,28 anosmie, slaapstoornissen (waaronder kataplexie en narcolepsie) en, recentelijk, autonome stoornissen met een serie gevallen van POTS (posturaal orthostatisch tachycardie syndroom).29
Een van de vragen waarover discussie bestaat is de prevalentie van psychiatrische manifestaties.
Ik ben van mening dat acute psychose meer een kenmerk is van lupus dan van APS, maar hierin kan ik me vergissen. Een van mijn patiënten, een vrouw met APS en OCD (obsessieve compulsieve stoornis), verbeterde met antistollingsbehandeling. Interessant is dat haar tienerzoon, ook een patiënt met OCD (en aPL positief), vond dat de neuropsychiatrische manifestaties veel minder prominent waren toen met aspirine behandeling werd begonnen.
Niet de Hersenen
Botten &gewrichten-Hebt u breuken opgelopen? Een vraag die misschien geen deel uitmaakt van de routine-anamnese bij APS patienten. En toch worden spontane botbreuken goed herkend na het verslag van 27 spontane metatarsale fracturen door Dr. Shirish Sangle bij APS patiënten.30
Anecdotische verslagen suggereren dat (ischemische) botbreuken een belangrijke manifestatie van de ziekte kunnen zijn: Mijn collega, professor Munther Khamashta, heeft een patiënt met het Hughes syndroom met normale DEXA en bijschildklier onderzoeken die 57 spontane botbreuken heeft gehad. Het is duidelijk dat dit een belangrijk gebied is voor klinisch onderzoek.
Zo ook is avasculaire necrose (AVN) heuppijn niet ongewoon bij onze APS patiënten. MRI heeft vroege AVN aangetoond in sommige gevallen zonder andere risicofactoren, zoals steroïden. Mijn klinische indruk is dat de heuppijn vaak verbetert wanneer met heparine of warfarine wordt gestart.
Hart-Een belangrijk punt van zorg is de aanwezigheid van angina en andere cardiale symptomen bij APS. Ondanks enkele vroege meldingen van myocardischemie en coronaire trombose, is het pas de laatste jaren dat publicaties die een hoge frequentie van deze complicaties aantonen, toenemen.
Twee voorbeelden zijn het onderzoek van Greco et al dat een relatief hoge prevalentie van positieve aPL-testen aantoont bij patiënten met cardiale ischemie, en de opvallende observatie dat vrouwelijke rokers die de pil gebruikten en aPL-positief waren, een relatief risico hadden van 22 maal voor het ontwikkelen van een myocardisch infarct.31,32
De cardiale verbanden worden versterkt door de melding van een associatie met het cardiale syndroom X, angina pectoris met normale coronaire angiografieën.33 Het is een redelijke gok dat aPL-testen een standaard zullen worden in de cardiologische kliniek, vooral bij symptomatische vrouwen onder de 40.
Zoals migraine is beroerte een van de erkende complicaties van APS/Hughes syndroom. Er zijn cijfers gerapporteerd van wel 1 op de 5 jonge beroerten (jonger dan 45 jaar) met een positieve aPL-test.
GI tract & lever-Sinds wij onze waarnemingen hebben gedaan over focale stenotische laesies in verschillende slagaders, waaronder de arteria celiacis en de arteria mesentericus, hebben wij ons meer gericht op symptomen van abdominale angina bij patiënten met aPL/APS.34 Dit is een moeilijk te kwantificeren aandoening, maar wij hebben een aantal gevallen gezien bij wie clopidogrel of heparine resulteerde in een (soms duidelijke) verbetering van de post-prandiale pijn.
Hoewel leverbetrokkenheid bij lupus zeldzaam is, worden abnormale leverfunctietesten bij APS frequent gezien. Hoewel deze een voorbode kunnen zijn van ernstige levertrombose, zoals het syndroom van Budd-Chiari of het HELLP-syndroom bij zwangerschap dat waarschuwt voor dreigende catastrofale APS, hebben ze vaker een meer goedaardige prognose.35,36
Een zeer positieve anamnese: In het begin van de jaren 1980 zag ik een tienermeisje met een DVT, positieve aPL en Budd-Chiari syndroom.
Prognose slecht?
Meer dan dertig jaar later is ze nog steeds gezond op een zorgvuldige levenslange behandeling met warfarine, beheerd door haar artsen in Portugal.
De ziekte van Goldblatt, de nier & APS-Renale slagadervernauwing, gezien op een duidelijke achtergrond van verder normale slagaders, kan Goldblatt’s vroege waarnemingen over de ontwikkeling van hypertensie bij dieren met experimenteel afgesloten nierslagaders nabootsen. De ontdekking door Sangle van gelokaliseerde laesies door stenose van de nierslagaders leidde tot gelijkaardige bevindingen in andere vaten, hetgeen theorieën opleverde over gelokaliseerde trombotische/endotheliale pathologie.37
Huid: livedo reticularis, een enigma-Hoewel huidzweren, verwijde aders en subunguale splinterbloedingen bekende gevolgen zijn van huidtrombose bij APS, heeft livedo reticularis een aura van mysterie.38,39
Diagnostisch gezien is de aanwezigheid ervan een belangrijke aanwijzing bij patiënten die verdacht worden van het Hughes syndroom – inclusief seronegatieve APS.
Terugkijkend op enkele van de aandoeningen die in dit artikel zijn genoemd – MS, migraine, meervoudige fracturen, geheugenproblemen – kun je je bijvoorbeeld afvragen of het zorgvuldig noteren van de aan- of afwezigheid van livedo van betekenis zou kunnen blijken bij de differentiële diagnose van deze aandoeningen.
Eén ding is zeker: De aanwezigheid van livedo voegt een extra dimensie toe aan de ernst van het klinische beeld.
Zwangerschap
Het hoofdverhaal van het syndroom is natuurlijk in de zwangerschap, waar het succespercentage van gezonde bevallingen in aPL-positieve zwangerschappen is gestegen van minder dan 15% tot meer dan 90%. Zonder twijfel is de diagnose en behandeling van deze gevallen een belangrijke vooruitgang geweest in de wereld van de verloskunde.40
Treurig genoeg hebben wij allen die met APS werken, aPL-positieve patiënten verzorgd (van wie sommigen vroeg miskramen hadden gehad) die laat in de zwangerschap een baby verloren. Doodgeboorte.
Twee jaar geleden publiceerde The Times of London een hoofdartikel met de titel, “The Stillbirth Scandal,” waarin de aandacht werd gevestigd op de slechte doodgeboortecijfers in het V.K.41 Toch hadden sommige gevallen van doodgeboorte bij de aPL-positieve vrouwen voorkomen kunnen worden. Zo bleek uit een recente studie uit Utah dat bij aPL-zwangerschappen de kans op doodgeboorte drie- tot vijfmaal zo groot was.42
Zouden meer routinematige aPL-tests tijdens de zwangerschap helpen? Kostenoverwegingen zijn van toepassing. Miskramen komen vaak voor, en er zijn talrijke oorzaken. De huidige aanbeveling is dan ook om alleen vrouwen met drie of meer miskramen te testen. Dit lijkt hard. Misschien kan een eenvoudige screening helpen.
Ik heb voorgesteld dat een deel van de eerste screening door de verloskundige of gynaecoloog een eenvoudige vragenlijst in drie delen zou moeten omvatten:
- Heeft u een trombose gehad?
- Lijdt u aan migraine?
- Heeft u een familiegeschiedenis van auto-immuunziekten (d.w.z., lupus, RA, multiple sclerose, schildklierziekte)?
Ik ben er zeker van dat zo’n eenvoudige vragenlijst kan helpen bij het identificeren van een kleine risicogroep.
In de meeste centra is er, zodra moeder en baby veilig naar huis zijn gestuurd, geen follow-up meer op lange termijn. Maar vaak geven APS-patiënten die zich op, laten we zeggen, 40-jarige leeftijd melden met een trombotisch probleem, een voorgeschiedenis van een miskraam 20 jaar eerder. In een ideale wereld verdienen vrouwen met recidiverende miskramen een regelmatige follow-up op lange termijn. Maar de wereld is verre van ideaal.
Lupus & APS
De vroege klinische studies van APS werden uitgevoerd in lupusklinieken, en zouden heel goed “lupuskenmerken” hebben kunnen omvatten. Misschien verrassend, heeft de tijd weinig verschil aangetoond tussen primaire APS en de APS geassocieerd met lupus. Er zijn ongetwijfeld enkele klassieke kenmerken van lupus (b.v. Libman Sachs endocarditis, beroerte, toevallen) die waarschijnlijker aPL-gerelateerd zijn. Het lijkt ook waarschijnlijk dat aPL positiviteit bij lupus een hogere chroniciteitsindex verleent.
Het verstrijken van de tijd heeft ook een positieve bevinding aan het licht gebracht: Het is zeer ongebruikelijk dat patiënten met primaire APS op latere leeftijd lupus ontwikkelen.
De grote 3
De associatie tussen het syndroom van Hughes, Sjögren’s en hypothyreoïdie komt zo vaak voor dat ik ze de grote 3 ben gaan noemen. Klinisch is het een belangrijke associatie omdat de klinische symptomen van de drie aandoeningen – vermoeidheid, koude bloedsomloop, pijnen en evenwichts- en geheugenproblemen – bij alle drie voorkomen. Op dezelfde manier worden veel van deze patiënten belast met het label fibromyalgie.
Elk van de drie onderling samenhangende syndromen kan goed reageren op behandeling-bijvoorbeeld, de klinische Sjögren’s op hydroxychloroquine en ga zo maar door. Veel van deze patiënten zijn op mijn twee bomen behandeling-wilg (aspirine) en cinchona (kinine).
Seronegatieve APS
Ik geloof dat een van de voordelen van de tijd van een arts in opleiding doorgebracht in het lab is de erkenning dat veel laboratoriumtests zijn open voor variatie. Vele, vele studies hebben getracht het belang van titer, immunoglobuline klasse, drievoudige of dubbele positiviteit, relevantie van “andere” aPL zoals anti-fosfatidyl-serine enz.43,44
In het algemeen hebben al deze testen relevantie, maar in de kliniek passen sommige niet, zoals die patiënten met alle klinische kenmerken van APS bij wie de aPL testen hardnekkig negatief blijven.
Enkele jaren geleden schreven we een artikel waarin we de term seronegatieve APS introduceerden, waarmee we de aandacht vestigden op patiënten met sterke klinische kenmerken van APS maar met negatieve tests.45 Het concept gaat terug op de begindagen van seronegatieve RA en seronegatieve lupus – beide labels waren weliswaar gebaseerd op klinische waarneming alleen, maar hadden belangrijke therapeutische en prognostische consequenties.
Drie mogelijke verklaringen voor seronegatieve APS zijn: 1) de diagnose is onjuist (onwaarschijnlijk in alle gevallen); 2) de voorheen positieve testen zijn in de loop van de tijd negatief geworden (in mijn ervaring ongebruikelijk); of 3) er zijn nieuwe testen nodig.46
Misschien wel de krachtigste reden voor ruimdenkendheid over seronegatieve APS komt uit familiestudies. Een paar weken geleden zag ik een eeneiige tweeling – de eerste met klassieke seropositieve APS, die later haar (absoluut) eeneiige tweelingzus meebracht. De tweede tweeling had identieke sets van symptomen, maar in tegenstelling tot de eerste tweeling, had zij negatieve aPL testen. Beide patiënten reageerden op de behandeling.
Eenmaal per jaar houden wij een patiënten bijeenkomst in ons ziekenhuis. Op de laatste bijeenkomst hebben we een eenvoudige anonieme vragenlijst geregeld met twee vragen: Bent u een patiënt met APS of een vriend/echtgenote? Heeft u naaste vrouwelijke familieleden (zus, moeder, tante) met een auto-immuunziekte (d.w.z. lupus, RA, schildklier, multiple sclerose, APS)? Het resultaat: Zestig procent van de patiënten had een positieve geschiedenis van auto-immuunziekten bij naaste familieleden. Minder dan 20% van de vrienden/echtgenoten antwoordden positief.
Het kan zijn dat mijn eigen ervaring scheefgetrokken is door vooringenomenheid bij het doorverwijzen van families van APS patiënten – maar seropositief of niet, de meeste patiënten met seronegatieve APS reageren even goed op behandeling.
Als sommige van deze individuen in de familiestudie in feite seronegatieve APS hadden en toch potentieel ontvankelijk waren voor behandeling, dan zijn de mogelijkheden intrigerend. Misschien zou een hoger percentage van onze migraine-, jonge beroerte-, jonge angina-patiënten baat kunnen hebben bij een nadere beschouwing van meer van de aanwijzingen voor APS – de droge Schirmer’s, de livedo, de familiegeschiedenis van auto-immuunziekte bijvoorbeeld.
Behandelingsaspecten
In veel opzichten is het teleurstellend te moeten bekennen dat er 30 jaar na dato nog maar weinig nieuwe behandelingen zijn. De introductie van de nieuwe orale anticoagulantia bij de behandeling van APS is voorspelbaar voorzichtig geweest, en het is te vroeg om te generaliseren.47
Statines, IVIG en hydroxychlorquine zijn in de mix gegooid en, natuurlijk, anti-B cel therapie heeft gunstige anekdotes gekregen. Een recente studie uit Parijs suggereerde dat sirolimus, gebruikt bij niertransplantatie, een beschermend effect zou kunnen hebben op aPL-geïnduceerde vasculopathie.48
In 2016 is de huidige behandeling van APS dus nog steeds grotendeels beperkt tot aspirine, clopidogrel, heparine en warfarine.
Lage dosis aspirine is, ondanks de tegenstanders ervan, natuurlijk eerste keus bij veel APS-patiënten. Clopidogrel blijft echter een nuttig alternatief bij patiënten met gastritis of bij astmapatiënten. Maar er is nog een derde rol voor clopidogrel – belangrijk in de echte wereld van de praktische geneeskunde – namelijk bij die patiënten die, om welke reden dan ook, aspirine hebben geprobeerd, zonder duidelijk voordeel.
Heparine-Laag moleculair gewicht heparine heeft, in de meeste landen, de oude heparine grotendeels vervangen, en daarmee is de vrees voor trombocytopenie en osteoporose grotendeels verdwenen. Dit is een belangrijk punt om te maken, omdat veel artsen terughoudend zijn met het verlengen van het gebruik van heparine.
Twee observaties: Ten eerste, een aantal patiënten verbetert dramatisch op heparine, om zich vervolgens minder goed te voelen op warfarine.
Waar nu naar toe? Wanneer doseringsproblemen, warfarineresistentie en therapietrouw (hopelijk) zijn uitgesloten, is een onmiddellijke optie een tijdelijke terugkeer naar heparine. In sommige gevallen is tijdelijk veranderd in semi-langdurig. In onze APS kliniek hebben we een paar dozijn van zulke patiënten die, uit vrije wil, twee jaar of langer op subcutane heparine zijn gebleven. Ja, zij hebben blauwe plekken gekregen, maar tot nu toe hebben wij geen verslechtering van de DEXA scans gezien.
De tweede (en zeer klinische) observatie betreft een heparine proef. Het is een regelmatige waarneming dat aPL/APS-patiënten die tijdens de zwangerschap heparine krijgen, vaak gedurende de volle acht of negen maanden hoofdpijnvrij zijn. Dit heeft ons ertoe gebracht een klinisch instrument te ontwikkelen – een therapeutische proef – dat ons goed van pas is gekomen. De proef bestaat uit een LMW heparinekuur van drie of vier weken.49
Laat me een voorbeeld geven van het gebruik ervan: Bij de aPL/APS-patiënt met steeds ernstiger hoofdpijn ondanks aspirine/clopidogrel (en met een normale hersen-MRI), kan een proef van 10.000 eenheden dalteparine (of enoxaparine) gedurende drie of vier weken aanzienlijke resultaten opleveren. Ten eerste kan het een verrassend duidelijke indicatie geven of antistolling de juiste weg is. Ten tweede kan het bij de getraumatiseerde patiënt die de bekende weg van meerdere consulten bij specialisten heeft afgelegd, met marginaal klinisch succes, een belangrijk keerpunt zijn – het eerste voelbare teken van verbetering.
Warfarine – Over warfarine valt weinig nieuws te zeggen. Het is door de media verguisd, maar het blijft een van de nuttigste medicijnen in ons arsenaal. Warfarine, om het eenvoudig te zeggen, beschermt tegen beroerte en hartaanval bij APS.
Er is al gewezen op de frequente noodzaak van een hogere INR bij vele APS patiënten – vooral bij die met neurologische kenmerken. Ik ben een sterk voorstander van het gebruik van zelftestende INR machines waar mogelijk bij onze patiënten.
Helaas verzetten sommige antistollingsklinieken zich tegen het gebruik van zelftestende machines. Voor mij is dit verkeerd. Kijk naar de vrijheid die zelftesten voor insuline-afhankelijke diabetici heeft bereikt.
Als artsen geloof ik dat we de plicht hebben (totdat er betere, nieuwere antistollingsmiddelen komen) om warfarine te ondersteunen als een grotendeels veilig, effectief geneesmiddel dat vele duizenden levens heeft gered.
In 2015 is de huidige behandeling van het syndroom van Hughes nog steeds grotendeels beperkt tot aspirine, clopidogrel, heparine & warfarine.
Botbreuken
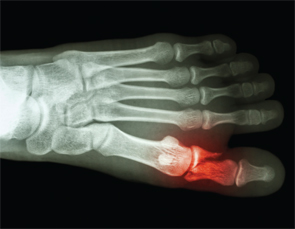
Spontane botbreuken worden goed herkend na het verslag van 27 spontane metatarsale fracturen door dr. Shirish Sangle bij APS-patiënten.
Image Credit: Puwadol Jaturawutthichai/.com
De familie- Het is geen verrassing dat een familiegeschiedenis een belangrijke aanwijzing is bij het syndroom van Hughes. Auto-immuunziekte (met name schildklier) duikt regelmatig op als diagnose bij familieleden van onze patiënten. Maar hoe vaak worden deze familiegevallen gediagnosticeerd? Voorbeelden zijn de 17-jarige dochter van een APS-patiënt die lijdt aan hoofdpijn en klierkoorts, de broer of zus met multiple sclerose of de moeder en tante van een pas gediagnosticeerde APS-patiënt die begin 40 een beroerte kregen.
Het is niet ondenkbaar dat APS de loop van de geschiedenis heeft veranderd, zoals in het geval dat mijn vriend, Dr. Gerald Weissmann, van Koningin Anne van Engeland, die 17 mislukte zwangerschappen had en kinderloos stierf, en daarmee een einde maakte aan het bewind van de Stuart’s en het begin inluidde van de Hannoveranen – met George III, de belastingen van de Amerikaanse kolonie, de revolutie en de geboorte van de V.S.50
De nakomelingen-Tot op heden hebben de meeste studies gesuggereerd dat de nakomelingen van aPL-positieve moeders geen grote nadelige gevolgen hebben (anders dan, misschien, het later ontwikkelen van overgeërfde APS kenmerken bij sommigen). Enkele verontrustende meldingen van foetale en neonatale problemen wijzen echter op een behoefte aan verder onderzoek. De lopende studies van Drs. Anne Parke, Angela Tincani, Maria Claire Boffa en anderen zullen mettertijd enkele van deze ontbrekende gegevens verschaffen.51,52
Classificatie vs. diagnose-
Geachte dokter, Ik zou het op prijs stellen als u mij over deze patiënte zou kunnen adviseren. Zij heeft trombose ontwikkeld bij gebruik van de orale anticonceptiepil. Zij heeft één positieve test gehad voor aPL, maar heeft 12 weken later geen herhalingstest gehad.
Zoals bij lupus worden indelingscriteria soms verward met diagnose. Veel patiënten komen niet gewapend met tests “12 weken na elkaar” (dit criterium werd ingevoerd om het risico te dekken dat een intercurrente infectie zou kunnen hebben geleid tot een voorbijgaande positieve aPL-test-niet een belangrijke factor in onze beoordeling van deze patiënt).
Er zijn ook financiële overwegingen, zoals in de volgende studie uit Beiroet, Libanon.
“Slechts 50,5% liet zowel aCL als LA testen. … De kosten van elke test bedroegen ongeveer 50 US$ voor de patiënt. … Het valt nog te bezien of de kosten van de test een gedeeltelijke verklaring vormen voor het zeer kleine percentage patiënten dat een bevestigende vervolgtest onderging.”
Het verstrijken van de tijd heeft ook een positieve bevinding opgeleverd: Het is zeer ongebruikelijk dat patiënten met primaire APS op latere leeftijd lupus ontwikkelen.
De erkenning van de vele niet-thrombotische manifestaties van APS heeft het belang van het scheiden van diagnose en classificatie nog groter gemaakt. Misschien zal de vooruitgang in het laboratorium bij het meten van potentiële risicomarkers ons mettertijd te hulp komen.44
Vliegangsangst-Deze klinische anekdote duikt regelmatig op in mijn kliniek. Zo vaak dat ik geloof dat het verder onderzocht moet worden. Een aantal van mijn APS patiënten, vooral voordat de behandeling is gestart, lijden ernstig aan een langdurige jetlag na een lange-afstandsvlucht, met vermoeidheid, hoofdpijn en verwardheid, soms dagenlang.
Interessant is dat, zodra de behandeling met heparine of warfarine met succes is begonnen, dit verschijnsel verdwijnt. Of deze symptomen verband houden met een lichte cerebrale hypoxie ten gevolge van een licht verlaagde cabinedruk is niet bekend. Niettemin zullen sommige van mijn patiënten met APS hun aspirinebehandeling vóór een langeafstandsvlucht aanvullen met een injectie van LMW heparine. Hoewel het placebo-effect aanzienlijk kan zijn, ben ik voldoende onder de indruk van de klinische ervaring van deze (oplettende) patiënten om te geloven dat het fenomeen van langdurige jetlag bij veel van onze patiënten zeer reëel is.
De toekomst-Tijdens het 14e Internationale Congres over Antifosfolipide Antilichamen dat in 2013 in Rio de Janeiro werd gehouden, werd mij gevraagd naar mijn voorspellingen over de toekomst van APS.23 Samengevat geloof ik dat:
- aPL-testen zullen wereldwijd en routinematig worden;
- Over-the-counter aPL-testkits zullen beschikbaar komen;
- Een substantiële subset van migrainelijders zal nieuwe hoop hebben;
- APS zal worden erkend als het belangrijkste verband tussen migraine en beroerte;
- Hartaanvallen bij jonge vrouwen (vooral onder de 45) zullen afnemen;
- Strokes bij mensen onder de 45 zullen afnemen;
- Sommige gevallen van versnelde aderverkalking zullen worden herkend als geassocieerd met (onbehandelde) aPL;
- Sommige gevallen van geheugenverlies zijn behandelbaar;
- APS zal een diepgaand effect blijven hebben op onze klinische beoordeling en behandeling van lupus; en
- Ten slotte, om op het openingsthema terug te komen, het aantal doodgeborenen zal afnemen, gedeeltelijk dankzij een meer pro-actieve benadering van aPL-testen tijdens de zwangerschap.
Om een zin uit het artikel van 1983 te herhalen:1
Voor degenen onder ons die gehard zijn in nihilisme door jaren van studie van verschillende auto-antilichamen bij SLE, is er een zeldzaam gevoel van opwinding over de implicaties van de associaties die nu gerapporteerd worden.
Dertig jaar later is die klinische opwinding nog steeds onverminderd.
 Graham R.V. Hughes, MD, FRCP, is reumatoloog en hoofd van het Lupus Centrum in Londen. Hij volgde zijn opleiding in The London Hospital en werkte twee jaar in New York aan de invoering van de DNA-bindingstest, onder leiding van Dr. Charles Christian. In 1971 opende hij een gespecialiseerde kliniek in Londen, die zich uitsluitend met lupus en aanverwante ziekten bezighoudt. Hij is stichter en redacteur van het internationale tijdschrift, Lupus. In 1983 beschreef hij het antifosfolipidensyndroom en in 1991 werd hem voor dit werk de ILAR-prijs (wereldonderzoek) toegekend. Andere onderscheidingen zijn Doctor Honoris Causa aan de Universiteiten van Marseille en Barcelona, en Master van de ACR.
Graham R.V. Hughes, MD, FRCP, is reumatoloog en hoofd van het Lupus Centrum in Londen. Hij volgde zijn opleiding in The London Hospital en werkte twee jaar in New York aan de invoering van de DNA-bindingstest, onder leiding van Dr. Charles Christian. In 1971 opende hij een gespecialiseerde kliniek in Londen, die zich uitsluitend met lupus en aanverwante ziekten bezighoudt. Hij is stichter en redacteur van het internationale tijdschrift, Lupus. In 1983 beschreef hij het antifosfolipidensyndroom en in 1991 werd hem voor dit werk de ILAR-prijs (wereldonderzoek) toegekend. Andere onderscheidingen zijn Doctor Honoris Causa aan de Universiteiten van Marseille en Barcelona, en Master van de ACR.
- Hughes GR. Trombose, abortus, cerebrale ziekte, en het lupus anticoagulans. Br Med J (Clin Res Ed). 1983 Oct 15;287(6399):1088-1089.
- Harris EN, Gharavi AE, Boey ML, et al. Anticardiolipine in antilichamen: Detection by radioimmunoassay and association with thrombosis in SLE. Lancet. 1983 Nov 26;2(8361):1211-1214.
- Boey ML, Colaco CB, Gharavi AE, et al. Thrombosis in SLE: Striking association with the presence of circulating lupus anticoagulant. Br Med J (Clin Res Ed). 1983 Oct 8;287:1021-1023.
- Hughes GR. De Prosser White oratie 1983: Bindweefselziekten en de huid. Clin Exp Dermatol. 1984 Nov;9(6):535-544.
- Asherson RA, Mackworth-Young CG, Boey ML, Hughes GRV. Pulmonary hypertension in systemic lupus erythematosus. Br Med J (Clin Res Ed). 1983 Oct 8;287(6398):1024-1025.
- Derue GJ, Englert HJ, Harris EN, et al. Foetal loss in systemic lupus: Associatie met anticardiolipine antilichamen. J Obstet Gynaecol. 1985;5(4):207-209.
- Hughes GR, Harris NN, Gharavi AE. Het anticardiolipinesyndroom. J Rheumatol. 1986 Jun;13(3):486-489.
- Hughes GR. Het syndroom van Hughes: Het anticardiolipinesyndroom. Een historische kijk. Lupus. 1998;7 Suppl 2:S1-S4.
- Carecchio M, Cantello R, Comi C. Revisiting the molecular mechanism in antiphospholipid syndrome: Beyond vascular damage. J Immunol Res. 2014;2014:239398.
- Bluestein HG, Zvaifler NJ. Brain-reactive lymphocytotoxic antibodies in the serum of patients with SLE. J Clin Invest. 1976 Feb;57(2):509-516.
- Bresnihan B, Oliver N, Grigor R, Hughes GR. Brain-reactivity of lymphocytotoxic anitibodies in systemic lupus erythematosus with and without cerebral involvement. Clin Exp Immunol. 1977 Dec;30(3):333-337.
- Bresnihan B, Hohmeister R, Cutting J, et al. The neuropsychiatric disorder in SLE: Evidence for both vascular and immune mechanisms. Ann Rheum Dis. 1979 Aug;38(4):301-306.
- Denburg SD, Behmann SA, Carbotte RM, et al. Lymfocytenantigenen in neuropsychiatrische systemische lupus erythematosus. Relationship of lymphocyte antibody specificities to clinical disease. Arthritis Rheum. 1994 Mar;37(3):369-375.
- Harris EN, Gharavi AE, Asherson RA, et al. Cerebral infarction in SLE. Associatie met anticardiolipine antilichamen. Clin Exp Rheumatol. 1984 Jan-Mar;2(1):47-51.
- Navarrete MG, Brey RL, Levine SR. “Cerebral disease in the antiphospholipid syndrome” in Hughes Syndrome-Antiphospholipid Syndrome. Khamashta MA, ed. Springer, London: 2000.
- Sanna G, Bertolaccini ML, Cuadrado MJ, et al. Central nervous system involvement in the antiphospholipid (Hughes) syndrome. Rheumatology (Oxford). 2003 Feb;42(2):200-213.
- Etminan M, Takkouche B, Isorna FC, Samii A. Risk of ischaemic stroke in people with migraine: Systemic review and meta-analysis of observational studies. BMJ. 2005 Jan 8;330(7482):63.
- Nencini P, Baruffi MC, Abbate R, et al. Lupus anticoagulant en anticardiolipine antilichamen in jonge volwassenen met cerebrale ischemie. Stroke. 1992 Feb;23(2):189-193.
- Hughes GR. Antifosfolipiden syndroom, migraine en beroerte. Lupus. 2010 Apr;19(5):555-556.
- Mackworth-Young CG, Hughes GR. Epilepsie: Een vroeg symptoom van systemische lupus erythematosus. J Neurol Neurosurg Psychiatry. 1985 Feb;48(2):185.
- Cimaz R, Meroni PL, Shoenfeld Y. Epilepsie als onderdeel van systemische lupus erythematosus en systemisch antifosfolipiden syndroom (Hughes syndroom). Lupus. 2006;15(4):191-194.
- Hughes GR. “Diplomatische epilepsie” in Understanding Hughes Syndrome. Springer-Verlag, Londen: 2009.
- Hughes GR. Het syndroom van Hughes/APS. 30 jaar later, wat hebben we geleerd? Openingstoespraak op het 14e internationale congres over antifosfolipide antilichamen. Rio de Janeiro, oktober 2013. Lupus. 2014;23:400-406.
- Cuadrado MJ, Khamashta MA, Ballesteros A, et al. Kunnen neurologische manifestaties van het Hughes (antifosfolipiden) syndroom worden onderscheiden van multiple sclerose? Analyse van 27 patiënten en overzicht van de literatuur. Geneeskunde (Baltimore). 2000 Jan;79(1):57-68.
- Hughes GR. Migraine, geheugenverlies, en “multiple sclerose.” Neurologische kenmerken van het antifosfolipiden (Hughes’) syndroom. Postgrad Med J. 2003 Feb;79(928):81-83.
- Uthman I, Noureldine MH, Berjawi A, et al. Hughes syndroom en multiple sclerose. Lupus. 2015 Feb;24(2):115-121.
- Cervera R, Asherson RA, Font J, et al. Chorea in het antifosfolipidensyndroom. Klinische, radiologische en immunologische karakteristieken van 50 patiënten uit onze klinieken en de recente literatuur. Geneeskunde (Baltimore). 1997 May;76(3):203-212.
- Baizabal-Carvallo JF, Bonnet C, Jankovic J. Bewegingsstoornissen bij systemische lupus erythematosus en het antifosfolipidensyndroom. J Neural Transm (Wenen). 2013 Nov;120(11):1579-1589.
- Schofield JR, Blitshteyn S, Shoenfeld Y, et al. Postural tachycardia syndrome (POTS) and other autonomic disorders in antiphospholipid (Hughes) syndrome (APS). Lupus. 2014 Jun;23(7):697-702.
- Sangle S, D’Cruz DP, Khamashta MA, et al. Antiphospholipid antibodies, systemic lupus erythematosus, and non-traumatic metatarsal fractures. Ann Rheum Dis. 2004 Oct;63(10):1241-1243.
- Greco TP1, Conti-Kelly AM, Greco T Jr., et al. Newer antiphospholipid antibodies predict adverse outcomes in patients with acute coronary syndrome. Am J Clin Pathol. 2009 Oct;132(4):613-620.
- Urbanus RT, Siegerink B, Roest M, et al. Antiphospholipid antibodies and risk of myocardial infarction and ischaemic stroke in young women in the RATIO study: Een case-control studie. Lancet Neurol. 2009 Nov;8(11):998-1005.
- Nair S, Khamashta MA, Hughes GR. Syndroom X en syndroom van Hughes. Lupus. 2002;11(5):332.
- Sangle SR, Jan W, Lau IS, et al. Coeliac artery stenosis and antiphospholipid (Hughes) syndrome/antiphospholipid antibodies. Clin Exp Rheumatol. 2006 May-Jun;24(3):349.
- Mackworth-Young CG, Melia WM, Harris EN, et al. Het Budd-Chiari syndroom. Mogelijke pathogenetische rol van anti-fosfolipide antilichamen. J Hepatol. 1986;3(1):83-86.
- Hanouna G, Morel N, Le Thi Huong D, et al. Catastrophic antiphospholipid syndrome and pregnancy: Een ervaring van 13 gevallen. Rheumatology (Oxford). 2013 Sep;52(9):1635-1641.
- Sangle SR, D’Cruz DP, Jan W, et al. Renal artery stenosis in antiphospholipid syndrome (Hughes) and hypertension. Ann Rheum Dis. 2003 Oct;62(10):999-1002.
- Englert HJ, Loizou S, Derue GG, et al. Clinical and Immunological features of livedo reticularis in lupus. Am J Med. 1989 Oct;87(4):408-410.
- Sangle SR, D’Cruz DP. Livedo reticularis: Een enigma. Isr Med Assoc J. 2015 Feb;17(2):104-107.
- Ateka-Barrutia O, Khamashta MA. De uitdaging van zwangerschap voor patiënten met SLE. Lupus. 2013 Oct;22(12):1295-1308.
- Hughes GR. Het doodgeboorteschandaal. Lupus. 2013 Jul;22(8):759-760.
- Silver RM, Parker CB, Reddy UM, et al. Antiphospholipid antibodies in stillbirth. Obstet Gynecol. 2013 Sep;122(3):641-657.
- Rodriguez-Garcia JL, Bertolaccini ML, Cuadrado MJ, et al. Clinical manifestations of antiphospholipid syndrome (APS) with and without antiphospholipid antibodies (the so-called ‘seronegative APS’). Ann Rheum Dis. 2012 Feb;71(2):242-244.
- Meroni PL, Chighizab CB, Rovelli F, et al. Antifosfolipidensyndroom in 2014: Meer klinische manifestaties, nieuwe pathogene spelers en opkomende biomarkers. Arthritis Res Ther. 2014;16(2):209.
- Hughes GR, Khamashta MA. Seronegatief antifosfolipidensyndroom. Ann Rheum Dis. 2003 Dec;62(12):1127.
- Rodguez-Garcia JL, Bertolaccini ML, Cuadrado MJ, et al. Clinical manifestations of antiphospholipid syndrome (APS) with and without antiphospholipid antibodies. Ann Rheum Dis. 2012 Feb;71(2):242-244.
- Giles I, Khamashta M, D’Cruz D, et al. A new dawn of anticoagulation for patients with antiphospholipid syndrome. Lupus. 2012 Oct;21(12):1263-1265.
- Canuad G, Bienaimé C, Taborin F, et al. Inhibitie van de mTORC pathway in het antifosfolipidensyndroom. New Eng J Med. 2014 Jul 24;371(4):303-312.
- Hughes GR. Heparine, antifosfolipide antistoffen en de hersenen. Lupus. 2012 Sep;21(10):1039-1040.
- Weissmann G. Queen Anne’s lupus: Fosfolipiden en het verloop van het rijk. FASEB J. 2014 Apr;28(4):1527-1530.
- Mekinian A, Lachassinne E, Nicaise-Roland P, et al. European registry of babies born to mothers with antiphospholipid syndrome. Ann Rheum Dis. 2013 Feb;72(2):217-222.
- Nalli C, Iodice A, Andreoti L, et al. Kinderen geboren uit SLE en APS moeders. Lupus. 2014 Oct;23(12):1246-1248.
- Major S, Pashayan N, Atweh S, et al. Praktijkpatronen van het antifosfolipidensyndroom in een tertiair opleidingsziekenhuis in Libanon. Lupus. 2002;11(11):759–764.