Generischer Name: Lidocainhydrochlorid
Dosierungsform: orale Lösung
Rx only
Ein topisches Anästhetikum für die Schleimhäute des Mundes und Rachens.
Nach dem Inverkehrbringen wurde über Fälle von Krampfanfällen, Herz-Lungen-Stillstand und Tod bei Patienten unter 3 Jahren berichtet, wenn Lidocain Viscous 2% nicht unter strikter Einhaltung der Dosierungs- und Anwendungsempfehlungen verabreicht wurde. Bei Zahnungsschmerzen sollte Lidocain Viscous 2% generell nicht angewendet werden. Bei anderen Erkrankungen sollte die Anwendung des Arzneimittels bei Patienten unter 3 Jahren auf die Fälle beschränkt werden, in denen sicherere Alternativen nicht zur Verfügung stehen oder bereits ausprobiert wurden, aber nicht erfolgreich waren.
Um das Risiko von schwerwiegenden unerwünschten Ereignissen bei der Anwendung von Lidocain Viscous 2% zu verringern, weisen Sie das Pflegepersonal an, sich streng an die vorgeschriebene Dosis und Häufigkeit der Verabreichung zu halten und die verschreibungspflichtige Flasche sicher außerhalb der Reichweite von Kindern aufzubewahren.
- BESCHREIBUNG
- Lidocain Topische Lösung zum Einnehmen – Klinische Pharmakologie
- Wirkungsmechanismus
- Hämodynamik
- Pharmakokinetik und Metabolismus
- Indikationen und Anwendung von Lidocain Topical Oral Solution
- Kontraindikationen
- Warnhinweise
- Lebensbedrohliche und tödliche Ereignisse bei Säuglingen und Kleinkindern
- Methämoglobinämie
- Vorsichtsmaßnahmen
- Informationen für Patienten
- Allgemeines
- Arzneimittelinteraktionen
- Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
- Schwangerschaft
- Stillende Mütter
- Anwendung bei Kindern
- Nebenwirkungen
- Zentralnervensystem
- Überdosierung
- Management von Lokalanästhetika-Notfällen
- DOSIERUNG UND ANWENDUNG
- Erwachsene
- Pädiatrie
- HOW SUPPLIED
- Packung/Etikettenanzeigetafel
- Packung/Etikettenanzeigetafel
BESCHREIBUNG
Lidocain Viscous 2% (Lidocainhydrochlorid orale topische Lösung USP) enthält ein Lokalanästhetikum und wird topisch verabreicht. Lidocain Viscous 2% (Lidocainhydrochlorid Oral Topical Solution USP) enthält Lidocainhydrochlorid, das chemisch als Acetamid, 2-(Diethylamino)-N-(2,6-dimethylphenyl)-, Monohydrochlorid bezeichnet wird und die folgende Strukturformel hat:
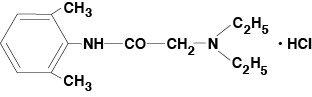
Die Summenformel von Lidocain ist C14H22N2O. Das Molekulargewicht beträgt 234,34.
Zusammensetzung der Lösung:
Jeder ml enthält 20 mg (2 %) Lidocainhydrochlorid USP und die folgenden inaktiven Bestandteile: Carboxymethylcellulose-Natrium, Aromastoffe, Methylparaben, Propylparaben, gereinigtes Wasser und Saccharin-Natrium.
Lidocain Topische Lösung zum Einnehmen – Klinische Pharmakologie
Wirkungsmechanismus
Lidocain stabilisiert die neuronale Membran durch Hemmung der Ionenflüsse, die für die Einleitung und Weiterleitung von Impulsen erforderlich sind, und bewirkt dadurch eine lokalanästhetische Wirkung.
Hämodynamik
Überhöhte Blutspiegel können Veränderungen des Herzzeitvolumens, des gesamten peripheren Widerstands und des mittleren arteriellen Drucks verursachen. Diese Veränderungen können auf eine direkte depressive Wirkung des Lokalanästhetikums auf verschiedene Komponenten des kardiovaskulären Systems zurückzuführen sein. Der Nettoeffekt ist normalerweise eine leichte Hypotonie, wenn die empfohlenen Dosierungen nicht überschritten werden.
Pharmakokinetik und Metabolismus
Lidocain wird nach örtlicher Verabreichung auf den Schleimhäuten absorbiert, wobei die Geschwindigkeit und das Ausmaß der Absorption von der Konzentration und der verabreichten Gesamtdosis, der spezifischen Applikationsstelle und der Dauer der Exposition abhängen. Im Allgemeinen erfolgt die Absorption von Lokalanästhetika nach örtlicher Anwendung am schnellsten nach intratrachealer Verabreichung. Lidocain wird auch aus dem Magen-Darm-Trakt gut resorbiert, aber aufgrund der Biotransformation in der Leber gelangt nur wenig intaktes Arzneimittel in den Kreislauf. Die Plasmabindung von Lidocain hängt von der Wirkstoffkonzentration ab, und die gebundene Fraktion nimmt mit steigender Konzentration ab. Bei Konzentrationen von 1 bis 4 mcg freier Base pro ml sind 60 bis 80 Prozent des Lidocains proteingebunden. Die Bindung hängt auch von der Plasmakonzentration des Alpha-1-Säure-Glykoproteins ab.
Lidocain überwindet die Blut-Hirn-Schranke und die Plazentaschranke, vermutlich durch passive Diffusion.
Lidocain wird in der Leber rasch metabolisiert, und die Metaboliten sowie das unveränderte Arzneimittel werden über die Nieren ausgeschieden. Die Biotransformation umfasst oxidative N-Dealkylierung, Ringhydroxylierung, Spaltung der Amidbindung und Konjugation. Die N-Dealkylierung, ein Hauptweg der Biotransformation, führt zu den Metaboliten Monoethylglycinexylidid und Glycinexylidid. Die pharmakologischen/toxikologischen Wirkungen dieser Metaboliten ähneln denen von Lidocain, sind aber weniger stark als diese. Ungefähr 90 % des verabreichten Lidocains werden in Form verschiedener Metaboliten ausgeschieden, weniger als 10 % werden unverändert ausgeschieden. Der Hauptmetabolit im Urin ist ein Konjugat von 4-Hydroxy-2,6-dimethylanilin.
Die Eliminationshalbwertszeit von Lidocain nach einer intravenösen Bolusinjektion beträgt typischerweise 1,5 bis 2 Stunden. Aufgrund der schnellen Metabolisierung von Lidocain kann jeder Zustand, der die Leberfunktion beeinträchtigt, die Kinetik von Lidocain verändern. Die Halbwertszeit kann sich bei Patienten mit Leberfunktionsstörungen um das Zweifache oder mehr verlängern. Nierenfunktionsstörungen haben keinen Einfluss auf die Lidocain-Kinetik, können aber die Akkumulation von Metaboliten erhöhen.
Faktoren wie Azidose und die Einnahme von ZNS-Stimulanzien und Depressiva beeinflussen die ZNS-Spiegel von Lidocain, die erforderlich sind, um sichtbare systemische Wirkungen hervorzurufen. Objektive unerwünschte Wirkungen werden mit zunehmenden venösen Plasmaspiegeln über 6 mcg freie Base pro ml immer deutlicher. Beim Rhesusaffen haben sich arterielle Blutspiegel von 18 bis 21 mcg/ml als Schwellenwert für konvulsive Aktivität erwiesen.
Indikationen und Anwendung von Lidocain Topical Oral Solution
Lidocain ist indiziert für die Herstellung einer topischen Anästhesie von gereizten oder entzündeten Schleimhäuten des Mundes und Rachens. Es ist auch nützlich, um das Würgen während der Aufnahme von Röntgenbildern und Zahnabdrücken zu reduzieren.
Kontraindikationen
Lidocain ist bei Patienten mit einer bekannten Überempfindlichkeit gegen Lokalanästhetika vom Amidtyp oder gegen andere Bestandteile der Lösung kontraindiziert.
Warnhinweise
Eine übermäßige Dosierung oder kurze Abstände zwischen den Dosen können zu hohen Plasmaspiegeln und schwerwiegenden unerwünschten Wirkungen führen. DIE PATIENTEN SOLLTEN ANGEWIESEN WERDEN, SICH STRIKT AN DIE EMPFOHLENEN DOSIERUNGS- UND VERABREICHUNGSRICHTLINIEN ZU HALTEN, WIE SIE IN DIESER PACKUNGSBEILAGE AUFGEFÜHRT SIND. DIE BEHANDLUNG SCHWERER UNERWÜNSCHTER REAKTIONEN KANN DEN EINSATZ VON ERSATZMITTELN, OXYGEN UND ANDEREN ERSATZMITTELN ERFORDERLICH MACHEN.
Lidocain sollte mit äußerster Vorsicht angewendet werden, wenn die Schleimhaut im Anwendungsgebiet traumatisiert ist, da unter solchen Bedingungen die Möglichkeit einer schnellen systemischen Resorption besteht.
Lebensbedrohliche und tödliche Ereignisse bei Säuglingen und Kleinkindern
Nach dem Inverkehrbringen wurde über Fälle von Krampfanfällen, Herz-Lungen-Stillstand und Tod bei Patienten unter 3 Jahren berichtet, wenn Lidocain Viscous 2% nicht unter strikter Einhaltung der Dosierungs- und Anwendungsempfehlungen verabreicht wurde. Bei Zahnungsschmerzen sollte Lidocain Viscous 2% generell nicht angewendet werden. Bei anderen Erkrankungen sollte die Anwendung des Arzneimittels bei Patienten unter 3 Jahren auf Situationen beschränkt werden, in denen sicherere Alternativen nicht zur Verfügung stehen oder versucht wurden, aber fehlgeschlagen sind.
Methämoglobinämie
Fälle von Methämoglobinämie wurden im Zusammenhang mit der Anwendung von Lokalanästhetika berichtet. Obwohl bei allen Patienten ein Risiko für Methämoglobinämie besteht, sind Patienten mit Glukose-6-Phosphat-Dehydrogenase-Mangel, angeborener oder idiopathischer Methämoglobinämie, Herz- oder Lungenproblemen, Säuglingen unter 6 Monaten und gleichzeitiger Exposition gegenüber Oxidationsmitteln oder deren Metaboliten anfälliger für die Entwicklung klinischer Manifestationen der Erkrankung. Wenn Lokalanästhetika bei diesen Patienten angewendet werden müssen, wird eine engmaschige Überwachung auf Symptome und Anzeichen einer Methämoglobinämie empfohlen.
Anzeichen einer Methämoglobinämie können sofort auftreten oder einige Stunden nach der Exposition verzögert werden und sind durch eine zyanotische Hautverfärbung und/oder eine anormale Färbung des Blutes gekennzeichnet. Die Methämoglobinwerte können weiter ansteigen; daher ist eine sofortige Behandlung erforderlich, um schwerwiegendere unerwünschte Wirkungen auf das zentrale Nervensystem und das Herz-Kreislauf-System, einschließlich Krampfanfällen, Koma, Herzrhythmusstörungen und Tod, abzuwenden. Setzen Sie Lidocain Viscous 2% und alle anderen Oxidationsmittel ab. Je nach Schwere der Anzeichen und Symptome können die Patienten auf eine unterstützende Behandlung ansprechen, z. B. Sauerstofftherapie, Flüssigkeitszufuhr. Ein schwereres klinisches Bild kann eine Behandlung mit Methylenblau, Austauschtransfusion oder hyperbarem Sauerstoff erfordern.
Vorsichtsmaßnahmen
Informationen für Patienten
Eltern und Betreuer sollten auf Folgendes hingewiesen werden:
– Bei Patienten unter 3 Jahren muss besonders darauf geachtet werden, dass die verordnete Dosis genau abgemessen wird und das Produkt nicht öfter als verordnet verabreicht wird. – Um die Genauigkeit zu gewährleisten, empfehlen wir Ihnen, ein Messgerät zu verwenden, um das richtige Volumen sorgfältig abzumessen. – Das Produkt sollte nur für die vorgeschriebene Indikation verwendet werden. – Um das Risiko eines versehentlichen Verschluckens zu verringern, sollte das Produktbehältnis fest verschlossen sein und das Produkt unmittelbar nach jeder Anwendung außerhalb der Reichweite von Kindern aufbewahrt werden. – Zeigt der Patient Anzeichen einer systemischen Toxizität (z. B. Lethargie, flache Atmung, Krampfanfälle), sollte sofort ein Arzt aufgesucht werden, und es sollte kein weiteres Produkt verabreicht werden. – Nicht verwendetes Produkt sollte so entsorgt werden, dass eine mögliche Exposition von Kindern und Haustieren vermieden wird.
Alle Patienten sollten sich darüber im Klaren sein, dass bei der Anwendung von Lokalanästhetika im Mund- oder Rachenraum die Erzeugung der Lokalanästhesie das Schlucken beeinträchtigen und somit die Gefahr der Aspiration erhöhen kann. Aus diesem Grund sollte nach der Anwendung von Lokalanästhetika im Mund- oder Rachenraum 60 Minuten lang keine Nahrung aufgenommen werden. Dies ist besonders wichtig bei Kindern, da sie häufig essen.
Eine Taubheit der Zunge oder der Wangenschleimhaut kann die Gefahr eines Beißtraumas erhöhen. Aus diesem Grund sollten keine Nahrungsmittel und/oder Kaugummi verwendet werden, während der Mund- oder Rachenraum betäubt ist.
Informieren Sie die Patienten darüber, dass die Anwendung von Lokalanästhetika eine Methämoglobinämie verursachen kann, einen ernsten Zustand, der umgehend behandelt werden muss. Weisen Sie Patienten oder Pflegepersonen darauf hin, sofort einen Arzt aufzusuchen, wenn bei ihnen oder einer ihnen anvertrauten Person folgende Anzeichen oder Symptome auftreten: blasse, graue oder blaue Haut (Zyanose), Kopfschmerzen, schneller Herzschlag, Kurzatmigkeit, Benommenheit oder Müdigkeit.
Allgemeines
Die Sicherheit und Wirksamkeit von Lidocain hängt von der richtigen Dosierung, der korrekten Technik, angemessenen Vorsichtsmaßnahmen und der Bereitschaft für Notfälle ab (siehe WARNHINWEISE und UNERWÜNSCHTE REAKTIONEN). Die niedrigste Dosierung, die zu einer wirksamen Anästhesie führt, sollte verwendet werden, um hohe Plasmaspiegel und schwerwiegende unerwünschte Wirkungen zu vermeiden. Wiederholte Gaben von Lidocain können aufgrund der langsamen Akkumulation des Arzneimittels und/oder seiner Metaboliten bei jeder wiederholten Gabe zu einem erheblichen Anstieg der Blutspiegel führen. Die Verträglichkeit hängt vom Zustand des Patienten ab. Geschwächte, ältere Patienten, akut kranke Patienten und Kinder sollten eine ihrem Alter, Gewicht und ihrer körperlichen Verfassung entsprechende, reduzierte Dosis erhalten. Lidocain sollte auch mit Vorsicht bei Patienten mit schwerem Schock oder Herzblock angewendet werden.
Lidocain sollte mit Vorsicht bei Personen mit bekannten Arzneimittelüberempfindlichkeiten angewendet werden. Bei Patienten, die auf Paraaminobenzoesäurederivate (Procain, Tetracain, Benzocain usw.) allergisch reagieren, wurde keine Kreuzsensitivität gegenüber Lidocain festgestellt.
Arzneimittelinteraktionen
Patienten, denen Lokalanästhetika verabreicht werden, haben ein erhöhtes Risiko, eine Methämoglobinämie zu entwickeln, wenn sie gleichzeitig den folgenden Arzneimitteln ausgesetzt sind, zu denen auch andere Lokalanästhetika gehören können:
Beispiele für Arzneimittel, die mit einer Methämoglobinämie assoziiert sind:
|
Klasse |
Beispiele |
|
Nitrate/Nitriten |
Nitroglycerin, Nitroprussid, Stickstoffoxid, Distickstoffoxid |
|
Lokalanästhetika |
Benzocain, Lidocain, Bupivacain, Mepivacain, Tetracain, Prilocain, Procain, Articain, Ropivacain |
|
Antineoplastische Mittel |
Cyclophosphamid, Flutamid, Rasburicase, Ifosfamid, Hydroxyharnstoff |
|
Antibiotika |
Dapson, Sulfonamide, Nitrofurantoin, Para-Aminosalicylsäure |
|
Antimalarials |
Chloroquin, Primaquin |
|
Antikonvulsiva |
Phenytoin, Natriumvalproat, Phenobarbital |
|
Andere Medikamente |
Acetaminophen, Metoclopramid, Sulfasalazin, Chinin |
Karzinogenese, Mutagenese, Beeinträchtigung der Fertilität
Tierversuche mit Lidocain zur Bewertung des karzinogenen und mutagenen Potentials oder der Auswirkungen auf die Fertilität wurden nicht durchgeführt.
Schwangerschaft
Teratogene Wirkungen
Schwangerschaft Kategorie B: Reproduktionsstudien wurden an Ratten mit Dosen bis zum 6,6-fachen der menschlichen Dosis durchgeführt und haben keine Hinweise auf eine Schädigung des Fötus durch Lidocain ergeben. Es gibt jedoch keine angemessenen und gut kontrollierten Studien an schwangeren Frauen. Da Reproduktionsstudien an Tieren nicht immer auf die Reaktion beim Menschen schließen lassen, sollte dieses Arzneimittel in der Schwangerschaft nur bei eindeutigem Bedarf angewendet werden.
Stillende Mütter
Es ist nicht bekannt, ob dieses Arzneimittel in die menschliche Milch ausgeschieden wird. Da viele Arzneimittel in die Muttermilch ausgeschieden werden, ist bei der Verabreichung von Lidocain an stillende Frauen Vorsicht geboten.
Anwendung bei Kindern
Die Dosierung bei Kindern sollte entsprechend dem Alter, dem Körpergewicht und der körperlichen Verfassung reduziert werden. Siehe ANWENDUNG UND VERABREICHUNG.
Nebenwirkungen
Nebenwirkungen nach der Verabreichung von Lidocain sind von ähnlicher Art wie bei anderen Amid-Lokalanästhetika. Diese unerwünschten Wirkungen sind im Allgemeinen dosisabhängig und können auf hohe Plasmaspiegel infolge einer übermäßigen Dosierung oder einer schnellen Resorption zurückzuführen sein oder auf eine Überempfindlichkeit, Idiosynkrasie oder verminderte Toleranz seitens des Patienten. Schwerwiegende unerwünschte Wirkungen sind im Allgemeinen systemischer Natur. Die folgenden Arten sind die am häufigsten berichteten:
Zentralnervensystem
Zentralnervensystem-Manifestationen sind erregend und/oder depressiv und können gekennzeichnet sein durch Benommenheit, Nervosität, Besorgnis, Euphorie, Verwirrung, Schwindel, Schläfrigkeit, Tinnitus, verschwommenes oder doppeltes Sehen, Erbrechen, Hitze-, Kälte- oder Taubheitsgefühle, Zuckungen, Zittern, Krämpfe, Bewusstlosigkeit, Atemdepression und Atemstillstand. Die Erregungserscheinungen können sehr kurz sein oder gar nicht auftreten; in diesem Fall kann die erste Erscheinung der Toxizität Schläfrigkeit sein, die in Bewusstlosigkeit und Atemstillstand übergeht.
Schläfrigkeit nach der Verabreichung von Lidocain ist in der Regel ein frühes Anzeichen für einen hohen Blutspiegel des Arzneimittels und kann als Folge einer schnellen Resorption auftreten.
Kardiovaskuläres System
Kardiovaskuläre Manifestationen sind in der Regel depressiv und zeichnen sich durch Bradykardie, Hypotonie und kardiovaskulären Kollaps aus, der zu Herzstillstand führen kann.
Allergisch
Allergische Reaktionen sind durch Hautläsionen, Urtikaria, Ödeme oder anaphylaktoide Reaktionen gekennzeichnet. Allergische Reaktionen können als Folge einer Überempfindlichkeit entweder gegenüber dem Lokalanästhetikum oder gegenüber dem in dieser Formulierung verwendeten Methylparaben und/oder Propylparaben auftreten. Allergische Reaktionen aufgrund einer Überempfindlichkeit gegenüber Lidocain sind äußerst selten und sollten, wenn sie auftreten, mit konventionellen Mitteln behandelt werden. Der Nachweis der Empfindlichkeit durch Hauttests ist von zweifelhaftem Wert.
Überdosierung
Akute Notfälle durch Lokalanästhetika stehen im Allgemeinen im Zusammenhang mit hohen Plasmaspiegeln, die bei der therapeutischen Anwendung von Lokalanästhetika auftreten. (Siehe UNERWÜNSCHTE REAKTIONEN, WARNHINWEISE und VORSICHTSMASSNAHMEN)
Management von Lokalanästhetika-Notfällen
Die erste Überlegung gilt der Vorbeugung, die am besten durch eine sorgfältige und ständige Überwachung der kardiovaskulären und respiratorischen Vitalzeichen und des Bewusstseinszustandes des Patienten nach jeder Lokalanästhetika-Verabreichung erreicht wird.
Der erste Schritt bei der Behandlung von Krämpfen besteht in der sofortigen Aufrechterhaltung eines freien Atemweges und einer assistierten oder kontrollierten Beatmung mit Sauerstoff. In Situationen, in denen geschultes Personal zur Verfügung steht, sollte die Beatmung aufrechterhalten und Sauerstoff durch ein System verabreicht werden, das einen sofortigen positiven Atemwegsdruck per Maske ermöglicht. Unmittelbar nach Einleitung dieser Beatmungsmaßnahmen sollte die Angemessenheit des Kreislaufs überprüft werden, wobei zu berücksichtigen ist, dass zur Behandlung von Krämpfen eingesetzte Medikamente bei intravenöser Verabreichung manchmal den Kreislauf beeinträchtigen. Sollten die Krämpfe trotz adäquater Atemunterstützung anhalten und der Zustand des Kreislaufs dies zulassen, können kleine Mengen eines ultrakurz wirksamen Barbiturats (wie Thiopental oder Thiamylal) oder eines Benzodiazepins (wie Diazepam) intravenös verabreicht werden. Der Kliniker sollte vor der Anwendung von Lokalanästhetika mit diesen krampflösenden Medikamenten vertraut sein. Die unterstützende Behandlung der Kreislaufdepression kann die Verabreichung von intravenöser Flüssigkeit und gegebenenfalls eines Vasopressors (z. B. Ephedrin) erfordern.
Wenn nicht sofort behandelt wird, können sowohl die Krämpfe als auch die Kreislaufdepression zu Hypoxie, Azidose, Bradykardie, Arrhythmien und Herzstillstand führen. Sollte es zu einem Herzstillstand kommen, sollten die üblichen kardiopulmonalen Wiederbelebungsmaßnahmen eingeleitet werden.
Dialyse ist bei der Behandlung einer akuten Überdosierung mit Lidocain von vernachlässigbarem Wert.
Die orale LD50 von Lidocain beträgt bei nicht nüchternen weiblichen Ratten 459 (346 bis 773) mg/kg (als Salz) und 214 (159 bis 324) mg/kg (als Salz) bei nüchternen weiblichen Ratten.
DOSIERUNG UND ANWENDUNG
Erwachsene
Die maximal empfohlene Einzeldosis von Lidocain für gesunde Erwachsene sollte so sein, dass die Lidocain-Dosis 4.5 mg/kg oder 2 mg/lb Körpergewicht und auf keinen Fall insgesamt 300 mg überschreitet.
Für die symptomatische Behandlung von gereizten oder entzündeten Schleimhäuten des Mundes und des Rachens beträgt die übliche Dosis für Erwachsene 15 ml unverdünnt. Bei der Anwendung im Mund sollte die Lösung im Mund herumgeschwenkt und ausgespuckt werden. Bei der Anwendung im Rachen sollte die unverdünnte Lösung gegurgelt werden und kann geschluckt werden. Diese Dosis sollte nicht in Abständen von weniger als drei Stunden verabreicht werden, und es sollten nicht mehr als acht Dosen in einem Zeitraum von 24 Stunden verabreicht werden. Die Dosierung sollte entsprechend dem Alter, dem Gewicht und der körperlichen Verfassung des Patienten angepasst werden (siehe VORSICHTSMASSNAHMEN).
Pädiatrie
Bei allen pädiatrischen Patienten muss auf eine korrekte Dosierung geachtet werden, da es Fälle von Überdosierung aufgrund unangemessener Dosierung gegeben hat.
Es ist schwierig, eine Höchstdosis für Kinder zu empfehlen, da diese in Abhängigkeit von Alter und Gewicht variiert. Bei Kindern über 3 Jahren, die eine normale fettfreie Körpermasse und eine normale Körperentwicklung haben, wird die Höchstdosis durch das Gewicht oder das Alter des Kindes bestimmt. Zum Beispiel: Bei einem Kind von 5 Jahren und einem Gewicht von 50 Pfund sollte die Lidocain-Dosis 75 bis 100 mg (3,7 bis 5 ml Lidocain) nicht überschreiten.
Bei Säuglingen und Kindern unter 3 Jahren sollte die Lösung genau abgemessen und nicht mehr als 1,2 ml mit einem Wattebausch auf die unmittelbare Umgebung aufgetragen werden. Warten Sie mindestens 3 Stunden, bevor Sie die nächste Dosis verabreichen; in einem Zeitraum von 12 Stunden dürfen maximal vier Dosen verabreicht werden. Lidocain sollte nur verwendet werden, wenn die zugrundeliegende Erkrankung eine Behandlung mit einem Produktvolumen von weniger als oder gleich 1,2 ml erfordert.
HOW SUPPLIED
Lidocain Viscous 2% (Lidocainhydrochlorid Oral Topical Solution USP)
Die 2%ige orale topische Lösung wird als klare, farblose, viskose Lösung geliefert.
NDC 0054-0548-44: Squeeze Bottle of 20 mL
NDC 0054-3500-49: Squeeze Bottle of 100 mL
Bei 20° bis 25°C (68° bis 77°F) lagern.
In einem kindersicheren Behälter gemäß USP/NF dispensieren.
Vor Gebrauch gut schütteln.
Vertrieben von: West-Ward
Pharmaceuticals Corp.
Eatontown, NJ 07724
Revised October 2018
Packung/Etikettenanzeigetafel
NDC 0054-3500-49 Lidocain Viscous (Lidocainhydrochlorid Oral Topical Solution USP) 100mL

Packung/Etikettenanzeigetafel
NDC 0054-0548-44 Lidocain viskos (Lidocainhydrochlorid orale topische Lösung USP) 15mL

| LIDOCAINE VISCOUS Lidocainhydrochlorid-Lösung |
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
| LIDOCAINE VISCOUS Lidocainhydrochlorid Lösung |
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
|
||||||||||||||
Etikettierer -. West-Ward Pharmaceuticals Corp. (080189610)
| Einrichtung | |||
| Name | Adresse | ID/FEI | Betriebe |
| West-Ward Columbus Inc. | 058839929 | HERSTELLUNG(0054-3500, 0054-0548) | |
Medizinischer Haftungsausschluss