Vorhofflimmern (AF) ist die häufigste anhaltende Tachyarrhythmie und tritt bei 1 bis 2 % der Allgemeinbevölkerung auf. Die Pulmonalvenenisolation (PVI) ist die wichtigste Methode zur Ablation von Vorhofflimmern.1 Obwohl dieses Verfahren bei Patienten mit paroxysmalem Vorhofflimmern das Wiederauftreten von Arrhythmien wirksam verhindert, ist es bei persistierendem Vorhofflimmern nur begrenzt erfolgreich.1,2 Erste Daten deuten darauf hin, dass das Wiederauftreten von Arrhythmien durch eine zusätzliche Leitungsablation oder eine komplexe fraktionierte Vorhofelektrogrammablation verringert werden könnte. Der Nutzen einer zusätzlichen Ablation über die PVI hinaus wurde jedoch durch die jüngsten Ergebnisse von Metaanalysen3 und randomisierten kontrollierten Studien4 nicht bestätigt, was die Bedeutung einer dauerhaften PVI auch bei persistierendem Vorhofflimmern unterstreicht.
In den letzten Jahren hat sich die Kryoballonablation zu einer praktikablen Alternative zur Radiofrequenz (RF)-Ablation entwickelt und sich bei Patienten mit paroxysmalem Vorhofflimmern als mindestens ebenso wirksam wie die PVI erwiesen. Die jüngsten Ergebnisse der FIRE & ICE-Studie haben die Debatte auf diesem Gebiet endgültig beigelegt.5 Darüber hinaus hat sich dieses Verfahren aufgrund seiner relativen Einfachheit, der schnelleren Lernkurve – und vielleicht noch wichtiger – der bemerkenswerten Reproduzierbarkeit6 in der klinischen Praxis durchgesetzt.6
Andererseits bleibt die interventionelle Behandlung von persistierendem Vorhofflimmern eine Herausforderung: Dieser Ansatz ist weder standardisiert noch perfektioniert worden, und es gibt Raum für Innovationen. In diesem Zusammenhang ist die Frage nach einer möglichen Rolle der Kryoablation interessant.
KLINISCHE BEWEISE
Obwohl das Interesse an der Wirksamkeit der Vorhofflimmerablation bei Patienten mit persistierendem Vorhofflimmern zunimmt, sind die Nachbeobachtungsdaten nach Verwendung des neuartigen 28-mm-Kryoballonkatheters der zweiten Generation (Arctic Front Advance, Medtronic Inc., Minneapolis, MN) noch begrenzt. Bislang wurden die Ergebnisse nach der Kryoballonablation bei persistierendem Vorhofflimmern indirekt durch Metaanalysen, nicht randomisierte Vergleiche7 und Beobachtungsstudien bewertet.8-10
Ciconte et al.9 berichteten, dass 60 % der Patienten mit persistierendem Vorhofflimmern nach der Behandlung mit dem neuen Kryoballonkatheter frei von atrialen Tachyarrhythmien waren. Die Dauer des persistierenden Vorhofflimmerns, die ein unabhängiger Prädiktor für das Wiederauftreten von Arrhythmien während der Nachbeobachtung war, spricht eindeutig für eine Ablation in früheren Stadien der Erkrankung.
In einer retrospektiven Studie mit 48 Patienten mit persistierendem Vorhofflimmern betrug die klinische Erfolgsrate nach einem Jahr 69 %.10
In einer weiteren einarmigen Studie wurde die Wirksamkeit der Kryoablation der zweiten Generation in einer Gruppe von 100 Patienten mit persistierendem Vorhofflimmern als Indexverfahren (mittlere Dauer 5,5 ± 3,7 Monate) untersucht.8 Nach einer mittleren Nachbeobachtungszeit von 10,6 ± 6,3 Monaten traten bei 67 % der Patienten nach einer dreimonatigen Austastphase keine erneuten Vorhoftachyarrhythmien auf. Der einzige signifikante unabhängige Prädiktor für ein Rezidiv war das Auftreten von Vorhoftachyarrhythmien während der Blanking-Periode.
In einer nicht-prospektiven, nicht-randomisierten Studie an einem einzigen Zentrum wurde die RF im Vergleich zur Kryoablation nur bei Patienten mit persistierendem Vorhofflimmern untersucht.7 In dieser Studie wurde das verfahrenstechnische Ergebnis der HF-Ablation (mit einem Kontaktkraft-Ablationskatheter) im Vergleich zur Kryoablation (mit dem 28-mm-Kryoballon der zweiten Generation) bei einer Kohorte von 100 Patienten mit medikamentenrefraktärem persistierendem Vorhofflimmern untersucht (die mittlere Dauer des Vorhofflimmerns betrug 7,2 bzw. 7,6 Monate in der HF-Ablations- und Kryoablationsgruppe). Sowohl die Verfahrens- als auch die Durchleuchtungszeiten waren in der Kryoablationsgruppe signifikant kürzer, aber die Rate der Patienten, die nach 12 Monaten Nachbeobachtung frei von Vorhofarrhythmien waren, war in beiden Gruppen ähnlich (60 % in der Kryoablations- gegenüber 56 % in der HF-Ablationsgruppe, P = .71). Eine multivariate Analyse ergab, dass die einzigen unabhängigen Prädiktoren für ein Scheitern die Dauer des persistierenden Vorhofflimmerns und das Auftreten von Rezidiven während der Blanking-Phase waren.
Schließlich wurden in einer prospektiven, multizentrischen, nicht randomisierten Studie die Ergebnisse nach einem einzigen Ablationsverfahren verglichen, bei dem die Kryoballonablation der ersten Generation nur zur PVI im Vergleich zur offenen HF-Ablation durch einen schrittweisen Ansatz in einer Kohorte von Patienten mit persistierendem Vorhofflimmern eingesetzt wurde.11 Die Ergebnisse, die bei einer mittleren Nachbeobachtungszeit von 15,6 ± 11,5 Monaten nach einer einzigen Ablation sowohl mit dem Kryoballon als auch mit RF eine Freiheit von Vorhofarrhythmien von etwa 55 % zeigten, entsprachen den verfügbaren Daten. Mehrere Ergebnisse waren bemerkenswert:
- –
Erstens waren die klinischen Ergebnisse in den beiden Behandlungsgruppen ähnlich, obwohl in der RF-Gruppe eine zusätzliche und umfangreichere Ablation über die PVI hinaus durchgeführt wurde.
- –
Zweitens war die Komplikationsrate bei beiden Techniken ähnlich.
- –
Drittens war die Verfahrensdauer bei der Kryoablation kürzer.
Es besteht nach wie vor Unklarheit über die Pathophysiologie und die optimale Strategie für die Ablation von persistierendem Vorhofflimmern, und daher bleibt das Erreichen einer dauerhaften PVI der Hauptpfeiler dieser Therapie.4 Um dies zu erreichen, scheint die Kryoablation eine valide therapeutische Alternative zur RF zu sein. Die Durchführung einer zusätzlichen Ablation zusätzlich zur PVI ist mit einer längeren Verfahrensdauer verbunden.4 Da der RF-Ablationsansatz nicht standardisiert wurde (die meisten Patienten im RF-Arm entwickelten zusätzliche Läsionen), ist unklar, ob die Ergebnisse auf die Energiequelle oder die Ablationsstrategie zurückzuführen sind. Darüber hinaus scheinen die mittelfristigen Ergebnisse bei Patienten mit persistierendem Vorhofflimmern durch zusätzliche biatriale Läsionen, die über die PVI hinausgehen, nicht signifikant verbessert zu werden.4
SHOOTING AT THE RIGHT TARGET?
Die Gründe für das Ausbleiben eines erhöhten Nutzens durch zusätzliche Ablation müssen noch geklärt werden. Eine Möglichkeit ist das iatrogene Potenzial eines Substratansatzes mit umfangreicherer Ablation, der die Entwicklung neuer Bereiche der Arrhythmogenese aufgrund von unvollständig ablatiertem Gewebe oder unvollständigen Leitungsblocklinien begünstigen kann. Eine andere Möglichkeit besteht darin, dass das schuldige Gebiet nicht routinemäßig identifiziert wird und weder komplexe fraktionierte Vorhofelektrogramme noch lineare Läsionen die optimalen ergänzenden Ziele für die Ablation sind.12 Bei dieser Hypothese besteht weiterhin die Notwendigkeit, das Auge des Sturms zu lokalisieren (indem Rotoren oder Ganglien ins Visier genommen werden),13 möglicherweise durch den Einsatz neuerer Mapping-Algorithmen. Die vorliegenden Daten stützen auch die Rolle der Vorhofflimmerdauer und folglich des elektrischen Vorhofflimmer-Remodeling (Vorhofflimmern erzeugt Vorhofflimmern), denn nur die Vorhofflimmerdauer war ein unabhängiger Prädiktor für das Wiederauftreten von Arrhythmien im Propensity-Score-Vergleich11 , wie zuvor von Tilz et al.2
berichtet wurde.2
Mehrere laufende Studien werden dazu beitragen, die Sicherheit und Wirksamkeit der Kryoablation bei Patienten mit persistierendem Vorhofflimmern zu klären. Bei der Studie Cryoballoon Ablation for Early Persistent Atrial Fibrillation (Cryo4 Persistent AF – NCT02213731) handelt es sich um eine europäische multizentrische, prospektive, einarmige Pilotstudie, die darauf abzielt, die Erfolgsrate der PVI nur durch Kryoablation nach einem Jahr bei Patienten mit persistierendem Vorhofflimmern zu bewerten, das seit weniger als 12 Monaten besteht. Diese Studie befindet sich noch in der Rekrutierungsphase und die ersten Ergebnisse werden für Ende 2017 erwartet. Das nächste Ziel ist der Vergleich der Ergebnisse in einer randomisierten Studie zwischen dem schrittweisen RF-Ansatz und der PVI-Kryoablation in einer homogenen Gruppe von Patienten mit persistierendem Vorhofflimmern. Die Ergebnisse dieser groß angelegten randomisierten Studie werden mit Spannung erwartet.
STÄRKEN UND GRENZEN
Bei Patienten mit persistierendem Vorhofflimmern liegen selbst die höchsten maximalen PV-Durchmesser (zwischen 20 mm und 23 mm) deutlich unter dem kritischen Wert von 28 mm (dem maximalen Durchmesser des in der klinischen Routine verwendeten Kryoballons).14 Aufgrund dieses Missverhältnisses zwischen den Durchmessern des Ballons und der PVs kommt der kühlende Teil des Geräts, wenn es am PV-Antrum positioniert wird, sowohl mit dem PV-Antrum als auch mit dem angrenzenden Vorhofgewebe in Kontakt, was ein wichtiger Vorteil dieses Verfahrens zu sein scheint. Kenigsberg et al.15 berechneten die Fläche des ablatierten Herzgewebes nach der PV-Kryoablation durch eine dreidimensionale elektroanatomische Spannungskartierung des linken Vorhofs nach der Kryoablation. Mit dieser Methode konnten diese Autoren sehr schön zeigen, dass nach der Kryoablation mit dem 28-mm-Kryoballongerät der Prozentsatz der linken Vorhofhinterwand, der elektrisch intakt blieb, nur 27 % betrug.
Auch wenn der Kryoballon konzeptionell nur auf die PVs abzielt, führt er auch zu einer erheblichen elektrischen Entlastung der Hinterwand des linken Vorhofs (Abbildung). Durch die Erweiterung des Umfangs des Kühlbereichs kann dieses Gerät einen kollateralen Nutzen bieten, indem es lokale Faktoren ablatiert, die zur Auslösung und Aufrechterhaltung von Vorhofflimmern beitragen, wie z. B. ganglionäre Plexi und Rotoren, was möglicherweise wichtige therapeutische Auswirkungen für Patienten mit persistierendem Vorhofflimmern hat.13 Dies könnte zumindest teilweise auch die Ergebnisse der oben genannten Studien erklären.
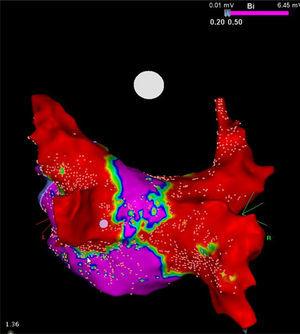
High-Density-Voltage-Map der Hinterwand nach einem Kryoablationseingriff bei einem Patienten mit persistierendem Vorhofflimmern. Man beachte den schmalen Korridor (lila), der zwischen den beiden großen Narben (rot) verbleibt, die mit dem 28-mm-Kryoballon Artic Front Advance (Medtronic, Minneapolis, MN, Vereinigte Staaten) erzeugt wurden. Mit freundlicher Genehmigung von Prof. Mario Oliveira, Santa Marta Hospital, Lissabon, Portugal.
Obwohl die Erfolgsraten der Kryoballontherapie in nicht randomisierten Studien mit Patienten mit persistierendem Vorhofflimmern mit denen der Hochfrequenztherapie vergleichbar sind, bleibt die relativ hohe Rate der Arrhythmierezidive in beiden Gruppen ungeklärt und könnte nicht nur auf die Erholung der Erregungsleitung in den PVs zurückzuführen sein. Diese Möglichkeit wurde in Studien erwähnt, in denen Bedenken geäußert wurden, ob nicht PV-fremde Quellen für das Rezidiv verantwortlich sind.9
Bei persistierendem Vorhofflimmern bleibt die invasive Behandlung aufgrund der vielfältigen Pathophysiologie schwierig. Neue mechanistische Erkenntnisse sind erforderlich, um einen individuell zugeschnittenen Ansatz bei persistierendem Vorhofflimmern zu ermöglichen, aber bis solche Erkenntnisse vorliegen, könnte eine alleinige PVI als erste Maßnahme ausreichend sein, zumindest für Patienten mit weniger schwerem persistierendem Vorhofflimmern. Auf der Grundlage dieses „weniger ist mehr“-Ansatzes könnte sich die Kryoballon-PVI als adäquate Ablationsstrategie bei persistierendem Vorhofflimmern erweisen, die eine zuverlässige PVI mit begleitendem Debulking des benachbarten Vorhofmyokards ermöglicht. Eine zusätzliche Substratmodifikation scheint keinen zusätzlichen Nutzen zu bringen. Dieses „minimalistische“ Verfahren ist eine akzeptable erste Option für Patienten mit relativ kurzem symptomatischem persistierendem Vorhofflimmern, d. h. mit „mehr Auslöser als Substrat“ (oder mit einem Substrat, das sich um die PVs-Ostien konzentriert…). Der große (28 mm) Kryoballon der zweiten Generation liefert in der Tat ähnliche Ergebnisse wie komplexere Verfahren mit HF-Energie und ausgefeilten Methoden. Bemerkenswert ist, dass die Lernkurve, die Reproduzierbarkeit und die Sicherheit für das Kryoballongerät in weniger erfahrenen Händen zu sprechen scheinen. In dieser Situation und bei der oben genannten Patientengruppe scheint die PVI mit dem großen Kryoballon der zweiten Generation ein vernünftiger erster Ansatz zu sein, der bei mehr als der Hälfte der Kandidaten eine signifikante Verbesserung bewirkt. Bei Patienten mit rezidivierendem Vorhofflimmern wird dieses erste Verfahren nicht nutzlos sein. Bei einem beträchtlichen Teil des bereits behandelten Substrats (rund um die rechte und linke PV-Antra) wird sich das zweite Verfahren, diesmal mittels RF, hauptsächlich auf Extra-PVs-Foci, fragmentierte Potenziale, Mikro- oder Makrorezidive usw. konzentrieren.
Unserer Meinung nach ist diese zweistufige Strategie mit dem Einsatz von Zentren mit geringem bis mittlerem Volumen vereinbar, die sich hauptsächlich auf PVIs konzentrieren und Hand in Hand mit tertiären Referenzzentren arbeiten, die die komplexeren Verfahren durchführen. Letztere werden sich mit den etwa 40 % der Patienten befassen müssen, bei denen es nach dem ersten „Kryo-Debulking“ zu einem Rezidiv kommt.
„Weniger ist mehr“, aber das ist noch nicht genug…
INTERESSENSKONFLIKTE
S. Boveda erhält Beratungshonorare von Medtronic, Boston Scientific und Livanova.