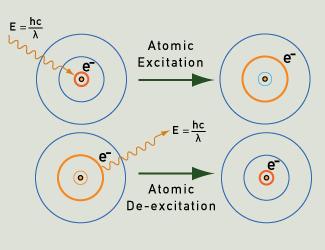
光は電子が励起されて基底状態に戻るときに放出されます。 それに比べて白熱は、高温の物体の温度に依存するピークを持つ連続的な光の帯を生成します。
ガスや蒸気の原子が、たとえば加熱したり電場をかけたりして励起されると、その電子は基底状態から高いエネルギーレベルに移動することができるようになります。 電子が基底状態に戻るとき、量子力学的な確率で明確に定義された経路をたどり、特定のエネルギーの光子を放出する。 このエネルギーが光の波長に対応するため、特定の色の光を発する。 834>

水素の線スペクトルの例。

ネオンの線スペクトル…各元素は正確に定義された線放出スペクトルを持っているので、科学者はそれらが作る炎の色で識別することができます。 たとえば、銅は青い炎、リチウムとストロンチウムは赤い炎、カルシウムはオレンジの炎、ナトリウムは黄色の炎、バリウムは緑の炎を出します。

この図は、特定の元素を燃やすことによって生じる独特の色を示しています。

酸素アセチレントーチの炎は3000℃以上で燃え、水中溶接に使えるほど高温です。
Flame
色からロウソクの炎の温度が分かります。 ろうそくの炎の内核は水色で、その温度は約1670K(1400℃)です。 それは炎の中で最も熱い部分です。 炎の内側の色は、黄色、オレンジ、そして最後に赤になります。 炎の中心から離れるほど、温度は低くなります。 赤い部分は1070K(800℃)あたりです。
炎の中のオレンジ、黄色、赤の色は色温度だけに関係しているのではありません。 ガスの励起も炎の色に大きな役割を果たす。 燃焼中の炎の主成分の1つは煤で、炭素化合物の複雑で多様な組成を持っている。 この炭素化合物の多様性により、電子が励起される量子状態が実質的に連続的に変化している。 そのため、電子が元の状態に戻るときに放出されるエネルギーによって、光の色が決まるのである
。