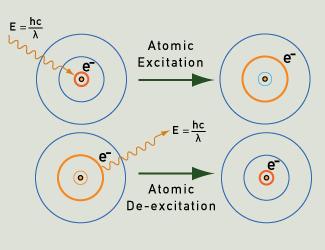
Lichtphotonen werden ausgesandt, wenn ein Elektron nach seiner Anregung in seinen Grundzustand zurückfällt.
Flammentests
Flammentests sind nützlich, weil Gasanregungen ein charakteristisches Linienemissionsspektrum für ein Element erzeugen. Im Vergleich dazu erzeugt die Glut ein kontinuierliches Lichtband mit einer Spitze, die von der Temperatur des heißen Objekts abhängt.
Wenn die Atome eines Gases oder Dampfes angeregt werden, zum Beispiel durch Erhitzen oder durch Anlegen eines elektrischen Feldes, können ihre Elektronen von ihrem Grundzustand auf höhere Energieniveaus übergehen. Bei ihrer Rückkehr in den Grundzustand senden sie auf klar definierten Wegen, die von Quantenwahrscheinlichkeiten abhängen, Photonen mit einer ganz bestimmten Energie aus. Diese Energie entspricht bestimmten Wellenlängen des Lichts, so dass bestimmte Lichtfarben entstehen. Jedes Element hat einen „Fingerabdruck“ in Form seines Linienemissionsspektrums, wie die folgenden Beispiele zeigen.

Linienspektrum für Wasserstoff.

Linienspektrum für Helium.

Linienspektrum für Neon.
Da jedes Element ein genau definiertes Linienemissionsspektrum hat, können Wissenschaftler sie anhand der Farbe der Flamme, die sie erzeugen, identifizieren. Zum Beispiel erzeugt Kupfer eine blaue Flamme, Lithium und Strontium eine rote Flamme, Kalzium eine orange Flamme, Natrium eine gelbe Flamme und Barium eine grüne Flamme.

Dieses Bild veranschaulicht die unterschiedlichen Farben, die beim Verbrennen bestimmter Elemente entstehen.

Eine Flamme aus einem Autogenbrenner brennt mit über 3000?C, heiß genug, um sie zum Schweißen unter Wasser zu verwenden.
Flamme
Die Farbe gibt Aufschluss über die Temperatur einer Kerzenflamme. Der innere Kern der Kerzenflamme ist hellblau und hat eine Temperatur von etwa 1670 K (1400 °C). Das ist der heißeste Teil der Flamme. Die Farbe im Inneren der Flamme wird gelb, orange und schließlich rot. Je weiter man sich vom Zentrum der Flamme entfernt, desto niedriger wird die Temperatur. Der rote Bereich liegt bei etwa 1070 K (800 °C).
Die orangen, gelben und roten Farben in einer Flamme haben nicht nur mit der Farbtemperatur zu tun. Auch Gasanregungen spielen eine wichtige Rolle bei der Flammenfarbe. Einer der Hauptbestandteile einer brennenden Flamme ist Ruß, der eine komplexe und vielfältige Zusammensetzung von Kohlenstoffverbindungen aufweist. Die Vielfalt dieser Verbindungen führt zu einem praktisch kontinuierlichen Bereich möglicher Quantenzustände, zu denen Elektronen angeregt werden können. Die Farbe des ausgestrahlten Lichts hängt von der Energie ab, die jedes Elektron bei der Rückkehr in seinen ursprünglichen Zustand abgibt.