Los átomos pueden ganar o perder electrones para formar iones en un proceso llamado ionización (los compuestos formados de esta manera se llaman compuestos iónicos). Cuando los compuestos iónicos se disuelven en agua, sus iones se separan unos de otros en un proceso llamado disociación. Una característica interesante del agua y de muchos otros compuestos covalentes es que también pueden disociarse en iones. A diferencia de los compuestos iónicos, como el cloruro de sodio, no se ionizan antes de disociarse; logran la ionización y la disociación al mismo tiempo.
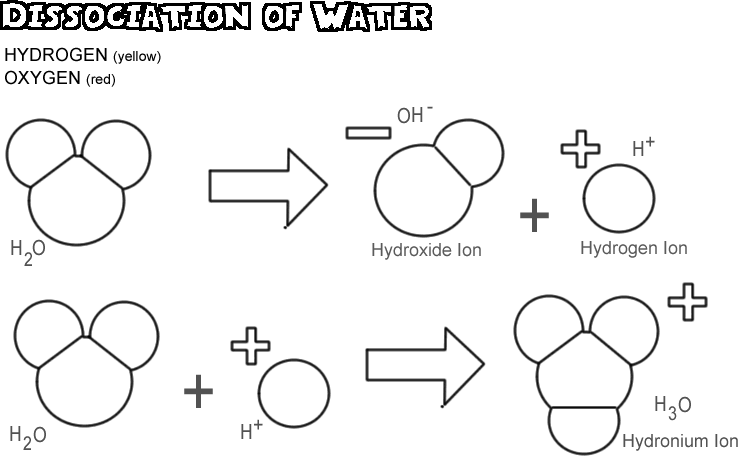
Disociación del agua
Cuando el agua se disocia, uno de los núcleos de hidrógeno deja su electrón con el átomo de oxígeno para convertirse en un ion hidrógeno, mientras que el oxígeno y los otros átomos de hidrógeno se convierten en un ion hidróxido. Como el ion hidrógeno no tiene ningún electrón para neutralizar la carga positiva de su protón, tiene una unidad completa de carga positiva y se simboliza como H+. El ion hidróxido retiene el electrón que le queda y, por tanto, tiene una unidad completa de carga negativa, simbolizada por OH-. El ión hidrógeno (protón) no se desplaza mucho tiempo por sí mismo antes de unirse al átomo de oxígeno de una segunda molécula de agua no ionizada para formar un ion hidronio (H3O +)
En cualquier muestra de agua, muy pocas de las moléculas se disocian en un momento dado: de hecho, sólo una de cada 550 millones. Sin embargo, hay un cambio constante; a medida que un ion hidrógeno se vuelve a unir a un ion hidróxido para formar una molécula de agua, otra molécula de agua se disocia para reemplazar al ion hidrógeno y al ion hidróxido en la solución.
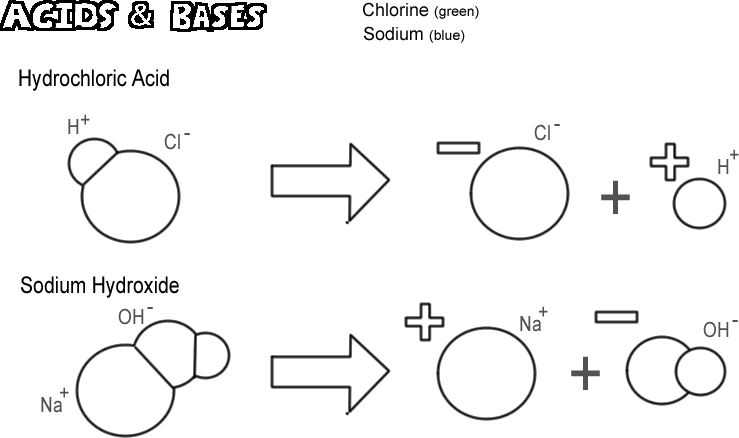
Ácido clorhídrico
Ciertas moléculas, iónicas y covalentes, se disocian de tal manera que liberan un ion hidrógeno sin liberar un ion hidróxido. Estas sustancias se llaman ácidos. Como un ion hidrógeno es realmente un solo protón en la mayoría de los casos, la definición química de un ácido es la de un «donante de protones». Si se «donan» muchos protones (iones de hidrógeno), el efecto puede ser muy profundo, como quemar la piel o disolver el metal. El ácido ilustrado es el ácido clorhídrico. El ácido clorhídrico puro es un gas, pero se disuelve fácilmente en agua para producir una solución de iones hidrógeno e iones cloruro. Como casi todo se disocia en el agua, se denomina ácido fuerte. Los ácidos que no se disocian completamente se llaman ácidos débiles.
Hidróxido de sodio
Lo contrario de un ácido es una base, también conocida como álcali. Una base fuerte típica es el hidróxido de sodio, el principal componente de la lejía. El hidróxido de sodio se disocia para formar un ion sodio y un ion hidróxido. Una base se define como un «aceptor de protones». Las bases más comunes producen un ion hidróxido cuando se disocian, y es el ion hidróxido el que acepta el protón. Una base fuerte puede provocar una quemadura en la piel mucho más grave que un ácido.
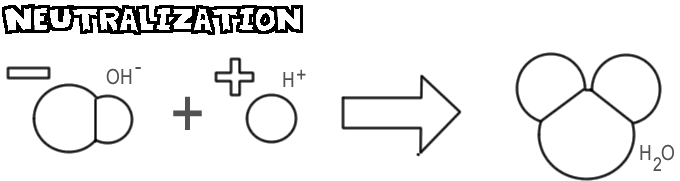
Neutralización
Cuando se mezclan una base y un ácido, el ion hidróxido y la base se combinan con el ion hidrógeno del ácido para formar agua. Este proceso se llama neutralización.
Preguntas:
1. ¿Qué ocurre cuando un átomo gana o pierde un electrón?