Was sind Enzyme und was bewirken sie in unserem Körper? Enzyme sind im Grunde Proteine, die von lebenden Organismen produziert werden, um bestimmte metabolische und biochemische Reaktionen im Körper zu bewirken. Sie sind biologische Katalysatoren, die die Reaktionen im Körper beschleunigen. Wir wollen mehr über sie herausfinden.
Vorgeschlagene Videos:
Was ist die Struktur von Enzymen?
Enzyme sind, wie bereits erwähnt, biologische Katalysatoren. Während sie einen Prozess beschleunigen, stellen sie eigentlich einen alternativen Weg für den Prozess zur Verfügung. Dabei bleiben die Struktur oder die Zusammensetzung der Enzyme jedoch unverändert.
Enzyme bestehen aus Tausenden von Aminosäuren, die auf eine bestimmte Art und Weise miteinander verbunden sind und verschiedene Enzyme bilden. Die Enzymketten falten sich zu einzigartigen Formen, die dem Enzym sein charakteristisches chemisches Potenzial verleihen. Die meisten Enzyme enthalten auch eine Nicht-Protein-Komponente, den so genannten Co-Faktor.
Weitere Themen unter Biomoleküle
- Biomakromoleküle
- Bindende Monomere
- Enzyme
- Stoffwechselgrundlage des Lebens
- Nukleinsäuren
- Polysaccharide
- Proteine
Typen von Enzymen:
Die im Körper ablaufenden biochemischen Reaktionen lassen sich grundsätzlich in 6 Typen einteilen und die Enzyme, die diese Reaktionen bewirken, werden entsprechend benannt:
- Oxidoreduktasen: Diese Enzyme bewirken Oxidations- und Reduktionsreaktionen und werden daher Oxidoreduktasen genannt. Bei diesen Reaktionen werden Elektronen in Form von Hydrid-Ionen oder Wasserstoffatomen übertragen. Wenn ein Substrat oxidiert wird, fungieren diese Enzyme als Wasserstoffspender. Diese Enzyme werden Dehydrogenasen oder Reduktasen genannt. Wenn das Sauerstoffatom der Akzeptor ist, werden diese Enzyme als Oxidasen bezeichnet.
- Transferasen: Diese Enzyme sind für die Übertragung von funktionellen Gruppen von einem Molekül auf ein anderes verantwortlich. Beispiel: Alanin-Aminotransferase, die die Alpha-Aminogruppe zwischen Alanin und Aspartat usw. verschiebt. Einige Transferasen übertragen auch Phosphatgruppen zwischen ATP und anderen Verbindungen, Zuckerreste, um Disaccharide zu bilden, wie die Hexokinase in der Glykolyse.
- Hydrolasen: Diese Enzyme katalysieren Reaktionen, die den Prozess der Hydrolyse beinhalten. Sie brechen Einfachbindungen auf, indem sie Wasser hinzufügen. Einige Hydrolasen fungieren als Verdauungsenzyme, weil sie die Peptidbindungen in Proteinen aufbrechen. Hydrolasen können auch eine Art von Transferasen sein, da sie das Wassermolekül von einer Verbindung auf eine andere übertragen. Beispiel: Glucose-6-phosphatase, die die Phosphatgruppe von Glucose-6-phosphat entfernt, so dass Glucose und H3PO4 übrig bleiben.
- Lyasen: Diese Enzyme katalysieren Reaktionen, bei denen funktionelle Gruppen hinzugefügt werden, um Doppelbindungen in Molekülen zu brechen, oder bei denen Doppelbindungen durch die Entfernung funktioneller Gruppen gebildet werden. Beispiel: Pyruvat-Decarboxylase ist eine Lyase, die CO2 aus Pyruvat entfernt. Andere Beispiele sind Deaminasen und Dehydratasen.
- Isomerasen: Diese Enzyme katalysieren Reaktionen, bei denen eine funktionelle Gruppe an eine andere Position innerhalb desselben Moleküls verschoben wird, so dass das entstehende Molekül tatsächlich ein Isomer des früheren Moleküls ist. Beispiel: Triosephosphat-Isomerase und Phosphoglucose-Isomerase zur Umwandlung von Glucose-6-phosphat in Fructose-6-phosphat.
- Ligasen: Diese Enzyme üben eine Funktion aus, die der der Hydrolasen entgegengesetzt ist. Während Hydrolasen Bindungen durch Hinzufügen von Wasser aufbrechen, bilden Ligasen Bindungen durch Entfernen des Wasseranteils. Es gibt verschiedene Unterklassen von Ligasen, die an der Synthese von ATP beteiligt sind.
Wie funktionieren Enzyme?
Für jede Reaktion im Universum ist Energie erforderlich. In Fällen, in denen keine Aktivierungsenergie vorhanden ist, spielt ein Katalysator eine wichtige Rolle, um die Aktivierungsenergie zu verringern und die Reaktion voranzutreiben. Dies funktioniert auch bei Tieren und Pflanzen. Enzyme helfen, die Aktivierungsenergie der komplexen Moleküle in der Reaktion zu verringern. Die folgenden Schritte vereinfachen, wie ein Enzym arbeitet, um eine Reaktion zu beschleunigen:
Schritt 1: Jedes Enzym hat eine „aktive Stelle“, an die sich eines der Substratmoleküle binden kann. So wird ein Enzym-Substrat-Komplex gebildet.
Schritt 2: Dieses Enzym-Substrat-Molekül reagiert nun mit dem zweiten Substrat, um das Produkt zu bilden, und das Enzym wird als zweites Produkt freigesetzt.
Es gibt viele Theorien, die erklären, wie Enzyme funktionieren. Aber es gibt zwei wichtige Theorien, die wir hier besprechen werden.
Theorie 1: Lock and Key Hypothesis
Dies ist die am meisten akzeptierte Theorie der Enzymwirkung.

Diese Theorie besagt, dass das Substrat genau in das aktive Zentrum des Enzyms passt, um einen Enzym-Substrat-Komplex zu bilden. Dieses Modell beschreibt auch, warum Enzyme so spezifisch in ihrer Wirkung sind, weil sie spezifisch für die Substratmoleküle sind.
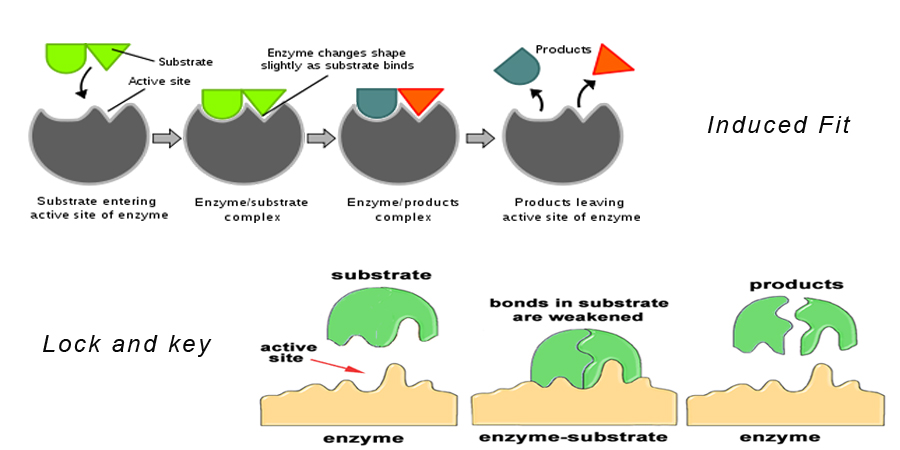
Theorie 2: Induzierte Passform-Hypothese
Sie ist ähnlich wie die Schloss-Schlüssel-Hypothese. Sie besagt, dass sich die Form des Enzymmoleküls bei Annäherung an das Substratmolekül so verändert, dass das Substratmolekül genau in die aktive Stelle des Enzyms passt.
Welche Faktoren beeinflussen die Enzymaktivität in der Zelle?
- Konzentration von Enzymen und Substraten: Die Reaktionsgeschwindigkeit steigt mit zunehmender Substratkonzentration bis zu einem Punkt, über den hinaus jede weitere Erhöhung der Substratkonzentration keine signifikante Änderung der Reaktionsgeschwindigkeit mehr bewirkt. Dies liegt daran, dass ab einer bestimmten Konzentration des Substrats alle aktiven Stellen des Enzyms besetzt sind und keine weitere Reaktion stattfinden kann.
- Temperatur: Mit der Erhöhung der Temperatur nimmt die Enzymaktivität zu, weil die kinetische Energie der Moleküle steigt. Es gibt einen optimalen Wert, bei dem die Enzyme am besten und maximal arbeiten. Diese Temperatur ist oft die normale Körpertemperatur des Körpers. Wenn die Temperatur über eine bestimmte Grenze hinaus ansteigt, beginnen die Enzyme, die eigentlich aus Proteinen bestehen, zu zerfallen und die Reaktionsgeschwindigkeit verlangsamt sich.
- pH: Enzyme reagieren sehr empfindlich auf Veränderungen des pH-Wertes und arbeiten in einem sehr kleinen Fenster zulässiger pH-Werte. Unterhalb oder oberhalb des optimalen pH-Wertes besteht die Gefahr, dass die Enzyme zerfallen und sich dadurch die Reaktion verlangsamt.
- Hemmstoffe: Das Vorhandensein bestimmter Stoffe, die die Wirkung eines bestimmten Enzyms hemmen. Dies geschieht, wenn sich die hemmende Substanz an die aktive Stelle des Enzyms anlagert und dadurch die Anlagerung des Substrats verhindert und den Prozess verlangsamt.
Gelöstes Beispiel für Sie
Q: Ein Enzym wirkt durch?
a. Erhöhen der Aktivierungsenergie
b. Verminderung der Aktivierungsenergie
c. Verringern des pH-Wertes
d. Erhöhung des pH-Wertes
Sol: a. Erhöhung der Aktivierungsenergie
Die Reaktanten machen nicht automatisch eine chemische Veränderung durch. Sie tun dies im Übergangszustand. Der Übergangszustand hat mehr freie Energie als die Reaktanten oder Produkte. Die Unfähigkeit der Reaktanten, sich zu verändern, weil sie für die Umwandlung in den Übergangszustand zusätzliche Energie benötigen, wird als „Energiebarriere“ bezeichnet. Die Energie, die zur Überwindung der Energiebarriere erforderlich ist, wird als „Aktivierungsenergie“ bezeichnet.