Periodická tabulka je tabulka, která systematicky uspořádává chemické prvky v tabulkové formě. Prvky jsou uspořádány zleva doprava v pořadí podle rostoucího atomového čísla. Atomové číslo je počet protonů a neutronů přítomných v jádrech prvku.
Podívejte se zde také na valenční elektrony:-
- Valenční elektrony vodíku
- Valenční elektrony helia
- Valenční elektrony lithia
- Valenční elektrony berylia
- Valenční elektrony boru
- Valenční elektrony uhlíku.
- Dusík Valenční elektrony
- Kyslík Valenční elektrony
- Fluor Valenční elektrony
- Neon Valenční elektrony
- Sodík Valenční elektrony
- Hořčík Valenční elektrony
- Hliník Valenční elektrony
- Křemík Valenční elektrony
- Fosfor Valenční elektrony
- Síra Valenční elektrony
- Chlor Valenční elektrony
- Argon Valenční elektrony
- Draslík Valenční elektrony Elektrony
- Vápník Valenční elektrony
- Skandium Valenční elektrony
- Titan Valenční elektrony
- Vanad Valenční elektrony
- Chrom Valenční elektrony
- Mangan Valenční elektrony
- Železo Valenční elektrony
- Kobalt Valenční elektrony
- Nikl Valenční elektrony
- Měď Valenční elektrony
- Zinek Valenční elektrony
- Gallium Valenční elektrony
- German Valenční elektrony Elektrony
- Arsen Valenční elektrony
- Seleni Valenční elektrony
- Brom Valenční elektrony
- Krypton Valenční elektrony
- Rubid Valenční elektrony
- Stronti Valenční elektrony
- YttriumValenční elektrony
- Zirkonium Valenční elektrony
- Niob Valenční elektrony
- Molybden Valenční elektrony
- Technecium Valenční elektrony
- Ruthenium Valenční elektrony
- Rhodium Valenční elektrony
- Palladium Valenční elektrony
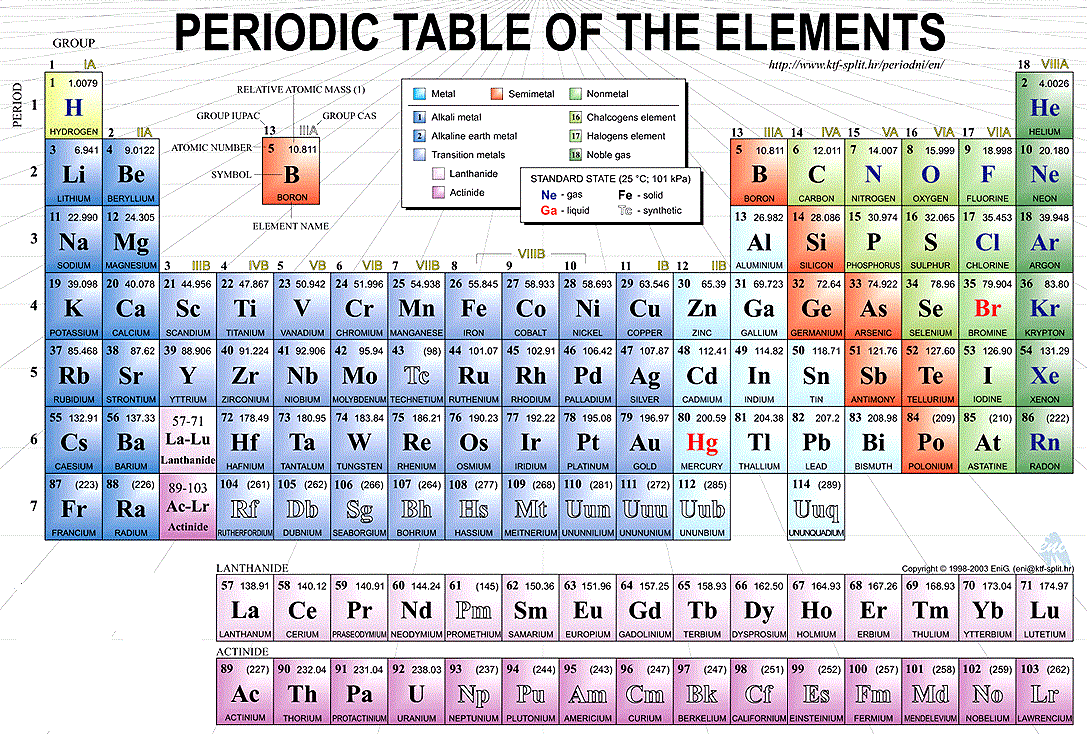

Vodorovné řádky periodické tabulky se nazývají periody, zatímco svislé sloupce jsou známy jako skupiny. Prvky jsou zařazeny do různých skupin v závislosti na jejich vlastních charakteristikách fyzikálních a chemických vlastností
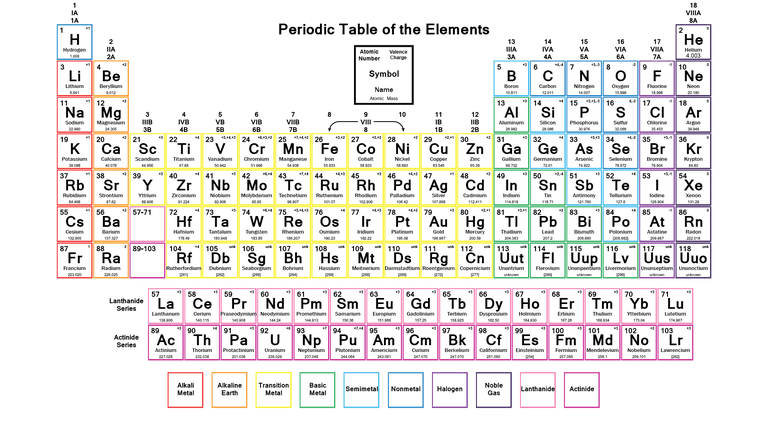
Označení periodické tabulky prvků
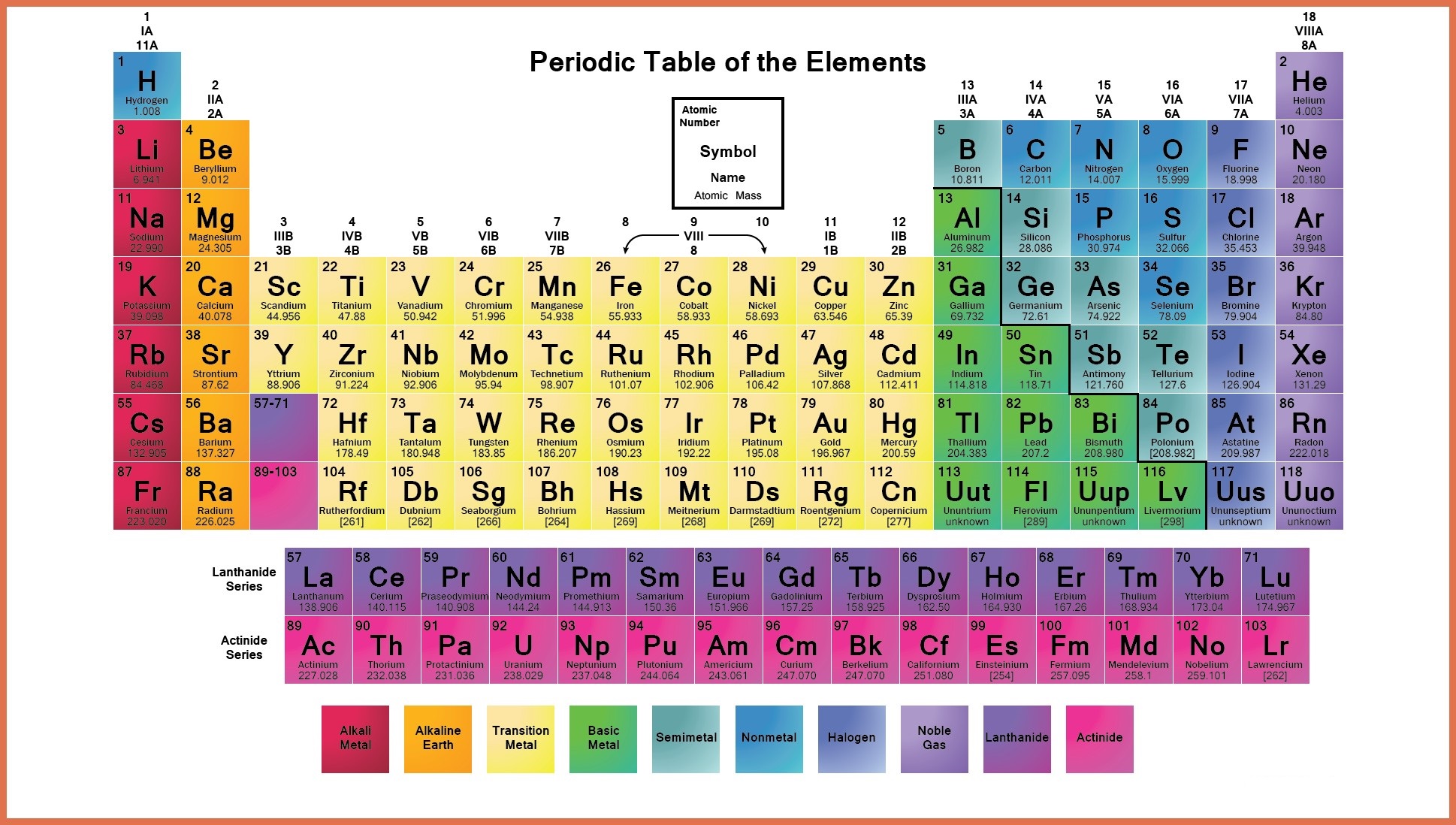
V periodické tabulce jsou různé typy prvků;
- Metaloidy: Prvky, které patří do této skupiny, mají vlastnosti kovů i nekovů. Například antimon, bor, germanium, křemík, arsen, tellur a polonium
- Alkalické kovy: Do první skupiny tabulky patří prvky Lithium, Sodík, Draslík, Rubidium, Cesium, Francium.
- Kovy alkalických zemin: Tyto kovy jsou umístěny ve druhé skupině periodické tabulky, například hořčík, berylium, stroncium, vápník, baryum, radium
- Přechodné kovy: Jedná se o přechodné kovy. Kujnost, tažnost a vodivost elektřiny jsou některé ze základních vlastností těchto prvků, například měď, nikl, chrom, rtuť, zlato a stříbro
- Přechodné prvky: Tyto prvky se nacházejí ve 3., 6. a 7. periodě tabulky. Jsou většinou vyrobeny člověkem, například kurium, cer, uran, europium atd.
- Nekovové kovy: Mezi tyto kovy patří vodík, uhlík, dusík, kyslík, fosfor, síra a selen
- Špatné plyny: Ušlechtilé plyny se nacházejí v 18. skupině periodické tabulky, například Neon, Argon, Helium, Krypton, Xenon a Radon.
Zde najdete valenci prvků
Kovy označené v periodické tabulce
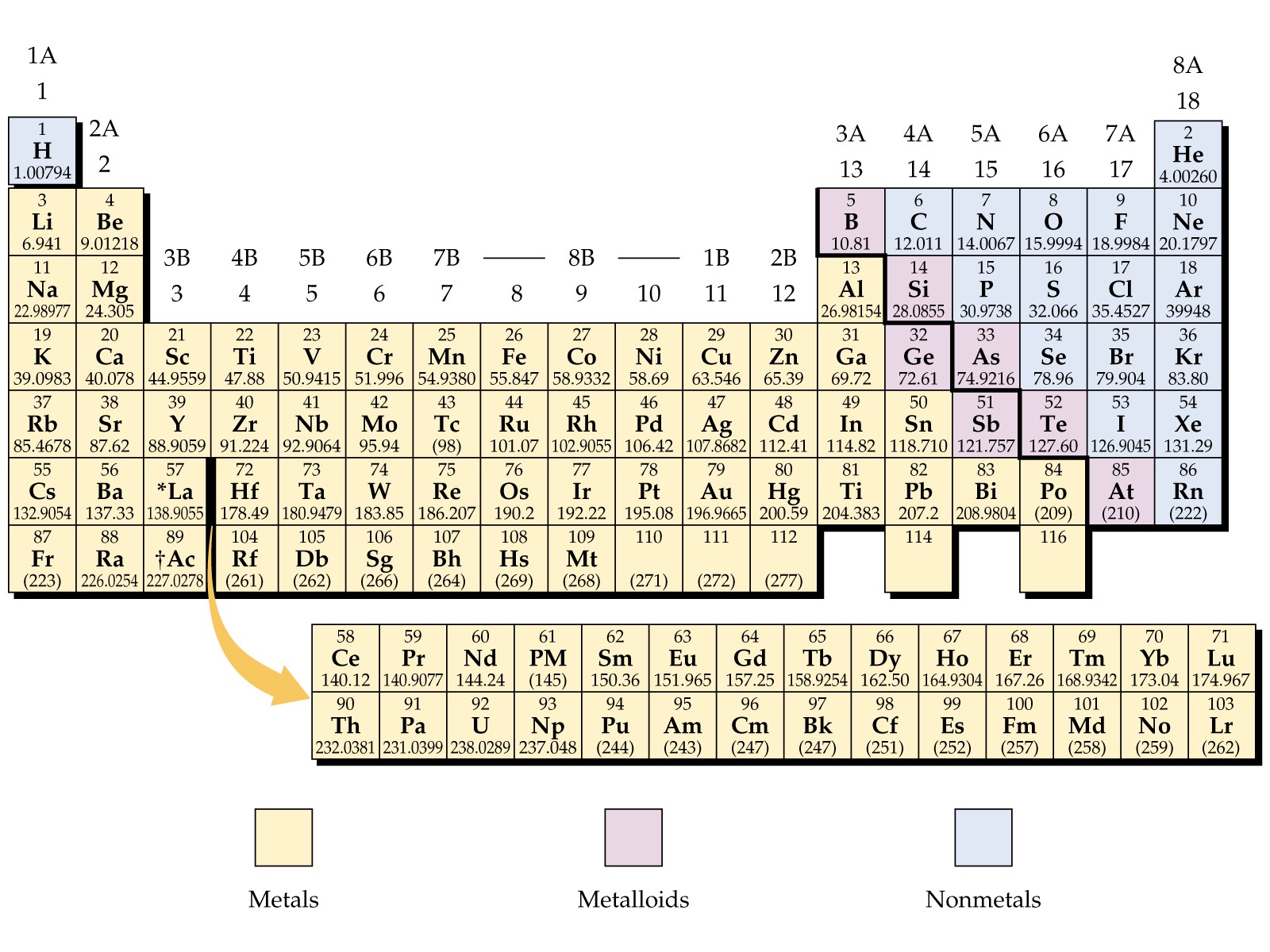

Prvky, které jsou v periodické tabulce klasifikovány jako kovy, mají řadu společných vlastností. Všechny kovy jsou při pokojové teplotě pevné s výjimkou rtuti, která je při pokojové teplotě kapalná. Všechny kovy vedou mají vlastnost teplo a elektřinu a jsou lesklé na pohled. Všechny kovy lze měnit na tenké dráty a plechy, tato vlastnost se nazývá tažnost a kujnost. Kromě těchto vlastností lze kovy charakterizovat také jejich schopností snadno ztrácet elektrony.
Pro tabulku elektronegativit a prázdnou tabulku periodické tabulky navštivte tento odkaz.
Periodická tabulka označená skupinami
Periodická tabulka označená skupinami je přiložena níže;
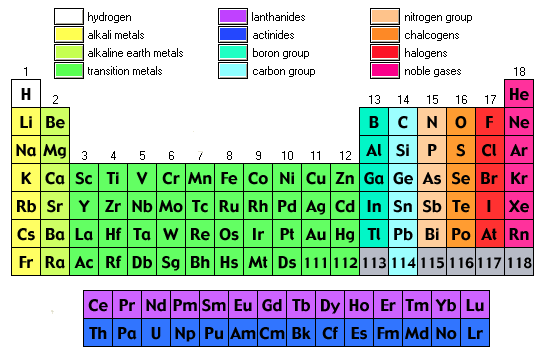

Periodická tabulka označená náboji
Periodická tabulka uvedená níže je označená náboji, pokud ji chcete, můžete si ji stáhnout níže;
Najdete zde náboje prvků

Nejnovější trendy periodické tabulky.