Co jsou enzymy a co dělají v našem těle? Enzymy jsou v podstatě bílkoviny, které produkují živé organismy, aby v těle vyvolaly určité metabolické a biochemické reakce. Jsou to biologické katalyzátory, které urychlují reakce v těle. Pojďme se o nich dozvědět více.
Jaká je struktura enzymů?
Enzymy, jak bylo uvedeno výše, jsou biologické katalyzátory. I když urychlují nebo zrychlují nějaký proces, ve skutečnosti poskytují alternativní cestu pro daný proces. Při tomto procesu však struktura nebo složení enzymů zůstává nezměněno.
Enzymy se ve skutečnosti skládají z 1000 aminokyselin, které jsou spojeny specifickým způsobem a tvoří různé enzymy. Řetězce enzymů se skládají do jedinečných tvarů a právě tyto tvary poskytují enzymu jeho charakteristický chemický potenciál. Většina enzymů obsahuje také nebílkovinnou složku známou jako kofaktor.
Prohlédněte si další témata v části Biomolekuly
- Biomakromolekuly
- Monomery spojující vazby
- Enzymy
- Metabolický základ života
- Nukleové kyseliny
- Polysacharidy
- Proteiny
Typy enzymů:
Biochemické reakce probíhající v těle jsou v zásadě 6 typů a enzymy, které tyto reakce vyvolávají, jsou podle toho pojmenovány:
- Oxidoreduktázy: Tyto enzymy vyvolávají oxidační a redukční reakce, a proto se nazývají oxidoreduktázy. Při těchto reakcích dochází k přenosu elektronů ve formě hydridových iontů nebo atomů vodíku. Při oxidaci substrátu působí tyto enzymy jako donor vodíku. Tyto enzymy se nazývají dehydrogenasy nebo reduktasy. Když je akceptorem atom kyslíku, nazývají se tyto enzymy oxidázy.
- Transferázy: Tyto enzymy jsou zodpovědné za přenos funkčních skupin z jedné molekuly na druhou. Příklad: alaninaminotransferáza, která přehazuje alfa-aminoskupinu mezi alaninem a aspartátem atd. Některé transferázy také přenášejí fosfátové skupiny mezi ATP a jinými sloučeninami, cukerné zbytky za vzniku disacharidů, např. hexokináza při glykolýze.
- Hydrolázy: Tyto enzymy katalyzují reakce, které zahrnují proces hydrolýzy. rozbíjejí jednoduché vazby přidáním vody. Některé hydrolázy fungují jako trávicí enzymy, protože rozbíjejí peptidové vazby v bílkovinách. Hydrolázy mohou být také typem transferáz, protože přenášejí molekulu vody z jedné sloučeniny na druhou. Příklad: Glukóza-6-fosfatáza, která odstraňuje fosfátovou skupinu z glukóza-6-fosfátu a zanechává glukózu a H3PO4.
- Lyázy: Tyto enzymy katalyzují reakce, při nichž se přidávají funkční skupiny za účelem přerušení dvojných vazeb v molekulách nebo při nichž dvojné vazby vznikají odstraněním funkčních skupin. Příklad: Pyruvát dekarboxyláza je lyáza, která odstraňuje CO2 z pyruvátu. Mezi další příklady patří deaminázy a dehydratázy.
- Isomerázy: Tyto enzymy katalyzují reakce, při nichž se funkční skupina přesune do jiné polohy v rámci téže molekuly tak, že výsledná molekula je ve skutečnosti izomerem předchozí molekuly. Příklad: triosefosfát izomeráza a fosfoglukóza izomeráza pro přeměnu glukóza-6-fosfátu na fruktóza-6-fosfát.
- Ligázy: Tyto enzymy plní opačnou funkci než hydrolázy. Tam, kde hydrolázy rozbíjejí vazby přidáním vody, ligázy vytvářejí vazby odstraněním vodní složky. Existují různé podtřídy ligáz, které zahrnují syntézu ATP.
Jak enzymy fungují?
K tomu, aby ve vesmíru proběhla jakákoli reakce, je zapotřebí energie. V případech, kdy není poskytnuta aktivační energie, hraje důležitou roli katalyzátor, který snižuje aktivační energii a provádí reakci. To funguje i u živočichů a rostlin. Enzymy pomáhají snižovat aktivační energii složitých molekul v reakci. Následující kroky zjednodušují fungování enzymu, který urychluje reakci:
Krok 1: Každý enzym má „aktivní místo“, na které se může vázat jedna z molekul substrátu. Tak vznikne komplex enzym-substrát.
Krok 2: Tato molekula enzymu-substrátu nyní reaguje s druhým substrátem za vzniku produktu a enzym se uvolní jako druhý produkt.
Existuje mnoho teorií, které vysvětlují, jak enzymy fungují. Existují však dvě důležité teorie, které zde probereme.
Teorie 1: Hypotéza zámku a klíče
Jedná se o nejpřijatelnější z teorií působení enzymů.

Tato teorie tvrdí, že substrát přesně zapadne do aktivního místa enzymu a vytvoří komplex enzym-substrát. Tento model také popisuje, proč jsou enzymy ve své činnosti tak specifické, protože jsou specifické pro molekuly substrátu.
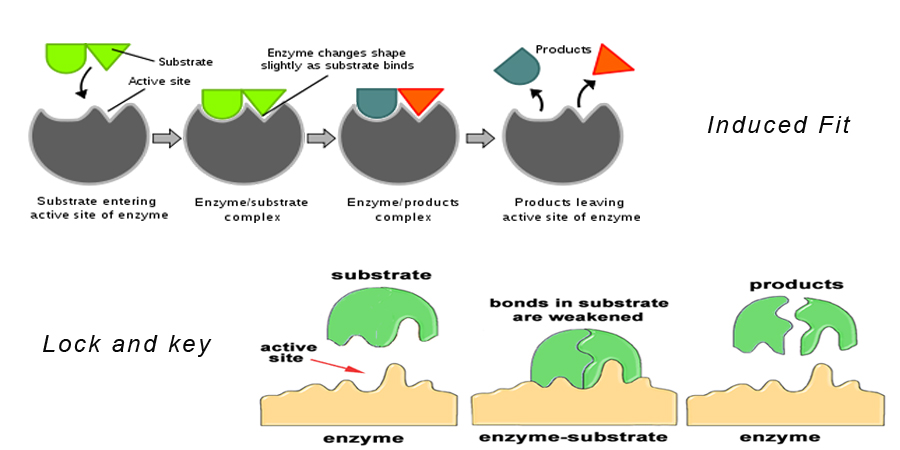
Teorie 2: Hypotéza indukovaného uložení
Tato teorie je podobná hypotéze zámku a klíče. Říká, že tvar molekuly enzymu se při přibližování k molekule substrátu mění tak, aby molekula substrátu přesně zapadla do aktivního místa enzymu.
Jaké faktory ovlivňují aktivitu enzymů v buňce?
- Koncentrace enzymů a substrátů: Rychlost reakce se zvyšuje s rostoucí koncentrací substrátu až do určitého bodu, za kterým již další zvýšení koncentrace substrátu nevede k výrazné změně rychlosti reakce. K tomu dochází proto, že po dosažení určité koncentrace substrátu jsou všechna aktivní místa na enzymu zaplněna a k další reakci nemůže dojít.
- Teplota: S rostoucí teplotou se aktivita enzymu zvyšuje, protože se zvyšuje kinetická energie molekul. Existuje optimální úroveň, kdy enzymy pracují nejlépe a maximálně. Tato teplota je často normální tělesná teplota organismu. Když se teplota zvýší nad určitou mez, enzymy, které jsou vlastně tvořeny bílkovinami, se začnou rozpadat a rychlost reakce se zpomalí.
- pH: Enzymy jsou velmi citlivé na změny pH a pracují ve velmi malém okně přípustných hodnot pH. Pod nebo nad optimální úrovní pH hrozí, že se enzymy rozpadnou, a tím se reakce zpomalí.
- Inhibitory: Přítomnost určitých látek, které inhibují působení určitého enzymu. K tomu dochází, když se inhibiční látka naváže na aktivní místo enzymu, čímž zabrání navázání substrátu a zpomalí proces.
Řešený příklad pro vás
Q: Enzym působí tak, že?
a. Zvyšuje aktivační energii
b. Snižuje aktivační energii
c. Snižuje pH
d. Zvýšení pH
Sol: a. Zvýšení aktivační energie
Reaktanty nepodléhají chemické změně automaticky. Činí tak v přechodném stavu. Přechodný stav má větší volnou energii než reaktanty nebo produkty. Neschopnost reaktantů podstoupit změnu v důsledku požadavku dodatečné energie na jejich převedení do přechodného stavu se nazývá „energetická bariéra“. Energie potřebná k překonání energetické bariéry se nazývá „aktivační energie“.